天津大学化学系有机化学复习资料
天津大学有机化学chapt17

N-H 伸 缩
N-H 弯 曲
C-N 伸 缩
N-H 摇 摆
异丁胺的红外光谱
N-H伸缩 伸缩 N-H弯曲 弯曲
C-N伸缩 伸缩
N-甲基苯胺的红外光谱 甲基苯胺的红外光谱
(五) 胺的化学性质 五 1.碱性和成盐 碱性和成盐
pKb 甲胺 3.38 二甲胺 3.27 三甲胺 4.21 氨 苯胺 对甲苯胺 4.76 9.37 8.92 对氯苯胺 9.85 对硝基苯胺 13.0
(CH3)3N
2.腈或酰胺的还原 腈或酰胺的还原
NC(CH2)8CN + 4H2
CH3O N CCH3
Ni,KOH,NH3,C2H5OH, 9 5 %
H2N(CH2)10NH2
CH3 N CH2CH3
LiAlH4,醚
工业上常采用高级脂肪酸经腈催化加氢的 方法高级脂肪伯胺。 方法高级脂肪伯胺。
C15H31COOH
C6H5N+H3Cl(C2H5N+H3)2SO42-
氯化苯铵
(CH3)3N+CH2C6H5Br-
硫酸二乙铵
(CH3)3N+CH2CH3OH-
溴化三甲苄铵
氢氧化三甲乙铵
(二) 胺的结构 二
氨、甲胺和三甲胺的结构如下图:
..
N H H H
CH3
..
N H H
..
N CH3 CH3 CH3
由于胺是棱锥形结构,当氮原子上有三个 由于胺是棱锥形结构, 不同的基时,它是手性分子。 不同的基时,它是手性分子。
2.硝基烷的性质 硝基烷的性质 a.硝基烷是无色的高沸点液体,常用作溶剂。 硝基烷是无色的高沸点液体,常用作溶剂。 硝基烷是无色的高沸点液体 b. 硝基烷具有明显的酸性。 硝基烷具有明显的酸性。
532002[有机化学] 天津大学考试题库及答案
![532002[有机化学] 天津大学考试题库及答案](https://img.taocdn.com/s3/m/ee110dcb3c1ec5da50e270bd.png)
有机化学复习题一、命名下列化合物或根据命名写出构造式1、(甲基环丙烷)2、(2-甲基丁烷)3、((Z)-1,2-二溴乙烯)4、(反-2-戊烯)5、(三乙胺)6、((R)-2-羟基丙酸)7、(对甲基苯甲醛)8、(环己烷)9、(N,N-二甲基乙酰胺)10、(甲苯)11、(叔丁醇)12、(对羟基苯甲醛)13、(苯甲酰氯)14、((E)-1-溴丙烯)15、间二甲苯:、邻苯二甲酸酐:17、呋喃: 18、苯甲醚:19、对甲基苯酚: 20、氯苯:21、N-甲基苯胺: 22、间氯苯甲酸:23、对氯甲苯:25、乙酰苯胺:26、乙醚:二、选择题1、下列分子中,属于非极性分子的是:( A )(A) CCl 4 (B )CH 2Cl 2 (C )CH 3OH (D )CH 3Cl2、下列自由基中,最不稳定的是:( B )(A)(B)(C)(D)3、下列投影式中,属于Newman 投影式的是:( B ) (A)(B)(C)(D)4、下列碳正离子中,参与超共轭C-H 键最多的是( D )(A)(B)(C)(D)5、下列化合物中,存在π-π共轭的是:( B ) (A)(B)(C)(D)6、甲苯与氯气在光照条件下的主要产物是:( A ) (A)(B)(C)(D)7、列化合物不具有手性的是:( A )(A)(B)(C)(D)8、下列离子亲核能力最强的是:( C ) (A)(B) (C)(D)9、下列化合物或离子中,不具有芳香性的是:( B )(A)(B)(C)(D)10、下列化合物,酸性最强的是:( D ) (A)(B)(C)(D)11、下列醇类化合物在与ZnCl 2的浓HCl 进行反应时,速率最大的是( D ) (A) (B)(C)(D)12、下列化合物在与亚硫酸氢钠发生亲核加成反应,反应活性最高的是( D ) (A)(B)(C)(D)13、下列酯类化合物在进行水答案反应时,反应速率最高的是:( B ) (A)(B)(C)(D)14、下列化合物中,酸性最强的是:( A ) (A) (B) (C)(D)15、下列化合物中,碱性最强的是:( C ) (A)(B)(C)(D) 16、下列酸性化合物或离子中,不属于Bronsted 酸的是:( A )(A) (B) HNO 3 (C) HCl(D)AlCl 317、下列结构式中,不能表示构造的是:( B ) (A)(B)(C)(D)18、已知烷烃分子式C 5H 10,发生自由基氯代反应时,一元取代物只有一种,那么该烷烃的构造式应为:( A ) (A)(B)(C) (D)19、下列化合物在与1,3-丁二烯进行Diels-Alder反应时活性最高的是( D )( A ) (B)(C) (D)20、下列化合物中不是Lewis酸的化合物是:(A)(A) CHCl3 (B) BF3(C) AlCl3 (D) FeCl321、下列化合物中,是与发生Diel-Aldel反应产物的是(C)(B)22、醛与酮的羰基在与HCN发生亲核加成反应时,速率最快的是(A)(A) HCHO(B)(C)(D)23具有手性中心的个数为(B)(A) 1 (B) 2(C) 3 (D) 424、下述化合物进行硝化反应会时,反应产物最可能是( C )(A)(B)(C)(D)三、完成下列各反应式1、答:2、答:3、答:4、答:5、答:6、答:7、答:8、答:9、答:10、答:11、答:12、13、答:14、答:15、答:16、答:17、答:18、答:19、答:20、答:21、答:22、答:23、答:24、答:四、合成题1、由合成答:1答:2答:2、以答:3答:3、由合成答:4答:4和合成答:11/ 11。
天津大学有机化学chapt4

CH2
CH C CH2 Cl
n
氯丁橡胶
(四) 二烯烃的结构
(1)丙二烯的结构
H
118.4 sp sp
2
C
0.108nm
C
CH2
H
0.131nm
丙二烯分子是线型非平面分子
(2) 1,3-丁二烯的结构
1,3-丁二烯分子中,碳 碳单键键长0.147nm, 比乙烷碳碳单键键长0.154nm短,由此可见 1,3-丁 二烯分子中碳碳之间的键长趋于平均化。
(七)离域体系的共振论表述法
(1)共振论的基本概念
共振论:即离域体系可以用几个经典结构的叠加来描述。
CH2 CH CH CH2
+
CH2 CH CH2 CH2
-
-
CH2 CH CH2 CH2+
1,3-丁二烯的共振杂化体
极限结构对共振杂化体的贡献原则:
(a)共价键数目相等,贡献相同
O O
-
CH2 CH CH2+
H2C+ CH CH2 R C
O
-
R C O
(b)共价键多的极限结构稳定,对杂化体贡献大。
CH2 CH CH CH2
+
CH2 CH CH2 CH2
-
-
CH2 CH CH2 CH2+
(c)电荷分离的极限结构稳定性低,对杂化体贡献小
(d)违反电负性原则极限结构对杂化体的贡献极小,忽略。
CH2 CH CH O+
O 顺丁烯二酸酐
+
CHO 115 oC , 2~4 h 甲苯 丙炔醛
CHO 82% 1,4 - 环己二烯甲醛
双烯体 亲双烯体
天津大学第五版有机化学答案用于合并

第一章 习题(一) 用简单的文字解释下列术语:(1) 有机化合物:碳氢化合物及其衍生物。
(2) 键能:形成共价键时体系所放出的能量。
(3) 极性键:成键原子的电负性相差为0.5~1.6时所形成的共价键。
(4) 官能团:决定有机化合物的主要性质的原子或原子团。
(5) 实验式:能够反映有机化合物元素组成的相对比例的化学式。
(6) 构造式:能够反映有机化合物中原子或原子团相互连接顺序的化学式。
(7)均裂:共价键断裂时,两个成键电子均匀地分配给两个成键原子或原子团,形成两个自由基。
(8) 异裂:共价键断裂时,两个成键电子完成被某一个成键原子或原子团占有,形成正、负离子。
(9) sp 2杂化:由1 个s 轨道和2个p 轨道进行线性组合,形成的3个能量介于s 轨道和p 轨道之间的、能量完全相同的新的原子轨道。
sp 2杂化轨道的形状也不同于s 轨道或p 轨道,而是“一头大,一头小”的形状,这种形状更有利于形成σ键。
(10) 诱导效应:由于成键原子的电负性不同而引起的电子云的转移。
诱导效应只能通过σ键传递,并且随着碳链增长,诱导效应迅速减弱。
(11) 氢键:由氢原子在两个电负性很强的原子之间形成“桥梁”而导致的类似化学键的分子间或分子内作用力。
氢键具有饱和性和方向性,但作用力比化学键小得多,一般为20~30kJ/mol 。
(12) Lewis 酸:能够接受的电子的分子或离子。
(二) 下列化合物的化学键如果都为共价键,而且外层价电子都达到稳定的电子层结构,同时原子之间可以共用一对以上的电子,试写出化合物可能的Lewis 结构式。
(1)C H 3N H 2 (2) C H 3O C H 3 (3)CH 3C OH O(4) C H 3C H =C H 2 (5) C H 3C C H (6) CH 2O 解:分别以“○”表示氢原子核外电子,以“●”表示碳原子核外电子,以“★”表示氧原子核外电子,以“△”表示氮原子核外电子,题给各化合物的Lewis 结构式如下:(1) CH HH H H。
天津大学有机化学第一章 取代基效应 Substitution

空间效应的作用:
1. 化合物(构象)的稳定性
HH CH3
H CH3 H
2. 化合物的酸碱性
O C OH
C CH3
CH3 CH3
pKa1 < pKa2
O C OH
当t-Butyl 在邻位时, 把羧基挤出了与苯环所在 平面,羧基的 -C效应消失。
3. 对反应活性的影响
伯卤代烷的乙醇解的相对速度是与中心碳原子 连接的烷基大小相关的:
σ-π 超共轭体系 σ- p 超共轭体系
四. 场效应 ( )
五. 空间效应 ( )
1. 对化合物稳定性的影响 2. 对化合物酸性的影响 3. 对反应活性的影响 4. 张力:F-张力,B-张力,角张力
高等有机化学的研究内容与目的
高等有机化学是有机化学的核心部分(core)
高等 有机化学
分子结构的 基本概念
含碳化合物的 反应性
化合物 中间体
结构
反应过程中的结构变化 反应机理
揭示反应的本质、内在规律,把有机反应有机地 联系起来。
第一章 取代基效应
(Substituent Effects)
H
H
H C Br + OH
H C OH + Br
H
H
反应的本质: 旧键的断裂,新键的生成 共价键的极性取决于取代基的效应
第一章 取代基效应 (Substituent Effects) ( )
取代基效应 ( ) 电子效应 ( )
一. 诱导效应 ( )
结构特征 ( ) 传递方式 传递强度 相对强度
二. 共轭体系 ( )
1. 共轭体系与共轭效应 2.结构特征 ( ) 3. 传递方式 ( )
4. 相对强度
【天津大学】优质课(化学专业)《有机化学》全册优秀课件

【烷wan】取完全之意,碳被氢完全饱和; 【烃ting】指碳tan氢qing化合物。
•烷烃(alkane)是指分子中的碳原子以单 键相连,其余的价键都与氢完全结合而成 的链状化合物
1、碳、氢原子的类型
CH3
CH3
1oH 2oH 3oH
H3C C CH2 CH CH3 1oC 2oC 3oC 4oC
-X -OH R-O-R -CHO -CO-COOH -NH2
CH3CH2Cl CH3CH2OH CH3-O-CH3 CH3CHO CH3COCH3 CH3COOH CH3CH2NH2
chloro-ol ether -al -one -oic acid -amine
有机化合物构造式的表达方式
• 电子式:用元素符号和电子符号表示化合物的 化学式叫电子式也叫路易斯式
合
合
化
化
物
物
合
合
物
物
链状化合物:开链化合物,脂肪族化合物,
H3C
CH2
CH3
CH2
H3C
CH3
H3C
碳环化合物: 脂环化合物:性质与无环化合物类似
芳香族化合物:有一些特殊性质,大 多含苯环
杂环化合物:含杂原子的环状化合物。杂 原子指除碳以外的其他原子,常见的有氧、 硫、氮等。
O
N
二、按官能团分类
C3H6O
O H3C C CH2 H
OH CH3 C CH2
{构型异构体
立体异构体
构象异构体
{顺反异构体 对映异构体
立体异构体:分子中原 子或原子团互相连接次 序相同,但空间排列方 式不同而引起的异构体。
顺反异构体:由于双键不能自由旋转或由于成 环碳原子的单键不能自由旋转而引起的立体异 构体。
天津大学考研有机化学综合复习
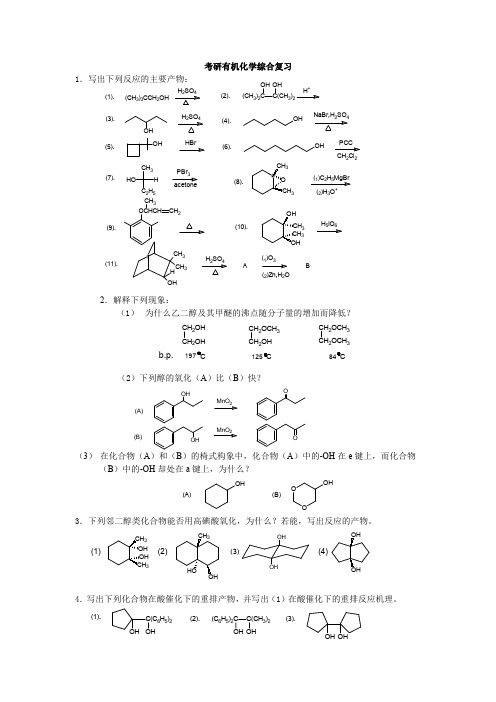
OH
O HBr
(1).
CH CH2
CH3
(2).
H2SO4
OH
OH
0C
(3).
H2SO4
O
OH
(4).
H+
OCH2CH CH2 (5).
HBr
O
8.RCOOCAr3 型和 RCOOCR3 型的酯,在酸催化水解时,由于可以生成稳定的碳正离子, 可发生烷-氧键断裂。请写出 CH3COOCPh3 在酸催化下的水解反应机理。 9.光学活性物质(Ⅰ)在酸存在下水解,生成的醇是外消旋混合物。请用反应机理加以解 释。
(4)一碱性化合物 A(C5H11N),它被臭氧分解给出甲醛,A 经催化氢化生成化合物 B (C5H13N),B 也可以由己酰胺加溴和氢氧化钠溶液得到。用过量碘甲烷处理 A 转变成一个 盐 C(C8H18NI),C 用湿的氧化银处理随后热解给出 D(C5H8),D 与丁炔二酸二甲酯反应给 出 E(C11H14O4),E 经钯脱氢得 3-甲基苯二酸二甲酯,试推出 A~E 的各化合物的结构,并写 出由 C 到 D 的反应机理。
(11). CH3NCO + EtOH
(12).
NH2
HNO2 A
NH (13).
NH H+
OH B
(14). (H3C)2C N N C(CH3)2
CN
CN
(15). C6H5CH2COCl
NaN3 A
KOH
B
C
(16).
PCl5
N OH
13.写出下列各消去反应所生成的主要产物:
(1). (CH3)2CHCHCH3OH+N(CH3)3
考研有机化学综合复习
1.写出下列反应的主要产物:
天津大学有机化学chapt11

对甲苯磺酰胺
CH3 SO2NHR +
RNH3Cl
+ -
N--烷基对甲苯磺酰胺
芳磺酰氯做为酰化剂可以进行芳环上的亲电取代反应
Cl SO2Cl
+
Cl
AlCl3
O
Cl
S O 4,4'-二氯二苯砜
Cl + HCl
芳磺酰氯也可以被还原
SO2Cl Zn—H2SO4
0 C
SH 苯硫酚 91%
CH3
Sodium 5-hydroxy naphthalene-1-sulfonate
Benzene-1,3- OH disulphonic acid
(二)芳磺酸的制法
(1)直接磺化
SO3H
H3C
SO3 H C 3 97%
SO3H
+ H3C
3%
SO3H NaOH
H25C12
SO3 H C 25 12
H25C12
赵海涛 聂建明
第一节
芳卤化合物
定义: 芳烃分子中的一个或几个氢原子被卤原 子取代后的化合物称为芳卤化合物。
分类:分为卤原子连接在芳环上和侧链上两种 类型。
Br
CH2Cl
CH2CH2Cl
lC
一、芳卤化合物的命名 二、芳卤化合物的制法 三、芳卤化合物的物理性质 四、芳卤化合物的化学性质
1.苯环位置对卤原子活泼性的影响 2.芳环上的亲核取代反应 3.芳环上的亲核反应机理 4.与金属作用 5. 芳环上的亲电取代反应
Cl C H
氯化苄的SN2反应过渡态
H
Nu
C.隔离型卤化物
2.芳环上的亲核取代反应
(1)水解 连在芳环上的卤原子一般较难水解, 需高温、高压和催化剂,反应才能进行。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
CH2OH CH2COOC2H5
OH
6). 与Wittig试剂反应
(Ph)3P + CH3CH2Br
(Ph)3PCH2CH3Br
PhLi (Ph)3P=CHCH3
O CH2CH3
NH2OH NH2NH2
NH2NH
CH3OC(CH3)3 CH3OCH2CH3
O O
H2C CH CH2Cl O
• 制备方法:
醇脱水及Williamson醚合成:
CH3CH2OH ONa
H2SO4 140oC
CH3CH2OCH2CH3
+ (CH3O)2SO2
ONa
+
Cl
OCH3 O
环氧化合物制备:
RCH=CH2
O RCOOH
H2C CH R O
醇羟基的反应特性
• 苯环上卤化,请注 意反应条件不同, 溴化的产物不同.
OH
O
+ H+
OH OH
OH
Br2 Br H2O
Br2 H2O, HBr
Br2 CCl4
OH Br
Br OH Br
Br OH
Br
醇羟基的反应特性
• 苯环上的磺化
OH H2SO4
OH
OH
+
SO3H H2SO4
SO3H
OH SO3H
RCR"
(2) H3O
R"
酚的合成
•异丙苯法 •磺化碱熔法 •芳卤的水解 •由重氮盐制备
•异丙苯法
+
CH2=CHCH3
H3PO4, 250oC 2.41MPa
O2, Na2CO3, H2O 90~130 oC
0.1-2% H2SO4 60~65 oC
OOH OH
•磺化碱熔法
H2SO4
NaOH 熔融
有机化学1B
赵温涛
第九章 醇和酚
命名:常见的有机化合物的命名要会。如
NH2CH2CH2OH ClCH2CH2OH
CH3CH2 H3C
H CH2OH
HOCH2CH2OH
OH PhCH2CH2OH
OH
OH CH3O
OH
OH
N
OH
醇的合成
由合成气合成(该方法不要求) 由烯烃合成
CO + H2
ZnO-CuO-Cr2O3 210~270oC
② 成醚: Williamson醚合成 ③ 成酯,酚成酯反应困难,应使用酸酐或酰氯进行
酚的酯可进行Fries重排。反应条件不一样,产物不同。 ④ 氧化反应
醇和酚的反应共性
① 酸性,利用酚的酸性进行分离. 与活泼金属的反应:
CH3CH2OH
Na
CH3CH2ONa
Mg CH3CH2OH
(CH3CH2O)2Mg
SO3Na CH OH NaCN
CN
CH OH HCl H2O
COOH CH OH
5). 格氏试剂等金属有机化合物反应
MgCl +
O (1) 纯醚 HCH
(2)H2O, H2SO4
(1) HC CNa O
(2) H3O+
C CH OH
O
(1)Zn, 甲苯
O + BrCH2COC2H5
(2) H3O+
O
4). 与氢氰酸的反应
O CH3CCH3
HCN
OH
CH3CCN CH3
C2H5OH H2SO4
CH3 CH2=CCOOC2H5
O CH3CH2CCH3 HCN
OH
CH3CH2CCH3 CN
HCl H2O
浓 H2SO4
OH
CH3CH2CCOOH CH3
CH3 CH3CH=CCOOH
CHO NaHSO3
I-
CH3CH2CH2OH + CH3I
HI
CH3CH2CH2I
CH3 H H3C C O CH3
CH3
CH3
H3C C CH3
+ CH3OH
I-
CH3
H3C C I
CH3
环氧的开环:请注意酸性条件及碱性条件下的开环方向不同,原理请见书。
H2C CH CH3 H+ O
H2C CH CH3 O H
H2O
OH2 H2C CH CH3
-H+
OH
OH
H2C CH CH3 OH
H2C CH CH3 O
H3N
H2C CH CH3 NH2 OH
H2C CH CH3 O
(1)PhMgBr (2) H3O+
OH PhCH2CHCH3
(1) PhMgBr
O
PhCH2CH2OH
(2) H3O+
第十一章 醛、酮和醌
• 命名:常见化合物: • 制备方法: • 醛酮的化学性质:主要分为三个大的类型:
Co催化剂 12300-3~01M75PoaC
CHO CH3CH2CH2CHO + CH3CHCH3
H2, Ni
CH2OH
133-50~M1P60a oC CH3CH2CH2CH2OH + CH3CHCH3
醇的合成 还原
O RCR' H2/Ni
或 H2/Pd
OH RCHR'
NaBH4
O RCR'
O RCOR'
第十章 醚和环氧化合物
• 命名部分: • 制备方法:
醇脱水及Williamson醚合成: 环氧化合物制备: • 醚的反应: 碱性 醚的酸催化断裂,醚的结构不同,断裂的方式不同。 环氧的开环:请注意酸性条件及碱性条件下的开环方向不同,
原理请见书。
• 命名部分:
CH3OCH3 CH3CH2OCH2CH3
RCH2OH
RCH2X
O RCOH
POCl3
O RCClLeabharlann RCH2OHSOCl2
RCH2Cl
O RCOH
O SOCl2 RCCl
醇羟基的反应特性
3). 脱水反应及邻二醇的嚬哪醇重排.
CH3 CH3 CH3 C C CH3
OH OH
Al2O3
CH3CH2OH
H2SO4 140 oC
CH3CH2OCH2CH3
CH3CH2OH
H2SO4 160 oC
CH2=CH2
CH3 CH3
H+
CH3 C C CH3
OH OH
重排
CH3 CH3 CH3 C C CH3
OH OH2
CH3 CH3 C C CH3
OH CH3
-H2O
CH3 CH3 CH3 C C CH3
OH
CH3 CH3 C C CH3
OH CH3
HO OH
SO3H
NaOH
SO3Na
ONa
OH
H+
•芳卤的水解
Cl NO2 NaOH
ONa NO2
OH
H+
NO2
•由重氮盐制备
NO2
Fe/ HCl(稀)
NH2
NaNO2, H2SO4 0~5oC
N2 HSO4
OH H2SO4
醇和酚的反应共性
① 酸性,利用酚的酸性进行分离,酸性的比较应会。与活泼 金属的反应:
OAc 165 oC
CH3 OH
O HO O
醇羟基的反应特性
• Kolbe_Schmitt反应
ONa + CO2
150-160 oC 0.5 MPa
OH COONa H+
OH COOH
OK 180-250 oC
+ CO2 2.02 MPa
COOK OH
COOH H+
OH
与甲醛的缩合及酚醛树脂部分请自学,不要求。
OH CH3CHCH3
K2Cr2O7, H2SO4(稀)
O CH3CCH3
R R C OH R C OH
R
OH
KIO4
Cr2O3 HOAC
NH MnO2
R2C O O
O O
O
醇羟基的反应特性
•弱碱性: •卤化反应,注意卤化时所用氢卤酸的活性比 较及 醇的种类的反应活性的比较. •脱水反应及邻二醇的嚬哪醇重排.
RCH=CH2
(1)Cl2, H2O (2) OH-
H2C CH R O
• 醚的反应: 碱性
ROR + BF3 AlCl3
BF3 ROR
AlCl3 ROR
醚的酸催化断裂,醚的结构不同,断裂的方式不同。
CH3CH2CH2OCH3 + HI
CH3 H3C C O CH3 + HI
CH3
H CH3CH2CH2OCH3
CH3OH
羰基合成 法(该方法不要求) 还原 格氏试剂
醇的合成 由烯烃合成
CO + H2
ZnO-CuO-Cr2O3 210~270oC
CH3OH
RCH=CH2
(1) H2SO4 (2) H2O
OH RCHCH2
RCH=CH2 H3PO4 ,P
OH RCHCH2
(1) 1/2 (BH3)2 RCH=CH2 (2) H2O2, OH-
加成反应:各种醛酮反应活性的比较
• 与水的反应 • 与亚硫酸氢钠加成反应:成盐溶于水,分离,再与酸或碱反应
被释放. • 与醇的反应:形成缩醛(酮),起保护作用,如: • 与氢氰酸的反应 • 格氏试剂等金属有机化合物反应, Reformasky反应 • 与Wittig试剂反应 • 与氨基反应:注意伯氨类与仲氨类化合物的区别。且对与反
