北京大学中级有机化学习题与答案
中级有机化学-裴坚

2. CF3CO2Et, -15 oC,
Cl
30 分钟,然后
O
3. HCl, HOAc, 70 oC, 4 h
87% (从 4 开始)
5
N
H
提示
4
nBuLi是一个金属化试剂。
新戊酰胺基团具有在苯环的金属锂化中有定位效应。
请预测其与金属反应的区域化学?
生成的金属锂化物在第二步反应中作为亲核试剂。
Advanced Organic Chemistry, Chapter 1, Jian Pei, College of Chemistry, Peking University,
解答
Cl
1. PivCl, aq. NaOH, MTBE, 30 oC,
30 分钟, -10 oC, 2 h, 97%
4
NH2
Advanced Organic Chemistry, Jian Pei, College of Chemistry, Peking University,
2
第一章 Efavirenz 的合成 (Merck, DuPont 1999)
F3C Cl
O NO H
Advanced Organic Chemistry, Chapter 1, Jian Pei, College of Chemistry, Peking University,
1. PivCl, aq. NaOH, MTBE, 30 oC,
30 min, -10 oC, 2 h, 97%
NH2 3
4
1. nBuLi, TMEDA, MTBE, -20 → 5 oC, 2 h, 然后
2. CF3CO2Et, -15 oC, 30 min, 然后
中级有机化学第三章习题答案
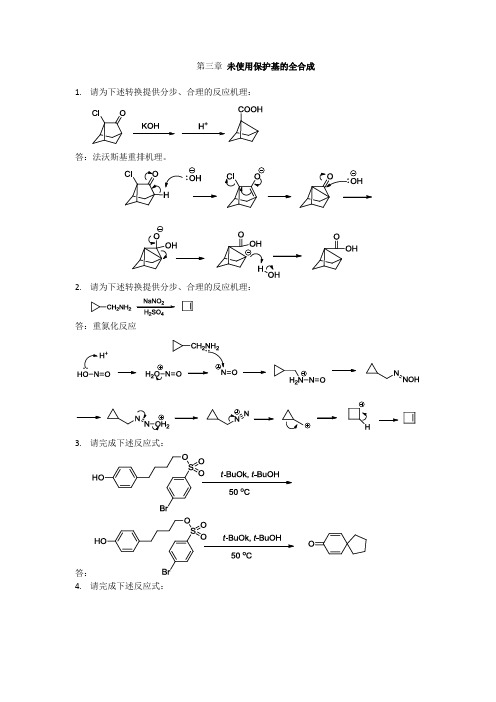
第三章未使用保护基的全合成1.请为下述转换提供分步、合理的反应机理:
答:法沃斯基重排机理。
2.请为下述转换提供分步、合理的反应机理:
答:重氮化反应
3.请完成下述反应式:
答:
4.请完成下述反应式:
答:5.请完成下述反应式:
答:
6.请为下述转换提供分步、合理的反应机理:
答:
7.请完成下述反应式:
答:
8.请为下述转换提供分步、合理的反应机理:
答:请观看问题8的视频讲解。
9.请为下述转换提供分步、合理的反应机理:
答:请观看问题9的视频讲解。
10.请为下述转换提供分步、合理的反应机理:答:。
600004 中级有机化学 作业(专升本)

《中级有机化学》作业一.选择题1.在下列化合物中,偶极矩最大的是( )。
A. B. C. C H C Cl2.根据当代的观点,有机物应该是( ) A. 来自动植物的化合物 B. 来自于自然界的化合物 C. 人工合成的化合物 D. 含碳的化合物3.1828年维勒(F. Wohler )合成尿素时,他用的是( )A. 碳酸铵B. 醋酸铵C. 氰酸铵D. 草酸铵E. 氰化钠 4.有机物的结构特点之一就是多数有机物都以( )。
A. 配价键结合B. 共价键结合C. 离子键结合D. 氢键结合E. 非极性键结合 5.根椐元素化合价,下列分子式正确的是( )A. C 6H 13B. C 5H 9C l2C. C 8H 16OD. C 7H 15OE. C 5H 12N 6.下列共价键中极性最强的是( )A. H-CB. C-OC. H-OD. C-BrE. C-N 7.在烷烃的自由基取代反应中,不同类型的氢被取代活性最大的是( ). A.一级 B. 二级 C. 三级 D.哪个都不是8.氟、氯、溴三种不同的卤素在同种条件下,与某种烷烃发生自由基取代时,对不同氢选择性最高的是( ) A.氟 B. 氯 C. 溴 9.在自由基反应中化学键发生( )A.异裂B. 均裂C. 不断裂D.既不是异裂也不是均裂 10.下列烷烃沸点最低的是( )A.正己烷B.2-甲基戊烷C.3-甲基戊烷D.2,-3二甲基丁烷 A. A >B >C B. A >C >B C. C >B >A D. B >C >A11.在具有同碳原子数的烷烃构造异构体中,最稳定的是 ( )的异构体.C H 3CH 2Cl C H 2CHClA. 支链较多B.支链较少C.无支链 12.下列卤代烃最易发生SN1反应的是( )A. B.C. D.13.下列亲核取代反应不容易发生的是( ). A. B.C.14.一般说来SN2反应的动力学特征是( )。
A. 一级反应B. 二级反应C. 可逆反应D. 二步反应 15.反应物的烃基结构对SN1反应速度影响的主要原因是( )。
北京大学有机化学有机化学考试卷和答案

北京大学化学学院考试专用纸姓名:学号:考试类别: A 卷考试科目:有机化学B 考试日期: 2010, 6, 30 阅卷教师:一、 命名下列化合物 (10分)(1)CH 3CCH 2CH 2CH 2CONH 2(2)(3)CH 32CH 23NCH 2CH 3OClBr4-氯戊酸甲酯 5-氧代己酰胺4-乙基-2-溴吡啶O 2(5)(4)CH 3CCHCH 2OHOH5-硝基-4-溴□恶唑 3,4-二羟基-2-丁酮二、按指定性能排序(10分)(1) 下列化合物酸性的强弱(由强到弱排列)。
c>b>a>d(2) 下列化合物碱性的强弱(由强到弱排列)。
c>b>a>d(3) 以下化合物发生亲电取代反应的速率(由大到小排列)。
b>c>d>a(4) 以下化合物与水发生水解反应的速率(由快到慢排列)。
c>a>d>b(5) 下列化合物的沸点(由高到低排列)。
d>a>b>c三、回答下列问题(15分)(1)画出下列化合物中异戊二烯结构单元,并指出它们各属于哪一类萜。
(A)(B)A:倍半萜,(2) 下图是甾族类天然产物的基本骨架。
其中,A环与B环以顺式或反式方式并联,C环与D环以反式方式并联。
(3) 用箭头指出下列化合物中哪些是缩醛,缩酮,半缩醛,半缩酮的碳原子。
(4) 将下列化合物的Fischer投影式改写成Haworth透视式。
(5) 将苄胺、苄醇及对甲苯酚的混合物分离为三种纯的组分。
CH2OHCH2NH2H3C OH苄胺苄醇对甲苯酚(A)(B)(C)(A)(B)ABBAHClC的钠盐的盐酸盐稀四、完成下列反应,写出主要产物结构(30分)1.2.3.4.5.6.7.8.9.10.11.12.13.14.15.五、化合物鉴别和结构推测(15分) (1) 用化学方法鉴别下列化合物CH 3CHO (A)(B)(C)CH 3CH 2CH 2CHCH 3OH (D)CHOCHO2/NaOH黄色沉淀黄色沉淀无沉淀无沉淀Fehling 试剂红色沉淀无沉淀PhNHNH 2无沉淀沉淀(2) 用化学方法鉴别下列化合物沉淀沉淀NaOH溶解不溶解PhSO 2ClNH 2NHCH 2CH 3CHCOOH COOHNH 2BrBr(A)(B)(C)(D)NaOH溶解不溶解溶解不溶解茚三酮实验,区分(C 和D )(3) 分子式为C 7H 15N 的化合物A ,与过量 CH 3I 反应,再与湿的Ag 2O 加热给出B (C 9H 19N ),B 与过量CH 3I 反应再与湿的Ag 2O 加热给出化合物C (C 7H 12)和三甲胺, C 用臭氧、锌处理可得两分子甲醛和3-氧代戊醛, 请写出化合物A, B ,C 的结构以及各步反应式。
126249-北京大学—中级有机化学-五、电环化反应

氧杂6π电环化
J. A. Porco, Jr. et al. J. Am. Chem. Soc. 2003, 125, 5095.
氧杂6π电环化
J. P. Malerich, D. Trauner. J. Am. Chem. Soc. 2003, 125, 9554.
氧杂6π电环化
J. A. Porco, et. al., J. Am. Chem. Soc, 2011, 133, 9952.
有机合成反应
李昂
中国科学院上海有机化学研究所
生命有机化学国家重点实验室
2014年11月10日
1
有机合成反应
一、概论
五、一些形成C–C键的基本反应
二、基础知识
烯醇和烯醇负离子化学
构象分析
有机锂、镁和铜试剂的制备和反应
有机反应的热力学和动力学 自由基反应
构象对反应活性的影响
烯基化反应
立体电子效应
六、周环反应
6电环化/芳构化
R. J. Huntley, R. L. Funk, Org. Lett. 2006, 15, 3403.
6电环化/芳构化:Xiamycin家族吲哚倍半萜的全合成
Zhanchao Meng, Haixin Yu, Li Li, Wanyin Tao, Hao Chen, Ming Wan, David J. Edmonds, Peng Yang, Jin Zhong, Ang Li, Nature Communications, DOI: 10.1038/ncomms7096.
4π电开环
L. A. Paquette, et al. J. Am. Chem. Soc. 2002, 124, 9199.
中级有机化学试题及答案

中级有机化学试题及答案一、选择题(每题2分,共20分)1. 下列化合物中,哪一个是醇?A. CH3COOHB. CH3OHC. CH3CH2OHD. CH3CH2COCH32. 以下哪种反应属于亲电加成反应?A. 醇的脱水反应B. 卤代烃的水解反应C. 烯烃与卤素的加成反应D. 醛的氧化反应3. 以下哪个化合物是芳香族化合物?A. 环己烷B. 环戊二烯C. 苯D. 环丁烷4. 以下哪种反应是消除反应?A. 醇的脱水生成烯烃B. 醛的还原生成醇C. 酯的水解生成醇和酸D. 卤代烃的水解生成醇5. 以下哪种化合物是烯醇?A. CH2=CH-CH2OHC. CH2=C=CH2D. CH3COCH36. 以下哪种化合物是醛?A. CH3CH2OHB. CH3CHOC. CH3COOHD. CH3CH2COOH7. 以下哪种反应是还原反应?A. 醛的氧化生成酸B. 烯烃的卤化C. 醛的还原生成醇D. 醇的脱水生成烯烃8. 以下哪种化合物是酮?A. CH3OHB. CH3CH2OHC. CH3COCH3D. CH3CH2CHO9. 以下哪种反应是取代反应?A. 卤代烃的水解B. 烯烃的卤化C. 醇的脱水D. 醛的氧化10. 以下哪种化合物是炔烃?A. CH≡CCH3B. CH2=CH2D. CH3CH2CH3答案:1-5 CBDCA 6-10 BBCAD二、填空题(每空2分,共20分)11. 醇的官能团是_________。
12. 芳香族化合物的特征是含有_________个或更多的共轭不饱和碳原子的环状结构。
13. 亲电加成反应中,亲电试剂首先攻击的是_________。
14. 消除反应中,两个相邻原子上的_________被移除,形成不饱和键。
15. 烯醇是一种特殊的_________,它含有一个碳碳双键和一个羟基。
答案:11. -OH 12. 4n+2 13. 不饱和键 14. 氢原子 15. 醇三、简答题(每题10分,共20分)16. 简述什么是亲核取代反应,并给出一个例子。
有机合成工(中级)理论知识试卷及答案

有机合成工(中级)理论知识试卷及答案称名位单名姓号证考准区地职业技能鉴定试题库有机合成工(中级)理论知识试卷注意事项:线1.考试时间:90分钟。
2.按要求在试卷的标封处填写姓名、准考证号和所在单位的名称。
3.仔细阅读各种题目的回答要求,在规定的位置填写您的答案。
4.不要在试卷上乱写乱画,不要在标封区填写无关的内容。
此题号一二总分阅卷人得分过得分评分人超一、判断题:(第1~30题,请将判断结果填入题前的括号中,正确的填“√”,错误的填“X”,每题1分,共30分)1.醇在分子内脱水可以天生醚。
()2.缩聚反应除天生高聚物外,同时还天生小分子物质。
()准3.分子结构中必须有不饱和的价键才能发生加成反应。
()4.化学平衡移动时,平衡常数的值一定随之改变。
()5.实际生产中,采用的传热面积应比计算的传热面积大10%~25%。
()6.画三视图时,左视图和俯视图的关系是宽相等。
()7.空冷器传热管上加翘片,是为了增大传热管的强度。
()不8.浮头式换热器不便于清洗和检修。
()9.进入夏季,工厂应对所有地沟、排水设施进行检查,清除排水障碍。
备足防汛物资,遇到险情满足需求。
()10.饱和蒸汽进一步吸收热量而具有一定过热度称为过热蒸汽。
()题11.气体的密度随温度变革而变革,但不随压强变革而变革。
()12.液体漫衍器的感化是使液体匀称地漫衍在填料上。
()13.筛板塔的主要缺点是操纵弹性小,筛孔简单堵塞。
()14.肯定最相宜回流比的准绳是操纵用度和设备扣头用度之和最小。
()答15.固体催化剂开车便可直接投运。
()16.弹簧管压力计是根据弹性元件的弹性变形和所受压力成正比的原理来工作的,当作用于弹性元件上的被测压力越大时,弹性元件的变形也越大。
()17.检定必须遵守的准绳:必须按国家计量检定系统表举行,必须执行计量检定例程,必生须按企业计量检定系统表进行。
()18.一般管网容量大,喘振振幅就大,频率就低;管网容量小,喘振振幅就小,频率就高。
有机化学课后习题参考答案

《有机化学》习题参考答案引 言这本参考答案是普通高等教育“十二五”规划教材《有机化学》(周莹、赖桂春主编,化学工业出版社出版)中的习题配套的。
我们认为做练习是训练学生各种能力的有效途径之一,是对自己所学内容是否掌握的一种测验。
因此,要求同学们在学习、消化和归纳总结所学相关知识的基础上完成练习,即使有些可能做错也没有关系,只要尽心去做就行,因为本参考答案可为读者完成相关练习后及时核对提供方便,尽管我们的有些参考答案(如合成题、鉴别题)不是唯一的。
北京大学邢其毅教授在他主编的《基础有机化学习题解答与解题示例》一书的前言中写道:“解题有点像解谜,重在思考、推理和分析,一旦揭开了谜底,就难以得到很好的训练。
” 这句话很符合有机化学解题的特点,特摘录下来奉献给同学们。
我们以为,吃透并消化了本参考答案,将会受益匪浅,对于报考研究生的同学,也基本够用。
第一章 绪论1-1解:(1)C 1和C 2的杂化类型由sp 3杂化改变为sp 2杂化;C 3杂化类型不变。
(2)C 1和C 2的杂化类型由sp 杂化改变为sp 3杂化。
(3)C 1和C 2的杂化类型由sp 2杂化改变为sp 3杂化;C 3杂化类型不变。
1-2解:(1) Lewis 酸 H +, R +,R -C +=O ,Br +, AlCl 3, BF 3, Li +这些物质都有空轨道,可以结合孤对电子,是Lewis 酸。
(2)Lewis 碱 x -, RO -, HS -, NH 2, RNH 2, ROH , RSH这些物质都有多于的孤对电子,是Lewis 碱。
1-3解:硫原子个数 n=5734 3.4%6.0832..07⨯=1-4解:甲胺、二甲胺和三甲胺都能与水形成氢键,都能溶于水。
综合考虑烷基的疏水作用,以及能形成氢键的数目(N 原子上H 越多,形成的氢键数目越多),以及空间位阻,三者的溶解性大小为:CH 3NH 2 >(CH 3)2NH >(CH 3)3N1-5解: 32751.4%1412.0Cn ⨯==,327 4.3%141.0H n ⨯==,32712.8%314.0N n ⨯==,3279.8%132.0S n ⨯==, 32714.7%316.0O n ⨯==, 3277.0%123.0Na n ⨯==甲基橙的实验试:C 14H 14N 3SO 3Na 1-6解: CO 2:5.7mg H 2O :2.9mg第二章 有机化合物的分类和命名2-1解:(1) 碳链异构(2)位置异构(3)官能团异构(4)互变异构2-2解:(1) 2,2,5,5-四甲基己烷 (2 ) 2,4-二甲基己烷(3)1-丁烯-3-炔(4)2-甲基-3-氯丁烷(5)2-丁胺(6)1-丙胺(7)(E)-3,4-二甲基-3-己烯(8)(3E,5E)-3-甲基-4,5-二氯-3,5-辛二烯(9)2,5-二甲基-2,4-己二烯(10)甲苯(11)硝基苯(12)苯甲醛(13)1-硝基-3-溴甲苯(14)苯甲酰胺(15)2-氨基-4-溴甲苯(16)2,2,4-三甲基-1-戊醇(17)5-甲基-2-己醇(18)乙醚(19)苯甲醚(20) 甲乙醚 (21) 3-戊酮 (22 ) 3-甲基-戊醛(23)2,4-戊二酮(24)邻苯二甲酸酐(25)苯乙酸甲酯(26)N,N-二甲基苯甲酰胺(27)3-甲基吡咯(28)2-乙基噻吩(29)α-呋喃甲酸(30)4-甲基-吡喃(31)4-乙基-吡喃(32)硬脂酸(33)反-1,3-二氯环己烷(34)顺-1-甲基-2-乙基环戊烷(35)顺-1,2-二甲基环丙烷2-3解:(1)CH3CHCH3CH3CH3CHCH3CH3C(2)CH3CHCH3CH2CH2CH2CH3C2H5(3)CH3CHCH3CHCH2C2CH3C2H525 (4)C2H5HCH3H(5) H2252CH2CH3(6)(7)HCH3HCH3HH(8)3(9)52H5 (10)(11) CH3NO2NO2 (12)H3(13) (14)OHCOOHBr(15) BrCHOCH3CH3 (16)CH3CH2OH(17) OH (18)OH BrBr(19)OHSO3HNO2(20)OO O(21) O(22)O(23)HCH3HCHO(24)H33(25)NHCH3O(26)NH2NH(27)NHO(28)S(29)NCH2H5OCH2H5(30) CH3(CH2)7CH=CH(CH2)7COOH(31)NH2ONH2(32)H2N-CONH-C-NH2(33) OOO(34)OCHO2-4解:(1)C H3CH2CH3CH3CHCH3CH3C命名更正为:2,3,3-三甲基戊烷(2)C H3CH2CHCHCH3CH3CH3(3)(4)(5)(6)(7)(8)2-5解:可能的结构式2-6解:(1)(2)CH3C2H5CH2CH2CH3CH2CH2CH2CH3(3)CH3CH3CH2CH2CH3CH3C2H5C2H5C2H5CH2CH2CH3 2-7解:1,3-戊二烯 1,4-戊二烯H2CH2CH32CH3H31-戊炔 2-戊炔H2C2H5CH3CH CH31,2-戊二烯 2,3-戊二烯H2333-甲基-1,2-丁二烯第三章饱和烃3-1解:(1) 2,3,3,4-二甲基戊烷 (2) 3-甲基-4-异丙基庚烷(3) 3,3-二甲基戊烷 (4) 2,6-二甲基-3,6-二乙基辛烷 (5) 2,5-二甲基庚烷 (6) 2-甲基-3-乙基己烷(7)2-甲基-4-环丙基自己烷(8)1-甲基-3-乙基环戊烷3-2解:(1)H3332CH3(2)(3) H333(4)(5) (6)3-3解:(1) 有误,更正为:3-甲基戊烷(2) 正确(3) 有误,更正为:3-甲基十二烷(4) 有误,更正为:4-异丙基辛烷(5) 4,4-二甲基辛烷(6) 有误,更正为:2,2,4-三甲基己烷3-4解:(3) > (2) > (5) > (1) > (4)3-5解:BrHH HHBr BrHHHHBrBrHHBrHHBrHB rHH(A)对位交叉式 (B)部分重叠式 (C)邻位交叉式 (D)全重叠式A>C>B>D3-6解:(1)相同 (2)构造异构(3)相同(4)相同(5)构造异构体 (6)相同3-7解:由于烷烃氯代是经历自由基历程,而乙基自由基的稳定性大于甲基自由基,故一氯甲烷的含量要比一氯乙烷的含量要少。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一章1-O-Methyllateriflorone的合成
1.请解释以下二个反应的不同点:
2.请为下述转换提供分步、合理的反应机理:
3.请完成下述反应式,写出所有可能的产物,并说明生成主产物的原因。
4.请为下述转换提供分步、合理的反应机理:
提示:[3,3]- 重排后的产物可能形成三元环后开环
5.请完成下述反应式,注意产物的立体化学问题:
6.请为下述转换提供分步、合理的反应机理,并说明主产物去甲基化的原因。
7.请为下述转换提供分步、合理的反应机理:
8.请完成下述反应式:
9.请为下述转换提供分步、合理的反应机理:
10.通常苯酚烯丙基醚在加热下发生Claisen重排后,是否可以接着发生分子内的Diels-Alder反应?
如可以,为什么?如不行,请解释其原因。
11.请为以下的转换提出二种可能的反应机理, 并请设计可以区分你所提出的二种机理的实验方法。
12.请画出下述反应的可能中间体结构,请判断此中间体在加热下可能形成的最终产物,并解释其原因:
,接着D-A反应和cope重排
13.请为下述转换提供分步、合理的反应机理:
14.本章学习的重点:
1)在苯环上引入酚羟基的方法;
2)酚羟基的保护以及酚醚的合成方法
3)Claisen重排反应,以及如何如何将claisen重排后的产物与Diels-Alder反应串联一起。
