一轮复习--晶体结构与性质
高三化学一轮复习——晶体结构与性质一

第34讲 晶体结构与性质(一)【考纲要求】1、理解离子键的形成,能根据离子化合物的结构特征解释其物理性质。
2、了解原子晶体的特征,能描述金刚石、二氧化硅等原子晶体的结构与性质的关系。
3、理解金属键的含义,能用金属键理论解释金属的一些物理性质。
4、了解化学键和分子间作用力的区别。
5、了解氢键的存在对物质性质的影响,能列举含有氢键的物质。
6、了解分子晶体与原子晶体、离子晶体、金属晶体的结构微粒、微粒间作用力的区别。
7、了解简单配合物的成键情况。
【课前预习区】一、认识晶体1、晶体的定义:微观粒子在空间按一定规律做周期性重复排列构成的固体物质2、晶体的特性:(1)有规则的几何外形(自范性:在适宜的条件下,晶体能够自发的呈现封闭的、规则的多面体外形。
) (2)有确定的熔点(3)各向异性:在不同的方向上表现不同的性质 (4)具有特定的对称性3、晶体是由晶胞堆积得到的,故晶胞就能反映整个晶体的组成。
利用晶胞可以求化学式——均摊法。
均摊法是指每个晶胞平均拥有的粒子数目。
若某个粒子为N 个晶胞所共有,则该粒子有1/N 属于此晶胞。
以正方体晶胞为例,晶胞中不同位置的粒子对晶胞的贡献为:顶点原子_______属于此晶胞 棱上原子_______属于此晶胞面上原子_______属于此晶胞 体内原子完全属于此晶胞若晶胞为六棱柱,则顶点原子有________属于此晶胞,棱上有________属于此晶胞。
练习、硼镁化合物刷新了金属化合物超导温度的最高记录。
该化合物晶体结构中的重复结构单元如图所示。
十二个镁原子间形成正六棱柱,两个镁原子分别在棱柱上底、下底的中心;六个硼原子位于棱柱内。
则该化合物的化学式可表示为( ) A 、Mg 14B 6 B 、MgB 2 C 、Mg 5B 12 D 、Mg 3B 2二、晶体结构1、金属晶体(1)金属键:_____________________________________________________________成键微粒:________________________特征: 影响金属键强弱因素及对金属性质的影响:(2)金属晶体:(3)金属晶体物理性质的解释● ○ BMg2、离子晶体(1)离子键:____________________________________________________________ 成键微粒:_________________ 特征:____________________________影响离子键强弱因素:(2)离子晶体定义:(3)晶格能:①影响因素②与离子晶体性质的关系:晶格能越大,形成的离子晶体越,且熔点越,硬度越。
2024版新教材高考化学全程一轮总复习课时作业17晶体结构与性质

课时作业17 晶体结构与性质一、选择题(每小题只有1个选项符合题意)1.下列说法不正确的是()A.Na2O中离子键的百分数为62%,则Na2O不是纯粹的离子晶体,是离子晶体与共价晶体之间的过渡晶体B.Na2O通常当作离子晶体来处理,因为Na2O是偏向离子晶体的过渡晶体,在许多性质上与纯粹的离子晶体接近C.Al2O3是偏向离子晶体的过渡晶体,当作离子晶体来处理;SiO2是偏向共价晶体的过渡晶体,当作共价晶体来处理D.分子晶体、共价晶体、金属晶体和离子晶体都有过渡型2.化合物形成的晶体结构多种多样。
如图所示的几种结构所表示的物质最有可能是分子晶体的是()A.①④B.②③C.①②D.④⑤3.美国LawreceLiermore国家实验室成功地在高压下将CO2转化为具有类似SiO2结构的共价晶体,下列关于CO2的共价晶体说法,正确的是()A.CO2的共价晶体和分子晶体互为同分异构体B.在一定条件下,CO2共价晶体转化为CO2分子晶体是物理变化C.CO2的共价晶体和CO2分子晶体具有相同的物理性质和化学性质D.在CO2的共价晶体中,每一个C原子结合4个O原子,每一个O原子跟两个C原子相结合4.铁有δ、γ、α三种同素异形体,如下图所示,三种晶体在不同温度下能发生转化。
下列说法不正确的是()A.将铁加热到1500℃分别急速冷却和缓慢冷却,得到的晶体类型相同B.αFe晶体中与每个铁原子等距离且最近的铁原子有6个C.若δFe晶胞边长为a cm,αFe晶胞边长为b cm,则两种晶体密度比为2b3∶a3 D.δFe晶体中与每个铁原子等距离且最近的铁原子有8个5.我国科学家合成了富集11B的非碳导热材料立方氮化硼晶体,晶胞结构如图。
下列说法正确的是()A.11BN和10BN的性质无差异B.该晶体具有良好的导电性C.该晶胞中含有14个B原子,4个N原子D.N原子周围等距且最近的N原子数为126.硫化锂是目前正在开发的锂离子电池的新型固体电解质,为立方晶系晶体。
2022届高三化学一轮复习考点特训晶体结构与性质含解析

晶体结构与性质一、选择题(共17题)1.北京大学和中国科学院的化学工作者已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子晶体,具有良好的超导性。
下列有关分析正确的是A.K3C60中只有离子键B.K3C60中碳元素显-3价C.该晶体在熔融状态下能导电D.C60与12C互为同素异形体2.下列关于氯化钠晶胞(如图)的说法正确的是()A.每个晶胞含有6个Na+和6个Cl-B.晶体中每个Na+周围有8个Cl-,每个Cl-周围有8个Na+C.晶体中与每个Na+最近的Na+有8个D.将晶胞沿体对角线AB作投影,CD两原子的投影将相互重合3.元素X的某价态离子X n+中所有电子正好充满K、L、M三个电子层,它与N3-形成晶体的晶胞结构如图所示。
下列说法错误的是()A.X元素的原子序数是19B.该晶体中阳离子与阴离子个数比为3∶1C.X n+中n=1D.晶体中每个X n+周围有2个等距离且最近的N3-4.元素X位于第4周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2;元素Y 基态原子的3p轨道上有1对成对电子。
X与Y形成的化合物的晶胞结构如图所示,下列关于该晶体的说法正确的是()A.该晶体属于原子晶体B.X2+的配位数为8,Y2-的配位数为4C.与每个Y2-距离最近且相等的Y2-共有12个D.该晶体的熔点比氧化锌高5.已知某离子晶体的晶胞示意图如图所示,其摩尔质量为Mg/mol,阿伏加德罗常数的值为N A,晶体的密度为dg/cm3下列说法中正确的是A.晶体晶胞中阴、阳离子的个数都为1B.晶体中阴、阳离子的配位数都是4C.该晶胞可能是NaCl的晶胞D.该晶体中两个距离最近的阳离子的核间距为4M/(N A d)cm6.CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中含有的哑铃形C22-的存在,使晶胞沿一个方向拉长(该晶胞为长方体)。
下列关于CaC2晶体的说法中正确的是()A.1个Ca2+周围距离最近且等距离的C22-数目为6B.6.4gCaC2晶体中含阴离子0.1molC.该晶体中存在离子键和共价键D.与每个Ca2+距离相等且最近的Ca2+共有12个7.下列各组晶体物质中,化学键类型相同,晶体类型也相同的是()①SiO2和SO3 ②晶体硼和HCl ③CO2和SO2④晶体硅和金刚石⑤晶体氖和Si3N4 ⑥硫黄和碘A.①②③B.④⑤⑥C.③④⑥D.①③⑤8.下列对一些实验事实的理论解释正确的是()选项实验事实理论解释A 氮原子的第一电离能大于氧原子氮原子 2p 能级原子轨道半充满B SO2为 V 形分子SO2分子中 S 原子采用 sp3杂化C 金刚石的熔点低于石墨金刚石是分子晶体,石墨是原子晶体D HF 的稳定性大于 HCl HF 分子间能形成氢键9.下列各组性质的比较中正确的是()A.离子半径:Na+>Mg2+>Al3+>F-B.酸性:HClO4<H2SO4<H3PO4C.稳定性:HF>HCl>PH3>H2SD.熔点:Na−K合金<Na<氯化钠<金刚石10.铁有如下δ、γ、α三种晶体结构,三种晶体在不同温度下能发生转化。
2024-2025学年高考化学一轮复习专题卷: 晶体结构与性质(含解析)

2025届高考化学一轮复习专题卷: 晶体结构与性质一、单选题1.下列推论正确的( )A.的沸点高于,可推测的沸点高于B.为正四面体结构,可推测出也为正四面体结构C.晶体是分子晶体,可推测晶体也是分子晶体,D.是碳链为直线型的非极性分子,可推测也是碳链为直线型的非极性分子2.有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( )A.①为简单立方堆积②为六方最密堆积③为体心立方堆积④为面心立方最密堆积B.每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个C.晶胞中原子的配位数分别为:①6,②8,③8,④12D.空间利用率的大小关系为:①<②<③<④3.下列叙述错误的是( )A.金属键无方向性和饱和性,原子配位数较高B.晶体尽量采取紧密堆积方式,以使其变得比较稳定C.因共价键有饱和性和方向性,所以原子晶体不遵循“紧密堆积”原理D.金属铜和镁均以ABAB…方式堆积4.环六糊精(D-吡喃葡萄糖缩合物)具有空腔结构,腔内极性较小,腔外极性较大,可包合某些分子形成超分子。
图1、图2和图3分别表示环六糊精结构、超分子示意图及相关应用。
下列说法错误的是( )4SiH 4CH 3PH 3NH 4NH +4PH +2CO 2SiO 26C H 38C HA.环六糊精属于寡糖B.非极性分子均可被环六糊精包合形成超分子C.图2中甲氧基对位暴露在反应环境中D.可用萃取法分离环六糊精和氯代苯甲醚5.下列反应的离子方程式正确的是( )A.去除废水中的:B.过氧化钠在潜水艇中作为的来源:C.沉淀溶于氨水:D.在溶液中滴加少量溶液:6.碳硼烷酸是一类超强酸,也是唯一能质子化富勒烯(如)但不会将其分解的酸,2Na S 2Hg +2+2-Hg +S HgS ↓2O 22222O 2H O 4OH O --++↑AgCl ()332AgCl 2NH Ag NH Cl⎡⎤+⎣⎦NaOH ()442NH AlSO ()34Al 4OHAl OH -+-⎡⎤+⎣⎦60C其结构如图所示。
2024届高考化学一轮复习:晶体结构与性质
第57讲晶体结构与性质[课程标准]1.了解晶体的类型,了解不同类型晶体中结构微粒、微粒间作用力的区别。
2.了解分子晶体、共价晶体、离子晶体、金属晶体结构与性质的关系。
3.了解晶胞的概念,能根据晶胞确定晶体的组成并进行相关的计算。
考点一晶体与晶胞1.晶体与非晶体晶体非晶体结构特征结构微粒周期性有序排列结构微粒无序排列性质特征自范性有无熔点固定不固定异同表现各向异性各向同性二者区别方法间接方法看是否有固定的熔点科学方法对固体进行X射线衍射实验2.获得晶体的三条途径(1)熔融态物质凝固。
(2)气态物质冷却不经液态直接凝固(凝华)。
(3)溶质从溶液中析出。
3.晶胞(1)晶胞:晶胞是描述晶体结构的基本单元。
(2)晶体中晶胞的排列——无隙并置①无隙:相邻晶胞之间没有任何间隙。
②并置:所有晶胞平行排列、取向相同。
(3)晶胞中粒子数目的计算——均摊法如某个粒子为n 个晶胞所共有,则该粒子有1/n 属于这个晶胞。
[正误辨析](1)冰和碘晶体中相互作用力相同()(2)凡有规则外形的固体一定是晶体()(3)固体SiO 2一定是晶体()(4)缺角的NaCl 晶体在饱和NaCl 溶液中会慢慢变为完美的立方体块()(5)晶胞是晶体中最小的“平行六面体”()(6)区分晶体和非晶体最可靠的方法是对固体进行X射线衍射实验()答案:(1)×(2)×(3)×(4)√(5)×(6)√1.如图是由Q 、R 、G 三种元素组成的一种高温超导体的晶胞结构,其中R 为+2价,G 为-2价,则Q 的化合价为。
解析:•R :8×18+1=2G :8×14+8×14+4×12+2=8●Q :8×14+2=4R 、G 、Q 的个数之比为1∶4∶2,则其化学式为RQ 2G 4。
由于R 为+2价,G 为-2价,所以Q 为+3价。
答案:+32.某晶体的一部分如图所示,这种晶体中A 、B 、C 三种粒子数之比是()A .3∶9∶4B .1∶4∶2C .2∶9∶4D .3∶8∶4B[A 粒子数为6×112=12;B 粒子数为6×14+3×16=2;C 粒子数为1;故A 、B 、C 粒子数之比为1∶4∶2。
2022版高考化学一轮复习专题九晶体结构与性质专题综合检测含解析

高考化学一轮复习:专题九晶体结构与性质【3年模拟】时间:40分钟分值:60分一、选择题(每题2分,共12分)1.(2020天津等级考适应性测试,2)下列可用于判断某物质为晶体的方法是( )A.质谱法B.红外光谱法C.核磁共振法D.X-射线衍射法答案 D A项,质谱法用于测定有机物的相对分子质量,不能用于判断某物质是否为晶体,错误;B项,红外光谱仪能测定有机物中的官能团和化学键类型,不能用于判断某物质是否为晶体,错误;C项,核磁共振法不能用于判断某物质是否为晶体,错误;D项,晶体与非晶体最本质的区别是组成物质的粒子在微观空间是否有序排列,X-射线衍射可以看到微观结构,可用X-射线衍射法鉴别晶体与非晶体,正确。
2.(2020烟台上学期期末,2)下列关于晶体的叙述正确的是( )A.晶体中只要有阳离子就一定有阴离子B.区分晶体和非晶体最可靠的方法是对固体进行X射线衍射实验C.分子晶体中共价键键能越大熔点和沸点越高D.金属晶体发生形变时,内部金属离子与“自由电子”的相互作用消失答案 B 金属晶体是由金属阳离子和自由电子构成的,所以晶体中有阳离子不一定存在阴离子,故A错误;区分晶体和非晶体的最可靠的科学方法是对固体进行X-射线衍射实验,故B 正确;分子晶体熔点和沸点与分子间作用力有关,与共价键键能无关,故C错误;金属晶体发生形变时其内部金属离子与“自由电子”发生滑动,但金属离子和自由电子之间的相互作用仍然存在,故D错误。
3.有关晶体的结构如下图所示,下列说法中不正确的是 ( )A.在图A 晶体中,距粒子B 最近且相等的粒子A 有6个B.在CO 2晶体中,每个晶胞平均占有4个原子C.在金刚石晶体中,碳原子与碳碳键个数比为1∶2D.该气态团簇分子的分子式为E 4F 4答案 B 图A 晶体中,粒子B 在棱上和体心,粒子A 位于顶点和面心,距粒子B 最近且相等的粒子A 有6个,A 项正确;在CO 2晶体中,CO 2分子位于顶点和面心,一个晶胞平均占有4个CO 2分子,共12个原子,B 项错误;在金刚石晶体中,每个碳原子形成4个碳碳键,每个碳碳键由两个C 原子形成,因此碳原子与碳碳键个数比为1∶2,C 项正确;D 图中是气态团簇分子不是晶胞,不用均摊法计算,分子式为E 4F 4,D 项正确。
高考化学一轮复习晶体的结构与性质专项训练知识点及练习题含答案
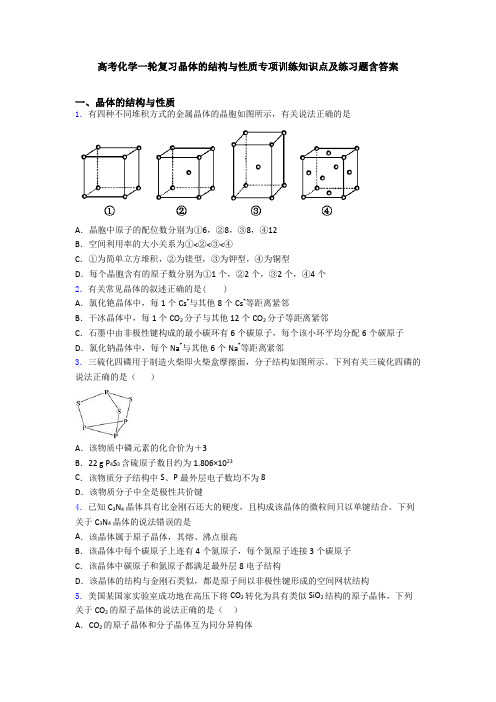
高考化学一轮复习晶体的结构与性质专项训练知识点及练习题含答案一、晶体的结构与性质1.有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是A.晶胞中原子的配位数分别为①6,②8,③8,④12B.空间利用率的大小关系为①<②<③<④C.①为简单立方堆积,②为镁型,③为钾型,④为铜型D.每个晶胞含有的原子数分别为①1个,②2个,③2个,④4个2.有关常见晶体的叙述正确的是( )A.氯化铯晶体中,每1个Cs+与其他8个Cs+等距离紧邻B.干冰晶体中,每1个CO2分子与其他12个CO2分子等距离紧邻C.石墨中由非极性键构成的最小碳环有6个碳原子,每个该小环平均分配6个碳原子D.氯化钠晶体中,每个Na+与其他6个Na+等距离紧邻3.三硫化四磷用于制造火柴即火柴盒摩擦面,分子结构如图所示。
下列有关三硫化四磷的说法正确的是()A.该物质中磷元素的化合价为+3B.22 g P4S3含硫原子数目约为1.806×1023C.该物质分子结构中S、P最外层电子数均不为8D.该物质分子中全是极性共价键4.已知C3N4晶体具有比金刚石还大的硬度,且构成该晶体的微粒间只以单键结合。
下列关于C3N4晶体的说法错误的是A.该晶体属于原子晶体,其熔、沸点很高B.该晶体中每个碳原子上连有4个氮原子,每个氮原子连接3个碳原子C.该晶体中碳原子和氮原子都满足最外层8电子结构D.该晶体的结构与金刚石类似,都是原子间以非极性键形成的空间网状结构5.美国某国家实验室成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,下列关于CO2的原子晶体的说法正确的是()A.CO2的原子晶体和分子晶体互为同分异构体B.在一定条件下,CO2的原子晶体转化为分子晶体是物理变化C.CO2的原子晶体和分子晶体具有相同的物理性质D.在CO2的原子晶体中,每个C原子周围结合4个O原子,每个O原子与2个碳原子结合6.下列叙述正确的是A.离子晶体中,只存在离子健,不可能存在其它化学键B.可燃冰中甲烷分子与水分子之间存在氢键C.Na2O2、NaHSO4晶体中的阴、阳离子个数比均为12D.晶体熔点:金刚石>食盐>冰>干冰7.氟在自然界中常以CaF2的形式存在。
2024届高考一轮复习化学课件:晶体结构与性质

2
考向2 计算晶体的密度和粒子之间的距离
例2.(2023辽宁六校协作体联考)氮化钼作为锂离子电池负极材料具有很好
的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方晶格的
八面体空隙中,晶胞结构如图所示,其中氮化钼晶胞参数为a nm,NA为阿伏
加德罗常数的值。下列说法正确的是( D )
A.氮化钼的化学式为 MoN2
磁元件的制作。其晶胞结构如图所示,已知晶胞参数为a pm,下列说法不正
确的是(
)
A.磷锡青铜的化学式为Cu3SnP
B.该晶胞中与Cu原子等距离且最近的Sn原子有4个
C.三种元素Cu、Sn、P在元素周期表中分别处于d区、p区、p区
D.Sn 和 P
√3
原子间的最短距离为 a
2
pm
答案 C
解析 由均摊法可知,晶胞中 Cu 原子数目为
的数目。
对点训练
1.(2023湖北十堰模拟)Mg2Si具有反萤石结构,晶胞结构如图所示,其晶胞参
数为a nm,NA为阿伏加德罗常数的值。下列叙述正确的是(
A.电负性:Mg>Si
B.Mg核外电子有3种不同的运动状态
C.Mg 与 Si
√3
之间的最近距离为 4 a
D.Mg2Si 的密度计算式为
nm
76
A ×(×10-7 )3
拥有的碳原子个数为2,碳原子采取的杂化方式是sp2。
易错辨析
(1)离子晶体由阴、阳离子构成,故晶体中只要有阳离子必定有阴离子。
(
×
)
(2)金属晶体能够导电是由于金属在外加电场作用下发生电离,产生电子。
(
×
)
(3)CO2由分子晶体转变为共价晶体,碳原子的杂化方式发生了变化。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
③镁型和铜型。
钾 型堆积方式堆积。若按__________ ABABAB 密置层的原子按____ 镁 型,按______________ ABCABCABC 的方式堆积为____ 铜 的方式堆积为____ 最密堆积 ,配位数 型。这两种堆积方式都是金属晶体的___________ 74% 。 均为12,空间利用率均为________
2.晶格能 (1)定义
气态离子 形成1摩尔离子晶体______ 释放 的能量,单位 __________ 正 值。 kJ/mol ,通常取_____ ________
第三讲
晶体结构与性质
复习课
考纲展示
1.了解原子晶体的特征,能描述金刚石、二氧 化硅等原子晶体的结构与性质的关系。 2.了解分子晶体与原子晶体、离子晶体、金属 晶体的构成粒子及粒子间作用力的区别。 3.理解金属键的含义,能用金属键理论解释金 属的一些物理性质。
热点关注 1.晶体与非晶体的区别,晶体中粒子的空间堆 积方式,晶胞的结构特点及其应用。
(4)区别晶体和非晶体的方法
晶体 的熔点较固定,而________ 非晶体 没有固定 ①熔点法:______
的熔点。
X-射线衍射法 :当单一波长的X-射线通过晶 ②_________________
分立的斑点或谱线 ,而非晶体 体时,会在记录仪上看到____________________
则没有。
(2)三维空间模型 ①简单立方堆积。 相邻非密置层原子的原子核在同一直线上,配位数为
Po 采取这种堆积方式。 _____ 6 。只有____
②钾型。 将非密置层上层金属原子填入下层的金属原子形成的
凹穴 _____ 中,每层都照此堆积。如____________ Na、K、Fe 等是这种堆积
方式,配位数为____ 8 。
2.晶胞 (1)概念
基本单元 。 描述晶体结构的_____________
(2)晶体中晶胞的排列——无隙并置
任何间隙 。 ①无隙:相邻晶胞之间没有__________ 平行 排列、_______ 取向 相同。 ②并置:所有晶胞_______
二、分子晶体和原子晶体 1.分子晶体 (1)结构特点
分子 。 ①晶体中只含______
金属阳 离子、 金属 自由电 子 键
由电子在热 __的 作用下与金属 原子频繁碰撞 ________ 而导热
,而弥漫在金属原子间的电子 气可以起到类似轴承中滚珠之
润滑剂 的作用 间________
形成电流
2.金属晶体的原子堆积模型 (1)二维空间模型
4 。 ①非密置层,配位数为____ 6。 ②密置层,配位数为___
(3)晶体的特点
高度有序 性。 ①外形和内部质点排列的_________
②晶体的许多物理性质(如强度)表现出_______ 各向异 性。
自范 性,即晶体能自发地呈现几何多面体 ③晶体具有_____ ___________
的性质。
(2)得到晶体的途径 ①熔融态物质凝固。 ②气态物质不经液态直接凝固。 ③溶质从溶液中析出。
氢键 。 范德华力,也可能有______ ②分子间作用力为_________
③分子密堆积。
(2)典型的分子晶体 ①冰
氢键,也存在_________ 范德华力, 水分子之间的主要作用力是_____ 4 个紧邻的水分子。 每个水分子周围只有____
②干冰 CO2分子之间存在_________,每个CO2分子周围有___ 个紧邻的CO2分子。
形成的一种“巨分子”。
差别很大 。 ③金属键的强度__________
(2)金属晶体的构成、通性及其ቤተ መጻሕፍቲ ባይዱ释。
金属晶 作用 体结构 力名 微粒 称 电子气中的自 自由电子在 电场中作
定向运动 _________
导电性
导热性
延展性
当金属受到外力作用时,金属
相对滑动 晶体中的各原子层就会 ______ 体系的排列方式 ,但不会改变其 ____________
而成的晶体。
(2)决定离子晶体结构的因素 ①几何因素:即晶体中正负离子的半径比决定晶体结 构。
电荷不同,配位数必然不同 ②电荷因素,即正负离子________________________ 。
纯粹程度 。 ③键性因素:离子键的__________
(3)一般物理性质。
熔 点和____ 沸 点,较大 一般地说,离子晶体具有较高的____ 硬度 、难于______ 压缩 。这些性质都是因为离子晶体中存在 的______ 较强的离子键。若要破坏这种作用需要____________ 较高的能量 。 着____________
2.晶胞中粒子个数及边长等的计算。
3.晶体类型与性质之间的关系。
4.晶体类型与粒子间作用力的关系。
5.四类晶体的特征及代表物质。
一、晶体的常识 1.晶体与非晶体 (1)晶体与非晶体的区别 分类 晶体 非晶体 是否有自范 性 有 没有 微观结构 原子在三维空间里呈__________ 周期性有序 排列 原子排列相对______ 无序
范德华力 12
2.原子晶体 (1)结构特点 ①晶体中只含原子。
共价键 结合。 ②原子间以__________ 三维空间网状 结构。 ③______________
(2)典型的原子晶体——金刚石
3 sp ①碳原子来取_____杂化轨道形成共价键,碳碳键之间
109° 28′ 夹角为________ 。 4 个碳原子结合。 ②每个碳原子与相邻的___
四、离子晶体 1.离子晶体 (1)概念
阴、阳离子间通过_________( 静电作用 指_________ 相互排斥 ①离子键:___________ 相互吸引 的平衡)形成的化学键。 和__________
离子键 结合 阳离子和阴离子 通过_______ ②离子晶体:由__________________
三、金属晶体 1.金属键 (1)“电子气理论”要点。
价电子 ①该理论把金属键描述为金属原子脱落下来的_______ 整块晶体 的“电子气”,被_________ 形成遍布_________ 所有原子 所共用,从 所有金属原子 维系在一起。 而把______________
金属阳离子、自由电子 通过________ ②金属晶体是由_____________________ 金属键
