晶体结构与性质知识要点归纳
晶体结构与性质知识点总结大一

晶体结构与性质知识点总结大一晶体结构与性质知识点总结晶体是由具有一定规则排列方式的原子、离子或分子组成的固体物质,拥有特定的结构和性质。
晶体结构与性质是材料科学与化学领域的重要基础知识,对于理解和研究材料的性质、制备工艺以及应用具有重要意义。
本文将对晶体结构与性质的相关知识点进行总结。
一、晶体结构1. 空间点阵:晶体的基本结构单位是晶胞,晶胞在空间的无限重复构成空间点阵。
六种常见的空间点阵包括:立方点阵、四方点阵、正交点阵、六方点阵、单斜点阵和三斜点阵。
2. 晶体的晶格参数:晶体的晶格参数是对晶格进行定量描述的基本参数,包括晶格常数、晶胞参数和晶胞角度。
晶格常数是指晶胞的尺寸,晶胞参数是指晶体中原子间距的大小,晶胞角度则描述了晶体中原子间的排列方式。
3. 晶体的晶系:根据晶体的对称性,可以将晶体分为七个晶系,分别为立方晶系、四方晶系、正交晶系、六方晶系、三斜晶系、单斜晶系和菱面晶系。
每个晶系都具有特定的组成、结构和性质。
4. 晶体结构类型:根据晶体结构的特征,可以将晶体分为离子晶体、共价晶体、金属晶体和分子晶体等。
各类晶体的结构特点不同,从而决定了它们的性质和用途。
5. 点阵缺陷:晶体中可能存在的点阵缺陷包括空位、层错、插入固溶体和间隙固溶体等。
这些点阵缺陷对晶体的导电性、热导率和力学性能等起着重要的影响。
二、晶体性质1. 光学性质:晶体在光的照射下表现出特定的光学性质,包括吸收、折射、散射和双折射等。
不同晶体的光学性质可用于光学器件、光纤通信和激光技术等领域。
2. 电学性质:晶体的电学性质与晶体结构和成分密切相关。
离子晶体具有良好的导电性,而共价晶体和分子晶体通常是绝缘体或半导体。
晶体的电导率、电介质性能和电子输运性质等是电学性质的重要指标。
3. 磁学性质:晶体的磁学性质与晶体结构和电子自旋有关。
常见的磁性晶体包括铁磁体、反铁磁体和顺磁体等。
磁性晶体在磁记录、磁存储和磁共振成像等方面具有广泛应用。
晶体结构与性质知识点

第三章晶体构造与性质第一节晶体的常识【知识点梳理】一、晶体与非晶体1、晶体与非晶体① 晶体:是内部微粒〔原子、离子或分子〕在空间按一定规律做周期性重复排列构成的物质。
② 非晶体:是内部的原子或分子的排列呈杂乱无章的分布状态的物质。
2、晶体的特征〔1〕晶体的根本性质晶体的根本性质是由晶体的周期性构造决定的。
① 自范性:a.晶体的自范性即晶体能自发的呈现多面体外形的性质。
b.“自发〞过程的实现,需要一定的条件。
晶体呈现自范性的条件之一是晶体生长的速率适当。
② 均一性:指晶体的化学组成、密度等性质在晶体中各局部都是一样的。
③ 各向异性:同一晶体构造中,在不同方向上质点排列一般是不一样的,因此,晶体的性质也随方向的不同而有所差异。
④ 对称性:晶体的外形与内部构造都具有特有的对称性。
在外形上,常有相等的对称性。
这种一样的性质在不同的方向或位置上做有规律的重复,这就是对称性。
晶体的格子构造本身就是质点重复规律的表达。
⑤ 最小内能:在一样的热力学条件下,晶体与同种物质非晶体固体、液体、气体相比拟,其内能最小。
⑥ 稳定性:晶体由于有最小内能,因而结晶状态是一个相对稳定的状态。
⑦ 有确定的熔点:给晶体加热,当温度升高到某温度便立即熔化。
⑧ 能使X射线产生衍射:当入射光的波长与光栅隙缝大小相当时,能产生光的衍射现象。
X射线的波长与晶体构造的周期大小相近,所以晶体是个理想的光栅,它能使X射线产生衍射。
利用这种性质人们建立了测定晶体构造的重要试验方法。
非晶体物质没有周期性构造,不能使X射线产生衍射,只有散射效应。
〔2〕晶体SiO2与非晶体SiO2的区别① 晶体SiO2有规那么的几何外形,而非晶体SiO2无规那么的几何外形。
② 晶体SiO2的外形与内部质点的排列高度有序,而非晶体SiO2内部质点排列无序。
③ 晶体SiO2具有固定的熔沸点,而非晶体SiO2无固定的熔沸点。
④ 晶体SiO2能使X射线产生衍射,而非晶体SiO2没有周期性构造,不能使X射线产生衍射,只有散射效应。
晶体结构与性质知识总结

晶体结构与性质知识总结晶体是由原子、离子或分子组成的固体,它们按照一定的规则排列而形成的,在空间上具有周期性的结构。
晶体的结构与性质密切相关,下面对晶体的结构和性质进行总结。
一、晶体的结构:1.晶体的基本单位:晶体的基本单位是晶胞,它是晶格的最小重复单位。
晶胞可以是点状(原子)、离子状(离子)或分子状(分子)。
2.晶格:晶格是一种理想的周期性无限延伸的结构,它由晶胞重复堆积而成。
晶格可以通过指标来描述,如立方晶系的简单立方晶格用(100)、(010)和(001)来表示。
3.晶系:晶体按照对称性的不同可以分为立方系、四方系、正交系、单斜系、菱面系、三斜系和六角系等七个晶系。
4.点阵:点阵是晶胞中原子、离子或分子的空间排列方式。
常用的点阵有简单立方点阵、体心立方点阵和面心立方点阵。
5.晶体的常见缺陷:晶体中常见的缺陷有点缺陷、线缺陷和面缺陷。
点缺陷包括空位、间隙原子和杂质原子等;线缺陷包括晶体的位错和附加平面等;面缺陷包括晶体的晶界、孪晶和堆垛疏松等。
二、晶体的性质:1.晶体的光学性质:晶体对光有吸收、透射和反射等作用,这取决于晶格结构和晶胞的对称性。
晶体在光学显微镜下观察时,有明亮的晶体颗粒。
2.晶体的热学性质:晶体的热学性质主要包括热容、热传导和热膨胀等。
晶体的热传导性能与晶胞的结构和相互作用有关,不同晶体的热传导性能差异很大。
3.晶体的电学性质:晶体的导电能力与晶体的结构和化学成分密切相关。
一些晶体可以具有金属导电性,例如铜、银和金等;而其他晶体可以具有半导体或绝缘体导电性。
4.晶体的力学性质:晶体的力学性质涉及到晶体的刚性、弹性和塑性等。
晶体在受力作用下可能发生形变,这取决于晶格的结构和原子、离子或分子之间的相互作用力。
5.晶体的化学性质:晶体的化学性质取决于晶体的成分和结构。
晶体可能与其他物质发生化学反应,形成新的物质。
晶体的化学性质对其功能和应用具有重要影响。
综上所述,晶体的结构与性质密切相关。
晶体相关知识点总结

晶体相关知识点总结一、基本概念1. 晶体的定义晶体是由原子、离子或分子按照一定的规则排列而形成的固体结构。
晶体具有高度有序性,具有一定的周期性和对称性。
晶体是凝聚态物质的一种主要形式,占据了固态物质的绝大部分。
2. 晶体的种类根据晶体结构的不同,晶体可以分为离子晶体、共价晶体、金属晶体和分子晶体等几种基本类型。
不同类型的晶体具有不同的物理性质和化学性质。
3. 晶体的分类根据晶体的外部形态,晶体可以分为单斜晶、正交晶、菱形晶、六方晶、四方晶、立方晶等几种基本类型。
不同类型的晶体具有不同的外部形态和对称性。
二、晶体结构1. 晶体的晶体结构晶体结构是指晶体中原子、离子或分子的排列方式和规律。
晶体结构可以分为周期性结构和非周期性结构两种形式。
周期性结构是指晶体中原子、离子或分子的排列具有一定的周期性,具有明显的晶格和对称性。
非周期性结构是指晶体中原子、离子或分子的排列没有明显的周期性,没有规则的晶格和对称性。
2. 晶体的晶格晶体的晶格是指晶体中原子、离子或分子所构成的三维空间排列的规则结构。
晶格可以分为周期性晶格和非周期性晶格两种类型。
周期性晶格是指晶格具有明显的周期性,有规则的排列和对称性。
非周期性晶格是指晶格没有明显的周期性,没有规则的排列和对称性。
3. 晶体的晶胞晶胞是指晶体中最小的具有完整晶体结构的基本单位。
晶胞可以分为原胞和扩展晶胞两种类型。
原胞是指晶体中最小的具有完整晶体结构的基本单位,包含了一个或多个原子、离子或分子。
扩展晶胞是指原胞在晶体结构中的重复排列,是构成晶体的基本单位。
三、晶体的生长1. 晶体生长的基本过程晶体生长是指在溶液、熔体或气相中,原子、离子或分子从溶液中萃取并在已生成的晶体上沉积,形成新晶体的过程。
晶体生长的基本过程包括成核、生长和成形几个阶段,成核是指溶液中原子、离子或分子聚集形成晶体的核心;生长是指晶体核心上原子、离子或分子的进一步沉积和排列生长;成形是指晶体的表面形态和结晶过程。
知识清单16 晶体结构与性质(教师版) 2025年高考化学一轮复习知识清单
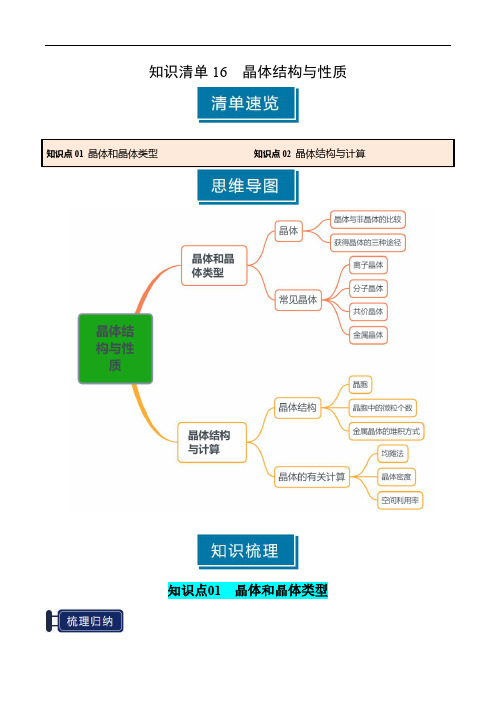
知识清单16晶体结构与性质知识点01晶体和晶体类型一、晶体1.晶体与非晶体的比较比较晶体非晶体结构特征结构微粒(原子、离子或分子)在三维空间里呈_周期性有序__排列结构微粒(原子、离子或分子)_无序__排列性质特征自范性_有___无__熔点_固定___不固定__异同表现_各向异性___无各向异性__实例水、NaCl、Fe玻璃、石蜡两者区别方法间接方法:测定其是否有固定的_熔点__科学方法:对固体进行_X-射线衍射__实验2.获得晶体的三种途径。
①熔融态物质凝固。
②气态物质冷却不经液态直接_凝固(凝华)__。
③溶质从溶液中析出。
3.非晶体、等离子体和液晶的比较聚集状态组成与结构特征主要性能非晶体内部微粒的排列呈现杂乱无章(长程无序,短程有序)的分布状态的固体某些非晶体合金强度和硬度高、耐腐蚀性强,非晶态硅对光的吸收系数大等离子体由电子、阳离子和电中性粒子组成,整体上呈电中性,带电离子能自由移动具有良好的导电性和流动性液晶内部分子的排列沿分子长轴方向呈现出有序的状态既具有液体的流动性、黏度、形变性,又具有晶体的导热性、光学性质等二、离子晶体1.离子晶体构成微粒_阴、阳离子__粒子间的相互作用力_离子键__方向性和饱和性没有方向性,没有饱和性离子键强弱阴、阳离子半径越小,所带电荷数越多,离子键越强。
硬度较大熔、沸点较高溶解性大多易溶于水等极性溶剂导电、导热性晶体不导电,水溶液或熔融态导电物质类别及举例金属氧化物(如K2O、Na2O)、强碱(如KOH、NaOH)、绝大部分盐(如NaCl)2.离子晶体的性质性质原因熔沸点离子晶体中有较强的离子键,熔化或升华时需消耗较多的能量。
所以离子晶体有较高的熔、沸点和难挥发性。
通常情况下,同种类型的离子晶体,离子半径越小,离子键越强,熔、沸点越高硬度硬而脆。
离子晶体表现出较高的硬度。
当晶体受到冲击力作用时,部分离子键发生断裂,导致晶体破碎导电性不导电,但熔融或溶于水后能导电。
高中化学选修3:晶体结构与性质知识点总结
一.晶体常识
1 .晶体与非晶体比较
2 .获得晶体的三条途径
①熔融态物质凝固。
②气态物质冷却不经液态直接凝固(凝华)。
③溶质从溶液中析出。
3 .晶胞
晶胞是描述晶体结构的基本单元。
晶胞在晶体中的排列呈“无隙并置”。
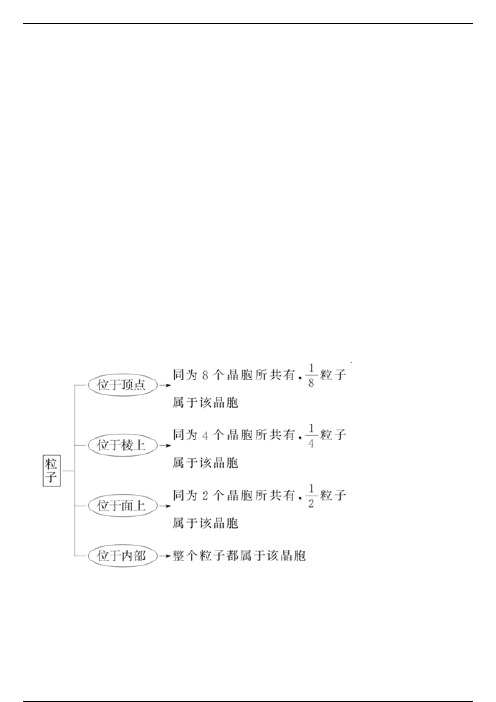
4 .晶胞中微粒数的计算方法 —— 均摊 法
如某个粒子为n个晶胞所共有,则该粒子有1/n属于这个晶胞。
中学中常见的晶胞为立方晶胞
立方晶胞中微粒数的计算方法如下:
注意:在使用“均摊法”计算晶胞中粒子个数时要注意晶胞的形状
二.四种晶体的比较
晶体熔、沸点高低的比较方法
(1)不同类型晶体的熔、沸点高低一般规律:原子晶体>离子晶体>分子晶体。
金属晶体的熔、沸点差别很大,如钨、铂等熔、沸点很高,汞、铯等熔、沸点很低。
(2)原子晶体
由共价键形成的原子晶体中,原子半径小的键长短,键能大,晶体的熔、沸点高.如熔点:金刚石>碳化硅>硅
(3)离子晶体
一般地说,阴阳离子的电荷数越多,离子半径越小,则离子间的作用力就越强,相应的晶格能大,其晶体的熔、沸点就越高。
(4)分子晶体
①分子间作用力越大,物质的熔、沸点越高;具有氢键的分子晶体熔、沸点反常的高。
②组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高。
③组成和结构不相似的物质(相对分子质量接近),分子的极性越大,其熔、沸点越高。
④同分异构体,支链越多,熔、沸点越低。
(5)金属晶体
金属离子半径越小,离子电荷数越多,其金属键越强,金属熔、沸点就越高。
三.几种典型的晶体模型。
晶体的结构和物理化学性质

晶体的结构和物理化学性质晶体是一种具有规则的、周期性的空间排列方式的固态物质,其结构和物理化学性质具有一定的特殊性。
一、晶体的结构晶体的结构是指晶体中原子、离子或分子的排列方式。
晶体结构的研究对于了解晶体的性质和应用具有重要意义。
1. 基本概念晶体结构的基本单位是晶胞,晶胞是一个空间点阵,由若干个格点组成。
晶体中的原子、离子或分子占据着这些格点,并以一定的方式连接在一起。
2. 晶体的对称性晶体的结构具有各种各样的对称性,包括旋转对称性、镜面对称性、轴对称性等。
晶体对称性的存在决定了晶体的物理性质和外观特征。
3. 晶体的晶系和晶格根据晶体结构的不同,晶体可以分为七个晶系:立方晶系、六方晶系、四方晶系、三方晶系、正交晶系、单斜晶系和三斜晶系。
每个晶系下又有不同的晶格类型,如简单立方晶格、面心立方晶格、体心立方晶格等。
二、晶体的物理化学性质晶体的结构决定了它们的物理性质和化学性质,下面我们将重点介绍晶体的几个重要性质。
1. 硬度晶体的结构紧密有序,其中的化学键比较稳定,因此晶体通常具有较高的硬度。
不同晶体的硬度不同,可以通过硬度测试来定量评估晶体的硬度。
2. 双折射部分晶体具有双折射现象,也就是将入射光线分为两束线偏振光。
这种现象是由于晶体结构中的非中心对称性所导致的。
3. 光学性质晶体对于光的吸收、透射和折射等具有一定的选择性。
某些晶体具有特殊的光学性质,如偏光现象、发光现象等。
4. 热稳定性晶体的结构相对稳定,因此对于温度变化的适应能力较强。
晶体在高温下不易改变结构,具有较高的熔点和热稳定性。
5. 热导率和电导率部分晶体具有较高的热导率和电导率,这是因为晶体的结构中存在导电或热导路径,使得能量传导效率较高。
6. 化学反应晶体在一定条件下可以发生化学反应,这是因为晶体中的化学键具有一定的活性。
晶体的表面也可以参与化学反应,与周围环境发生相互作用。
综上所述,晶体的结构和物理化学性质密切相关,晶体的不同结构决定了其不同的性质。
晶体结构与性质知识总结(完善)

3—1、晶体的常识一、晶体和非晶体1、概述——自然界中绝大多数物质是固体,固体分为和两大类.*自范性——晶体能自发地呈现多面体外形的性质.本质上,晶体的自范性是晶体中粒子在微观空间里呈现周期性有序排列的宏观表象。
*晶体不因颗粒大小而改变,许多固体粉末用肉眼看不到规则的晶体外形,但在显微镜下仍可看到。
* 晶体呈现自范性的条件之一是晶体生长的速率适当,熔融态物质凝固速率过快常得到粉末或没有规则外形的块状物。
*各向异性——晶体的许多物理性质如强度、热导性和光导性等存在各向异性即在各个方向上的性质是不同的二、晶胞1、定义——描述晶体结构的基本单元.2、特征-—(1)习惯采用的晶胞都是体,同种晶体所有的晶胞大小形状及内部的原子种类、个数和几何排列完全相同。
(2)整个晶体可以看作是数量巨大的晶胞“无隙并置"而成。
<1〉所谓“无隙”是指相邻晶胞之间没有任何间隙;〈2> 所谓“并置”是指所有晶胞都是平行排列的,取向相同。
3、确定晶胞所含粒子数和晶体的化学式——均摊法分析晶胞与粒子数值的关系(1)处于内部的粒子,属于晶胞,有几个算几个均属于某一晶胞。
(2)处于面上的粒子,同时为个晶胞共有,每个粒子有属于晶胞.(3)处于90度棱上的粒子,同时为个晶胞共有,每个粒子有属于晶胞.(4)处于90度顶点的粒子,同时为个晶胞共有,每个粒子有属于晶胞;处于60度垂面顶点的粒子,同时为个晶胞共有,每个粒子有属于晶胞;处于120度垂面顶点的粒子,同时为个晶胞共有,每个粒子有属于晶胞。
4、例举三、分类晶体根据组成粒子和粒子之间的作用分为分子晶体、原子晶体、金属晶体和离子晶体四种类型。
3—2、分子晶体和原子晶体一、分子晶体1、定义——只含分子的晶体。
2、组成粒子——。
3、存在作用—-组成粒子间的作用为(),多原子分子内部原子间的作用为。
*分子晶体中定含有分子间作用力,定含有共价键。
*分子间作用力于化学键.4、物理性质(1)熔沸点与硬度-—融化和变形只需要克服,所以熔沸点、硬度,部分分子晶体还可以升华。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
离子键强弱 ——离子键越强,熔沸点越高! 离子半径越小,离子所带电荷越多,离子键越强。
四、影响离子晶体配位数的因素有:
1、正负离子的半径比 2、正负离子的电荷比 3、离子键的纯粹程度
1.在下列四种有关性质的叙述中,可能属 于金属晶体的是( B ) A.由分子间作用力结合而成,熔点低 B.固体或熔融后易导电,熔点在1 000℃ 左右 C.由共价键结合成网状结构,熔点高 D.固体不导电,但溶于水或熔融后能导电
4.下列关于离子晶体性质的叙述中不 正确的是( ) D A.离子晶体具有较高的熔沸点 B.离子晶体具有较大的硬度
C.离子晶体在熔融状态时都能导电 D.离子晶体中阴、阳离子个数比为 1∶1
5.能说明某晶体属于离子晶体的是 ( D ) A.一定溶于水 B.固态不导电,水溶液能导电 C.有较高的熔点 D.固态不导电,熔融时能导电
NaCl 801 Al2O3 2 073
AlF3 1 291 CO2 -57
AlCl3 190 SiO2 1 723
A. 铝的化合物的晶体中有的是离子晶体 B.表中只有BCl3和干冰是分子晶体 C.同族元素的氧化物可形成不同类晶体 D.不同族元素的氧化物可形成相同类晶体
8.下列各项所述的数字不是6的是 A.在NaCl晶体中,与一个Na+最 近的且距离相等的Cl-的个数 B.在金刚石晶体中,最小的环上 的碳原子个数 C.在二氧化硅晶体中,最小的环 上的原子个数 D.在石墨晶体的片层结构中,最 小的环上的碳原子个数 C
一、原子晶体
1、定义:原子间以共价键相结合而形成的空间 网状结构的晶体。 2、最小微粒:原子 3、微粒之间的作用关系: —— 共价键 4、融化和沸腾时破坏的作用: ——共价键 5、原子晶体的共性
硬度大,熔沸点高(一般2000℃以上), 难溶,导电性差。
7、原子晶体判定方法:
(1)、最小微粒 —— 原子 原子晶体
归纳四类晶体的结构和性质
晶体类型 原子晶体 分子晶体 金属晶体
构成粒子 相互作用 熔、沸点 硬度 延展性 原子 共价键 分子 范德华力
离子晶体
阴阳离子 离子键 熔点较高、沸点高 硬而脆
金属阳离子 和自由电子
金属键 一般较高 部分较低 一般较高 部分较低
高
高硬度
低
硬度较小
不良 差
金刚石 SiO2
不良 差
2.钛酸钡的热稳定性好,介电常数高, 在小型变压器、话筒和扩音器中都有 应用。钛酸钡晶体的晶胞结构示意图 如图所示,它的化学式是( D A.BaTi8O12 B.BaTi4O6 C.BaTi2O4 D.BaTiO3
3.下面的排序不正确的是( A.晶体熔点的高低:
C
)
B.硬度由大到小:金刚石>碳化硅>晶 体硅 C.熔点由高到低:Na>Mg>Al D.晶格能由大到小: NaF>NaCl>NaBr>NaI
11.(2008·四川)下说法中正确的 D A.离子晶体中每个离子的周围均吸 引着6个带相反电荷的离子 B.金属导电的原因是在外加电场的 作用下金属产生自由电子,电子定 向运动 C.分子晶体的熔沸点低,常温下均 呈液态或气态 D.原子晶体中的各相邻原子都以共 价键相结合
12.下列各组物质的晶体中,化学 键类型相同、晶体类型也相同的 是 ( )
二、离子晶体的判定
最小微粒:阴阳离子
1、强碱 2、绝大多数盐(常见 典型物质: 的除AlCl3、HgCl2外)
离子晶体
3、活泼金属氧化物、过氧 化物、碳化物(CaC2)及氮 化物(Mg3N2)
熔点: 一般300℃ ~ 1000℃之间
导电性: 固态时不导电,而在熔融状 态和水溶液中都能导电。
三、决定分子晶体熔沸点高低及硬度大 小的因素
三、决定分子晶体熔沸点高低及硬度大 小的因素 分子间作用力和氢键 —— 分子间作用力越大,氢键作用力越强, 物质的熔沸点越高,硬度越大。 四、分子晶体熔沸点高低判定:
1、组成和结构相似的分子晶体,一般相对分 子 质量越大,熔沸点越高。 2、组成和结构不相似的分子晶体,分子极性越大, 熔沸点越高. 例如:CO > N2 3、同分异构体之间,一般支链越多,熔沸点越低。 4、根据物质在相同条件下的状态判定 S> L> g
6.下列叙述肯定正确的是( B ) A.在离子晶体中不可能存在非极 性键 B.在共价化合物的分子晶体中不 可能存在离子键 C.在极性分子中不可能存在非极 性键 D.在原子晶体中不可能存在极性 共价键
7.下列数据是对应物质的熔点,据此做 出的下列判断中错误的是 ( B )
Na2O 920 BCl3 -107
A.SO2、SiO2 B.CO2、H2O C.NaCl、HCl D.CCl4、KCl
B
2、下列式子中,真实表示物质分子组 成的是( ) A、H2SO4 B、NH4Cl C、SiO2 D 、C 4、下列各组物质中,化学键类型相同、 晶体类型也相同的是( ) A、CaCl2和Na2O2 B、碘、氖 C、CO2和H2O D、CCl4和KCl
二、分子晶体判定方法:
1、最小微粒 —— 分子 (1)、所有非金属氢化物
(2)、常见的除:金刚石、石墨、 2、物质类别 晶体硅、锗、硼等外部分非金属单质 (3)、常见的除SiO2外的部分 非 金属 氧化物 (4)、几乎所有的酸 (5)、除有机盐外的绝大多数有 机物晶体 3、物质熔点 —— 一般300℃以下
9.四种晶体的晶胞,其离子排列方式 如图所示,其中化学式不属AB型的是B
10.科学家最近发现一种由钛原子和碳原子构成 的气态团簇分子,如图所示:图中顶点和面心 的原子都是钛原子,棱的中心和体心的原子都 是碳原子,该分子的化学式是( B ) • A.Ti13C14 B.Ti14C13 C.Ti4C5 D.TiC
下表列出了有关晶体的说明,有错 误的是( )
选项 A B C D
晶体名称
组成晶体微粒 名称 晶体内存在的 结合力
碘化钾
阴、阳 离子
干冰
氖
二氧化硅
分子
原子
原子
离子键 范德华力
共价键
共价键
6、下列各项所述的数字不是6的是 ( )
A.在NaCl晶体中,与一个Na+最近的且距离相等的Cl-的个数
B.在金刚石晶体中,最小的环上的碳原子个数 C.在二氧化硅晶体中,最小的环上的原子个数 D.在石墨晶体的片层结构中,最小的环上的碳原子个数 7、下列说法正确的是(NA为阿伏加德罗常数) A.124 g P4含有P—P键的个数为4NA B.12 g石墨中含有C—C键的个数为1.5NA C.12 g金刚石中含有C—C键的个数为NA D.60gSi02中含Si—O键的个数为2NA 8. 共价键、离子键和范德华力都是微粒之间的不同作用力,下列含有两种结合 力的是 ( ) ①Na2O2 ②SiO2 ③石墨 ④金刚石 ⑤NaCl ⑥白磷 A.①②④ B.①③⑥ C.②④⑥ D.③④⑤ ( )
(2)、典型物质 ——金刚石,晶体硅、锗,
SiO2晶体、SiC及Si3N4等
(3)、物质熔点
—— 一般在2000℃以上 8、决定原子晶体熔沸点高低及硬度大小的因素 共价键的强弱 —— 共价键越强,物质的熔沸点越高,硬 度越大
一、金属晶体
知识要点小结
1、定义:金属阳离子和自由电子之间的较强作用 2、最小微粒:金属阳离子和自由电子 3、微粒之间的作用关系: —— 金属键 4、融化和沸腾时破坏的作用: ——金属键 5、金属晶体的共性 容易导电、导热、有延展性、有金属光泽等。
7、金属晶体判定方法:
(1)、最小微粒
—— 金属阳离子和自由电子
金属晶体 (2)、物质类别
——固态金属单质、决定金属晶体熔沸点高低及硬度大小的因素
金属键的强弱 ——金属键越强,熔沸点越高,硬度越大。
一、离子晶体
知识要点小结
1、定义: 2、最小微粒: 阴阳离子 3、微粒之间的作用关系: —— 离子键 4、融化和沸腾时破坏的作用: ——离子键 5、离子晶体的共性 离子晶体具有熔沸点较高,硬度较大,难挥 发难压缩的特点。离子晶体在固态时不导电,而 在熔融状态和水溶液中都能导电。
良好 良好
不良
固态不导电
熔化状态和溶液导电
导电性
典型实例
冰 干冰 Na、Fe等 碘等
NaOH、NaCl
一、分子晶体
1、定义: 只含分子的晶体称为分子晶体。 2、最小微粒: 分子 3、微粒之间的作用关系: —— 分子间作用力或分子间作用力和氢键 4、融化和沸腾时破坏的作用: ——分子间作用力或分子间作用力和氢键 5、分子晶体的共性 硬度小、熔沸点低(一般300℃以下 ),易 挥发,固态或熔融状态下都不导电,溶解性一般 遵循“ 相似相溶”原理。
