第三章 微专题6 晶体结构的分析与计算
晶体结构分析与计算

晶体结构分析与计算湖南省浏阳市第一中学潘丹张水强410300在2005年高考考纲中,在思维能力中增加了“对原子、分子、化学键等微观结构有一定的三维想象能力”的要求。
三维想象能力可能通过“晶体结构”试题来体现,而“晶体结构”这一知识点前几年是高考的热点之一(如92年的金刚石、96年的SiO2 、97年的C60、98年的GBO、99年的NiO等等)。
间隔了几年,笔者认为有必要引起广大考生足够的重视。
本文从最常见的几种晶体结构题型入手,分析晶体结构有关的问题,帮助同学们更好地掌握晶体结构的内容,培养空间想象能力和形象思维能力。
一、常见的几种晶体结构分析(一)、氯化钠晶体1、NaCl晶体是一种简单立方结构——Na+和Cl-交替占据立方体的顶点而向空间延伸。
2、在每个Na+周围最近且等距离(设边长为a)的Cl-有6个,在每个Cl-周围最近且等距离的Na+有6个。
3、在每个Na+周围最近且等距离(平面对角线为2a)的Na+有12个,在每个Cl-周围且最近等距离(平面对角线为2a)的Cl-有12个。
(二)、氯化铯晶体1、CsCl晶体是一种立方体心结构——每8个Cs+、8个Cl-各自构成立方体。
在每个立方体的中心有一个异种离子(Cl-或Cs+)。
2、在每个Cs+周围最近且等距离的Cl-(设为3a/2)有8个。
在每个Cl-周围最近且等距离的Cs+有8个。
3、在每个Cs+周围最近且等距离(必为a)的Cs+有6个,在每个Cl-周围最近且等距离的Cl-有6个。
(三)、金刚石晶体1、金刚石晶体是一种空间网状结构——每个C原子与另4个C原子以共价键结合,前者位于正四面体中心,后者位于正四面体顶点。
2、晶体中所有C—C键键长相等(1.55×10-10m),键角相等(均为109028'),晶体中最小碳环由6个C组成且六者不在同一平面内。
3、晶体中每个C原子参与了4条C—C键的形成,而在每条键中的贡献只有一半,故C原子个数与C—C键数之比为1:4×21=1:2。
高中化学新教材同步选择性必修第二册第3章微专题6:晶体结构的分析与计算
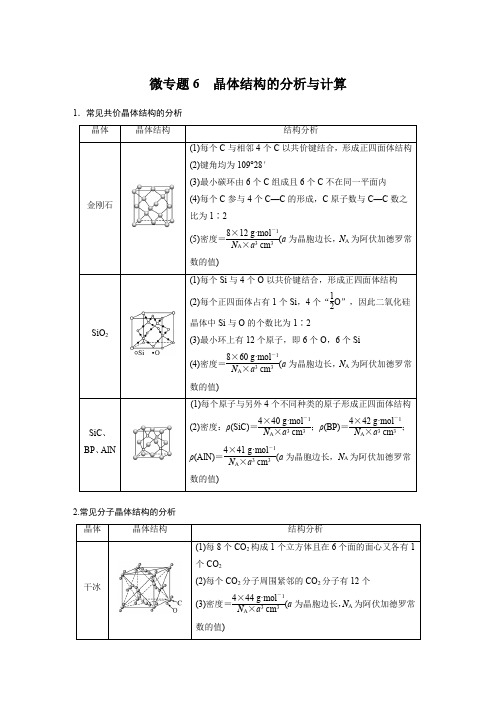
微专题6晶体结构的分析与计算1.常见共价晶体结构的分析晶体晶体结构结构分析金刚石(1)每个C与相邻4个C以共价键结合,形成正四面体结构(2)键角均为109°28′(3)最小碳环由6个C组成且6个C不在同一平面内(4)每个C参与4个C—C的形成,C原子数与C—C数之比为1∶2(5)密度=8×12 g·mol-1N A×a3 cm3(a为晶胞边长,N A为阿伏加德罗常数的值)SiO2(1)每个Si与4个O以共价键结合,形成正四面体结构(2)每个正四面体占有1个Si,4个“12O”,因此二氧化硅晶体中Si与O的个数比为1∶2(3)最小环上有12个原子,即6个O,6个Si(4)密度=8×60 g·mol-1N A×a3 cm3(a为晶胞边长,N A为阿伏加德罗常数的值)SiC、BP、AlN (1)每个原子与另外4个不同种类的原子形成正四面体结构(2)密度:ρ(SiC)=4×40 g·mol-1N A×a3 cm3;ρ(BP)=4×42 g·mol-1N A×a3 cm3;ρ(AlN)=4×41 g·mol-1N A×a3 cm3(a为晶胞边长,N A为阿伏加德罗常数的值)2.常见分子晶体结构的分析晶体晶体结构结构分析干冰(1)每8个CO2构成1个立方体且在6个面的面心又各有1个CO2(2)每个CO2分子周围紧邻的CO2分子有12个(3)密度=4×44 g·mol-1N A×a3 cm3(a为晶胞边长,N A为阿伏加德罗常数的值)白磷密度=4×124 g·mol-1N A×a 3 cm 3(a为晶胞边长,N A为阿伏加德罗常数的值)3.常见离子晶体结构的分析NaCl型CsCl型ZnS型CaF2型晶胞配位数684F-:8;Ca2+:4密度的计算(a为晶胞边长,N A为阿伏加德罗常数的值)4×58.5 g·mol-1N A×a3 cm3168.5 g·mol-1N A×a3 cm34×97 g·mol-1N A×a3 cm34×78 g·mol-1N A×a3 cm31.AB型化合物形成的晶体结构多种多样。
晶体结构的分析和计算

一、晶胞对组成晶胞的各质 点的占有率
立方晶胞
体心: 1 面心: 1/2 棱边: 1/4 顶点: 1/8
有关晶体的计算
1、当题给信息为晶体中最小重 复单元——晶胞(或平面结构)中 的微粒排列方式时,要运用空间想 象力,将晶胞在三维空间内重复延 伸,得到一个较完整的晶体结构, 形成求解思路。
例1:
因C60分子含30个双键,与极活泼的F2发生加成反应即可生成C60F60 (只 要指__出__“___C_6_0_含__3_0_个__双__键__”__即__可__,_但__答__“__因__C_6_0_含__有__双__键__”__不__行__)____.
(3)通过计算,确定C60分子所含单键数.C60分子所含单键数为___________. 可由欧拉定理计算键数(即棱边数):60+(12+20)-2=90 C60分子中单键为:90-30=60
例4:
金刚石晶体中 含有共价键形成的 C原子环,其中最
小的C环上有__6___
个C原子。
巩固练习一:
石墨晶体的层状结构,层内 为平面正六边形结构(如图), 试回答下列问题: (1)图中平均每个正六边形占
有C原子数为__2__个、占有的碳 碳键数为__3__个。
(2)层内7个六元环完全占有
的C原子数为1_4____个,碳原子
2、当题给信息为晶体中微粒 的排列方式时,可在晶体结构中 确定一个具有代表性的最小重复 单元——晶胞为研究对象,运用 点、线、面的量进行解答。
例2:
右图是石英晶 体平面示意图(它实 际上是立体的网状结 构),其中硅、氧原 子数之比为____.
1:2
例3:Байду номын сангаас
如图直线交点处 的圆圈为NaCl晶体中 Na+或Cl-所处位置, 晶体中,每个Na+周 围与它最接近的且距 离相等的Na+个数为: ____ 12
浅谈有关晶体结构的分析和计算

浅谈有关晶体结构的分析和计算 摘要:晶体结构的分析和计算是历年全国高考化学试卷中三个选做题之一,本文从晶体结构的粒子数和化学式的确定,晶体中化学键数的确定和晶体的空间结构的计算等方面,探讨有关晶体结构的分析和计算的必要性。
关键词:晶体、结构、计算、晶胞在全国统一高考化学试卷中,有三个题目是现行中学化学教材中选学内容,它们分别《化学与生活》、《有机化学基础》和《物质结构与性质》。
虽然三个题目在高考时只需选做一题,由于是选学内容,学生对选学内容往往重视不够,所以在高考时学生对这部分题目得分不够理想。
笔者对有关晶体结构的分析和计算进行简单的归纳总结,或许对学生学习有关晶体结构分析和计算有所帮助,若有不妥这处,敬请同仁批评指正。
一、有关晶体结构的粒子数和化学式确定(一)、常见晶体结构的类型1、原子晶体(1)金刚石晶体中微粒分布:①、每个碳原子与4个碳原子以共价键结合,形成正四面体结构。
②、键角均为109°28′。
③、最小碳环由6个碳组成并且六个碳原子不在同一平面内。
④、每个碳原子参与4条C-C 键的形成,碳原子与C-C 键之比为1:2。
(2)二氧化硅晶体中微粒分布①、每个硅原子与4个氧原子以共价键结合,形成正四面体结构。
②、每个正四面体占有1个Si ,4个“21氧”,n(Si):n(O)=1:2。
③、最小环上有12个原子,即:6个氧原子和6个硅原子.2、分子晶体:干冰(CO 2)晶体中微粒分布①、8个CO 2分子构成立方体并且在6个面心又各占据1个CO 2分子。
②、每个CO 2分子周围等距离紧邻的CO 2分子有12个。
3、离子晶体(1)、NaCl 型晶体中微粒分布①、每个Na +(Cl -)周围等距离且紧邻的Cl -(Na +)有6个。
每个Na +周围等距离紧邻的Na +有12个。
②、每个晶胞中含4个Na +和4个Cl -。
(2)、CsCl 型晶体中微粒分布①、每个Cs +周围等距离且紧邻的Cl -有8个,每个Cs +(Cl -)周围等距离且紧邻的Cs +(Cl -)有6个。
浅谈有关晶体结构的分析和计算讲解学习

浅谈有关晶体结构的分析和计算浅谈有关晶体结构的分析和计算摘要:晶体结构的分析和计算是历年全国高考化学试卷中三个选做题之一,本文从晶体结构的粒子数和化学式的确定,晶体中化学键数的确定和晶体的空间结构的计算等方面,探讨有关晶体结构的分析和计算的必要性。
关键词:晶体、结构、计算、晶胞在全国统一高考化学试卷中,有三个题目是现行中学化学教材中选学内容,它们分别《化学与生活》、《有机化学基础》和《物质结构与性质》。
虽然三个题目在高考时只需选做一题,由于是选学内容,学生对选学内容往往重视不够,所以在高考时学生对这部分题目得分不够理想。
笔者对有关晶体结构的分析和计算进行简单的归纳总结,或许对学生学习有关晶体结构分析和计算有所帮助,若有不妥这处,敬请同仁批评指正。
一、有关晶体结构的粒子数和化学式确定(一)、常见晶体结构的类型1、原子晶体(1)金刚石晶体中微粒分布:①、每个碳原子与4个碳原子以共价键结合,形成正四面体结构。
②、键角均为109°28′。
③、最小碳环由6个碳组成并且六个碳原子不在同一平面内。
④、每个碳原子参与4条C-C键的形成,碳原子与C-C键之比为1:2。
(2)二氧化硅晶体中微粒分布①、每个硅原子与4个氧原子以共价键结合,形成正四面体结构。
②、每个正四面体占有1个Si ,4个“21氧”,n(Si):n(O)=1:2。
③、最小环上有12个原子,即:6个氧原子和6个硅原子.2、分子晶体:干冰(CO 2)晶体中微粒分布①、8个CO 2分子构成立方体并且在6个面心又各占据1个CO 2分子。
②、每个CO 2分子周围等距离紧邻的CO 2分子有12个。
3、离子晶体(1)、NaCl 型晶体中微粒分布①、每个Na +(Cl -)周围等距离且紧邻的Cl -(Na +)有6个。
每个Na +周围等距离紧邻的Na +有12个。
②、每个晶胞中含4个Na +和 4个Cl -。
(2)、CsCl 型晶体中微粒分布①、每个Cs +周围等距离且紧邻的Cl -有 8个,每个Cs +(Cl -)周围等距离且紧邻的Cs +(Cl -)有6个。
晶体结构的分析与计算

B
化学式: AB
2. 写出下列离子晶体的化学式
练
习
Y
X
Ca
O
Ti
该晶体的化学式为
该晶体的化学式为
XY2(或Y2X)
CaTiO3
3.1987年2月,朱经武(Paul Chu)
教授等发现钇钡铜氧化合物在90K温
练
习
度下具有超导性。若该化合物晶体的
晶胞结构如图所示,则该化合物的化 学式可能是 C A.YBa2CuO7-X C.YBa2Cu3O7-X 。 B.YBa2Cu2O7-X D.YBa2Cu4O7-X
Ba O Y
Cu
练
子,如右图所示: 顶点和面心的原子是钛原子, 棱的中心和体心的原子是碳原子, 它的化学式是( Ti14C13 ) --Ti --C
习
4.最近发现一种由钛原子和碳原子构成的气态团簇分
例 题 (二)、晶体中距离最近的微粒数的计算:
例2.在氯化钠晶体(如图)中,与氯离子距离最近的钠离
①C60分子中每个碳原子只跟相邻的3个碳原子形成化学键;
②C60分子只含有五边形和六边形; ③多面体的顶点数、面数和棱边数的关系,遵循欧拉定理: 顶点数+面数-棱边数=2 据上所述,可推知C60分子有12个五边形和20个六边形,C60分子所 含的双键数为30.请回答下列问题: 金刚石 (1)固体C60与金刚石相比较,熔点较高者应是____________,理由是: 金刚石属原子晶体,而固体C60不是,故金刚石熔点较高. (答出“金刚石属原子晶体”即可) ________________________________________________________. (2)试估计C60跟F2在一定条件下,能否发生反应生成C60F60(填“可能”或 可能 “不可能”)_______________,并简述其理由: 因C60分子含30个双键,与极活泼的F2发生加成反应即可生成C60F60 (只要 指出“C60含30个双键”即可,但答“因C60含有双键”不行) ________________________________________________________. (3)通过计算,确定C60分子所含单键数.C60分子所含单键数为___________. 可由欧拉定理计算键数(即棱边数):60+(12+20)-2=90 C60分子中单键为:90-30=60
晶体结构的分析与计算

(3)GaAs的熔点为1 238 ℃,密度为ρ g·cm-3,其晶胞结构如图所示。该 晶体的类型为__原__子__晶__体__,Ga与As以_共__价___键结合。Ga和As的摩尔质量 分别为MGa g·mol-1和MAs g·mol-1,原子半径分别为rGa pm和rAs pm,阿 伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为 _4_π_×__13_0(_-M_30G_Na_+A_ρ_M(_r_A3G_sa)+__r_3A_s)_×__1_0_0_%___。
123456
3.(2020·四川武胜烈面中学高 二期中)有四种不同堆积方式 的金属晶体的晶胞如图所示, 下列有关说法正确的是 A.①为简单立方堆积,②为六方最密堆积,③为体心立方堆积,④为面
心立方最密堆积
√B.每个晶胞都是规则排列的
C.晶胞中原子的配位数分别为:①6,②8,③8,④12 D.空间利用率的大小关系为:①<②<③<④
4.(2020·哈尔滨第六中学高二期中)以NA表示阿伏加德罗常数的值,下列 说法错误的是
A.18 g冰(图1)中含O—H键数目为2NA B.28 g晶体硅(图2)中含有Si—Si键数目为2NA
√C.44 g干冰(图3)中含有NA个晶胞结构单元
D.石墨烯(图4)是碳原子单层片状新材料,12 g石墨烯中含C—C键数目为1.5NA
123456
解析 在氯化钠晶体中,Na+和Cl-的配位数都是6,则距离Na+最近的 六个Cl-形成正八面体,A项正确; 分子晶体的构成微粒是分子,每个分子为一个整体,所以该分子的化学 式为E4F4或F4E4,B项正确; 锌采取六方最密堆积,配位数为12,C项错误; KO2晶体中每个K+周围有6个紧邻的O-2 ,每个 O-2 周围有6个紧邻的K+, D项正确。故选C。
化学《晶体结构的分析和计算》精品PPT课件

例右图2是:石英晶
体平面示意图(它实 际上是立体的网状结 构),其中硅、氧原
子数之比为__1:_2_.
例3:
如图直线交点处 的圆圈为NaCl晶体中 Na+或Cl-所处位置, 晶体中,每个Na+周 围与它最接近的且距 离相等的Na+个数为: _1__2_
例4:
金刚石晶体中 含有共价键形成的 C原子环,其中最
巩固练习二:
已知晶体硼的基本结构 单元是由硼原子组成的正二 十面体,如图所示:其中有 二十个等边三角形的面和一 定数目的顶点,每个顶点为 一个硼原子,试通过观察分 析右图回答:此基本结构单 元是由_1_2_个硼原子构成,有 _3_0_个B-B化学键,相邻B-B键 的键角为_6_0_0_.
巩固练习三:
小结
一、晶胞对质点的占有率的计算 二、有关晶体的计算
写在最后
经常不断地学习,你就什么都知道。你知道得越多,你就越有力量 Study Constantly, And You Will Know Everything. The More
You Know, The More Powerful You Will Be
结束语
感谢聆听
不足之处请大家批评指导
Please Criticize And Guide The Shortcomings
讲师:XXXXXX XX年XX月XX日
1.当题给信息为晶体中最小重复 单元——晶胞(或平面结构)中的微 粒排列方式时,要运用空间想象力, 将晶胞在三维空间内重复延伸,得到 一个较完整的晶体结构,形成求解思 路。
学与问
图3-9依次是金属钠、金属锌、碘、金刚石晶胞 的示意图,数一数,它们分别平均含几个原子?
图 3-9 钠、锌、碘、金刚石晶胞示意图
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
微专题6晶体结构的分析与计算
1.常见共价晶体结构的分析
晶体晶体结构结构分析
金刚石(1)每个C与相邻4个C以共价键结合,形成正四面体结构
(2)键角均为109°28′
(3)最小碳环由6个C组成且6个C不在同一平面内
(4)每个C参与4个C—C的形成,C原子数与C—C数之比为1∶2
(5)密度=
8×12 g·mol-1
N A×a3 cm3
(a为晶胞边长,N A为阿伏加德罗常数的值)
SiO2(1)每个Si与4个O以共价键结合,形成正四面体结构
(2)每个正四面体占有1个Si,4个“
1
2O”,因此二氧化硅晶体中Si与O的个数比为1∶2
(3)最小环上有12个原子,即6个O,6个Si
(4)密度=
8×60 g·mol-1
N A×a3 cm3
(a为晶胞边长,N A为阿伏加德罗常数的值)
SiC、BP、AlN (1)每个原子与另外4个不同种类的原子形成正四面体结构
(2)密度:ρ(SiC)=
4×40 g·mol-1
N A×a3 cm3
;ρ(BP)=
4×42 g·mol-1
N A×a3 cm3
;ρ(AlN)=
4×41 g·mol-1
N A×a3 cm3
(a为晶胞边长,N A为阿伏加德罗常数的值)
2.常见分子晶体结构的分析
晶体晶体结构结构分析
干冰(1)每8个CO2构成1个立方体且在6个面的面心又各有1个CO2
(2)每个CO2分子周围紧邻的CO2分子有12个
(3)密度=
4×44 g·mol-1
N A×a3 cm3
(a为晶胞边长,N A为阿伏加德罗常数的值)。
