鲁教版九年级化学全册9.2金属的化学性质教案
新版鲁教版初中化学九年级下册【备课】全册教案:9.2 金属的性质

鲁教版初中化学重点知识精选化学是一门非常有意思的学科,充满了新奇的实验!鲁教版初中化学和你一起共同进步学业有成!第二节金属的化学性质教学目标:1.知道镁、铝、铁、铜等常见金属与氧气的反应。
2.认识常见金属与盐酸、硫酸及盐溶液的置换反应,并能解释日常生活中的一些现象。
3.能说出常见金属的活动性顺序,了解金属活动性顺序的意义。
4.通过我国古代湿法冶金术介绍,增强学生民族自豪感和爱国主义情感。
学情分析:学生已经知道了镁带、铁丝能在氧气中燃烧,铜能跟氧气反应,镁与盐酸、硫酸反应等事实,但这些知识是零碎不系统的。
本节课应从复习金属的化学性质入手,使学生对不同的金属化学活泼性不同产生一定的感性认识,在此基础上再来认识金属在水溶液中与酸或盐反应的情况,归纳其活动性规律。
重点:金属的化学性质、置换反应、金属活动性顺序。
难点:金属活动性顺序的应用,判断金属与酸或盐溶液能否反应。
教学媒体:铝粉、铁丝、铜丝、铝片、锌片、盐酸、硫酸、硫酸铜溶液、硝酸银溶液、氯化钠溶液、滤纸、坩埚钳、酒精灯、试管等。
教学方法:实验探究法、自学研究法、讲述法、讨论归纳法。
教学过程:一、金属与氧气的反应(引导复习)许多金属在一定条件下能与氧气发生化学反应,请写出下列反应的化学方程式:①镁与氧气的反应②铁与氧气的反应③铜与氧气的反应(活动天地)铝粉的燃烧引导学生仔细观察实验现象,并书写反应的化学方程式。
(交流共享)分析哪些原因可以导致金属与氧气反应的难易和剧烈程度不同?二、金属与酸的反应(引导)很多金属不仅可以跟氧气反应,还能与盐酸或硫酸反应;请写出下列反应的化学方程式:①镁与盐酸的反应②锌与硫酸的反应(实验探究)金属与酸的反应盐酸稀硫酸铁铜铝引导学生观察实验现象并分析下列问题:①哪些金属能与盐酸、稀硫酸反应?哪些金属不能与盐酸、稀硫酸反应?②比较三种金属与酸反应的难易和剧烈程度,将三种金属的活动性按由强到弱排列。
(小结)金属活动性顺序并板书,介绍谐音记忆方法:“加盖那煤炉,心铁西迁,轻,统共一百斤。
秋鲁教版化学九年级下册9.2《金属的化学性质》优秀教案2(重点资料).doc

Zn+2AgNO3=== Zn(NO3)2+2Ag
分组讨论,交流课下收集的有关资料及金属制品。
联系生产生活实际进行识记
学生思考
分 组讨论交流,各组派代表回答问题。
观察、识记
阅读、考、讨论,完成在线测试。
阅读、回答、总结,得出合金的定义。
出来
练习:1、下列物质能否发生化学反应?写出能反应的化学方程式并判断它们是否为置换反应。
(1)银和稀盐酸(2)锌和硫酸铜(3)铜和硫酸锌(4)铝和硝酸银
2、黄 铜(含锌和铜)与黄金的外观很相似,你能利用金属的化学性质采用两种方法来鉴别它们吗?
回答:用火烧变 黑的为铜,2Cu + O2 === 2CuO放入稀盐酸中,有气泡产生的是黄铜,
金属的化学性质
教学目标
1)知道铁、铝、铜等常见金属与氧气的反应
2)初步认识常见金属与盐酸、硫酸的置换反应,以及与盐溶液的置换反应,能用置换反应解释一些与日常生活有关的化学问题。3)能用金属活动顺序表对有关的置换反应进行判断,并能利用金属活动 顺序表解释一些与日常生活有关的化学问题。
教学重点、难点
金属活动性顺序
判断:由单质和化合物反 应,生成另外的单质和化合物的反应是否叫
置换反应?回答:不是,例如:
S + 2KNO3 + 3C == K2S + 3CO2 + N2
金属活动性顺序的应用1、位置越靠前,活动性越强
2、位 于氢前面的金属能置换出盐酸、稀硫酸中的氢
3、位于前面的金属能把位于后面的金属从它们化合物的溶液里置换
对金属活动性顺序的初步探究
鲁教版化学九年级下册金属的化学性质 第2课时 教案

【长话短说】过本节课的学习,你知道了金属的哪些化学性质?请将本节课的内容绘制成心智图
学生自主总结本节课的主要内容
将上一节课的内容同本节课的内容想联系,完成系统性知识体系
旧知回顾
引入正题
培养实验操作能力、观察能力、思维推理能力和同学间的合作使学生通过活动,自己发现金属活动性顺序,既有所获,又体验了成功的快感。
在讨论、交流中,吸取别人有益的意见,让不同的意识在碰撞中相互同化。创设轻松和谐的探究氛围,发展学生想象力,将真实事物以“图景“形式与学生的认知特点协调。
将所学知识运用的现实生活中,让学生来解决生活动的相关问题。
通过本节课的学习,你是否找到了鉴别真金和假黄金(铜锌合金)的另一种方法呢?
方法三:取少量硫酸铜溶液(或硝酸银溶液等,位置排在金前面锌后面的金属盐溶液均可)于试管中,将少量样品放入其中,若样品表面有红色物质生成,则是假黄金,无现象是真金。
生回顾,讨论、总结。
学生回答:实验现象
生分组实验,分工明确,观察现象,书写化学方程式,归纳结论。
实验
现 象
化学反应方程式
结论
铜丝浸入AgNO3溶液中
铜丝浸入AlCl3溶液中
铁丝浸入CuSO4溶液中(湿法炼铜)
【总结结论】
铜能把银从硝酸银的溶液中置换出来。
铜不能把铝从氯化铝的溶液中置换出来。
铁能把铜从硫酸铜的溶液中置换出来。
在金属活动性顺序表中,位置靠前的金属可以
把位于其后的金属从它们的盐溶液中置换出来
9.2金属的化学性质教案
学习
目标
1.探究金属与金属化合物溶液反应的条件,掌握判断金属活动性强弱的方法
2.能用金属活动性顺序对有关的置换反应进行简单地判断,并能利用金属活动性顺序解释一些与日常生活有关的化学问题。
九年级化学下册第九单元金属第二节金属的化学性质教案(新版)鲁教版

多媒体
课型
新授课
教法学法
讲授法
课时
第一课时
步骤
师生互动设计
二次备课
教学资源
1. 软硬件资源:实验室用具(试管、滴定管、酒精灯等),多媒体投影仪,白板,教学卡片,实验药品(金属铁、铜、锌等,稀盐酸,硫酸铜溶液等)。
2. 课程平台:人教版化学九年级下册教材,教学课件。
3. 信息化资源:在线化学知识库,实验视频,金属化学性质相关研究论文。
五、总结回顾(用时5分钟)
今天的学习,我们了解了金属的化学性质的基本概念、重要性和应用。同时,我们也通过实践活动和小组讨论加深了对金属化学性质的理解。最后,如果有任何疑问或不明白的地方,请随时向我提问。
知识点梳理
1. 金属的物理性质:金属的一般物理性质,如金属的导电性、导热性、延展性等。
2. 金属的化学性质:
a. 金属与氧气的反应:金属与氧气反应生成金属氧化物,如铁的氧化、铜的氧化等。
b. 金属与酸的反应:金属与酸反应生成盐和氢气,如铁与稀盐酸的反应、锌与硫酸的反应等。
c. 金属与盐溶液的反应:金属与盐溶液反应生成新的金属和盐,如铁与硫酸铜溶液的反应、铜与硝酸银溶液的反应等。
3. 金属的活动性:金属的活动性顺序,活泼金属与不活泼金属的区分,以及活动性对金属反应的影响。
答案的正确性:检查学生的作业答案是否正确,了解他们对金属的化学性质知识点的掌握程度。
解题过程:关注学生在解题过程中的思路和方法,评估他们的科学思维能力。
创新意识:鼓励学生在作业中展示自己的创新思维,如在解决问题时提出新的观点和方法。
作业态度:评估学生在完成作业时的态度,如是否认真、是否按时完成等。
板书设计
3. 学生可能遇到的困难和挑战:在本节课的学习中,学生可能会对金属与盐溶液的反应机理理解起来有困难,尤其是对于反应条件和反应速度的理解。此外,学生可能对实验结果的分析和解释感到挑战,需要教师给予具体的指导和鼓励。还有一些学生可能会对实验中出现意外情况感到困惑,教师需要提前准备,引导学生正确处理实验中的问题。
九年级化学全册 第九单元《金属》第二节 金属的化学性质(第2课时)教案 鲁教版
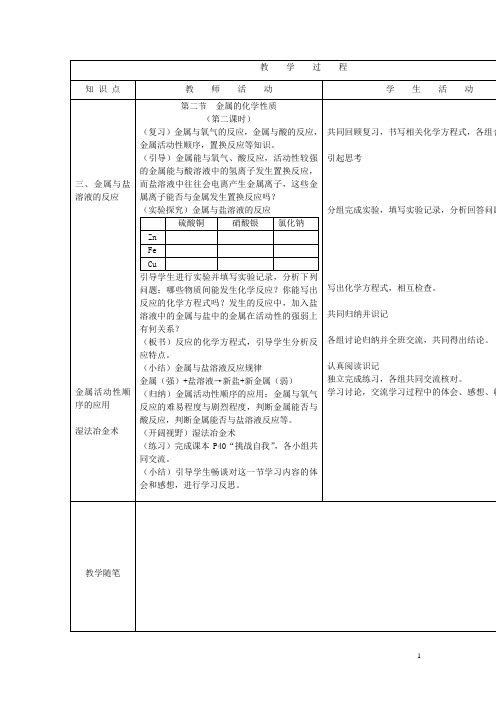
硫酸铜
硝酸银
氯化钠
Zn
Fe
Байду номын сангаасCu
引导学生进行实验并填写实验记录,分析下列问题:哪些物质间能发生化学反应?你能写出反应的化学方程式吗?发生的反应中,加入盐溶液中的金属与盐中的金属在活动性的强弱上有何关系?
(板书)反应的化学方程式,引导学生分析反应特点。
(小结)金属与盐溶液反应规律
金属(强)+盐溶液→新盐+新金属(弱)
(归纳)金属活动性顺序的应用:金属与氧气反应的难易程度与剧烈程度,判断金属能否与酸反应,判断金属能否与盐溶液反应等。
(开阔视野)湿法冶金术
(练习)完成课本P40“挑战自我”,各小组共同交流。
(小结)引导学生畅谈对这一节学习内容的体会和感想,进行学习反思。
共同回顾复习,书写相关化学方程式,各组合作检查。
引起思考
分组完成实验,填写实验记录,分析回答问题。
写出化学方程式,相互检查。
共同归纳并识记
各组讨论归纳并全班交流,共同得出结论。
认真阅读识记
独立完成练习,各组共同交流核对。
学习讨论,交流学习过程中的体会、感想、收获。
教学随笔
九年级化学全册 第九单元《金属》第二节 金属的化学性质(第2课时)教案 鲁教版
教 学 过 程
知 识 点
教 师 活 动
学 生 活 动
三、金属与盐溶液的反应
金属活动性顺序的应用
湿法冶金术
第二节 金属的化学性质
(第二课时)
(复习)金属与氧气的反应,金属与酸的反应,金属活动性顺序,置换反应等知识。
(引导)金属能与氧气、酸反应,活动性较强的金属能与酸溶液中的氢离子发生置换反应,而盐溶液中往往会电离产生金属离子,这些金属离子能否与金属发生置换反应吗?
鲁教版九年级下册化学 9.2金属的化学性质 教案设计

《金属的化学性质》教学设计一、教学目标知识与技能:(1)知道铁、铝、铜等常见金属与氧气的反应。
(2)初步认识常见金属与盐酸、硫酸的置换反应,以及与盐溶液的置换反应,能用置换反应解释一些与日常生活有关的化学问题。
(3)能用金属活动性顺序对有关的置换反应进行简单地判断,并能利用金属活动性顺序解释一些与日常生活有关的化学问题。
过程与方法:(1)体验和学习利用控制实验条件进行科学探究的方法,学会运用控制实验条件探究金属活动性顺序。
(2)学习通过对实验现象进行筛选、对比、归纳、分析、进行信息处理,获取科学结论的科学方法。
情感态度与价值观:(1)通过对五彩纷呈的化学现象的观察,激发学生的好奇心和求知欲,进一步激发学习化学的兴趣。
(2)培养学生的合作意识以及勤于思考、勇于创新实践、严谨求实的科学精神。
(3)了解化学与日常生活和生产的密切关系,提高学生解决实际问题的能力。
(4)在有趣的实验与老师的点拨中轻松掌握化学知识,体验到学习的快乐。
二、教学重难点:重点:金属活动性顺序的理解和应用难点:(1)用置换反应和金属活动性顺序判断反应能否发生。
(2)用置换反应和金属活动性顺序解释某些与生活有关的化学问题。
对实验事实进行筛选、分析、归纳、综合等科学方法的建构。
三、教学方法分析:实验探究法;多媒体辅助教学法;小组合作交流、讨论、归纳相结合的教学方法。
四、教学准备:多媒体课件、试管、镊子、酒精灯、坩埚钳、镁条、铝丝、锌粒、铜片、稀盐酸、稀硫酸五、教学过程设计:(第一课时)师生双边活动细目流程教师活动学生活动设计意图问题情景导入展示:金戒指,黄铜视频:不法分子以黄铜冒充黄金进行诈骗活动。
讨论:1.人们为何会上当2.现请你设计一个实验方案鉴别真假黄金。
【小结】前两种方法利用的是金属物理性质,后一种方法利用的是金属的化学性质。
【过渡】要想更好的使用金属,就需要了解金属的各种性质。
上节课我们学习了金属的物理性质,本节课我们来学习金属的化学性质。
最新鲁教版化学九年第二节《金属的化学性质》教案

最新鲁教版化学九年第二节《金属的化学性质》教案单元第二节金属的化学性质【教学目标】1、知识与技能:(1)、知道常见金属铝、铁、铜等常见金属与氧气的反应;(2)、初步认识常见金属铝、铁、铜等与盐酸、硫酸的反应;(3)、了解化合反应、分解反应、置换反应的区别,并能正确区分它们;(4)、培养学生实验、观察、分析、归纳的能力及解决实际问题的能力。
2、过程与方法(1)、通过对日常生活中有关现象的整理,了解金属与氧气的反应,并从中归纳出几种金属的活动性顺序。
(2)、通过知识的对比让学生初步掌握分析问题的能力以及交流协作能力。
(3)、引导学生主动参与知识的获取过程,学习科学探究的方法,培养学生科学探究的能力;通过实验和游戏培养学生团队合作精神。
3、情感态度与价值观(1)、通过对实验的探究、分析,培养学生严谨、认真、实事求是的科学态度。
(2)、使学生在实验探究、讨论中学会与别人交流、合作,增强协作精神。
【学情分析】在本课学习之前,学生已经学习了非金属元素氧、碳及化合物的知识,也对金属的性质有所了解,但知识体系不够完整。
通过本节内容的学习可对酸、碱、盐的知识加强巩固。
另外,本节内容贴近生活实际,可丰富学生的知识,开拓视野。
【重点、难点】重点是金属与氧气、酸的反应;金属活动性顺序及置换反应。
难点是引导学生主动参与对金属活动性顺序的探讨,学习科学探究的方法。
【教学方法】自主学习、问题引导、实验探究【教学准备】多媒体课件、被氧化的铝片、粘有铝粉的滤纸条、铜丝、坩埚钳、火柴、酒精灯、试管、试管架、镊子、镁条、锌粒、铁钉、铜片、稀盐酸、稀硫酸等第二节金属的化学性质一、金属与氧气的反应镁、铝比较活泼,铁、铜次之,金最不活泼二、金属与酸的反应1、活动性顺序:Mg>Zn>Fe>Cu2、置换反应。
鲁教版化学九年级下册 9.2《金属的化学性质》教案(1)

《金属的化学性质》教学设计
黄岛区博文中学
经过半年的学习,学生已经掌握了一定的化学知识和学习方法,可以在回顾联系所学知识的基础上拓展延伸新的内容。
金属的化学性质是第七单元的重点,而本节内容中的教学重点则是金属活动性顺序的理解与掌握,围绕研究金属活动性顺序,这节课主要研究了金属的前两个化学性质,即金属与氧气的反应和金属与酸的反应。
导入新课:本节课先展示几幅金项链金手镯图片,并观看新闻报道:某电视广告出售的黄金首饰经过实验验证不但不含金,还含有有害物质,长期佩戴对身体有害。
从而引入新课:要了解金属的化学性质,辨识生活中的一些现象。
讲金属与氧气的反应的时候,先回顾学过的铁镁等与氧气反应的实验现象,再由教师演示铝与氧气的反应,让学生进行对比分析,为金属的活动性顺序做准备!
讲金属与酸的反应的时候,先回顾金属与酸的反应,在此基础上提出问题:是不是所有的金属都能与酸反应,反应的剧烈程度一样吗?然后让学生带着问题进行实验探究,通过自己的动手操作,认真观察,讨论分析金属的活动性顺序!充分调动学生积极学习的兴趣,提高学生的自主学习能力!最后设计几个小问题对本节内容加以巩固!
本节课教学主要采用问题发现、主动探究、合作学习、讨论交流、实践应用的方式展开教学,培养学生的学习习惯和学习方法,充分尊重学生的主体地位,积极发挥教师的主导作用。
这就是我这节课的大致的设计思路,在我们同组老师的大力帮助下,才完成了这次教学任务,希望各位老师多多批评指正!。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
盐酸
稀硫酸
铁
铜
铝
2.在实验的基础上提出问题:
(1)哪些金属能与盐酸、稀硫酸发生反应?反应后生成了什么气体?哪些金属不能与盐酸、稀硫酸发生反应?
(2)比较三种金属分别与盐酸、稀硫酸反应的难易和剧烈程度,将三种金属的活动性按由强到弱的顺序进行排列。
3.引出金属活动性顺序:从以上实验可以看出,铁、铝能置换出盐酸或稀硫酸中的氢元素,而铜不能置换出酸中的氢元素。由此得出,这几种金属的活动性顺序:铁、铝比铜活泼。而铝跟酸反应比铁剧烈,则铝的活动性比铁强。
第二环节:实验探究几种金属与酸的反应
1.学生实验探究金属与酸的反应情况
实验目的:能否通过实验的方法比较镁、锌、铁、铜的金属活动性?
实验用品:铁丝、铜丝、铝条、稀盐酸、稀硫酸、试管
实验要求:每4名学生为一组,分工合作进行实验探究,并将全体学生分成A、B两大组
A组:取3支试管,分别加入一小段铁丝、铜丝、铝条,然后分别加入少量的稀盐酸(控制相似的实验条件,即保证同种酸的体积相同),仔细观察并记录实验现象,填写实验报告。
6.了解新金属材料的发展和改善金属材料性能的主要方法。
教学目标
知识与能力
1认识常见金属与盐酸、硫酸及与盐溶液的置换反应,并能解释日常生活中的一些现象。
2能说出常见金属的活动性顺序,了解金属活动性顺序的意义。
3通过我国古代湿法冶金术介绍,增强学生民族自豪感和爱国主义情感。
过程与方法
初步学会运用观察、实验等方法获取信息,能用文字、图表和化学语言表述有关信息,初步学会运用比较、分类、归纳、概括等方法对获取的信息加工使学生逐步形成良好学习习惯和方法。
2.引入新课:上节课,我们已经知道许多金属能跟氧气反应,如镁、铁、铝、铜等,不同的金属与氧气反应的难易和剧烈程度不同,不同金属在高温下的化学反应中表现出的活动性不同。
【说明:以情境引入课题,使学生感受到化学在实际生活中的应用,从而引发学生探求知识的欲望。同时既可以复习第一课时有关金属和氧气的反应知识,又可以引出金属的其它化学性质。】
板书设计
第二节金属的化学性质
一、金属与氧气的反应
二、金属与酸的反应
三、金属与盐的反应
教学过程:
第一环节:创设问题情境
1.设置问题:黄金饰品中的假货常常鱼目混珠,社会上有些不法分子时常以黄铜冒充黄金进行诈骗活动。因为黄铜(铜、锌合金)单纯从颜色、外型上看,与黄金极为相似,所以很难区分,现请你设计一个实验方案鉴别真假黄金。(学生一般从测密度、硬度、用火烧等方面回答。)
3
镁
双手紧掐颈部
翻白眼
Mg+H2SO4=MgSO4+H2↑
4
排名次的理由是:镁反应最快,在酸中呆的时间最短,名次最后;铜不反应,应得冠军。第四环节:实验探究金属与盐的反应
1.实验探究金属与盐的反应
实验目的:金属能否与盐溶液发生置换反应?
一、金属与氧气的反应
1铝和氧气的反应
反应方程式:
现象:剧烈燃烧,发出耀眼白光,放热,生成白色固体(同镁)
2铝的耐腐蚀性
36页多识一点
常温下铝与氧气反应生成氧化铝,形成致密坚硬的薄膜,组织内部铝被氧化,起到了保护作用。所以,铝制品具有良好的抗腐蚀性。
金属也能与稀酸反应,这节课我们将一起探究金属在溶液中的反应。
Fe + HCl — Fe + H2SO4—
Al + HCl — Al + H2SO4—
2.观察上述反应的化学方程式,分析这些反应有什么共同特点?
3.得出置换反应定义:由一种单质与一种化合物反应,生成另一种单质与另一种化合物,这类反应叫做置换反应。
4.强调:铁跟稀盐酸化亚铁,给人体补充铁元素,可以预防缺铁性贫血。
金属的化学性质
课题
第二节金属的化学性质
内容标准
1.区别金属和非金属,了解常见金属的主要性质和用途。
2.举出金属冶炼发展的历程对社会进步的作用及对环境影响的典型例子。
3.通过典型金属和酸以及某些盐的反应,认识金属活动性顺序。
4.说出腐蚀条件和防止金属腐蚀常用的方法。
5.说出废弃金属对环境的影响,形成自觉回收金属的意识。
【说明:在实验的基础上,根据实验事实,写出反应的化学方程式,并根据反应物、生成物的特点得出置换反应的定义。】
猜它是谁
教师:(设置游戏场景,有四个金属王国的“潜水运动员”要比赛潜水时间)学生分别装稀盐酸、稀硫酸设置“游泳池”。学生用肢体语言、表情、声音等表现比赛的过程,同组学生在纸上写出“运动员姓名”(金属名称)和潜水时的变化(化学方程式)。
【说明:学生亲眼看到了上述三种金属与酸反应的难易和剧烈程度不同,通过比较、讨论,容易认知这三种金属的活动性强弱,从而为后面给出金属活动性顺序打下基础。】
第三环节:活动天地
1.在上面的实验中,铁分别与盐酸、稀硫酸反应生成氯化亚铁,硫酸亚铁,并放出氢气;铝分别与盐酸、稀硫酸反应生成氯化铝、硫酸铝,并放出氢气。试写出这些反应的化学方程式。
人们经过长期的实践,总结出常见金属在溶液中的活动性顺序如下:
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
在金属活动性顺序中,金属的位置越靠前,它的活动性就越强;
学生讨论:金属活动顺序中为什么有氢的位置?有何作用?
排在氢前面的金属能与酸反应放出氢气,而排在氢后面的金属不能与酸反应放出氢气。
学生:(此时游戏化)各组学生用桌上的药品做实验,通过观察实验现象后讨论结论,并商量“表演方法”。
各组学生的表演形式不一样。现举一组学生表演例子:
运动员
肢体语言
表情
变化
名次
铜
摇晃、抖腿
冷笑
无气体产生
1
铁
耸肩、腿颤
皱眉、抽冷气
Fe+H2SO4=FeSO4+H2↑
2
锌
浑身乱晃
呲牙咧嘴
Zn+H2SO4=ZnSO4+H2↑
情感、态度、价值观
培养学生的合作意识以及勤于思考、严谨求实、勇于创新和实践的科学精神,培养学生辩证唯物主义观点,保持和增强对化学现象的好奇心和探究欲,发展学习化学的兴趣。
教学重点难点分析教法及学法
重点:金属活动性顺序
难点:置换反应
教法学法:
课前准备
本次教学需要演示实验器材:铝粉、滤纸、坩埚钳、酒精灯、火柴;分组实验器材:试管、锌片、铁丝、铜丝、铝条、稀盐酸、稀硫酸、硫酸铜溶液、硝酸银溶液、氯化钠溶液等。
