苯的取代反应实验
苯的结构和性质

CH2CH3 |
CH3 |
| CH3
甲苯(C7H8) 乙苯( C8H10) 对二甲苯(C8H10) 六甲基苯(C12H18)
苯环与侧链的相互影响将使苯的同系物 具有特性!
甲苯、二甲苯的化学性质实验
实验 实验现象 结论
(1)甲苯中滴加几 溶液褪色 甲苯易被氧化 滴高锰酸钾溶液 (2)二甲苯中滴加 溶液褪色 二甲苯易被氧化 几滴高锰酸钾溶液 (3)甲苯中滴加几 液体分层,上层 滴溴水 呈橙红色,下层 甲苯与溴不反应 几乎无色。
验 证
2、如何通过实验验证 这些结构是否合理?
……
P.66
实验现象 实验1 苯浮在水面上 高锰酸钾溶液不褪色 液体分两层,上层呈橙 红色,下层几乎无色 实验3 燃烧产生明亮火焰 并伴有浓黑烟 结论 苯不溶于水且比水轻 苯分子中不含C=C、 C ≡C
实验2
苯可燃烧,含碳量高
蛇形苯环图
凯库勒式提出:
1.苯是无色有特殊气味的液体 是一种重要溶剂. 2.苯的熔沸点低: 易挥发
3.密度比水小,不溶于水
二、苯的化学性质
1、苯的燃烧: 实验现象:火焰明亮且伴有黑烟。 ——与乙炔燃烧现象相同 2C6H6+15O2
点燃
12CO2+6H2O
不能与高锰酸钾溶液反应 ——与烷烃相似
动画模拟:苯与溴的反应
2、苯的取代反应:
Br Br Br Br
(2)苯的邻位二溴取代物的结构简式?
Br Br Br Br Br Br
小结: 能证明苯不是单双键交替结构的事实:
1、苯不能使酸性KMnO4溶液褪色、 苯也不能使溴水因反应而褪色 2、苯的邻位二元取代只有一种
Br Br
而一种凯库勒式有两种:
Br Br Br Br
苯环和二氯甲烷的傅克反应

苯环和二氯甲烷的傅克反应
苯环和二氯甲烷之间的傅克反应是有机化学中的一种重要反应,它通常在惰性溶剂中进行。
该反应的反应物是苯环(C6H6)和二氯甲烷(CH2Cl2),产物是1,1-二氯环己烷(C6H10Cl2)。
傅克反应是一种亲电取代反应,涉及到一个亲电试剂(这里是二氯甲烷)和一个芳香化合物(这里是苯环)之间的反应。
傅克反应通常需要催化剂存在,常用的催化剂包括氟化铯(CsF)或氟化银(AgF)等。
傅克反应的机理如下:
1. 初始阶段,催化剂(如氟化铯)使二氯甲烷发生亲电化,生成亲电试剂CH2Cl+。
2. 芳香环(苯环)中的π电子云与亲电试剂中的亲电中心(CH2Cl+)发生反应。
亲电试剂攻击苯环中的一个氢原子,形成一个过渡态。
3. 过渡态经历重排和亲核攻击的步骤,最终生成1,1-二氯环
己烷作为主要产物。
傅克反应是一种选择性较好的反应,通常只发生单取代。
此外,傅克反应对苯环上的取代基有一定的容忍性,因此可以应用于合成有机化合物的过程中。
需要注意的是,傅克反应是一个亲电取代反应,因此在实验条件下要注意反应的安全性和操作规范,避免对实验人员造成伤害。
同时,傅克反应的条件和反应物选择也需要根据具体的实验要求进行调整。
总结起来,苯环和二氯甲烷的傅克反应是一种重要的有机合成反应,通过亲电取代的机制在苯环上引入取代基。
这一反应对于有机化学合成和功能化合物的制备具有重要意义。
苯发生取代反应

苯发生取代反应引言:苯是一种重要的有机化合物,其具有稳定的芳香性质和特殊的反应性。
苯可以通过取代反应引入不同的基团,从而获得具有不同性质和用途的化合物。
本文将介绍苯发生取代反应的基本原理、常见的取代反应类型以及一些具体的例子。
一、苯发生取代反应的基本原理苯分子中的π电子云非常稳定,使得苯具有较高的芳香性。
然而,由于苯的芳香性质,苯分子的化学反应相对较难进行。
为了破坏苯分子的芳香性,需要引入一个具有较强电子亲和力的试剂,使其与苯发生反应。
这样,就可以实现苯的取代反应。
二、常见的苯取代反应类型1. 电子亲和性取代反应:在这种反应中,试剂中的取代基具有较强的电子亲和力,可以与苯分子中的π电子云结合。
常见的电子亲和性取代反应有硝化反应、卤代反应等。
2. 亲核取代反应:在这种反应中,试剂中的取代基具有亲核性,可以与苯分子中的正电荷结合。
常见的亲核取代反应有硝基取代反应、氨基取代反应等。
3. 自由基取代反应:在这种反应中,试剂中的取代基具有较强的自由基性质,可以与苯分子中的氢原子发生取代反应。
常见的自由基取代反应有氯代反应、溴代反应等。
三、具体例子1. 硝化反应:将苯与浓硝酸和浓硫酸混合加热,可使苯发生硝基取代反应,生成硝基苯。
反应方程式如下:苯+ HNO3 → 硝基苯 + H2O2. 卤代反应:将苯与溴或氯气反应,可使苯发生氯代或溴代反应,生成氯苯或溴苯。
反应方程式如下:苯+ Cl2 → 氯苯 + HCl苯+ Br2 → 溴苯 + HBr3. 氨基取代反应:将苯与氨气反应,可使苯发生氨基取代反应,生成苯胺。
反应方程式如下:苯+ NH3 → 苯胺结论:苯发生取代反应是有机化学中的重要反应之一。
通过取代反应,苯可以引入不同的基团,从而获得具有不同性质和用途的化合物。
硝化反应、卤代反应和氨基取代反应是苯取代反应中的常见类型。
通过了解苯发生取代反应的基本原理和具体例子,我们可以更好地理解和应用这一重要的有机化学反应。
首先亲电试剂E+进攻苯环

RCl + AlCl3
R+ + AlCl4-
RCH=CH2 + HF ROH + BF3
+
RCHCH3 + F-
+
ROHBF3
R+ + HOBF3-
+ CH3CH2)2 +
CH3
+ HNO3
H2SO4 30℃
CH3
CH3
NO2
+
NO2
邻硝基甲苯 对硝基甲苯
• 硝基甲苯继续硝化,可得到2,4,6-三硝基甲苯,即炸药TNT。
• 硝化反应中的亲电试剂是硝酰正离子NO2+。
HNO3 + H2SO4 H2O+NO2 + H2SO4
H2O+NO2 + HSO4NO2+ + H3O+ + HSO4-
• 亲电取代反应机理分两步:首先亲电试剂E+进攻苯环,形成π-络合物,进而生 成σ-络合物(碳正离子中间体)。
+ E+
快
E+ 慢
π-络合物
H +E σ-络合物
• 该碳正离子可用以下三个共振式来表示:
+H
H
H
H
E
E
E
+
+
E
• 反应机理第二步:试剂中的负离子从sp3杂化的碳原子上夺取一个质子而恢 复了闭合共轭离域体系,从而降低了体系的能量。
苯及其衍生物的化学性质
• 苯环是一个平面结构,离域的π电子云分布在环平面的上方和下方,它像烯烃中的π电子一样, 能够对亲电试剂提供电子,但是,苯环具有稳定的环状闭合共轭体系,难以被破坏,所以苯环 很难进行亲电加成反应,而容易进行亲电取代。
2020高二化学实验9苯的取代反应学案

苯的取代反应锥形瓶中滴加硝酸银溶液,将烧瓶中的液体倒入盛有少量水的烧杯中,观察现象什么现象说明发生了取代反应?导管口有白雾。
锥形瓶里滴入硝酸银溶液后生成浅黄色沉淀,说明苯跟溴反应时苯环上的一个氢原子被溴原子取代,生成溴化氢取出试管,将液体倒入盛有冷水的烧杯中,观察现象实验装置图实验现象整个烧瓶充满红棕色气体,在导管口有白雾;向锥形瓶滴加硝酸银溶液后有浅黄色沉淀生成;烧瓶里的液体倒入冷水烧杯中,烧杯底部有褐色不溶于水的液体生成反应后将试管中的液体倒入烧杯中后,烧杯底部有黄色油状物质出反应方程式注意事项①应用液溴,不能用溴水②要使用Fe 作催化剂,无催化剂不反应③锥形瓶中的导管不能插入液面以下,防止倒吸,因HBr 极易溶于水④一般发生一取代,溴苯是无色油状液体,密度比水大,实验中溶解了溴而呈褐色①试剂的加入顺序:浓硝酸、浓硫酸、苯②水浴加热,温度计插入水浴中,温度不能过高,控制在50~60℃即可,如超过70℃,则主要发生磺化反应生成苯磺酸③浓H2SO4 的作用:催化剂、吸水剂④纯硝基苯为无色、具有苦杏仁味的油状液体,其密度大于水。
实验中制备的硝基苯因溶解了NO2 呈黄色。
1.以下实验或操作能达到目的的是()A.乙烷中含有杂质乙烯,可用催化加氢的方式除去B.可以用溴水鉴别环己烷和苯C.可用酸性高锰酸钾溶液鉴别苯、环己烯、乙醇三种无色液体D.将无水乙醇与3mol ·L- 1H2SO4 混和共热至170℃制乙烯【答案】C【解析】A.乙烯在催化加氢过程中不能实现完全转化,故不能用催化加氢的方式除去,应用溴水除去,故错误;B.环己烷和苯都不与溴水反应,发生萃取时现象相同,故不能用溴水鉴别,故错误;C.环己烯不溶于水,故其与高锰酸钾溶液分层,振荡后溶液褪色;乙醇和高锰酸钾溶液不分层,振荡后溶液褪色;苯不溶于酸性高锰酸钾溶液,也不能使其褪色,故能鉴别,故正确。
D.无水乙醇与浓硫酸共热到170℃可以得到乙烯,3mol·L-1 H2SO4是稀硫酸,故不能达到目的。
04苯环上的取代反应
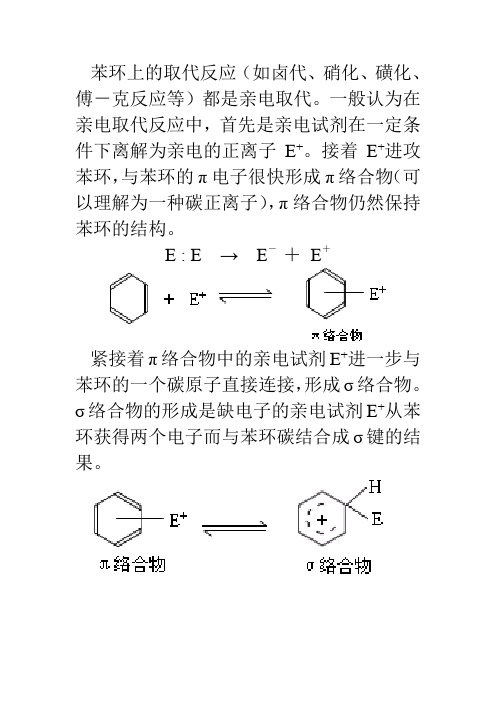
苯环上的取代反应(如卤代、硝化、磺化、傅-克反应等)都是亲电取代。
一般认为在亲电取代反应中,首先是亲电试剂在一定条件下离解为亲电的正离子E+。
接着E+进攻苯环,与苯环的π电子很快形成π络合物(可以理解为一种碳正离子),π络合物仍然保持苯环的结构。
E : E →E-+E+
紧接着π络合物中的亲电试剂E+进一步与苯环的一个碳原子直接连接,形成σ络合物。
σ络合物的形成是缺电子的亲电试剂E+从苯环获得两个电子而与苯环碳结合成σ键的结果。
此时,与亲电试剂E+形成σ键这个碳原子由sp2杂化轨道变成sp3杂化轨道,碳环上的π电子只剩下四个,即四个π电子分布在五个碳原子上。
所以碳环不再是原来的稳定的共轭体系,而是缺电子共轭体系。
这种缺电子共轭体系,有失去氢质子而恢复原来稳定的共轭体系的趋势。
σ络合物很快失去氢质子后,与亲电试剂E+形成σ键这个碳原子又由sp3杂化轨道变成sp2杂化轨道,恢复到了原来的稳定的共轭体系。
此反应历程可以用下面的式子表示:
综上所述,芳烃亲电取代反应历程可以表示如下:
现以苯的卤代为例分析亲电取代反应历程:
首先,在Fe或FeBr3存在下,Br2异裂为
Br+:
Br+进攻苯环形成π络合物,继而转化为σ络合物:
σ络合物中苯环脱去一个氢质子又恢复原来的稳定结构:
硝化反应中的亲电试剂为硝基正离子(NO2+),磺化反应中则为SO3H+,傅-克烷基化和酰基化反应中则为烷基正离子(R +)和酰基正离子(ROC+)。
由于烷基正离子有异构化为更稳定的C+的趋势,故当烷基化试剂中含有的碳原子个数超过3时,一般主要生成重排后的烷基衍生物。
苯环上取代反应的定位规则

苯环上原有的取代基对新导入取代基有影响,这种影响包括反应活性和进入位置两个方面。
通常,苯环上原有的第一取代基称为定位基,从大量实验事实的分析总结中发现,定位基的定位作用遵循一定的规律,这一规律称为苯环上亲电取代反应定位规律(又称定位规则)。
下面分别讨论定位基的类型;定位规则的理论解释;二元取代苯的定位规律;定位规律的应用。
(一)定位基的类型1.邻、对位定位基。
这类定位基的结构特征是定位基中与苯环直接相连的原子不含不饱和键(芳烃基例外),不带正电荷,且多数具有未共用电子对。
常见的邻、对位定位基及其反应活性(相对苯而言)如下:强致活基团:―NH2(―NHR,―NR2),―OH中致活基团:―OCH3(―OR),―NHCOCH3(-NHCOR)弱致活基团:―ph(―Ar),―CH3(-R)弱致钝基团:―F,―Cl,―Br,―I这类定位基多数使亲电取代反应较苯容易进行,但卤素例外。
2.间位定位基。
这类定位基的结构特征是定位基中与苯环直接相连的原子一般都含有不饱和键(-CX3例外)或带正电荷。
常见的间位定位基及其定位效应从强到弱顺序如下:―N+H3,―N+R3,―NO2,―CF3,―CCl3,―CN,―SO3H,―COH,―COR,―CO OH,―COOR,―CONH2等。
这类定位基属致钝基团,通常使苯环上亲电取代反应较苯难进行,且排在越前面的定位基,定位效应越强,反应也越难进行。
(二)定位规则的理论解释苯环上的取代反应是亲电取代反应。
因此,从反应活性的角度分析,凡有助于提高苯环上电子云密度的基团,就能使苯环活化,反应活性提高;反之,凡是使环上电子云密度降低的基团,就能使苯环钝化,反应活性降低。
从反应位置的角度分析,当苯环上没有取代基时,环上六个碳原子的电子云密度是均等的;但当苯环上有取代基时,由于取代基的电子效应沿着苯环共轭体系传递。
在环上出现了出现了电子云密度的疏密交替分布现象。
第二个取代基总是进入苯环上电子云密度相对较大的部位,从而使这些碳原子上的取代物占了多数。
苯环上取代反应的定位规则

苯环上原有的取代基对新导入取代基有影响,这种影响包括反应活性和进入位置两个方面。
通常,苯环上原有的第一取代基称为定位基,从大量实验事实的分析总结中发现,定位基的定位作用遵循一定的规律,这一规律称为苯环上亲电取代反应定位规律(又称定位规则)。
下面分别讨论定位基的类型;定位规则的理论解释;二元取代苯的定位规律;定位规律的应用。
(一)定位基的类型1.邻、对位定位基。
这类定位基的结构特征是定位基中与苯环直接相连的原子不含不饱和键(芳烃基例外),不带正电荷,且多数具有未共用电子对。
常见的邻、对位定位基及其反应活性(相对苯而言)如下:强致活基团:―NH2(―NHR,―NR2),―OH中致活基团:―OCH3(―OR),―NHCOCH3(-NHCOR)弱致活基团:―ph(―Ar),―CH3(-R)弱致钝基团:―F,―Cl,―Br,―I这类定位基多数使亲电取代反应较苯容易进行,但卤素例外。
2.间位定位基。
这类定位基的结构特征是定位基中与苯环直接相连的原子一般都含有不饱和键(-CX3例外)或带正电荷。
常见的间位定位基及其定位效应从强到弱顺序如下:―N+H3,―N+R3,―NO2,―C F3,―CCl3,―CN,―SO3H,―COH,―COR,―COOH,―COOR,―CONH2等。
这类定位基属致钝基团,通常使苯环上亲电取代反应较苯难进行,且排在越前面的定位基,定位效应越强,反应也越难进行。
(二)定位规则的理论解释苯环上的取代反应是亲电取代反应。
因此,从反应活性的角度分析,凡有助于提高苯环上电子云密度的基团,就能使苯环活化,反应活性提高;反之,凡是使环上电子云密度降低的基团,就能使苯环钝化,反应活性降低。
从反应位置的角度分析,当苯环上没有取代基时,环上六个碳原子的电子云密度是均等的;但当苯环上有取代基时,由于取代基的电子效应沿着苯环共轭体系传递。
在环上出现了出现了电子云密度的疏密交替分布现象。
第二个取代基总是进入苯环上电子云密度相对较大的部位,从而使这些碳原子上的取代物占了多数。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
[原理]
用铁作催化剂(实际起催化作用的是FeBr3,FeBr3由Fe与Br2反应生成),苯能跟溴发生反应,苯环里的氢原子能被溴原子取代生成溴苯。
[用品]
铁架台、烧瓶、导管、锥形瓶、苯、液溴
[操作]
(1)装置如图。
先检查装置的气密性。
在圆底小烧瓶里加入5mL苯和2mL液溴,轻轻振荡,使苯与溴混合均匀。
此时因无催化剂,苯与溴不发生反应。
(2)在混合液冷却后,将准备好的还原铁屑(约)或几枚去锈的小铁钉,迅速放入小烧瓶中,立即用带有长玻璃导管的单孔橡皮塞塞好。
一般情况下反应即可开始,液面上会有小气泡产生,随后反应逐渐剧烈,半分钟后液体呈沸腾状态。
在锥形瓶内导管口附近出现大量白雾(反应中生成的溴化氢溶于水而成的酸雾)。
锥形瓶中导管不插入液面以下,原因是避免锥形瓶中的水倒吸入烧瓶中。
(3)等反应结束后,先检验锥形瓶里的氢溴酸。
把锥形瓶里的液体在两支试管各倒少许,在其中一支试管中加入石蕊试液(会变红);另一支试管中滴入几滴AgNO3溶液(会有浅黄色的AgBr沉淀析出)。
Ag+ + Br- = AgBr↓
(4)把烧瓶里的液体倒入盛有冷水的烧杯里,在烧杯底部有红褐色不溶于水的液体,这就是反应中生成的溴苯。
纯净的溴苯是无色液体,制取时往往因溶解了少量的溴而呈红褐色。
可用水或10%NaOH溶液进行洗涤,洗去FeBr3和没有反应的溴,能够得到无色透明的油状液体。
[注意]
(1)装置的气密性必须良好。
(2)装置中跟烧瓶口垂直的一段导管,起导气兼冷凝作用,以防止溴和苯的蒸气挥发出来,减少苯和溴的消耗以及它们对环境的污染,所以它应有一定的长度,一般不小于25cm。
(3)在盛放液溴的试剂瓶中,液溴上面是一层溴的饱和水溶液,取用时必须将吸管插入下层液溴部分,以吸取纯溴。
所用的苯应用无水氯化钙干燥,所用的烧瓶和导管也应是干燥的。
否则反应比较困难,甚至不反应。
(4)这个反应是放热的,一般不需加热,如开始要加热时,只用热水浴微微加热(30~40℃)即可。
(5)此反应不宜太剧烈,如反应过于剧烈时,可把烧瓶浸在盛冷水的烧杯中冷却。
反应温度过高,会增加苯和溴的挥发和副反应的产物二溴苯的产量。
(6)为了防止反应进行得过于猛烈,所用铁屑不宜太细,更不宜用铁粉代替铁屑。
(7)液溴容易挥发,又有很强的腐蚀性,取用液溴时一定要注意安全,不要沾在手上。
最好戴上橡皮手套,在通风橱内取。
万一沾到皮肤上,应立即用水冲洗,再用酒精擦净,然后涂上甘油。
苯的硝化反应实验
①浓硫酸的作用:催化剂、吸水剂
②配制混合酸时,要将浓硫酸慢慢倒入浓硝酸中,并不断搅拌。
以减少浓硝酸的挥发与分解。
③浓硝酸和浓硫酸的混合酸要冷却到50~60℃以下,再慢慢滴入苯,边加边振荡,因为反应放热,温度过高,苯易挥发,且硝酸受热易分解,同时苯和浓硫酸在70~80℃时会发生反应。
④本实验采用水浴加热,温度计的水银球必须插入水浴中,水浴加热容易控制恒温,且易使被加热物受热均匀。
⑤什么时候采用水浴加热?需要加热,而且一定要控制在100℃以下,均可采用水浴加热。
如果超过100 ℃,还可采用油浴(0~300℃)、沙浴温度更高。
⑥使用带长导管的玻璃管,目的是使挥发出的反应物得到冷凝并使其流回到反应管中——冷凝回流。
(硝基苯的沸点:℃)
⑦不纯的硝基苯显黄色,因为溶有NO2。
提纯硝基苯的方法是:加入NaOH溶液,分液。
