高中化学双向细目表(精选.)
高中化学双向细目表【VIP专享】
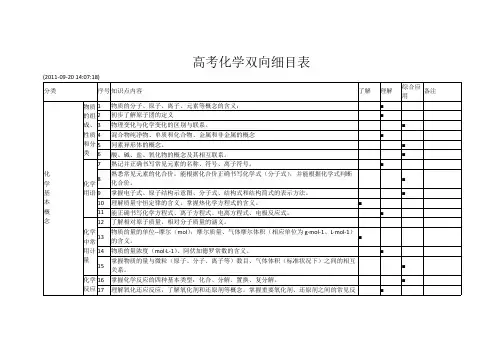
高考化学双向细目表(2011-09-20 14:07:18)分类序号知识点内容了解理解综合应用备注1物质的分子、原子、离子、元素等概念的含义;■2初步了解原子团的定义■3物理变化与化学变化的区别与联系。
■4混合物纯净物、单质和化合物、金属和非金属的概念 ■ 5同素异形体的概念。
■ 物质的组成、性质和分类6酸、碱、盐、氧化物的概念及其相互联系。
■ 7熟记并正确书写常见元素的名称、符号、离子符号。
■ 8熟悉常见元素的化合价。
能根据化合价正确书写化学式(分子式),并能根据化学式判断化合价。
■ 9掌握电子式、原子结构示意图、分子式、结构式和结构简式的表示方法。
■ 10理解质量守恒定律的含义。
掌握热化学方程式的含义。
■化学用语11能正确书写化学方程式、离子方程式、电离方程式、电极反应式。
■ 12了解相对原子质量、相对分子质量的涵义。
13物质的量的单位--摩尔(mol ),摩尔质量、气体摩尔体积(相应单位为g·mol-1、L·mol-1)的含义。
■14物质的量浓度(mol·L-1)、阿伏加德罗常数的含义。
■ 化学中常用计量15掌握物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)之间的相互关系。
■ 16掌握化学反应的四种基本类型:化合、分解、置换、复分解。
■化学基本概念化学反应17理解氧化还应反应,了解氧化剂和还原剂等概念。
掌握重要氧化剂、还原剂之间的常见反■应。
18能判断氧化还原反应中电子转移的方向和数目,并能配平反应方程式。
■与能量19了解化学反应中的能量变化,吸热反应、放热反应、反应热、燃烧热和中和热及新能源的开发等概念。
■20了解溶液的涵义■21了解溶液的组成,理解溶液中溶质的质量分数的概念。
■22了解饱和溶液、不饱和溶液的概念。
了解溶解度的概念。
了解温度对溶解度的影响及溶解度曲线。
■23初步了解结晶、结晶水、结晶水合物、风化、潮解的概念。
■溶液24了解胶体的概念及其重要性质和应用。
2023-2024学年第二学期高二年段期中六校联考双向细目表
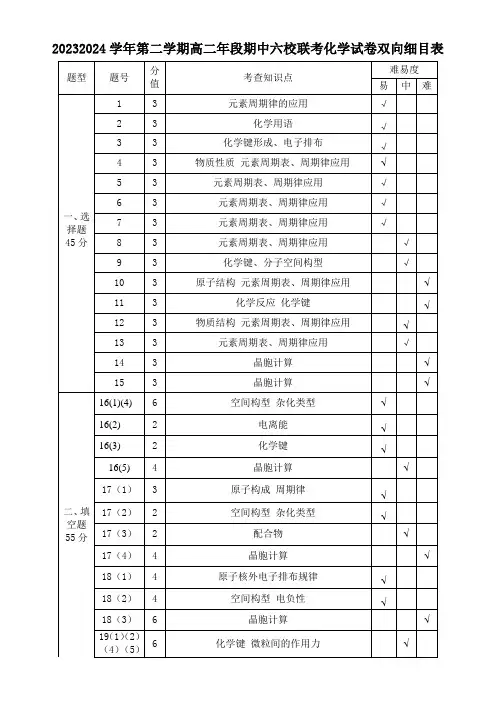
化学键
√
16(5)
4
晶胞计算
√
17(1)
3
原子构成 周期律
√
17(2)
2
空间构型 杂化类型
√
17(3)
2
配合物
√
17(4)
4
晶胞计算
√
18(1)
4
原子核外电子排布规律
√
18(2)
4
空间构型 电负性
√
18(3)
6
晶胞计算
√
19(1)(2)(4)(5)
6
化学键 微粒间的作用力
√
19(3)
2
电离方程式
√
20232024学年第二学期高二年段期中六校联考化学试卷双向细目表
题型
题号
分值
考查知识点
难易度
易
中
难
一、选择题
45分
1
3
元素周期律的应用
√
2
3
化学用语
√
3
3
化学键形成、电子排布
√
4
3
物质性质 元素周期表、周期律应用
√5Βιβλιοθήκη 3元素周期表、周期律应用
√
6
3
元素周期表、周期律应用
√
7
3
元素周期表、周期律应用
√
8
3
元素周期表、周期律应用
√
9
3
化学键、分子空间构型
√
10
3
原子结构 元素周期表、周期律应用
√
11
3
化学反应 化学键
√
12
3
物质结构 元素周期表、周期律应用
√
高中化学必修1双向细目表

22.硅、二氧化硅、硅酸盐
√
23、N2.NO2.HNO3
√
24.氨气、氨水、铵盐
√
25.次氯酸,浓硫酸,浓硝酸的强氧化性
√
必修1命题细目表
章
考点
认知能力
题号
题型
分值
预计
难度
实测难度
知道
了解理解Βιβλιοθήκη 应用必修1第一章1.化学实验安全
√
2.常见离子检验(Cl-、SO42-、CO32-、Al3+、Fe3+、NH4+)
√
3.分离提纯的方法(过滤、蒸发、蒸馏、萃取)
√
4.物质的量、阿伏伽德罗常数
√
5.配制一定物质的量浓度的溶液
√
6.物质的质量、摩尔质量、物质的微粒数、物质的量、气体摩尔体积、物质的量浓度等之间的关系
√
必修1第二章
7、物质的分类方法
√
8、胶体、丁达尔效应
√
9、离子反应
√
10、离子共存
√
11.氧化还原反应
√
12.举例说明生产、生活中常见的氧化还原反应
√
必修1第三章
13.钠、铝、铁、铜等金属及其重要化合物的物理性质
√
14.钠、铝、铁、铜等金属与氧气、水、酸、碱、盐溶液反应的共性和个性
√
15.氧化钠、氧化铝、氧化铁、氧化铜等金属氧化物与水、酸、碱溶液的反应
√
16.氢氧化铝、氢氧化铁、氢氧化亚铁的制备
√
17、碳酸钠、碳酸氢钠在水中的溶解性、热稳定性、与酸的反应,及它们的鉴别方法
√
18、Fe3+的氧化性;Fe3+和Fe2+之间的相互转化
√
必修1第四章
19、氯、氮、硫、硅等非金属及其重要化合物的物理性质
高中化学必修2双向细目表

17、乙烯的结构、性质、用途、加成反应
√
18、苯的结构、性质、用途
√
19、乙烯、氯乙烯、苯的衍生物在化工生产中的重要作用
√
20、乙醇的结构、性质、用途
√
21、乙酸的结构、性质、用途、酯化反应
√
22、糖类、油脂、蛋白质的组成、主要性质及其在日常生活中的应用
√
必修2第四章
23、金属的冶炼
√
24、海水资源的开发利用
√
必修2第二章
7、化学键与化学反应中的能量变化
√
8、吸热反应和放热反应
√
9、化学能与热能的相互转化在生产、生活中的实例
√
10、原电池的概念和原理
√
11、化学能与电能的转化关系及应用
√
12、化学电源
√
13、化学反应的速率
√
14、化学反应的限度
√
15、控制反应条件在生产和科学研究中的作用
√
必修2第三章
16、甲烷的结构、性质、用途、取代反应
√
25、高分子材料的合成(加聚反应)及在生活中的应用
√26、酸雨的防治√27、无磷洗涤剂的使用
√
28、合成新物质对人类生活的影响、绿色化学
√
必修2命题细目表
章
考点
认知能力
题号
题型
分值
预计
难度
实测难度
知道
了解
理解
应用
必修2第一章
1、原子结构(元素、核素、同位素、质量数涵义)
√
2、原子核外电子排布(1~18号元素的原子结构示意图)
√
3、元素周期律
√
4、元素周期表
√
5、化学键(离子键、共价键、离子化合物、共价化合物)
高三化学月考知识点双向细目表
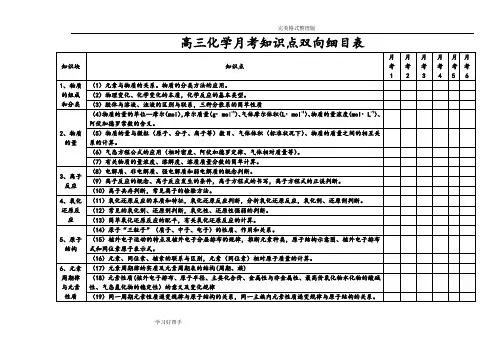
(47)合金的概念,能列举合金材料的重要应用
13、非金属及其化合物的性质
(48碳、硅及其重要化合物的性质。
(49)氯及其重要化合物的性质,卤素的性质递变。
(50)硫及其重要化合物的性质。
(51)氮及其重要化合物的性质。
(19)同一周期元素性质递变规律与原子结构的关系,同一主族内元素性质递变规律与原子结构的关系。
知识块
知识点
7、化学键与物质性质
(20)化学键的概念,离子键、共价键的概念和形成过程。
(21)共价键的强弱判断,键能、键长与分子稳定性的关系,共价键的极性、分子的的极性概念及判断。
(22)离子化合物、共价化合物判断,共价键的表示方法(电子式、结构式),离子键的表示方法(电子式),用电子式表示化合物的形成过程。
14.油脂的组成、结构与性质
15.氨基酸的组成、结构特点和主要化学性质,氨基酸与人体健康的关系。
16.蛋白质的组成、结构和性质。
四、合成高分子化合物
17.合成高分子的组成与结构特点,依据简单合成高分子的结构分析其链节和单体。
18.加聚反应和缩聚反应的特点。
19.新型高分子材料的性能及其在高新技术领域中的应用。
(58)合成高分子化合物的方法(加聚、缩聚),高分子材料的合成反应及单体判断。
知识块
知识点
15、化学实验
(59)化学实验室常用仪器的用途和使用方法。绘制和识别典型化学仪器装置图。实验室常用试剂的使用和保存方法。
(60)化学实验的基本操作方法。过滤和蒸发、蒸馏和萃取等分离和提纯原理、方法及实验注意事项。
9.烃类在有机合成和有机化工中的重要作用。
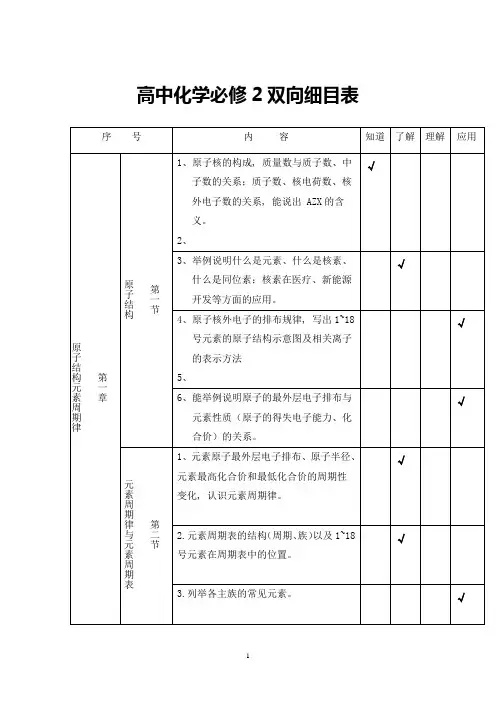
高中化学必修2双向细目表
√
3、主族元素在元素周期表中的位置、原子结构、元素性质三者之间的关系, 初步学会运用元素周期表。
4、
√
5、判断元素原子得失电子能力的方法, 并能进行简单应用。
6、
√
7、元素周期律和元素周期表对其他与化学相关的科学技术具有指导作用。
√
第二章
化学键化学反应与能量
第一节
化学与键与化学反应
1、 认识相邻原子间存在强烈的相互作用, 化学键的含义。
√
2.通过对甲烷燃烧、甲烷与氯气光照下反应等演示实验的观察、思考、分析、推论, 引导学生掌握甲烷的化学性质, 知道甲烷与氯气的反应属于取代反应。
√
3.学会书写1—5个碳原子烷烃的结构式、结构简式, 了解同分异构现象, 能写出丁烷和戊烷的同分异构体的结构简式。
√
4、以甲烷为例, 认识有机化合物分子具有立体的结构, 初步培养学生空间想象能力。
√
第二节
化学反应的快慢和限度
1.了解化学反应速率的概念;知道浓度、温度和催化剂对化学反应速率的影响。
√
2.知道什么是可逆反应;了解化学平衡的特征, 建立化学平衡的观点。
√
3.知道外界条件会改变化学平衡状态。并能说明改变反应条件对化学反应的调控作用。
√
4.化学平衡状态的标志及判断方法。
√
第三节
化学反应的利用
高中化学必修2双向细目表
序号
内容
知道
了解
理解
应用
第一章
原子结构元素周期律
第一节
原子结构
1、原子核的构成, 质量数与质子数、中子数的关系;质子数、核电荷数、核外电子数的关系, 能说出 AZX的含义。
2、
√
高中化学双向细目表
高中化学双向细目表高考化学双向细目表分类序号知识点内容1 物质的组成、性质和分类2 化学基本概念3 物质的分子、原子、离子、元素等概念的含义;初步了解原子团的定义4 物理变化与化学变化的区别与联系5 混合物、纯净物、单质和化合物、金属和非金属的概念6 同素异形体的概念7 酸、碱、盐、氧化物的概念及其相互联系8 熟记并正确书写常见元素的名称、符号、离子符号9 熟悉常见元素的化合价;能根据化合价正确书写化学式(分子式),并能根据化学式判断化合价10 掌握电子式、原子结构示意图、分子式、结构式和结构简式的表示方法;理解质量守恒定律的含义;掌握热化学方程式的含义11 能正确书写化学方程式、离子方程式、电离方程式、电极反应式12 了解相对原子质量、相对分子质量的涵义13 掌握物质的量的单位--摩尔(mol),摩尔质量、气体摩尔体积(相应单位为g·mol-1、L·mol-1)的含义14 物质的量浓度(mol·L-1)、阿伏加德罗常数的含义15 掌握物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)之间的相互关系16 掌握化学反应的四种基本类型:化合、分解、置换、复分解17 理解氧化还原反应,了解氧化剂和还原剂等概念;掌握重要氧化剂、还原剂之间的常见反应18 能判断氧化还原反应中电子转移的方向和数目,并能配平反应方程式19 了解化学反应中的能量变化,吸热反应、放热反应、反应热、燃烧热和中和热及新能源的开发等概念20 了解溶液的涵义21 了解溶液的组成,理解溶质的质量分数的概念22 了解饱和溶液、不饱和溶液的概念;了解溶解度的概念;了解温度对溶解度的影响及溶解度曲线23 初步了解结晶、结晶水、结晶水合物、风化、潮解的概念24 了解胶体的概念及其重要性质和应用25 了解原子的组成及同位素的概念26 掌握原子序数、核电荷数、质子数、中子数、核外电子数,以及质量数与质子数、中子数之间的相互关系注:综合应用部分不在此表中列出。
高中化学选修4双向细目表
10、酸碱中和滴定
√
第四章 电化学基础
1、原电池原理、电极反应式和总反应方程式的书写
√
2、常见化学电源的种类、原理
√
3、电解池原理、电极反应式和总反应方程式的书写
√
4、电解在氯碱工业、精炼、电镀、电冶金等方面的应用
√
5、化学腐蚀和电化学腐蚀原因,危害
√
6、防止金属腐蚀的措施、原理
√
高中化学选修四双向细目表
章节
考点
认知能力
了解
理解
应用
第一章化学反应与能量
1、焓变和反应热的含义
√
2、热化学方程式的含义
√
3、正确书写热化学方程式
√
4、盖斯定律
√
5、运用盖斯定律进行有关反应热的计算
√
第二章化学反应速率和化学平衡
1、化学反应速率的概念、计算、测定
√
2、活化能的概念,催化剂的重要作用
√
3、温度、浓度、压强和催化剂对化学反应速率影响
√
4、化学反应的可逆性及化学平衡的建立
√
5、化学平衡的特征
√
6、化学平衡常数
√
7、化学平衡常数及反应物的转化率的相关计算
√
8、温度、浓度和压强对化学平衡的影响
√
9、用勒夏特列原理分析化学平衡移动
√
10、化学反应速率和化学平衡的调控在生活、生产和科学研究领域中的重要作用
√
11、利用焓变和熵变说明化学反应的方向
√
第三章水溶液中的离子平衡
1、强电解质、弱电解质的概念
√
2、电解质在水中的电离以及电解质溶液的导电性
√
3、水的电离,离子积常数√4、液pH的含义及测定方法√
高考化学必考知识点双向细目表
高考化学必考知识点双向细目表分类序号知识点内容近三年高考再现化学基本概念物质的组成、性质和分类1物质的分子、原子、离子、元素等概念的含义;17 18 193物理变化与化学变化的区别与联系。
28盐类反应中的基础涉及84混合物纯净物、单质和化合物、金属和非金属的概念5 同素异形体的概念。
6酸、碱、盐、氧化物的概念及其相互联系。
化学用语7熟记并正确书写常见元素的名称、符号、离子符号。
熟悉常见元素的化合价。
能根据化合价正确书写化学式(分子式),并能根据化学式判断化合价。
8,综合化合价,共价键主要考C族元素27,综合元素周期律68熟悉常见元素的化合价。
能根据化合价正确书写化学式(分子式),并能根据化学式判断化合价。
掌握电子式、原子结构示意图、分子式、结构式和结构简式的表示方法。
能正确书写化学方程式、离子方程式、电离方程式、电极反应式。
化学中常用计量12了解相对原子质量、相对分子质量的含义。
11,综合原子结构中等6,氧化还原涉及简单13物质的量的单位--摩尔(mol),摩尔质量、气体摩尔体积(相应单位为g·mol-1、L·mol-1)。
14物质的量浓度(mol·L-1)、阿伏加德罗常数。
15掌握物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)之间的相互关系。
化学反应与能量16掌握化学反应的四种基本类型:化合、分解、置换、复分解。
12氧化还原、物质的量、化学计算中等26题一问6,综合部份物质的量计算,主要得失电子守恒、部份氧化还原,中上13题氧化与离子综合10,得失电子守恒,方程式配平17理解氧化还应反应,了解氧化剂和还原剂等概念。
掌握重要氧化剂、还原剂之间的常见反应。
18能判断氧化还原反应中电子转移的方向和数目,并能配平反应方程式。
19了解化学反应中的能量变化,吸热反应、放热反应、反应热、燃烧热和中和热及新能源的开发等概念。
26,热方程,反应热7分11热化学书写反应热,中等7热化学书写反应热,中等溶液20 了解溶液的含义8涉及21 了解溶液的组成,理解溶液中溶质的质量分数的概念。
高考化学知识点双向细目表
分类 序号
知识点内容
了解 理解 掌握
1 分子、原子、离子、元素等概念的含义;
√
物质的组 成、性质
和分类
2 原子团的定义 3 物理变化与化学变化的区别与联系。 4 混合物和纯净物、单质和化合物、金属和非金属的概念 5 同素异形体的概念。
√ √ √
√
6 酸、碱、盐、氧化物的概念及其相互联系。
√
51 离子反应的概念、离子反应发生的条件。常见离子的检验。
√
52 难溶电解质的沉淀溶解平衡及沉淀转化的本质(不要求计算)。
√
以上各部分知识的综合应用
综合 应用
√ √ √
√ √ √ √ √
√
题型 选择题 填空题
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√
√ √
√
√
√
√ √ √
√ √
√
√
√
√
√
√
√
√
√ √ √
√
√ √
√
34
能源是人类生存和社会发展的重要基础。化学在解决能源危机中的重要 作用。
√
35 原电池和电解池的工作原理。常见电源的种类及其工作原理。
√
36 写出电极反应和电池反应方程式。
37 金属发生电化学腐蚀的原因,金属腐蚀的危害,防止金属腐蚀的措施。
√
38 化学反应速率的概念、反应速率的定量表示方法。
√
39 催化剂在生产、生活和科学研究领域中的重大应用。
√
7 熟记并正确书写常见元素的名称、符号、离子符号。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4、原子核结构,理解质量数的含义,构成原子的微粒间的关系,元素、核素、同位素的涵义
√
第二节
元素周期律
1、原子核外电子的排布规律,1~20号元素的原子结构示意图;原子最外层电子排布与元素的原子得失电子能力和化合价的关系
√
2、元素原子核外电子排布,原子半径,主要化合价的周期性变化。
√
3、第三元素和ⅰA族,ⅶA族元素为例,掌握同周期,同主族元素性质的递变规律,并能运用原子结构理论初步解释这些递变规律
√
2、浓度、温度、固体的表面积、催化剂等条件对化学反应速率的影响
√
3、建立化学平衡的观点
√
4、理解化学平衡的特征
√
5、几种化学反应进行限度的因素
√
6、区分某条件对化学反应速率和可逆反应的方向性。
√
第三章有机化合物
第一节
最简单的有机化合物——甲烷
1、明确什么是有机化合物,理解有机化合物种类繁多、数量巨大的原因,体会到有机物对人们的生产、生活的影响
√
3、认识石油的成分,石油分馏、裂化和裂解的基本原理,石油分馏和裂解的产品和用途,乙烯的加聚反应
√
4、理解加聚反应的概念和原理,能够书写常见的加聚反应方程式
√
5、造成环境污染的主要原因,常见污染物及治理措施。绿色化学的原理和意义,认识环境和人类生存发展的密切关系,增强环保意识,树立可持续发展意识
√
最新文件仅供参考已改成word文本。方便更改
第一节
化学能与热能
1、断裂化学键要吸收能量,生成化学键要放出能量
√
2、化学能和热能是相互转化的,并且符合能量守恒
√
3、什么是吸热反应和放热反应,并通过实验亲身体验放热反应和吸热反应,记住常接触的化学反应中哪些是放热反应,哪些是吸热反应。
√
4、物质变化和能量变化是普遍存在的,它们符合质量守恒和能量守恒定律
√
第二节
化学能与电能
1、火力发电中的能量转化
√
2、原电池的原理
√
3、氧化还原反应是使化学能转换为电能的关键
√
4、通过对原电池装置的分析,掌握原电池正、负极判断方法
√
5、通过原电池装置来判断金属的活动性顺序
√
6、几种发展中的化学电源
√
7、学会自己设计原电池
√
第三节
化学反应的速率和限度
1、化学反应速率的涵义及表示方法,并能进行化学反应速率的简单计算
√
2、甲烷的组成和物理性质,掌握甲烷的正四面体结构和化学性质
√
3、烷烃的物理性质及其性质的变化规律,烷烃的结构、性质和烷烃的命名方法
√
4、取代反应,同分异构现象和同分异构体
√
第二节
来自石油和煤的两种基本化工原料
1、石油的分馏及其产品和用途,石油的裂化和裂解
√
2、煤的干馏和综合利用
√
3、煤、石油的组成和石油产品、煤干馏产品的广泛用途
√
4、乙烯、苯的组成和结构特征,和它们的主要性质
√
5、乙烯的物理性质和主要用途,和实验室制法
√
6、掌握苯的结构式及其重要的化学性质,了解苯及其同系物在组成、结构、性质上的异同
√
7、初步学会烃的有关简单计算
√
第三节
生活中两种常见的有机物
1、乙醇的物理性质,乙酸和乙酸乙脂的物理性质
√
2、乙醇的生理作用和工业制法
√
第四章
化学与可持续发展
第一节
开发利用金属矿物和海水资源
1、了解金属冶炼的一般原理,理解金属冶炼方法的选择同金属活动性的关系,了解常见金属的冶炼方法
√
2、了解金属回收的重要意义,树立资源保护,环境保护的意识
√
3、海水中微量元素的存在和应用,以及对工业生产和高科技领域的潜在价值,认识综合开发利用海水资源的重要意义
√
3、理解乙醇的结构,通过分析乙醇的结构式掌握乙醇在发生化学反应时的断键位置,从而推断乙醇所具有的化学性质
√
4、乙酸的物理性质以及它与人们生活的关系
√
5、通过分析乙醇和乙酸的结构式,掌握它们发生脂化反应的原理以及实验的操作方法,分析实验现象,会熟练地书写该化学方程式
√
6、了解乙酸的通性,并通过设计实验来验证次氯酸、碳酸和乙酸的酸性强弱顺序
√
4、掌握蒸馏法淡化海水的原理及操作,通过对海水中提取溴、碘等知识的学习,进一步学习卤族单质和其化合物的性质,同时学会应用氧化还原原理设计实验探究物质氧化性或还原相对强弱的方法
√
第二节
化学与资源综合利用、环境保护
1、了解煤的组成及煤包含的元素种类,了解煤的综合利用的途径
√
2、了解煤干馏的原理和煤干馏的产物极其主要用途
√
4、原子结构、元素性质及该元素在周期表中的位置三者间的关系,学会运用周期表
√
第三节
化学键
1、化学键的含义及离子键和共价键的形成,进一步认识物质的构成
√
2、离子化合物和共价化合物的概念,能区分离子化合物和共价化合物
√
3、书写常见简单化合物、单质的电子式;能用电子式表示简单物质的形成过程
√
第二章
化学反应与能量
√
7、掌握乙酸的分子结构和化学性质,了解乙酸的用途、制法等
√
第四节
基本营பைடு நூலகம்物质
1、油脂的组成、结构、重要性质和用途,酯和油脂的联系和区别
√
2、油脂的应用,肥皂和硝化甘油等日常生活中的知识
√
3、掌握糖类的主要代表物的组成和性质,了解淀粉、纤维素的组成和性质
√
4、掌握蛋白质的基本性质,认识蛋白质是生命现象最基本的物质基础
高中化学必修2双向细目表
序 号
内 容
知道
了解
理解
应用
第一章
物质结构元素周期律
第一节
元素周期表
1、元素周期表的结构以及周期、族等概念
√
2、原子结构与元素在周期表中位置间的关系
√
3、通过对碱金属、卤族元素性质的探究,理解元素性质与原子结构以及元素在周期表中的位置的相互关系,掌握碱金属和卤族元素的相似性和递变性
