人教版高一化学必修一金属及其化合物知识点总结
高中化学必修一第三章金属及其化合物知识点总结

一、钠及其化合物K钠2、氧化钠以及过氧化钠第1页共7页第2页共7页3、碳酸钠以及碳酸氢钠第3页共7页(1)除杂问题1、NeuCO,固(NaHCO,固):加热【ZNaHCOFNeuCa+lLO+CO? f 】2、NmCO,溶液(NaHCOj:适量氢氧化钠【NaHg+NaOHuNmCOs+ILO】3、NaHCOs 溶液(Na2C05):通入过量C()2【Na2C0s+C03+H30=2NaHC0s ](2 )、如何鉴别Na2CO3和NaHCOs两种溶液?1、溶解量的多少:N Q CO S比NaHCOs易溶于水;2、温度变化:N&2C03溶于水比NaHCOs放出热量多;3、比较碱性强弱:分别加入几滴酚酿,看溶液变红的程度,更红的是NH2C03;4、加热固体:NaaCOs稳定,NaHCOs受热易分解产生C02;5、加入稀HC1: Nd2CO3的反应速率比NaHCOs慢;6、配成溶液滴加入SC12溶液:有沉淀生成的是Na2C03o(不可用Ca(OH)2或Ba(0H)2)二、焰色反应实验步骤:洗、烧、蘸、烧、观简要记忆步骤:用洁净的钳丝先蘸点盐酸灼烧,再蘸点待测溶液灼烧,观察现象。
第4页共7页钠:黄色火焰钾:(透过蓝色钻玻璃)紫色火焰三、铝及其化合物仁铝(两性金属)2、氧化铝(两性氧化物)3、氢氧化铝(两性氢氧化物)4、铝盐第5页共7页净水作用A1"+3H2O=A1(OH)3+3H+明矶与水反应生成的氢氧化铝胶体具有吸附性,吸附水中的悬浮物而使其下沉5、铝三角匚A1(OH)3->A1 卄:A1(OH)3+3H+=A13++3H2O匚A F+T A1(OH)3 : AP++ 3NH3 H2O== Al(OH)"+3NELrAI3>3OH =A1(OH)31【少量强碱】Al卄:OH = 1:3AI3++3A1O2+6H2O=4A1(OH)31 (A严与AKh•不能共存)rAl(OH)3->AlO2: Al(OH)j+OH =AIO2+2H1OrA1O2- ->A1(OH)3: A1O2 +H*+H2O=AI(OH)31【少量强酸】(A1O2 与FT不能大量共存)匚AKh JA1 卄:A1O2+4H*=A13*+2H2O【过量强酸】A严:H*=l:4LA13+->A1O2 : A13++4OH =AIO2+2H2O【过量强碱】Al3* : OH = 1:4四、铁及其化合物K铁铁在地壳中的含量仅次于氧、硅、铝,居第四位。
高一化学金属及其化合物知识点总结

高一化学金属及其化合物知识点总结高一化学金属及其阴离子知识点总结高一化学金属及其化合物知识点总结1.特质的存在形式有两种:游离态和化合态。
(1)钠镁铬只以化合态形式存在:钠元素的主要存在形式是氯化钠,镁元素的存在形式有菱镁矿,铝元素的缺少存在形式有铝土矿。
(2)铁元素有四种存在形式:游离态的陨铁和化合态的铁矿石。
2.金属单质的用途:(1)利用钠元素的特征焰色(黄色)制高压钠灯,高压钠灯的透雾力强,可以做航标灯;利用钠单质的熔点低等,钠钾合金常温下呈液态,做原子反应堆的导热剂;利用钠单质制备过氧化钠,利用钠单质还原熔融态铋的四氯化钛制备金属钛。
(2)镁条燃烧发出耀眼的白光,用来做照明弹。
(3)利用铝的良好导电性,做导线。
利用铝块和铝粉的颜色都是暗红色,铝粉制成银粉(白色涂料)。
3.金属化合物的用途:(1)硫酸钡做漂白剂,过氧化钠做水下作业、坑道下作业的供氧剂;氯化钠、碳酸钠、醋酸做食品添加剂;氯化钠原料做为制备单质钠和氯气的加工,氯化钠做为提纯氢氧化钠、氢气、氯气的原料。
(2)氧化镁的熔点高,做耐高温的材料:耐火管、耐火坩埚、耐高温的实验仪器。
(3)明矾做净水剂。
4.金属的分类:(1)根据冶金工业标准分类:铁(铬、锰)为黑色金属,其余金属(钠镁铝等)为有色金属。
(2)根据密度分类:密度大于 4.5g/cm3的金属是重金属:如铁、铜、铅、钡,密度小于4.5g/cm3的金属是轻金属:如钠、镁、铝。
5.氧化物的分类:二元化合物,其中第三种元素是氧元素,并且氧元素呈负二价的化合物是氧化物。
(1)氧化物(根据氧化物中澳氧元素的混合物种类)分为金属氧化物和非金属氧化物。
(2)金属氧化物归为酸性氧化物、碱性氧化物、两性氧化物。
(3)非金属氧化物归为酸性氧化物、不成盐氧化物。
(4)氧化物(根据氧化物是否与碱或酸反应生成盐)分为成盐氧化物和不成盐氧化物(CO、NO)。
(5)成盐氧化物分为酸性氧化物、碱性氧化物、两性氧化物。
人教版高中化学必修一第三章金属及其化合物知识点总结,文档

高一化学金属及其化合物知识点总结1.元素的存在形式有两种:游离态和化合态。
1〕钠镁铝只以化合态形式存在:钠元素的主要存在形式是氯化钠,镁元素的存在形式有菱镁矿,铝元素的存在形式有铝土矿。
2〕铁元素有两种存在形式:游离态的陨铁和化合态的铁矿石。
2.金属单质的用途:1〕利用钠元素的特征焰色〔黄色〕制高压钠灯,高压钠灯的透雾力强,可以做航标灯;利用钠单质的熔点低,钠钾合金常温下呈液态,做原子反响堆的导热剂;利用钠单质制备过氧化钠,利用钠单质复原熔融态的四氯化钛制备金属钛。
2〕镁条燃烧发出耀眼的白光,用来做照明弹。
〔3〕利用铝的良好导电性,做导线。
利用铝块和铝粉的颜色都是银白色,铝粉制成银粉〔白色涂料〕。
3.金属化合物的用途:1〕过氧化钠做漂白剂,过氧化钠做水下作业、坑道下作业的供氧剂;氯化钠、碳酸钠、碳酸氢钠做食品添加剂;氯化钠做为制备单质钠和氯气的原料,氯化钠做为制备氢氧化钠、氢气、氯气的原料。
2〕氧化镁的熔点高,做耐高温的材料:耐火管、耐火坩埚、耐高温的实验仪器。
3〕明矾做净水剂。
4.金属的分类:1〕根据冶金工业标准分类:铁〔铬、锰〕为黑色金属,其余金属〔钠镁铝等〕为有色金属。
2〕根据密度分类:密度大于3的金属是重金属:如铁、铜、铅、钡,密度小于3的金属是轻金属:如钠、镁、铝。
5.氧化物的分类:二元化合物,其中一种元素是氧元素,并且氧元素呈负二价的化合物是氧化物。
1〕氧化物〔根据氧化物中非氧元素的种类〕分为金属氧化物和非金属氧化物。
2〕金属氧化物分为酸性氧化物、碱性氧化物、两性氧化物。
3〕非金属氧化物分为酸性氧化物、不成盐氧化物。
〔4〕氧化物〔根据氧化物是否与碱或酸反响生成盐〕分为成盐氧化物和不成盐氧化物〔CO、NO〕。
5〕成盐氧化物分为酸性氧化物、碱性氧化物、两性氧化物。
6〕酸性氧化物分为高价态的金属氧化物〔Mn2O7〕和非金属氧化物〔CO2〕。
7〕碱性氧化物只能是金属氧化物〔CaO〕。
〔8〕两性氧化物只能是金属氧化物〔Al2O3、ZnO〕。
高一人教版化学必修一知识点:第三章 金属及其化合物

高一人教版化学必修一知识点:第三章金属及其化合物
高一人教版化学必修一知识点:第三章金属及
其化合物
化学与人类进步和社会发展的关系非常密切,它的成就是社会文明的重要标志。
查字典化学网为大家推荐了高一人教版化学必修一知识点,请大家仔细阅读,希望你喜欢。
一、金属活动性
K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb>(H>)Cu>Hg>Ag>Pt>Au
二、金属一般比较活泼,容易与O2反应而生成氧化物,可以与酸溶液反应而生成H2,特别活泼的如Na等可以与H2O 发生反应置换出H2,特殊金属如Al可以与碱溶液反应而得到H2。
三、 Al2O3为两性氧化物,Al(OH)3为两性氢氧化物,都既可以与强酸反应生成盐和水,也可以与强碱反应生成盐和水。
四、Na2CO3和NaHCO3比较
碳酸钠碳酸氢钠
俗名纯碱或苏打小苏打
色态白色晶体细小白色晶体
水溶性易溶于水,溶液呈碱性使酚酞变红易溶于水(但比Na2CO3溶解度小)溶液呈碱性(酚酞变浅红)
热稳定性较稳定,受热难分解受热易分解
2NaHCO3 Na2CO3+CO2↑+H2O。
人教版高一化学金属及其化合物知识点总结

金属及其化合物1.金属原子的最外层电子排布特点(金属原子最外层电子数较少。
易失去最外层电子。
)2.在物理性质上金属有哪些共性?(常温下除汞外均为晶体,有金属光泽,是热、电的良导体,大多有良好的延展性。
)3.金属的化学性质(1)金属与氧气的反应①钠与氧气反应---常温:4Na + O2错误!未找到引用源。
2Na2O加热:2Na + O2△Na2O2;所以Na应保存在煤油中②铝与氧气反应:通常与氧气易反应,生成致密的氧化物起保护作用4Al + 3O2错误!未找到引用源。
2Al2O3加热铝箔时,由于外层氧化膜的熔点比铝的熔点高,故熔化的液态铝并不滴落。
除去氧化膜的铝箔加热很快生成新的氧化膜,熔化的液态铝并也不滴落。
③铁与氧气反应:3Fe + 2O2点燃Fe3O4(Fe2O3·FeO)(2)金属与水的反应①钠与水反应:2Na + 2H2O 错误!未找到引用源。
2NaOH + H2↑;实验现象:钠浮在水面上,熔成小球,在水面上游动,有哧哧的声音,最后消失,在反应后的溶液中滴加酚酞,溶液变红。
②铝与水反应:加热时微弱反应③铁与水反应:高温与水蒸气反应3Fe + 4H2O(g) 高温 Fe3O4+ 4H2↑。
(3)金属与酸的反应①钠与酸反应:如2Na + 2HCl 错误!未找到引用源。
2NaCl + H2↑,Na放入稀盐酸中,是先与酸反应,酸不足再与水反应。
因此Na放入到酸中Na是不可能过量的。
比钠与水的反应剧烈多。
②与酸反应:强氧化性酸,如浓硫酸和浓硝酸在常温下,使铝发生钝化现象;加热时,能反应,但无氢气放出;非强氧化性酸反应时放出氢气。
③与酸反应:强氧化性酸:常温下浓硫酸和浓硝酸使铁钝化。
加热时,与强氧化性反应,但无氢气放出。
非强氧化性酸:铁与酸反应有氢气放出。
(4)某些金属与碱反应:和强碱溶液反应:2Al + 2NaOH + 2H2O 错误!未找到引用源。
2NaAlO2 + 3H2↑。
高一化学必修一人 第三章知识总结

第三章金属及其化合物结构梳理一、本章知识结构梳理(一)金属的通用性金属的物理通用性:有金属光泽、有延展性、导电、导热。
但不同金属在密度、硬度、熔沸点等方面差别较大,这也是金属单质的一大特点。
金属的化学性质是具有还原性,主要表现在金属能与非金属、水、酸、某些盐发生反应。
金属的还原性有很大差别,其还原性强弱与金属原子的结构密切相关,一般说来,金属原子的半径越大,最外层电子越少,金属的还原性越强。
由金属活动性顺序表分析金属知识的规律(二)钠及钠的化合物1、钠的性质(1)钠的物理性质:银白色、质软、比水轻、熔点低(2)钠的化学性质:与非金属反应:2Na+Cl2点燃2NaCl (白烟)2Na+S==Na2S与O2反应:缓慢氧化:4Na+O2== 2Na2O (白色固体)剧烈燃烧:2Na+O2== Na2O2(淡黄色固体)与H2O 反应:2Na+2H2O==2NaOH+H2↑(2Na+2H2O==2Na++2OH―+H2↑)与酸反应:2Na+2H+==2Na++H2↑与盐溶液反应:(先与水作用生成NaOH,NaOH再与盐发生复分解反应) 2Na+2H2O+CuSO4 ==C u(O H)2↓+Na2SO4 +H2↑6Na+6H2O+2FeCl3==2Fe(O H)3↓+6NaCl+3H2↑2、钠的氧化物3、碱------氢氧化钠白色固体,易潮解。
俗名苛性钠,烧碱,火碱。
一元强碱,具有碱的通性,即: 能与酸反应生成盐和水,例:NaOH+HCl==NaCl+H 2O能与酸性氧化物反应生成盐和水,例:2NaOH+CO 2==Na 2CO 3+H 2O 能与某些盐发生复分解反应,例:2NaOH+CuCl 2==C u (O H )2↓+2NaCl4、盐------碳酸钠和碳酸氢钠1、铁的氧化物的转化34.铁三角二、本章知识综合应用1、滴加顺序不同,实验现象不同(1)稀Na2CO3溶液与稀盐酸间的反应向Na2CO3溶液中逐滴加入稀盐酸,开始时无气体产生,达到一定量后才有气泡冒出,由少到多的过程中依次发生下列反应:Na2CO3+HCl==NaCl+NaHCO3NaHCO3+HCl==NaCl+CO2↑+H2O向稀盐酸中逐滴加入稀Na2CO3溶液立即有气泡冒出,由少到多只发生下列反应:2HCl+Na2CO3==2NaCl+CO2↑+H2O(2) 稀AlCl3溶液与稀NaOH溶液间的反应向AlCl3溶液中滴加NaOH溶液直至过量时发生的反应依次为:Al3++3OH―==A l(O H)3↓A l(O H)3+OH―==AlO2―+2H2O现象:白色沉淀逐渐增多,继续加NaOH溶液沉淀逐渐溶解,直至完全消失。
金属及其化合物知识点总结
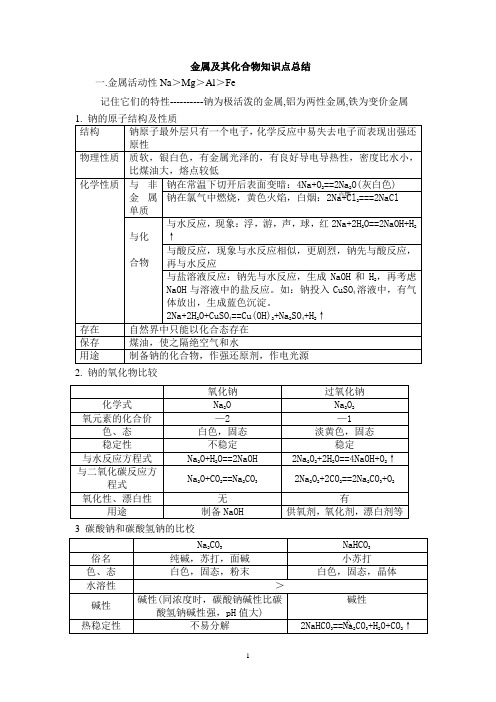
金属及其化合物知识点总结一.金属活动性Na>Mg>Al>Fe记住它们的特性----------钠为极活泼的金属,铝为两性金属,铁为变价金属1. 钠的原子结构及性质结构钠原子最外层只有一个电子,化学反应中易失去电子而表现出强还原性物理性质质软,银白色,有金属光泽的,有良好导电导热性,密度比水小,比煤油大,熔点较低化学性质与非金属单质钠在常温下切开后表面变暗:4Na+O2==2Na2O(灰白色)钠在氯气中燃烧,黄色火焰,白烟:2Na+Cl2===2NaCl与化合物与水反应,现象:浮,游,声,球,红2Na+2H2O==2NaOH+H2↑与酸反应,现象与水反应相似,更剧烈,钠先与酸反应,再与水反应与盐溶液反应:钠先与水反应,生成NaOH和H2,再考虑NaOH与溶液中的盐反应。
如:钠投入CuSO4溶液中,有气体放出,生成蓝色沉淀。
2Na+2H2O+CuSO4==Cu(OH)2+Na2SO4+H2↑存在自然界中只能以化合态存在保存煤油,使之隔绝空气和水用途制备钠的化合物,作强还原剂,作电光源2. 钠的氧化物比较3 碳酸钠和碳酸氢钠的比校Na2CO3NaHCO3俗名纯碱,苏打,面碱小苏打色、态白色,固态,粉末白色,固态,晶体水溶性>碱性碱性(同浓度时,碳酸钠碱性比碳酸氢钠碱性强,pH值大)碱性热稳定性不易分解2NaHCO3==Na2CO3+H2O+CO2↑氧化钠过氧化钠化学式Na2O Na2O2氧元素的化合价—2 —1 色、态白色,固态淡黄色,固态稳定性不稳定稳定与水反应方程式Na2O+H2O==2NaOH 2Na2O2+2H2O==4NaOH+O2↑与二氧化碳反应方程式Na2O+CO2==Na2CO32Na2O2+2CO2==2Na2CO3+O2氧化性、漂白性无有用途制备NaOH 供氧剂,氧化剂,漂白剂等点燃△与盐酸反应 Na 2CO 3+2HCl==2NaCl+H 2O+CO 2↑NaHCO 3+HCl==NaCl+H 2O+CO 2↑ 与氢氧化钠溶液 不反应NaHCO 3+NaOH==Na 2CO 3+H 2O 与澄清石灰水 Na 2CO 3+Ca(OH)2=CaCO 3↓+2NaOHNaHCO 3+Ca(OH)2=CaCO 3↓+H 2O+NaOH与二氧化碳 Na 2CO 3+H 2O+CO 2=2NaHCO 3 不反应与氯化钙溶液 Na 2CO 3+CaCl 2=CaCO 3↓+2NaCl不反应用途重要化工原料,可制玻璃,造纸等治疗胃酸过多,制作发酵粉等4. 铝及其化合物 Ⅰ、铝①物理性质:银白色,较软的固体,导电、导热,延展性 ②化学性质:Al —3e -==Al 3+a 、与非金属:4Al+3O 2==2Al 2O 3,2Al+3S==Al 2S 3,2Al+3Cl 2==2AlCl 3b 、与酸:2Al+6HCl==2AlCl 3+3H 2↑,2Al+3H 2SO 4==Al 2(SO 4)3+3H 2↑常温常压下,铝遇浓硫酸或浓硝酸会发生钝化,所以可用铝制容器盛装浓硫酸或浓硝酸c 、与强碱:2Al+2NaOH+2H 2O==2NaAlO 2(偏铝酸钠)+3H 2↑(2Al+2OH -+2H 2O==2AlO 2-+3H 2↑)大多数金属不与碱反应,但铝却可以d 、铝热反应:2Al+Fe 2O 3===2Fe+Al 2O 3,铝具有较强的还原性,可以还原一些金属氧化物Ⅱ、铝的化合物①Al 2O 3(典型的两性氧化物)a 、与酸:Al 2O 3+6H +==2Al 3++3H 2Ob 、与碱:Al 2O 3+2OH -==2AlO 2-+H 2O ②Al(OH)3(典型的两性氢氧化物):白色不溶于水的胶状物质,具有吸附作用 a 、实验室制备:AlCl 3+3NH 3·H 2O==Al(OH)3↓+3NH 4Cl ,Al 3++3NH 3·H 2O==Al(OH)3↓+3NH 4+b 、与酸、碱反应:与酸 Al(OH)3+3H +==Al 3++3H 2O 与碱 Al(OH)3+OH -==AlO 2-+2H 2O ③KAl(SO 4)2(硫酸铝钾) KAl(SO 4)2·12H 2O ,十二水和硫酸铝钾,俗名:明矾KAl(SO 4)2==K ++Al 3++2SO 42-,Al 3+会水解:Al 3++3H 2O Al(OH)3+3H +因为Al(OH)3具有很强的吸附型,所以明矾可以做净水剂 5. 铁①物理性质:银白色光泽,密度大,熔沸点高,延展性,导电导热性较好,能被磁铁吸引。
化学必修一第三章《金属及其化合物》主要知识及化学方程式总结

化学必修一第三章《金属及其化合物》主要知识及化学方程式总结化学必修一第三章《金属及其化合物》主要知识及化学方程式总结高一化学必修I第三章主要知识及化学方程式一、钠及其化合物的性质:1.钠在空气中缓慢氧化:4Na+O2==2Na2O2.钠在空气中燃烧:2Na+O2====Na2O23.钠与水反应:2Na+2H2O=2NaOH+H2↑现象:①钠浮在水面上;②熔化为银白色小球;③在水面上四处游动;④伴有响声;⑤滴有酚酞的水变红色。
4.过氧化钠与水反应:2Na2O2+2H2O=4NaOH+O2↑5.过氧化钠与二氧化碳反应:2Na2O2+2CO2=2Na2CO3+O26.碳酸氢钠受热分解:2NaHCO3==Na2CO3+H2O+CO2↑7.氢氧化钠与碳酸氢钠反应:NaOH+NaHCO3=Na2CO3+H2O8.在碳酸钠溶液中通入二氧化碳:Na2CO3+CO2+H2O=2NaHCO39.苏打(纯碱)与盐酸反应①盐酸中滴加纯碱溶液Na2CO3+2HCl=2NaCl+H2O+CO2↑CO32-+2H+=H2O+CO2↑②纯碱溶液中滴加盐酸,至过量Na2CO3+HCl=NaHCO3+NaClCO32-+H+=HCO3-NaHCO3+HCl=NaCl+H2O+CO2↑HCO3-+H+=H2O+CO2↑10.小苏打与盐酸反应NaHCO3+HCl=NaCl+H2O+CO2↑HCO3-+H+=H2O+CO2↑二、铝及其化合物的性质1.铝与盐酸的反应:2Al+6HCl=2AlCl3+3H2↑2.铝与强碱的反应:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑3.铝在空气中氧化:4Al+3O2==2Al2O34.氧化铝与酸反应:Al2O3+6HCl=2AlCl3+3H2O5.氧化铝与强碱反应:Al2O3+2NaOH+3H2O=2Na[Al(OH)4]6.氢氧化铝与强酸反应:Al(OH)3+3HCl=AlCl3+3H2O7.氢氧化铝与强碱反应:Al (OH)3+NaOH=Na[Al(OH)4]8.实验室制取氢氧化铝沉淀:Al3++3NH3H2O=Al(OH)3↓+3NH4+9.NaAlO2与强酸反应:NaAlO2+HCl+H2O=Al(OH)3↓+NaClAlO2-+H++H2O=Al(OH)3↓10.NaAlO2与弱酸反应(以CO2为例)1△点燃CO2少量:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-CO2过量:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-三、铁及其化合物性质1.Fe2+及Fe3+离子的检验:①Fe2+的检验:(浅绿色溶液)a)加氢氧化钠溶液,产生白色沉淀,继而变灰绿色,最后变红褐色。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三章金属及其化合物第一节金属的化学性质一、钠及其化合物(一)钠Na1、单质钠的物理性质:钠质软、银白色、熔点低、密度比水的小但比煤油的大。
2、单质钠的化学性质:①钠与O2反应常温下:4Na + O2=2Na2O (新切开的钠放在空气中容易变暗)加热时:2Na + O2==Na2O2(钠先熔化后燃烧,发出黄色火焰,生成淡黄色固体Na2O2。
)钠在空气中的变化过程:Na―→Na2O―→NaOH―→Na2CO3·10H2O(结晶)―→Na2CO3(风化),最终得到是一种白色粉末。
一小块钠置露在空气中的现象:银白色的钠很快变暗(生成Na2O),跟着变成白色固体(NaOH),然后在固体表面出现小液滴(NaOH易潮解),最终变成白色粉未(最终产物是Na2CO3)。
②钠与H2O反应2Na+2H2O=2NaOH+H2↑离子方程式:2Na++2H2O=2Na++2OH-+H2↑(注意配平)实验现象:钠浮在水面上,熔成小球,在水面上游动,有哧哧的声音,最后消失,在反应后的溶液中滴加酚酞,溶液变红。
“浮——钠密度比水小;游——生成氢气;响——反应剧烈;熔——钠熔点低;红——生成的NaOH遇酚酞变红”。
③钠与盐溶液反应如钠与CuSO4溶液反应,应该先是钠与H2O反应生成NaOH与H2,再和CuSO4溶液反应,有关化学方程式:2Na+2H2O=2NaOH+H2↑CuSO4+2NaOH=Cu(OH)2↓+Na2SO4总的方程式:2Na+2H2O+CuSO4=Cu(OH)2↓+Na2SO4+H2↑实验现象:钠熔成小球,在液面上四处游动,有蓝色沉淀生成,有气泡放出K、Ca、Na三种单质与盐溶液反应时,先与水反应生成相应的碱,碱再和盐溶液反应④钠与酸反应:2Na+2HCl=2NaCl+H2↑(反应剧烈)离子方程式:2Na+2H+=2Na++H2↑3、钠的存在:以化合态存在。
4、钠的保存:保存在煤油或石蜡中。
5、工业制钠:电解熔融的NaCl :2NaCl(熔融) 2Na + Cl 2↑6、钠的用途:① 在熔融的条件下钠可以制取一些金属,如钛、锆、铌、钽等;② 钠钾合金是快中子反应堆的热交换剂;③ 钠蒸气可作高压钠灯,发出黄光,射程远,透雾能力强。
(二)氧化钠和过氧化钠1、Na 2O 2O + H 2O == 2NaOH,Na 2O + CO 2 == Na 2CO 3,Na 2O + 2HCl == 2NaCl + H 2O .另外:加热时,2Na 2O + O 2 == 2Na 2O 22、Na 2O 2:淡黄色固体是复杂氧化物,易与水和二氧化碳反应。
2Na 2O 2 + 2H 2O == 4NaOH + O 2 ;2Na 2O 2 + 2CO 2 == 2Na 2CO 3 + O 2 (作供氧剂)。
因此Na 2O 2常做生氧剂,同时,Na 2O 2还具有强氧化性,有漂白作用。
如实验:Na 2O 2和水反应后的溶液中滴加酚酞,变红后又褪色。
(三)钠盐:Na 2CO 3与NaHCO 3的性质比较 通电白色固体,是碱性氧化物,具有碱性氧化物的通性:★注意几个实验的问题:1、向饱和的Na2CO3溶液中通足量的CO2有晶体NaHCO3析出。
2、Na2CO3溶液与稀HCl的反应①:向Na2CO3溶液中滴加稀HCl,先无气体,后有气体,如果n(HCl)小于n(Na2CO3)时反应无气体放出。
发生的反应:先Na2CO3 + HCl == NaCl + NaHCO3,后NaHCO3 + HCl == NaCl + H2O +CO2↑②向稀HCl中滴加Na2CO3溶液,先有气体,反应是:Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑如果用2mol的Na2CO3和2.4mol的稀HCl反应,采用①方法放出CO2是0.4mol;采用方法放出CO2为1.2mol。
希望同学们在解题时要留意。
3、Na2CO3溶液和NaHCO3溶液的鉴别:取两种试液少量,分别滴加CaCl2或BaCl2溶液,有白色沉淀的原取溶液为Na2CO3,另一无明显现象的原取溶液为NaHCO34、侯氏制碱法反应式:NaCl + NH3 + CO2 + H2O == NaHCO3 + NH4Cl.注意:在生产中应先在饱和的NaCl溶液中先通入NH3,后通入CO2,NaHCO3晶体析出过滤,在滤液中加入NaCl细末和通NH3析出NH4Cl晶体为副产品。
NH4Cl晶体析出后的母液进行循环试用,提高原料的利用率。
(四)氢氧化钠NaOH:俗称烧碱、火碱、苛性钠,易潮解,有强腐蚀性,具有碱的通性。
二、铝及其化合物(一)铝的性质1、物理性质:银白色金属,质较软,但比镁要硬,熔点比镁高。
有良好的导电、导热性和延展性。
2、化学性质:铝是较活泼的金属。
①通常与氧气易反应,生成致密的氧化物起保护作用。
4Al + 3O2 == 2Al2O3。
同时也容易与Cl2、S等非金属单质反应。
②与酸反应:强氧化性酸,如浓硫酸和浓硝酸在常温下,使铝发生钝化现象;加热时,能反应,但无氢气放出;非强氧化性酸反应时放出氢气。
(2Al+6H+=2Al3++3H2↑)③与强碱溶液反应:2Al + 2NaOH + 2H2O == 2NaAlO2 + 3H2↑(2Al+2OH-+2H2O=2AlO2-+3H2↑ )④与某些盐溶液反应:如能置换出CuSO4、AgNO3等溶液中的金属。
⑤铝热反应:铝与某些金属氧化物的反应(如V、Cr、Mn、Fe的氧化物)叫做铝热反应2Al + Fe2O3高温Al2O3 + 2Fe。
Al 和Fe2O3的混合物叫做铝热剂。
利用铝热反应焊接钢轨。
(二)氧化铝(Al2O3)白色固体,熔点高(2054℃),沸点2980℃,常作为耐火材料;是两性氧化物。
我们常见到的宝石的主要成分是氧化铝。
有各种不同颜色的原因是在宝石中含有一些金属氧化物的表现。
如红宝石因含有少量的铬元素而显红色,蓝宝石因含有少量的铁和钛元素而显蓝色。
工业生产中的矿石刚玉主要成分是α-氧化铝,硬度仅次于金刚石,用途广泛。
两性氧化物:既能与强酸反应又能与强碱反应生成盐和水的氧化物。
Al2O3 + 6HCl == 2AlCl3 + 3H2O ,Al2O3 + 2NaOH == 2NaAlO2 + H2O 。
Al2O3是工业冶炼铝的原料,由于氧化铝的熔点高,电解时,难熔化,因此铝的冶炼直到1886年美国科学家霍尔发现在氧化铝中加入冰晶石(Na3AlF6 ),使氧化铝的熔点降至1000度左右,通电铝的冶炼才快速发展起来,铝及其合金才被广泛的应用。
2Al2O3 4Al + 3O2↑。
(三)氢氧化铝(Al(OH)3)白色难溶于水的胶状沉淀,是两性氢氧化物。
加热易分解。
两性氢氧化物:既能与强酸又能与强碱反应生成盐和水的氢氧化物。
Al(OH)3 + 3HCl == AlCl3 + 3H2O, Al(OH)3 + NaOH == NaAlO2 + 2H2O.2Al(OH)3Al2O3 +3 H2O(四)铝的冶炼铝是地壳中含量最多的金属元素,自然界中主要是以氧化铝的形式存在。
工业生产的流程:铝土矿(主要成分是氧化铝)→用氢氧化钠溶解过滤→向滤液中通入二氧化碳酸化,过滤→氢氧化铝→氧化铝→铝。
主要反应:Al2O3 + 2NaOH == 2NaAlO2 + H2O ,CO2 + 3H2O + 2NaAlO2 == 2Al(OH)3↓+Na2CO3,2Al(OH)3△Al2O3 +3 H2O ,2Al2O3通电4Al + 3O2↑。
(五)铝的用途:铝有良好的导电、导热性和延展性,主要用于导线、炊具等,铝的最大用途是制合金,铝合金强度高,密度小,易成型,有较好的耐腐蚀性。
迅速风靡建筑业。
也是飞机制造业的主要原料。
(六)明矾的净水:化学式:KAl(SO4)2·12H2O,它在水中能电离:KAl(SO4)2 == K+ + Al3+ + 2SO42-。
铝离子与水反应,生成氢氧化铝胶体,具有很强的吸附能力,吸附水中的悬浮物,使之沉降已达净水目的。
Al3+ + 3H2O == Al(OH)3 (胶体)+ 3H+。
知识整理:①(Al(OH)3)的制备:在氯化铝溶液中加足量氨水。
AlCl3 + 3NH3·H2O == Al(OH)3↓+3NH4Cl 。
②实验:A、向氯化铝溶液中滴加氢氧化钠溶液,现象是先有沉淀,后溶解。
反应式:先Al3+ + 3OH- == Al(OH)3↓, 后Al3+ + 4OH- == AlO2- + 2H2O。
B、向氢氧化钠溶液中滴加氯化铝溶液,现象是开始无沉淀,后来有沉淀,且不溶解。
反应式:先Al3+ + 4OH- == AlO2- + 2H2O,后Al3+ + 3AlO2- + 6H2O == 4Al(OH)3↓。
③实验:向偏铝酸钠溶液中通二氧化碳,有沉淀出现。
CO2 + 3H2O + 2NaAlO2 == 2Al(OH)3↓+ Na2CO3。
④将氯化铝溶液和偏铝酸钠溶液混和有沉淀出现。
Al3+ + 3AlO2- + 6H2O == 4Al(OH)3↓。
⑤实验:A、向偏铝酸钠溶液中滴加稀盐酸,先有沉定,后溶解。
△反应的离子方程式:AlO 2- + H + + H 2O == Al(OH)3 ,Al(OH)3 + 3H + == Al 3+ + 2H 2O 。
B 、向稀盐酸中滴加偏铝酸钠溶液,先无沉淀,后有沉淀且不溶解。
反应的离子方程式:AlO 2- + 4H + == Al 3+ + 2H 2O ,3AlO 2- + Al 3+ + 6H 2O == 4Al(OH)3↓。
⑥三、铁及其化合物 (一)铁 Fe1、单质铁的物理性质:铁片是银白色的,铁粉呈黑色,纯铁不易生锈,但生铁(含碳杂质的铁)在潮湿的空气中易生锈。
(原因:形成了铁碳原电池。
铁锈的主要成分是Fe 2O 3)。
2、单质铁的化学性质:① 与非金属单质反应:3Fe +2O 2 Fe 3O 4(现象:剧烈燃烧,火星四射,生成黑色的固体)2Fe + 3Cl 2 2FeCl 3,Fe + S FeS 。
② 与非氧化性酸反应:Fe +2HCl =FeCl 2+H 2↑ ( Fe +2H +=Fe 2++H 2↑ ) 常温下铝、铁遇浓硫酸或浓硝酸钝化。
加热能反应但无氢气放出。
③ 与盐溶液反应:Fe +CuSO 4=FeSO 4+Cu ( Fe +Cu 2+=Fe 2++Cu );Fe +2 FeCl 3 == 3FeCl 2④ 与水蒸气反应:3Fe + 4H 2O(g)高温Fe 3O 4 + 4H 2↑(二) 铁的氢氧化物 △点燃点燃(三)Fe 2+、Fe 3+的检验(四)铁三角S、I 2、Cu 2+H +C l 2、B r 2、H N O 3 H 2S O 4(浓)O 2、Cl 2、HNO 3、H 2SO 4(浓)、(其它如:Br 2、H 2O 2、MnO 4-)Fe 、Cu 、H 2S 、S 2-、I -、H 2、C O 、C、活泼金属H2、C O、C 、活泼金属FeFe 3+Fe 2+Fe 与弱氧化剂反应,如H +、Cu 2+ 、I 2 、S 等;用还原剂如H 2 、CO 等还原FeO 或用Mg 、Zn 、Al 等还原Fe 2+盐溶液。
