实验八血糖的测定(葡萄糖氧化酶法)
生化实验(五)-----(综合性实验一) 血糖的测定 - (葡萄糖氧化酶法)(对比法、标准曲线法)

β-D葡萄糖+O2 +H2O
葡萄糖氧化酶(GOD)
β-D葡萄酸+H2O2
H2O2 +4-氨基安替吡啉+苯酚
过氧化物酶(POD)
H2O+红色醌式物质
原理
505nm有最大吸收峰
正常血糖水平为80—120毫克/100ml,
在糖尿病及肾上腺皮质机能亢进和脑下垂体
机能亢进的患者血中葡萄糖含量可显著升高,
(综合性实验一)
实验五
血糖的测定
(葡萄糖氧化酶法)
一、实验目的和要求:
1. 掌握酶联法测定血糖含量的基本原理。 2. 熟悉分光光度计的操作。 3. 掌握血糖正常水平及其测定的临床意义。 4. 复习血糖的来源、去路及其调节的有关理 论知识。
二、基本原理:
葡萄糖为一含醛基的已糖,在pH7.0条件, 葡萄糖氧化酶(glucose oxidase, GOD)可催化 血样中葡萄糖氧化生成葡萄糖酸及过氧化氢。 后者在过氧化物酶(peroxidase, POD)的 作用下与苯酚,4-氨基安替毗啉氧化缩合成红 色醌式物质,在505nm处有最大吸收峰。 标本中葡萄糖含量与吸光度成正比,可求 得血样中葡萄糖的含量。
饥饿时,血糖水平可下降。
三、实验器材与试剂:
【器 材】 1. 硬质中试管 2. 容量瓶、烧杯、玻璃棒 3. 电子天平 4. 微量移液器 【试 剂】 1. 工作液(酶酚混合试剂) 2. 葡萄糖 3. 双蒸水 4. 待测样品
四、实验操作:
1. 取硬质中试管三支,分别标以1、2、3 号,
2. 按下表操作:混匀后同时将三支试管 置于37℃水浴中,保温10分钟, 3. 在波长505nm处比色。以空白管调零, 读取标准管及测定管吸光度。(即测 得A样和A标)
葡萄糖氧化酶法测定血糖的原理_概述及解释说明

葡萄糖氧化酶法测定血糖的原理概述及解释说明1. 引言1.1 概述本文旨在介绍葡萄糖氧化酶法测定血糖的原理,并对其进行详细的解释和说明。
血糖测定是医学和生物科学领域中非常重要的一项实验技术,用于评估人体内的葡萄糖水平以及相关代谢功能的异常情况。
葡萄糖氧化酶法是一种常用的血糖测定方法,其基本原理是利用特定酶对葡萄糖进行氧化反应并与辅助试剂发生显色反应,从而间接地测定血液中的葡萄糖含量。
1.2 文章结构本文将按照以下结构进行展开:首先,介绍葡萄糖氧化酶的简要概况和血糖测定方法的总体概述;其次,详细讲解葡萄糖氧化酶法测定血糖的基本原理;然后,描述实验步骤并给出操作流程;接着,分析实验结果并讨论其中的意义和影响因素;最后,总结实验结论并展望未来该领域的研究意义和发展方向。
1.3 目的本文的目的是全面而清晰地介绍葡萄糖氧化酶法测定血糖的原理,帮助读者了解该方法在实际应用中的作用和意义。
通过本文的阅读,读者可以深入了解葡萄糖氧化酶法的基本理论和操作流程,并对实验结果进行准确而详细的分析与讨论。
同时,本文也旨在提供对该方法局限性和未来发展方向进行探讨,并为相关研究人员提供参考,促进该领域的进一步发展和突破。
2. 葡萄糖氧化酶法测定血糖的原理:2.1 葡萄糖氧化酶简介:葡萄糖氧化酶是一种存在于细胞内的酶类,在生物体中起到将葡萄糖转化为能量的重要作用。
该酶主要参与细胞内氧化还原反应,并催化葡萄糖与辅酶NAD+之间的反应。
在此过程中,葡萄糖被氧化成葡萄糖酸,并产生还原型辅酶NADH。
2.2 血糖测定方法概述:血液中的血糖水平是一个重要的生理指标,可以提供人体能量供给的信息。
因此,血糖水平的测定对于诊断和治疗许多代谢性疾病非常重要。
目前,有多种方法用于测定血液中的血糖浓度,其中最常用且最经典的方法就是使用葡萄糖氧化酶法。
2.3 葡萄糖氧化酶法的基本原理:葡萄糖氧化酶法是一种非常敏感和特异性的测定血糖浓度的方法。
该方法基于葡萄糖氧化酶与葡萄糖的特异性反应,通过检测在该反应中生成的还原型辅酶NADH的产生量来间接测定血液中的血糖浓度。
血糖测定操作步骤及评分标准

选手班级: 选手姓名: 选手学号: 标本号:血糖测定(葡萄糖氧化酶法)竞赛时间:15分钟一、说明1.本题满分100分,完成时间15分钟。
2.要求独立完成,不得相互询问或讨论。
3.考核成绩为操作过程评分、操作结果评分和考核时间评分之和。
4.全部操作过程时间和操作后处理时间计入时间限额。
二、实验原理葡萄糖氧化酶(GOD )催化葡萄糖氧化成葡萄糖酸(D-葡萄糖酸δ内酯),并产生过氧化氢:葡萄糖+2H 2O+O 2葡萄糖酸+2H 2O 2在色原性氧受体(如联大茴香胺、4-氨基安替比林偶氮酚)的存在下,过氧化物酶催化过氧化氢,氧化色原物质,生成有色化合物。
其颜色深浅与血清葡萄糖含量成正比。
三、实验器材721分光光度计、小号试管≤7支、试管架1个、手动可调式移液器5~50μl 、1ml 和10ml 刻度吸管各两支、记号笔1支、水浴箱、擦镜纸,废物容器等。
四、实验试剂葡萄糖标准液、生理盐水、0.1mol/L 磷酸盐缓冲液、酶试剂、酚试剂等组成的试剂盒。
五、实验标本 新鲜血清。
六、操作步骤取3支小试管,按表进行操作。
先配制10ml 酶酚混合试剂(试剂比例R1:R2=9:1)。
加入物(ml ) 测定管 标准管 空白管 血清0.03 葡萄糖标准应用液0.03 生理盐水0.03 酶酚混合试剂3.03.03.0混匀,置37℃水浴中,保温10min ,分光光度计波长500nm ,比色杯光径1.0cm ,以空白管调零,分别读取标准管和测定管的吸光度。
七、数据记录与计算1.数据记录标准管吸光度测定管吸光度裁判签名确认2.计算血清葡萄糖浓度(写出计算公式及过程)裁判签名确认八、报告(如:血清葡萄糖:△.△△ mmol/L)。
裁判签名确认选手班级:选手姓名:选手学号:标本号:血糖测定(葡萄糖氧化酶法)评分标准序号项目考核内容分值扣分标准扣分得分1 准备工作报告参赛项目及序号5漏缺一项 1 着白大衣、帽、口罩、手套并按要求佩戴参赛签着装不整、漏缺某一项 1 仪表端庄、头发符合要求仪容、着装不整 1 小号试管、试管架、移液器及配套吸头、记号笔1支缺选及多选、台面凌乱 1检查仪器、试剂、标本状态并摆在操作台合理位置无检查 12 操作①试管编号②空白管加蒸馏水30µl③标准管加葡萄糖标准液30 µl④测定管加血清30µl⑤各管分别加酶工作液3ml⑥各管置37℃水浴保温10分钟取出比色12试管无编号 1空白管加蒸馏水 1标准管加葡萄糖标准 1测定管加血清30µl 1各管分别加酶工作液 1加液顺序错 1加错液 1加液量不准确 1无混匀 1混匀不规范 1无水浴 1水浴时间不准确 1反应液无倒回原试管 23 用722分光光度计比色①调波长(500nm)②清洗比色杯,将各管溶液倒入比色杯,置比色槽中③调“T 100%”和“T 0”,重复2次④进行比色测定,记录读数,反应液倒回原试管⑤回位至显示器出现“100.0”13无调波长 1调波长不准 1无调T100% 1无调T0 1分光光度计闭盖预热 1双手碰触变色杯光滑面 1比色后无洗干净比色杯 1未用擦镜纸擦拭比色杯 1比色杯未正确放比色槽 1显示器未稳定时读数 1⑥洗干净比色杯(三次)比色液体未达杯高一半 1反应液无倒回原试管 1读数不准确 14 数据与报告原始记录完整、规范5不完整、不规范 1 单位正确不正确 1 公式正确不正确 1 计算方法正确不正确 1 报告完整、正确不完整、不正确 15 计数结果相对误差=(︱X-T︱/T)(X为计数值,T为靶值)56(︱X-T︱/T)×56分、相对误差≥20%扣56分6 文明操作操作完成后台面的处理 1 摆放无序,用物随意放 1 将使用过的一次性物品弃入污物缸或指定位置。
血糖的测定实验报告

血糖的测定实验报告一、实验目的。
本实验旨在通过测定血糖的方法,掌握血糖的测定原理和技术,以及了解血糖测定的临床意义。
二、实验原理。
血糖是机体内最主要的能量来源,其浓度的高低对人体健康有着重要的影响。
血糖的测定方法主要有生化法、酶法和电化学法等。
本实验采用了酶法测定血糖浓度,其原理是将血糖在葡萄糖氧化酶的催化下氧化成葡萄糖酸,同时生成的过氧化氢与酶标试剂中的间苯二酚发生氧化还原反应,产生有色产物,最终通过比色法测定血糖的浓度。
三、实验材料和仪器。
1. 实验材料,新鲜全血、血糖测定试剂盒、蒸馏水。
2. 实验仪器,恒温水浴器、显微镜、吸光度计。
四、实验步骤。
1. 取一定量的新鲜全血,离心得到血浆。
2. 用吸光度计预热至37℃。
3. 取血浆加入血糖测定试剂盒中,按照说明书进行操作。
4. 将混合液放入吸光度计中测定吸光度值。
5. 用标准曲线法计算血糖浓度。
五、实验结果。
经过实验测定,得到不同血糖浓度下的吸光度值,利用标准曲线法计算出血糖浓度如下:样品1,血糖浓度为5.2mmol/L。
样品2,血糖浓度为7.8mmol/L。
样品3,血糖浓度为9.5mmol/L。
六、实验分析。
根据实验结果,我们可以得出结论,血糖浓度与吸光度值呈正相关关系,血糖浓度越高,吸光度值越大。
通过实验数据的分析,我们可以初步判断被测样品中的血糖浓度。
七、实验结论。
本实验通过酶法测定血糖浓度的方法,成功地测定了不同样品中的血糖浓度。
实验结果表明,该方法准确可靠,可以用于临床血糖测定。
八、实验注意事项。
1. 实验中要注意操作规范,避免污染和误差。
2. 实验过程中需保持仪器的清洁和稳定。
3. 实验后要及时清洗实验仪器和归还实验材料。
九、实验改进。
在今后的实验中,可以尝试其他血糖测定方法,比较其准确性和实用性,以及对不同因素的影响。
十、参考文献。
1. 王明. 生化实验技术[M]. 北京,高等教育出版社,2008.2. 张华. 临床检验技术[M]. 北京,人民卫生出版社,2010.十一、致谢。
17 生物化学实验--葡萄糖氧化酶法测定血糖含量
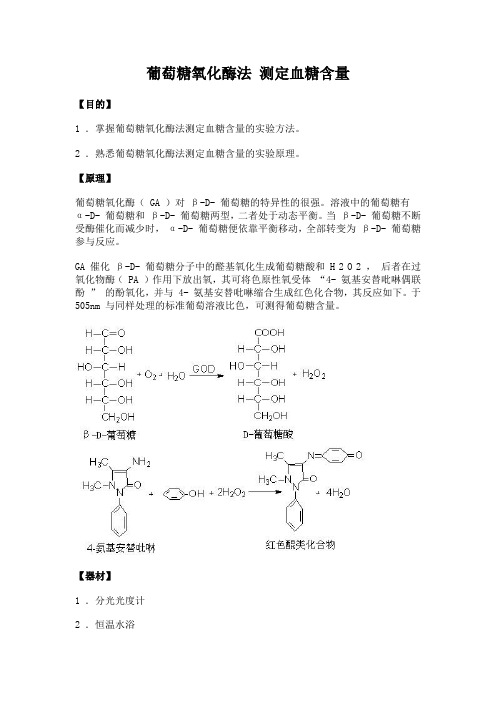
葡萄糖氧化酶法测定血糖含量【目的】1 .掌握葡萄糖氧化酶法测定血糖含量的实验方法。
2 .熟悉葡萄糖氧化酶法测定血糖含量的实验原理。
【原理】葡萄糖氧化酶( GA )对β-D- 葡萄糖的特异性的很强。
溶液中的葡萄糖有α-D- 葡萄糖和β-D- 葡萄糖两型,二者处于动态平衡。
当β-D- 葡萄糖不断受酶催化而减少时,α-D- 葡萄糖便依靠平衡移动,全部转变为β-D- 葡萄糖参与反应。
GA 催化β-D- 葡萄糖分子中的醛基氧化生成葡萄糖酸和 H 2 O 2 ,后者在过氧化物酶( PA )作用下放出氧,其可将色原性氧受体“4- 氨基安替吡啉偶联酚” 的酚氧化,并与 4- 氨基安替吡啉缩合生成红色化合物,其反应如下。
于505nm 与同样处理的标准葡萄溶液比色,可测得葡萄糖含量。
【器材】1 .分光光度计2 .恒温水浴3 .微量加样器4 .刻度吸量管5 .中号试管【试剂】1 . 0.01mol/L pH7.0 磷酸盐缓冲液无水 Na 2 HPO 4 18.5g 和 KH 2 PO 4 5.3g 溶于 800ml 蒸馏水中,用少量 1mol/L 的 NaOH 或 HCl 调 pH 至 7.0 ,再加蒸馏水稀释至 1L 。
2 .酶试剂取 GA1200 单位、 PA1200 单位, 4- 氨基安替吡啉 10mg 、叠氮钠 100mg ,加上述磷酸盐缓冲液至 80ml 左右,调 pH 至 7.0 ,再加同上缓冲液至 100ml ,混匀。
冰箱内保存可稳定 3 个月。
3 .酚试剂酚 100mg 溶于 100ml 蒸馏水中。
因酚易在空气中氧化成红色,可先配制成 50g /dl ,贮棕色瓶中,用前稀释。
4 .酶 - 酚混合试剂将试剂 2 、 3 等量混合。
冰箱内保存可稳定 1 个月。
5 .葡萄糖标准贮存液( 20mg/ml )无水 D- 葡萄糖于80 ℃ 烤箱内干燥恒重,冷却后,称取 2.0g 以 0.25% 苯甲酸溶解、稀释定容至 100ml 。
血糖试验实验报告

一、实验目的1. 掌握血糖测定的原理和方法。
2. 熟悉血糖正常范围及意义。
3. 理解胰岛素和肾上腺素对血糖浓度的影响。
二、实验原理血糖是指血液中的葡萄糖,是人体细胞的主要能量来源。
血糖浓度受到胰岛素和肾上腺素等激素的调节。
胰岛素可以降低血糖,而肾上腺素则可以提高血糖。
本实验采用葡萄糖氧化酶法测定血糖浓度,通过比较不同实验条件下血糖浓度的变化,了解胰岛素和肾上腺素对血糖浓度的影响。
三、实验器材1. 仪器:血糖仪、葡萄糖氧化酶法试剂、试管、移液器、恒温水浴箱等。
2. 试剂:葡萄糖标准液、胰岛素、肾上腺素、生理盐水等。
四、实验步骤1. 标准曲线的绘制:将葡萄糖标准液分别加入试管中,按比例加入试剂,混合均匀,置于恒温水浴箱中反应一定时间。
然后测定各管中葡萄糖浓度,以葡萄糖浓度为横坐标,吸光度为纵坐标,绘制标准曲线。
2. 实验组制备:将实验动物(如家兔)分为实验组和对照组。
实验组注射一定剂量的胰岛素,对照组注射等量的生理盐水。
两组动物在相同条件下饲养一段时间。
3. 血糖测定:分别从实验组和对照组动物体内采集血液,测定血糖浓度。
4. 肾上腺素影响实验:在实验组动物注射胰岛素后,再注射一定剂量的肾上腺素,重复步骤3,观察血糖浓度的变化。
五、实验结果1. 标准曲线绘制:根据实验数据绘制标准曲线,得出葡萄糖氧化酶法测定血糖浓度的方法。
2. 实验组与对照组血糖浓度比较:实验组血糖浓度显著低于对照组,说明胰岛素可以降低血糖。
3. 肾上腺素影响实验:注射肾上腺素后,实验组血糖浓度显著升高,说明肾上腺素可以升高血糖。
六、实验分析1. 葡萄糖氧化酶法是一种准确、简便的血糖测定方法,适用于临床和科研。
2. 胰岛素可以降低血糖,这是胰岛素的主要生理作用。
胰岛素通过促进葡萄糖进入细胞,促进糖原合成,抑制糖原分解和糖异生,从而降低血糖。
3. 肾上腺素可以升高血糖,这是肾上腺素的主要生理作用。
肾上腺素通过抑制胰岛素分泌,促进糖原分解和糖异生,从而升高血糖。
实验报告血糖的测定
一、实验目的1. 掌握血糖测定的原理和方法。
2. 了解血糖水平与人体健康的关系。
3. 培养实验操作技能,提高实验数据分析能力。
二、实验原理血糖是指在血液中葡萄糖的浓度。
正常人体血糖水平相对稳定,维持在一定范围内。
血糖的测定对于糖尿病等疾病的诊断和治疗具有重要意义。
本实验采用葡萄糖氧化酶法测定血糖浓度。
葡萄糖氧化酶法是一种测定血糖的常用方法,其原理是葡萄糖在葡萄糖氧化酶的催化下,与氧气反应生成葡萄糖酸和过氧化氢,过氧化氢在过氧化物酶的作用下,使色原物质氧化产生颜色变化,根据颜色变化程度,可以计算出样品中的葡萄糖浓度。
三、实验材料1. 试剂:葡萄糖标准溶液、显色剂、显色剂储备液、反应缓冲液、显色剂工作液、空白试剂、待测血液样品。
2. 仪器:微量移液器、移液管、移液器、酶标仪、试管、水浴锅、吸管、滤纸等。
四、实验步骤1. 标准曲线绘制(1)取6支试管,分别加入0、0.5、1.0、1.5、2.0、2.5ml葡萄糖标准溶液,加入0.5ml反应缓冲液。
(2)将各试管充分混匀,置于水浴锅中,恒温30分钟。
(3)取出试管,加入0.5ml显色剂,充分混匀,室温放置10分钟。
(4)以空白试剂为参比,用酶标仪在波长540nm处测定各管吸光度。
(5)以葡萄糖浓度为横坐标,吸光度为纵坐标,绘制标准曲线。
2. 待测样品测定(1)取6支试管,分别加入0.5ml反应缓冲液、0.5ml显色剂、0.5ml待测血液样品。
(2)将各试管充分混匀,置于水浴锅中,恒温30分钟。
(3)取出试管,加入0.5ml显色剂,充分混匀,室温放置10分钟。
(4)以空白试剂为参比,用酶标仪在波长540nm处测定各管吸光度。
(5)根据标准曲线,计算待测样品的血糖浓度。
五、实验结果与分析1. 标准曲线绘制:根据实验数据绘制标准曲线,线性范围为0-2.5mmol/L。
2. 待测样品测定:根据标准曲线计算,待测样品的血糖浓度为3.8mmol/L。
六、实验结论本实验采用葡萄糖氧化酶法测定血糖浓度,实验结果准确可靠。
葡萄糖氧化酶法测定血糖浓度
肾上腺素由肾上腺髓质分泌的一种儿茶酚胺激素 。 肾上腺素升高血糖机制: 在应激状态、内脏神经刺激和低血糖等情况下, 肾上腺素被释放入血液循环,促进糖原分解并升 高血糖,促进脂肪分解,促进非糖物质向血糖的 转化,使血糖浓度增大。
一、血糖测定
福林-酚试剂法
葡萄糖氧化酶法
邻甲苯胺法
葡萄糖氧化酶法原理
葡萄糖氧化酶(GOD 葡萄糖酸+H2O2 葡萄糖+O2+H2O ) 氧化,37oC H2O2 + 苯酚 + 4-氨基安替吡啉 37oC 辣根过氧化物酶(POD ) Trinder反应 H2O +红色醌亚胺 + O2 溶液在505nm下有吸收峰,可用比色法测定,得出葡萄糖的浓度 。
结果记录
标准(ml) 正常 (ml) 注射激素后(ml) 空白(ml)
A 血糖浓度 增高率
பைடு நூலகம்
动脉血
血细胞、大分子蛋白质等
二、 尿糖
尿糖是指尿中的糖类,主要是 指尿中的葡萄糖。正常情况下 ,肾小管能将肾小球滤过的葡 部分水 、无机 萄糖全部重吸收回血液,当血 盐、葡 糖>肾糖阈8.96-10.08mmol/L, 超过肾小管的重吸收能力,部分 二、萄糖、 维生素 葡萄糖随尿排出。尿糖的测定 、尿素 虽然不能单纯作为糖尿病的诊 等 断标准,但是从某种层面上也 能反映一些问题。
葡萄糖氧化酶法测定血糖浓度
生物化学与分子生物学专业 XXX 邮箱:
一.实验要求
1.掌握血糖测定原理,计算方法,参考正常值,临床意义。 2.了解尿糖的测定及意义。
二.实验内容
1.收集耳缘静脉血,制备血浆,葡萄糖氧化法比色测定血糖浓度。
2.收集尿液,班氏法测定。
血糖
血糖(blood glucose,BG)指血浆(清)中的糖类物质,主 要为葡萄糖。 一.血糖的来源: 食物、糖原的分解、糖异生。 二. 血糖的去路: 有氧氧化、转换成非糖物质、尿排出、糖酵解。
血糖的定量测定(葡萄糖氧化酶法)
血糖的定量测定(葡萄糖氧化酶法)血糖是指血液中葡萄糖的含量。
葡萄糖是人体主要的能量来源,血糖的测定是检查人体内部能量代谢状态的重要项目之一。
这篇文章将介绍血糖定量测定的实验原理、方法以及实验注意事项。
一、实验原理血糖的定量测定方法主要是利用葡萄糖氧化酶将血液中的葡萄糖在催化反应下转化为过氧化氢和D-酮糖酸,利用过氧化氢的比色法来测定血糖的含量。
具体反应式为:(1)葡萄糖+O2+H2O→葡萄糖氧化酶 D-酮糖酸+H2O2(2)2H2O2+Fe2+→2H2O+Fe3++O2(3)Fe3++TSC(三硝基苯胺)→FeTSC3(红色化合物)其中,TSC(三硝基苯胺)为过氧化氢的比色试剂,用Fe2+作催化剂促进反应进行,所生成的红色化合物FeTSC3与过氧化氢的浓度呈线性关系。
二、实验材料1.血糖标准品:10mmol/L2.葡萄糖氧化酶3.三硝基苯胺(TSC)、醋酸钠、乙二胺四醋酸盐二水合物(EDTA•2H2O)、氢氧化钠(NaOH)4.0.1mol/L磷酸盐缓冲液(pH7.5)5.准确量杯、试管、离心管、吸光度计、恒温水浴器、移液管三、实验步骤1.制备血清样品:将血液放置静置后离心取血清,制成5mmol/L、10mmol/L、15mmol/L、20mmol/L的葡萄糖标准品。
2.实验组织:3个组别,每组3个试管。
A组:加1mL的10mmol/L葡萄糖标准品;B 组:加1mL的血清标本;C组:加入1mL的磷酸盐缓冲液作为对照组。
注意,每组要做三个平行实验。
3.反应体系准备:①将实验组织中的标准品、血清样本和磷酸盐缓冲液分别加入3毫升离心管中。
②分别加入1mL葡萄糖氧化酶。
③分别加入1mL EDTA全部气泡排除。
⑤每组混合后放置在37℃下反应20分钟。
⑥在上述反应过程中,加入2毫升0.1mol/L的NaOH溶液使溶液呈碱性,使催化反应更为稳定。
4.吸光测定:将反应充分混合后,吸取适量的样品,放到吸光度计槽,设定波长为505nm,用对照组值进行比较,计算出各组的吸光度,并根据标准曲线计算出各样本的葡萄糖含量。
血糖测定实验实验报告
一、实验目的1. 了解血糖测定的原理和方法。
2. 掌握血糖测定仪器的操作方法。
3. 掌握血糖正常范围及其临床意义。
4. 通过实验,提高实验操作技能和数据分析能力。
二、实验原理血糖是指血液中的葡萄糖含量,是人体能量代谢的重要物质。
血糖浓度在正常情况下保持相对稳定,对维持人体生理功能具有重要意义。
血糖测定是通过检测血液中的葡萄糖含量来确定血糖水平的方法。
常用的血糖测定方法有血糖仪法、试纸法和化学法等。
本实验采用血糖仪法进行血糖测定,其原理是利用葡萄糖氧化酶催化葡萄糖氧化反应,产生过氧化氢,过氧化氢在过氧化物酶的催化下与色原性氧受体缩合,形成红色化合物。
通过测定该红色化合物的吸光度值,可以计算出血液中的葡萄糖含量。
三、实验材料与仪器1. 实验材料:新鲜血液、生理盐水、葡萄糖标准液、葡萄糖氧化酶试纸、缓冲液、葡萄糖氧化酶试剂盒等。
2. 实验仪器:血糖仪、微量移液器、试管、吸管、恒温水浴锅、电子天平等。
四、实验步骤1. 标准曲线的制作:取6个试管,分别加入0、0.1、0.2、0.3、0.4、0.5毫升的葡萄糖标准液,再分别加入0.5毫升的缓冲液,充分混匀。
用微量移液器取0.1毫升混合液滴在葡萄糖氧化酶试纸上,与标准比色卡进行比对,记录吸光度值。
2. 血糖测定:取3个试管,分别加入0.5毫升新鲜血液、生理盐水和葡萄糖标准液。
再分别加入0.5毫升的缓冲液,充分混匀。
用微量移液器取0.1毫升混合液滴在葡萄糖氧化酶试纸上,与标准比色卡进行比对,记录吸光度值。
3. 数据处理:根据标准曲线,计算出血液、生理盐水和葡萄糖标准液中的葡萄糖含量。
五、实验结果1. 标准曲线:通过制作标准曲线,得到葡萄糖浓度与吸光度值之间的关系。
2. 血糖测定结果:- 血液中的葡萄糖含量:XX毫克/分升;- 生理盐水中的葡萄糖含量:XX毫克/分升;- 葡萄糖标准液中的葡萄糖含量:XX毫克/分升。
六、实验分析1. 血糖浓度在正常情况下保持相对稳定,对维持人体生理功能具有重要意义。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验十 血糖的测定
血液中的葡萄糖称血糖。
正常人血糖浓度较恒定,维持在3.9mmol /L ~6.1mmol /L 之间。
血糖浓度的相对恒定是机体进行正常生理活动的前提条件之一,有着双重实际意义:其一,维持稳定的能源供给,满足机体在各种生理状态下对能量的需求。
其二,保证机体不因进食致血糖浓度过高,导致糖的丢失。
因此,血糖的测定是临床生化检验实验室的常规检测项目。
血糖测定按其发展过程及反应原理的不同,大致分三类:氧化还原法 ,缩合法(主要有邻甲苯胺法),酶法(主要有己糖激酶法和葡萄糖氧化酶法)。
下边介绍两种方法供选择。
一、葡萄糖氧化酶法
【目的】
1. 了解葡萄糖氧化酶法测定血糖的原理,能进行血糖测定的操作。
2. 掌握血糖测定的临床意义。
【原理】
葡萄糖氧化酶 (glucose oxidase ,GOD) 能将葡萄糖氧化为葡萄糖酸和过氧化氢。
后者在过氧化物酶 (peroxidase ,POD)作用下,分解为水和氧的同时将无色的4-氨基安替比林与酚氧化缩合生成红色的醌类化合物,即 Trinder 反应。
其颜色的深浅在一定范围内与葡萄糖浓度成正比,在505nm 波长处测定吸光度,与标准管比较可计算出血糖的浓度。
反应式如下:
2H 2O 2+4-氨基安替比林+酚
红色醌类化合物
POD
2H 2O
2H 2O 2
O 2葡萄糖+葡萄糖酸+
GOD
+
【器材】
试管、吸管、试管架、恒温水浴箱、分光光度计 【试剂】
1. 0.1mol/L 磷酸盐缓冲液(pH7.0)
称取无水磷酸氢二钠8.67g 及无水磷酸二氢钾5.3g 溶于800ml 蒸馏水中,用1mol/L 氢氧化钠(或1mol/L 盐酸)调节pH 至7.0,然后用蒸馏水稀释至1L 。
2. 酶试剂
称取过氧化物酶1200U ,葡萄糖氧化酶1200U ,4-氨基安替比林10mg ,叠氮钠100mg ,溶于上述磷酸盐缓冲液80ml 中,用1mol/L NaOH 调pH 至7.0,加磷酸缓冲液至100ml 。
置冰箱保存,4℃可稳定3个月。
3. 酚溶液
称取重蒸馏酚100mg溶于100ml蒸馏水中(酚在空气中易氧化成红色,可先配成500g/L 的溶液,贮存于棕色瓶中,用时稀释),用棕色瓶贮存。
4. 酶酚混合试剂
取上述酶试剂与酚溶液等量混合,4℃可以存放一个月。
5. 12mmol/L苯甲酸溶液
溶解苯甲酸1.4g于蒸馏水约800ml中,加温助溶,冷却后加蒸馏水至1L。
6.葡萄糖标准贮存液(100mmol/L)
称取已干燥恒重的无水葡萄糖1.802g,溶于12mmol/L苯甲酸溶液约70ml中,并移入100ml容量瓶内,再以12mmol/L苯甲酸溶液加至100ml。
7.葡萄糖标准应用液(5mmol/L)
吸取葡萄糖标准贮存液5.0ml 于100ml 容量瓶中,加12mmol/L 苯甲酸溶液至刻度。
【操作】
取3 支试管,编号,按下表操作。
表3-12 血糖测定操作步骤
加入物 (ml) 空白管标准管测定管
血清--0.02
葡萄糖标准液-0.02 -
蒸馏水0.02 --
酶酚混合液 3.0 3.0 3.0
混匀,置 37 ℃水浴中保温 15分钟,在波长 505nm 处比色,以空白管调零,读取标准管及测定管吸光度。
【计算】
测定管吸光度
血糖(mmol/L)= ×5
标准管吸光度
标准管吸光度
血清葡萄糖(mmol/L)=
×5
测定管吸光度
【注意事项】
1.测定结果如超过20mmol/L,应将标本用生理盐水稀释后再测定,结果乘以稀释倍数。
2.若酶酚混合试剂呈红色,应弃之重配。
因标本和标准用量少,其加量是否准确对测定结果影响较大,故其加量必须准确。
3.GOD-POD法的第一步反应特异性高,而由POD催化的第二步指示反应是非特异性的,易受标本中尿酸、维生素C、谷胱甘肽、胆红素等还原物的干扰,这些物质与色素原竞争H202,使测定结果偏低。
4.Trinder反应由Trinder于1969年提出。
后经许多学者改进,采用2,4-二氯酚、2-羟-3,5-二氯苯磺酸等代替苯酚,由于这些化合物氧化生成的色素的摩尔吸光系数均高于苯酚,使反应灵敏度得以提高。
【正常参考范围】
3.9~6.1mmol/L
【临床意义】
1. 生理性高血糖可见于摄入高糖饮食或注射葡萄糖后,或精神紧张、交感神经兴奋,肾上腺分泌增加时。
2. 病理性高血糖
⑴糖尿病:病理性高血糖常见于胰岛素绝对或相对不足的糖尿病患者。
⑵对抗胰岛素的激素分泌过多:如甲状腺功能亢进、肾上腺皮质功能及髓质功能亢进、腺垂体功能亢进、胰岛α-细胞瘤等。
⑶颅内压增高:颅内压增高(如颅外伤、颅内出血、脑膜炎等)刺激血糖中枢,出现高血糖。
⑷脱水引起的高血糖:如呕吐、腹泻和高热等也可使血糖轻度增高。
3. 生理性低血糖饥饿或剧烈运动、注射胰岛素或口服降血糖药过量。
4. 病理性低血糖
⑴胰岛素分泌过多:由胰岛β细胞增生或胰岛β细胞瘤等引起。
⑵对抗胰岛素的激素分泌不足:如腺垂体功能减退、肾上腺皮质功能减退和甲状腺功能减退等。
⑶严重肝病患者:肝贮存糖原及糖异生功能低下,不能有效调节血糖。
【结果及分析】
【思考题】
1. 血糖有哪些来源和去路,机体是如何调节血糖浓度恒定的?
2. 酶试剂为什么要用磷酸缓冲液配制,用蒸馏水是否可以,为什么?
二、邻甲苯胺法
【目的】
了解测定血糖的原理和方法,要求在实验中培养学生严谨的作风和准确地进行实际操作的能力。
【原理】
葡萄糖在热的醋酸溶液中与邻甲苯胺缩合生成葡萄糖邻甲苯胺,后者脱水生成雪夫(Schiff)碱,再经结构重排,生成有色化合物。
颜色的深浅与葡萄糖含量成正比。
其反应式如下:
葡萄糖 + 邻甲苯胺葡萄糖邻甲苯胺
-H2O
葡萄糖邻甲苯胺雪夫碱
【器材】
试管、吸管、试管架、恒温水浴箱、分光光度计
【试剂】
1.邻甲苯胺试剂
于940ml冰醋酸中加入硫脲1.5g, 邻甲苯胺60ml,混合,直至硫脲完全溶解,置棕色试剂瓶中,室温保存。
新配试剂应放置24小时后(待老化)使用。
此试剂腐蚀性强,避免接触皮肤,应用自动吸管加液。
2.12mmol/L苯甲酸溶液
于900ml 蒸馏水中加入苯甲酸1.4g,加热助溶,冷却后置于1L容量瓶中,加蒸馏水至刻度。
3.葡萄糖标准储存液(100mmol/L)
称取无水葡萄糖(预先置80℃烤箱干燥至恒重,移置干燥器内保存)1.802g,溶解于80ml苯甲酸溶液中,移置100ml容量瓶中,再加苯甲酸溶液至刻度。
4.葡萄糖标准应用液(5mmol/L)
取葡萄糖标准储备液5ml,置于100ml容量瓶中,加苯甲酸溶液至刻度。
【操作】
1.取16×150mm试管3支按下表进行操作:
表3-13 血糖测定操作步骤
试剂(ml)测定管标准管空白管
血清或血浆0.1 ——
葡萄糖标准应用液—0.1 —
蒸馏水——0.1
邻甲苯胺试剂 3.0 3.0 3.0
2.将上述各管混匀放入沸水浴中加热12分钟,取出用自来水冷却5分钟。
注意在煮沸时水浴中的水面必须高于试管内的液面。
否则则温度不均而影响比色。
3.用波长630nm分光光度计进行比色,空白管调零点,读取测定管与标准管吸光度。
4.计算
测定管吸光度
血糖(mmol/L)= ×5
标准管吸光度
5.本测定法空腹血糖正常值为3.89~6.11 mmol/L(70~110mg/dl)。
【临床意义】同上。
【结果及分析】
【思考题】
讨论血糖升高和降低的临床意义及其维持恒定的因素?。
