张新平:2019年与2018年全国高考理综I卷化学实验题对比赏析
张新平:2019年与2018年全国高考理综I卷化学工艺流程题对比赏析29页PPT

1、最灵繁的人也看不见自己的背脊。——非洲 2、最困难的事情就是认识自己。——希腊 3、有勇气承担命运这才是英雄好汉。——黑塞 4、与肝胆人共事,无字句处读书。——周恩来 5、阅读使人充实,会谈使人敏捷,写作使人精确。——培根
张新平:2019年与2018年全国高考理 综I卷化学工艺流程题对比赏析
11、用道德的示范来造就一个人,显然比用法律来约束他更有价值。—— 希腊
12、法律是无私的,对谁都一视同仁。在每件事上,她都不徇私情。—— 托马斯
13、公正的法律限制不了好的自由,因为好人不会去做法律不允许的事 情。——弗劳德
14、法律是为了保护无辜而制定的。——爱略特 15、像房子一样,法律和法律都是相互依存的。——伯克
2018高考全国卷Ⅰ化学试题详解与评析

2018⾼考全国卷Ⅰ化学试题详解与评析⼀、选择题6. 磷酸亚铁锂(LiFePO4)电池是新能源汽车的动⼒电池之⼀。
采⽤湿法冶⾦⼯艺回收废旧硫酸亚铁锂电池正极⽚中的⾦属,其流程如下:下列叙述错误的是A. 合理处理废旧电池有利于保护环境和资源再利⽤B. 从“正极⽚”中可回收的⾦属元素有Al、Fe、LiC. “沉淀”反应的⾦属离⼦为Fe3D. 上述流程中可⽤硫酸钠代替碳酸钠【答案】D【解析】正极⽚碱溶时铝转化为偏铝酸钠,滤渣中含有磷酸亚铁锂,加⼊硫酸和硝酸酸溶,过滤后滤渣是炭⿊,得到含Li、P、Fe的滤液,加⼊碱液⽣成氢氧化铁沉淀,滤液中加⼊碳酸钠⽣成含锂的沉淀,据此解答。
A、废旧电池中含有重⾦属,随意排放容易污染环境,因此合理处理废旧电池有利于保护环境和资源再利⽤,A正确;B、根据流程的转化可知从正极⽚中可回收的⾦属元素有Al、Fe、Li,B正确;C、得到含Li、P、Fe的滤液,加⼊碱液⽣成氢氧化铁沉淀,因此“沉淀”反应的⾦属离⼦是Fe3+,C正确;D、硫酸锂能溶于⽔,因此上述流程中不能⽤硫酸钠代替碳酸钠,D错误。
答案选D。
评析:此题是创新题,估计明年⾼考不会出现。
这题的素材是考⽣⾮常熟悉的,近年来在许多模拟题出现过。
2017年,2013年全国卷出现过,其中2013年的题⽬还被选⽤到考试说明中,⽐较早的是在2009年四川卷中就出现过此素材。
把流程题改造成选择题,并且放在第⼀题,出乎许多考⽣的意料。
流程题改造成选择题,在以前的浙江⾼考卷中经常出现,⽽且各地的模拟题也出现过,这题可以说是全国卷选择题的创新点。
考前我预测选择题创新点会在元素化合物上做⽂章,竟然⾔中。
所以我们备考时,⼀定要注意⾼考真题,许多经典的素材会重复使⽤,其它省份优秀的题型也要关注。
2. 下列说法错误的是A. 蔗糖、果糖和麦芽糖均为双糖B. 酶是⼀类具有⾼选择催化性能的蛋⽩质C. 植物油含不饱和脂肪酸酯,能使Br₂/CCl4褪⾊D. 淀粉和纤维素⽔解的最终产物均为葡萄糖【答案】A【解析】A、果糖不能再发⽣⽔解,属于单糖,A错误;B、绝⼤多数酶是具有催化活性和⾼度选择性的蛋⽩质,B正确;C、植物油属于油脂,其中含有碳碳不饱和键,因此能使Br2/CCl4溶液褪⾊,C正确;D、淀粉和纤维素均是多糖,其⽔解的最终产物均为葡萄糖,D正确。
2018年高考化学试卷分析及2019年高考备考建议

2018年高考化学试卷分析及2019年高考备考建议一.2018年高考化学总体难度评测整体来看,2018年全国一卷的题目符合最新考纲的要求,综合考查了“双基”知识、化学基本原理与应用。
在试题结构方面,今年和去年基本一致,但是在难度方面,今年要比去年容易不少,总体难度为两星半。
选择题部分历年来压轴都会在13题,主要考查溶液中的离子平衡,今年13题考查了电解池,没有“压轴”应该有的难度。
非选择题部分的实验题考查了一个较简单的实验组装图,题目基本和广一模的题目类似,工艺流程图的题目也较为简单,之前作为中档题出现的反应原理在今年反倒是非选择题中难度较大的题目,溶解平衡在这次高考中也没有考查。
题目尽管难度不大,但是有一些细节问题仍旧需要学生留意,如12题的元素推断中“W和Z形成的化合物可与浓硫酸反应”是这道题的突破口,对元素化学的基础要求还是比较高的;13题的电解池中考查到了电势的问题,属于平时练习较少的一类考点。
选做题部分“有机化学基础”和“物质结构基础”两道题也都中规中矩,难度适中,可以看出高考命题的特点:重视学生的选择多样性。
当然,尽管今年题目难度不大,命题人都本着既有利于高校选拔新生,又有利于中学实施素质教育的命题思想,注重对基础知识和基本能力的考查,化学学科思想和能力方法也在试题中得到较好的体现。
在考查学生掌握化学知识的过程中,力求突出对学生学科能力和学科素质的考查,体现了促进学生发展的理念。
二.全国一卷化学结构特点题型题号分值作答要求难度分布选择题7 6单选题,四个选项中只有一个选项是符合题目一般7-11为简单题,12题为中档题,13题为难题。
简单题注重化学和生活的练习,难题侧8 69 610 611 6要求的。
重化学思维的考查。
12 613 6必考题26 14常规题型,三道题目必须作答。
26题为实验题,27题为工艺流程图类问题,28题为化学反应原理的考查,考查主要涉及文字表述、计算、方程式书写。
张新平:2019年与2018年全国高考理综I卷化学工艺流程题对比赏析

回答下列问题:
(NH4)2SO4
(3)根据H3BO3的解离反应:H3BO3+H2O
H++B(OH)4−
,Ka=5.81×10−10,可判断H3BO3是_一__元__弱__酸;在“过滤2”前
,将溶液pH调节至3.5,目的是__转ห้องสมุดไป่ตู้__化__为__H_3_B_O__3_,。促进析出
信息解读:解离反应、可逆、一个H+、及Ka值,可得 H3BO3为一元弱酸。
MgSO4
回答下列问题:
(NH4)2SO4
(4)在“沉镁”中生成Mg(OH)2·MgCO3沉淀的离子方程式
为__________,
母液经加热后可返回___________工序循环使用。由碱式碳酸
镁制备轻质氧化镁的方法是_________。
知识点链接: 镁离子与碳酸根离子的双水解。
信息解读: 镁离子与碳酸根离子的双水解,产物是 Mg(OH)2·MgCO3,另一产物是碳酸(或其分解物)或HCO3-。
回答下列问题: (1)在95 ℃“溶浸”硼镁矿粉,产生的气体在“吸收”中
反应的化学方程式为N__H__3+__N__H_4。HCO3=(NH4)2CO3
知识点链接:酸式盐在过量的碱中中和成正盐。如 NaOH+NaHCO3=Na2CO3.
SiO2、 Fe2O3、 Al2O3
[2019·国I]
Mg2B2O5·H2O 、SiO2及少量 Fe2O3、Al2O3
2019年的T26与2018年的T27相比较,化学 原理考查点完全不同,元素化合物知识点的考查 点也差异大。
2019·2018·国I化学工艺流程题比较
2018
2019
化学
2019年高考理科综合能力测试化学卷(全国课标Ⅰ卷)分析报告 pdf
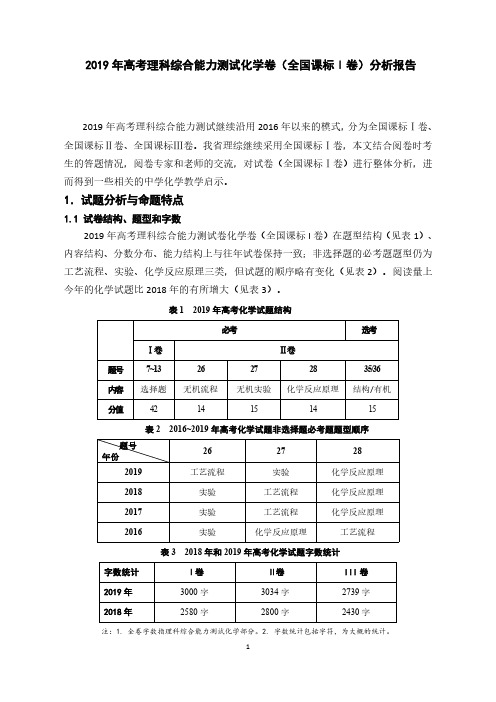
1.1 试卷结构、题型和字数 2019 年高考理科综合能力测试卷化学卷(全国课标 I 卷)在题型结构(见表 1)、
内容结构、分数分布、能力结构上与往年试卷保持一致;非选择题的必考题题型仍为 工艺流程、实验、化学反应原理三类,但试题的顺序略有变化(见表 2)。阅读量上 今年的化学试题比 2018 年的有所增大(见表 3)。
查学生对冰和 HCl 微观结构的探析。第 13 题通过新化合物
的结构,
考查学生基于原子结构和价健知识认识物质世界的能力:从结构图中“W+”推出 W 是
Li 或 Na,X 可能是 C 或 Si(形成四个共价键),Z 可能是 H 或 F 或 Cl(能形成一个
共价键),结合题干信息“Z 核外最外层电子数是 X 核外电子数的一半”得出 X 是 Si、
C
B
A
35)
杂化轨道理论、配合物
4
晶体类型及结构微粒间作用力;金
B
35(3)(4)
刚石晶胞及相关计算
3+6
有机物的结构和 命名 研究有机化合物 选 的一般方法 修 烃和卤代烃 5
烃的含氧衍生物
C
8C,36(1)(2)(3) 共面共线;官能团的名称;手性碳; 6*+1+2+
同分异构体
3
A
A
36(5)(7)
烃的溴代反应条件和反应类型
1+1*
含氧官能团的名称,醛基的性质,
C 36(1)(3)(4)(6) 酯化反应所需条件与试剂,酯的水 1*+3*+2
解反应
+2
3
续表 4:
考纲要求
2019 年考查知识及赋分
2018年高考理综I卷化学试题总体评价

2018年高考理综I卷化学试题总体评价2018年理综化学试题在题型、分值设置等方面保持相对稳定,抓住对主干知识的重点考察的同时,兼顾对学生能力、方法、学科素养的综合考察。
体现了化学试题近年来“遵循考纲,稳中求变,注重能力,综合创新”的一贯命题风格一、注重基础,突出主干,稳重求变试题涉及的知识内容覆盖了必修和选修的内容,每道题目考查的知识点明确、具体,突出了所考查范围内的主干知识。
例如第7题化学与资源回收再利用,第8题第11题有机物的性质与结构,第9题实验基础,第10题阿伏伽德罗常数,12题元素周期表和周期律及元素化合物的基本性质,第13题电化学原理。
第26题以“醋酸亚铬制备”为背景重点考查实验方案的设计与评价。
第27题(1)(3)化学方程式和电极方程式的的书写,(4)氧化还原滴定的简单计算。
28题(2)反应热的计算、平衡常数Kp的计算、平衡移动原理的应用等均属于高中化学必备的主干知识。
第35题以锂及其化合物为载体,考查了核外电子排布与能量关系、离子半径大小比较原因分析、离子空间构型、杂化类型判断、化学键类型判断、第一电离能、键能、晶格能、晶胞计算。
第36题通过由化合物A制备W的合成路线,考查有机物命名、反应类型、反应条件、分子式、同分异构体、官能团名称、简单合成路线表述等基本知识。
考查方式与2017年基本类似,选择题部分减少了水溶液中电离平衡图像的考察,增加了阿伏伽德罗常数的考察。
二、立意高远、注重能力,全面考察学生的化学核心素养试题坚持能力立意,素材呈现方式灵活多样,要求学生通过对实际事物、图像、实验装置、实验现象、结构模型的观察,综合运用所学的化学知识解决社会、生产、生活中的实际问题,突出考查了学生获取和分析信息能力、问题解决能力和实验探究能力,全面检测学生的核心素养。
例如第7题化学与资源回收再利用,突出资源的可持续利用、努力践行社会主义核心价值观;第13题电化学题型新颖,学生需要从文字信息和图像中获取信息并解决问题,题目本身不但和物理学科有一定交叉,还对污染防治有重要的现实意义。
2018年高考理科综合全国Ⅰ卷化学试题解析与启示
2018年高考理科综合全国Ⅰ卷化学试题解析与启示总体来看,2018年高考理科综合全国Ⅰ卷化学试题相对简单,难度不大,但是需要对考点的掌握比较熟练才能得高分。
以下是本人的解析与启示。
1. 尿素通式计算题(第1题)此题为考查学生对元素周期表的运用,虽然难度较为简单,但是也是必须牢记的基本公式,可见元素周期表中的C为含有一个电子的电负性最小的元素之一,故其与N形成的分子极性较小,使得尿素分子中氢键较弱,火爆性较小,所以尿素价格相对廉价。
2. 镁的消耗量计算题(第2题)此题为考查学生对化学计算方法的应用,较为简单,只需要掌握一定的化学计算方法就可以求解。
由电化学原理可知,电解质溶液中金属产生的物质量与放电量成正比,即$m=itF/n$。
解题时易错点为:1) 成分不清,注意即可;2)电流的时间单位:秒(秒)。
3. 构选题(第3题)此题为考查学生对有机物结构和化学键的理解,在解题时需要从分子的构造及分子的化学结构、分子间的相互作用入手,分析分子内部的键及分子间的力,找出各单体结构之间的安排关系。
4. 食品中硫酸盐含量的检测(第4题)此题为考查学生对卤素的特性及其外部环境的影响。
由于硫酸盐是一种较为常见的化合物,在市面上出售的多种食品中往往会含有硫酸盐成分,脱硫过程中会产生气体SO2,SO2对许多生物的影响非常大,SO2可被吸收,对人体造成的不良影响尤为危险,例如引起哮喘、过敏反应等。
5. 大气污染及其防治(第5题)此题为考查学生对大气污染因素及其防治措施的掌握。
大气污染是指大气中的气体、颗粒物和液体等污染物对环境和人体所造成的危害及其恶劣影响。
大气污染治理的措施可以从技术角度出发,包括降低发生污染的量、消减污染物排放量、促进环保产业发展、控制粉尘、靠窗户等方法,也可以从绿色发展角度出发,推广使用环保型汽车、建设生态城市等方法。
从大气环境调控的宏观角度出发,可以加强政府的法律和管理力度,遵循公众需求和区域管理原则,建立健全的监测、预警、预测、监管体系。
2018年高考理科综合(全国Ⅰ卷)化学试题解析与启示
稳中求新 注重素养 考查能力 兼顾基础——2018年全国高考Ⅰ卷理综化学试题的特点评析及2019年备
稳中求新注重素养考查能力兼顾基础———2018年全国高考Ⅰ卷理综化学试题的特点评析及2019年备考策略■广东省珠海市教育研究中心黄立生张立云2018年教育部考试中心命制的全国高考理科综合试题Ⅰ卷,主要适用地区为广东、河南、河北、山西、江西、湖北、湖南、安徽、福建和山东等10个省份使用,严格贯彻《关于深化考试招生制度改革的实施意见》基本要求,做到高考考试内容改革与高校人才选拔要求和国家课程标准相一致,尤其是要科学设计命题内容,增强基础性、综合性,着重考查考生独立思考和运用所学知识分析问题解决问题的能力。
本试题的总体设计贯彻了2017版《普通高中化学课程标准》提出“必备知识、关键能力、学科素养、核心价值”的考查目标,体现了科技创新、理论联系实际及文化自信的新时代要求与教育教学改革导向。
一、2018年理科综合化学试题特点评析(一)试卷的结构简析2018年全国高考Ⅰ卷理科综合化学试题的题型和分数分布与2017年全国高考Ⅰ卷基本一致。
在试卷结构上,这两年的化学试题都是第Ⅰ卷为选择题,第Ⅱ卷为非选择题。
其中,第Ⅰ卷选择题为7道且均为单选,每道题6分共42分;第Ⅱ卷非选择题中这两分试卷均要求考生作答4道大题,其中3道题目为必做题(分别为化学实验题、反应原理题、化工流程题)共计43分,1道为选做题(分别为“物质结构与性质”“有机化学基础”两个模块的试题)。
(二)试题总体特点分析2018年全国高考Ⅰ卷理科综合化学试题考查内容涵盖《2018年普通高等学校招生全国统一考试大纲:化学》中“化学学科特点和研究基本方法”“化学基本概念、基本原理和基本技能”“常见无机物及其应用”“常见有机物及其应用”“化学实验”“物质结构与性质”和“有机化学基础”等专题内容,并渗透了灵活多样的信息处理与应用能力考查。
试题知识覆盖面广,稳中求新,难度适中,总体难度与去年相差不大,具有连续性和稳定性,在立意上与社会生活、生产等紧密联系,在策略上注重化学基础知识、主干知识考查,在创新上积极探索化学基本方法的运用、分析解决问题的关键能力与基本化学学科素养的考查。
张新平:2019年与2018年全国高考理综I卷化学工艺流程题对比赏析共29页PPT
张新平:2Байду номын сангаас19年与2018年全国高考理 综I卷化学工艺流程题对比赏析
16、云无心以出岫,鸟倦飞而知还。 17、童孺纵行歌,斑白欢游诣。 18、福不虚至,祸不易来。 19、久在樊笼里,复得返自然。 20、羁鸟恋旧林,池鱼思故渊。
谢谢你的阅读
❖ 知识就是财富 ❖ 丰富你的人生
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
0.5。
H2O2氧化Fe2+时,还消耗H+,故要……
[2019·国I]
[2016·国II]28(5)丁组同学向盛有H2O2溶液的试管中加入 几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子 方程式为________;一段时间后,溶液中有气泡出现,并 放热,随后有红褐色沉淀生成。产生气泡的原因是 ________,生成沉淀的原因是________(用平衡移动原理解: (1)步骤①的目的是去除废铁屑表面的油污,方法是
____碱__煮__水___洗__。
27.(15分)
[2019·国I]
硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利 用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁
铵,具体流程如下:
[赏析]实验流程图解读
(3)步骤③中选用足量的H2O2,理由是_____________。分批加入H2O2,同时为 了____________,溶液要保持pH小于0.5。
(4)步骤⑤的具体实验操作有__________,经干燥得到硫酸铁铵晶体样品。 (5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数。将样品加热到150 ℃ 时,失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为__________。
回答下列问题: (1)步骤①的目的是去除废铁屑表面的油污,方法是_____________。 (2)步骤②需要加热的目的是____________,温度保持80~95℃,采用的 合适加热方式是____________。铁屑中含有少量硫化物,反应产生的气体需 要净化处理,合适的装置为___________(填标号)。
去除废铁屑 表面的油污
NaOH(aq)
→H2
加快反应速率
2Fe2++H2O2+2H+ =2Fe3++2H2O
FeSO4
蒸发、结晶、
回答下列问题:
过滤、洗涤、
( 2 ) 步 骤 ② 需 要 加 热 的 目 的 是 _ _ _ _ _ _ _ _ _ _ 干_ _燥, 温 度 保 持
80~95℃,采用的合适加热方式是__热___水__浴_____。铁屑中含有少
水均需经煮沸后迅速冷却)
[NH4Fe(SO4)2·xH2O]//除油污方法/ 加热方法及加热的目的/酸性毒气 的吸收及装置选择/双氧水的使用
理由及其使用方法/Fe、Fe2+、 Fe3+的性质/ 蒸发结晶/热重分析法 计算结晶水数确定化学式 .[无方程
式书写]
2019·2018·国I实验题比较2
2018
铵,具体流程如下:
[赏析]实验流程图解读
去除废铁屑 表面的油污
NaOH(aq)
→H2
2Fe2++H2O2+2H+ =2Fe3++2H2O
FeSO4
蒸发、结晶、
把Fe2+全部氧化为Fe3+,且不引入杂质 过滤、洗涤、 (3)步骤③中选用足量的H2O2,理由是_______干__燥____。
分批加入H2O2,同时为了_防__止__F_e_3_+_水__解_,溶液要保持pH小于
2019
背景 小题数
制备醋酸亚铬 [(CH3COO)2Cr·2H2O]
4
得分点(空)
8
基本操作(原理) 煮沸/冷却结晶/过滤//排空 气/压强差
基本仪器(名称填空) 分液(或滴液)漏斗
制备硫酸铁铵 [NH4Fe(SO4)2·xH2O]
5
8
加热及加热法/防倒吸/蒸 发结晶/过滤(洗涤) 防止倒吸装置(选择)
27.(15分)
[2019·国I]
硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利 用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁
铵,具体流程如下:
[赏析]实验流程图解读
去除废铁屑 表面的油污
NaOH(aq)
文字解读:“干净铁
屑”→洗涤(水洗) ;“方法是”→碱除
油污,加热加速。或
80~95℃,采用的合适加热方式是__热___水__浴_____。铁屑中含有少
量硫化物,反应产生的气体需要净化处理,合适的装置为 ___________(填标号)知。识点链接:FeS+2H+=H2S↑+FeSO4
用碱吸收硫化氢并防止倒吸。
C
27.(15分)
[2019·国I]
硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利 用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁
量硫化物,反应产生的气体需要净化处理,合适的装置为
___________(填标号)。
27.(15分)
[2019·国I]
硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废 为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:
[赏析]实验装置图与文字解读
回答下列问题: ( 2 ) 步 骤 ② 需 要 加 热 的 目 的 是 _加_快_ _反_ _应_ _速_ _率_ _ , 温 度 保 持
2019年与2018年全国高考理综I卷 化学实验题对比赏析
张新平
2019·2018·国I实验题比较1
实验 题
(有 机/无 机)
2018
26(14分)
2019
27(15分)
废铁屑来制备硫酸铁铵
醋酸亚铬[(CH3COO)2Cr·2H2O]制备
//操作目的简答、仪器名称/反应 离子方程式/气体与压强/化学实 验基本操作/装置缺陷。(用蒸馏
(5)2Fe2++H2O2+2H+=2Fe3++2H2O;Fe3+催化H2O2 分解产生O2;H2O2分解放热,促进Fe3+的水解,平衡Fe3+ +3H2O=Fe(OH)3+3H+正向移动。 随着H+被消耗,平衡正向移动,生成氢氧化铁沉淀。
[2019·国I]
(4)步骤⑤的具体实验操作有__________,经干燥得到硫酸 铁铵晶体样品。加热(蒸发)浓缩、冷却结晶、过滤(洗涤)
元化
计算 化学用语填空
HClH2Zn/Cr3+/(CH3COO)2Cr /CH3COONa
0 离子方程式
油脂/FeFe2+Fe3+的性质 /H2S/(NH4)2SO4Fe2(SO4)3
1 化学式
实验装置 装置评价
制备实验装置图
指出装置缺陷
制备实验流程图
无
27.(15分)
[2019·国I]
硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废 为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:
