2010版GMP无菌及非无菌要求的制剂生产洁净度要求
新版2010GMP附录(原料药)

附录2:原料药第一章范围第一条本附录适用于非无菌原料药生产及无菌原料药生产中非无菌生产工序的操作。
第二条原料药生产的起点及工序应当与注册批准的要求一致。
第二章厂房与设施第三条非无菌原料药精制、干燥、粉碎、包装等生产操作的暴露环境应当按照D级洁净区的要求设置。
第四条质量标准中有热原或细菌内毒素等检验项目的,厂房的设计应当特别注意防止微生物污染,根据产品的预定用途、工艺要求采取相应的控制措施。
第五条质量控制实验室通常应当与生产区分开。
当生产操作不影响检验结果的准确性,且检验操作对生产也无不利影响时,中间控制实验室可设在生产区内。
第三章设备第六条设备所需的润滑剂、加热或冷却介质等,应当避免与中间产品或原料药直接接触,以免影响中间产品或原料药的质量。
当任何偏离上述要求的情况发生时,应当进行评估和恰当处理,保证对产品的质量和用途无不良影响。
第七条生产宜使用密闭设备;密闭设备、管道可以安置于室外。
使用敞口设备或打开设备操作时,应当有避免污染的措施。
第八条使用同一设备生产多种中间体或原料药品种的,应当说明设备可以共用的合理性,并有防止交叉污染的措施。
第九条难以清洁的设备或部件应当专用。
第十条设备的清洁应当符合以下要求:(一)同一设备连续生产同一原料药或阶段性生产连续数个批次时,宜间隔适当的时间对设备进行清洁,防止污染物(如降解产物、微生物)的累积。
如有影响原料药质量的残留物,更换批次时,必须对设备进行彻底的清洁。
(二)非专用设备更换品种生产前,必须对设备(特别是从粗品精制开始的非专用设备)进行彻底的清洁,防止交叉污染。
(三)对残留物的可接受标准、清洁操作规程和清洁剂的选择,应当有明确规定并说明理由。
第十一条非无菌原料药精制工艺用水至少应当符合纯化水的质量标准。
第四章物料第十二条进厂物料应当有正确标识,经取样(或检验合格)后,可与现有的库存(如储槽中的溶剂或物料)混合,经放行后混合物料方可使用。
应当有防止将物料错放到现有库存中的操作规程。
(2010年版)GMP无菌药品附录(最新整理)

无菌药品附录第一章范围第一条无菌药品是指法定药品标准中列有无菌检查项目的制剂和原料药,包括无菌制剂和无菌原料药。
第二条本附录适用于无菌制剂生产全过程以及无菌原料药的灭菌和无菌生产过程。
第二章原则第三条无菌药品的生产须满足其质量和预定用途的要求,应当最大限度降低微生物、各种微粒和热原的污染。
生产人员的技能、所接受的培训及其工作态度是达到上述目标的关键因素,无菌药品的生产必须严格按照精心设计并经验证的方法及规程进行,产品的无菌或其它质量特性绝不能只依赖于任何形式的最终处理或成品检验(包括无菌检查)。
第四条无菌药品按生产工艺可分为两类:采用最终灭菌工艺的为最终灭菌产品;部分或全部工序采用无菌生产工艺的为非最终灭菌产品。
第五条无菌药品生产的人员、设备和物料应通过气锁间进入洁净区,采用机械连续传输物料的,应当用正压气流保护并监测压差。
第六条物料准备、产品配制和灌装或分装等操作必须在洁净区内分区域(室)进行。
第七条应当根据产品特性、工艺和设备等因素,确定无菌药品生产用洁净区的级别。
每一步生产操作的环境都应当达到适当的动态洁净度标准,尽可能降低产品或所处理的物料被微粒或微生物污染的风险。
第三章洁净度级别及监测第八条洁净区的设计必须符合相应的洁净度要求,包括达到“静态”和“动态”的标准。
第九条无菌药品生产所需的洁净区可分为以下4个级别:A级:高风险操作区,如灌装区、放置胶塞桶和与无菌制剂直接接触的敞口包装容器的区域及无菌装配或连接操作的区域,应当用单向流操作台(罩)维持该区的环境状态。
单向流系统在其工作区域必须均匀送风,风速为0.36-0.54m/s (指导值)。
应当有数据证明单向流的状态并经过验证。
在密闭的隔离操作器或手套箱内,可使用较低的风速。
B级:指无菌配制和灌装等高风险操作A级洁净区所处的背景区域。
C级和D级:指无菌药品生产过程中重要程度较低操作步骤的洁净区。
以上各级别空气悬浮粒子的标准规定如下表:悬浮粒子最大允许数/立方米洁净度级别静态动态(3)≥0.5μm≥5.0μm(2)≥0.5μm≥5.0μm A级(1)352020352020B级3520293520002900C级3520002900352000029000D级352000029000不作规定不作规定注:(1)为确认A级洁净区的级别,每个采样点的采样量不得少于1立方米。
2010版GMP无菌及非无菌要求的制剂生产洁净度要求

09版GMP无菌及非无菌要求的制剂生产洁净度要求无菌药品生产所需的洁净区可分为以下4个级别:A级:相当于100级(层流)高风险操作区,如:灌装区、放置胶塞桶、敞口安瓿瓶、敞口西林瓶的区域及无菌装配或连接操作的区域。
通常用层流操作台(罩)来维持该区的环境状态。
层流系统在其工作区域必须均匀送风,风速为0.36-0.54m/s。
应有数据证明层流的状态并须验证。
在密闭的隔离操作器或手套箱内,可使用单向流或较低的风速。
B级:相当于100级(动态)指无菌配制和灌装等高风险操作A级区所处的背景区域。
C级(相当于10,000级)和D级(相当于100,000级)指生产无菌药品过程中重要程度较次的洁净操作区。
以上各级别空气悬浮粒子的标准规定如下表:注:(a)指根据光散射悬浮粒子测试法,在指定点测得等于和/或大于粒径标准的空气悬浮粒子浓度。
应对A级区“动态”的悬浮粒子进行频繁测定,并建议对B级区“动态”也进行频繁测定。
A级区和B级区空气总的采样量不得少于1米3,C级区也宜达到此标准。
(b)生产操作全部结束,操作人员撤离生产现场并经15~20分钟自净后,洁净区的悬浮粒子应达到表中的“静态”标准。
药品或敞口容器直接暴露环境的悬浮粒子动态测试结果应达到表中A级的标准。
灌装时,产品的粒子或微小液珠会干扰灌装点的测试结果,可允许这种情况下的测试结果并不始终符合标准。
(c)为了达到B、C、D级区的要求,空气换气次数应根据房间的功能、室内的设备和操作人员数决定。
空调净化系统应当配有适当的终端过滤器,如:A、B和C级区应采用不同过滤效率的高效过滤器(HEPA)。
(d)本附录中“静态”及“动态”条件下悬浮粒子最大允许数基本上对应于ISO14644-10.5μm悬浮粒子的洁净度级别。
(e)这些区域应完全没有大于或等于5μm的悬浮粒子,由于无法从统计意义上证明不存在任何悬浮粒子,因此将标准设成1个/米3,但考虑到电子噪声、光散射及二者并发所致的误报因素,可采用20个/米3的限度标准。
2010版新版GMP规范附录

《药品生产质量管理规范(2010修订)》附录2011-02-25目录无菌药品 (3)第一章范围 (3)第二章原则 (3)第三章洁净度级别及监测 (3)第四章隔离操作技术 (7)第五章吹灌封技术 (8)第六章人员 (8)第七章厂房 (9)第八章设备 (11)第九章消毒 (11)第十章生产管理 (12)第十一章灭菌工艺 (14)第十二章灭菌方法 (15)第十三章无菌药品的最终处理 (18)第十四章质量控制 (18)第十五章术语 (19)第八十一条下列术语含义是: (19)原料药 (20)第一章范围 (20)第二章厂房与设施 (20)第三章设备 (20)第四章物料 (21)第五章验证 (22)第六章文件 (24)第七章生产管理 (25)第八章不合格中间产品或原料药的处理 (28)第九章质量管理 (29)第十章采用传统发酵工艺生产原料药的特殊要求 (30)第十一章术语 (32)生物制品 (34)第一章范围 (34)第二章原则 (34)第三章人员 (35)第四章厂房与设备 (35)第五章动物房及相关事项 (37)第六章生产管理 (38)第七章质量管理 (40)第八章术语 (40)血液制品 (41)第一章范围 (41)第二章原则 (41)第三章人员 (41)第四章厂房与设备 (42)第五章原料血浆 (42)第六章生产和质量控制 (44)第七章不合格原料血浆、中间产品、成品的处理 (45)中药制剂 (46)第一章范围 (46)第二章原则 (46)第三章机构与人员 (46)第四章厂房设施 (47)第五章物料 (48)第六章文件管理 (49)第七章生产管理 (49)第八章质量管理 (50)第九章委托生产 (51)第十章术语 (52)附录1无菌药品第一章范围第一条无菌药品是指法定药品标准中列有无菌检查项目的制剂和原料药,包括无菌制剂和无菌原料药。
第二条本附录适用于无菌制剂生产全过程以及无菌原料药的灭菌和无菌生产过程。
新版GMP洁净度等级A、B、C、D
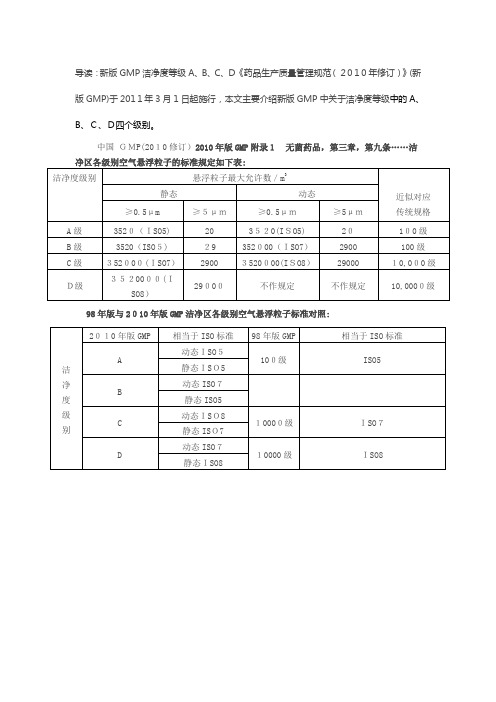
导读:新版GMP洁净度等级A、B、C、D《药品生产质量管理规范(2010年修订)》(新版GMP)于2011年3月1日起施行,本文主要介绍新版GMP中关于洁净度等级中的A、B、C、D四个级别。
98年版与2010年版GMP洁净区各级别空气悬浮粒子标准对照:新版GMP洁净度等级A、B、C、DA级洁净区洁净操作区的空气温度应为20-24℃洁净操作区的空气相对湿度应为45%-60%操作区的风速:水平风速≥0.54m/s垂直风速≥0.36m/s高效过滤器的检漏大于99.97%照度:>300lx-600lx噪音:≤75db(动态测试)B级洁净区洁净操作区的空气温度应为20-24℃洁净操作区的空气相对湿度应为45%-60%房间换气次数:≥25次/h压差:B级区相对室外≥10Pa,同一级别的不同区域按气流流向应保持一定的压差。
高效过滤器的检漏大于99.97%照度:>300lx-600lx噪音:≤75db(动态测试)C级洁净区洁净操作区的空气温度应为20-24℃洁净操作区的空气相对湿度应为45%-60%房间换气次数:≥25次/h压差:C级区相对室外≥10Pa,同一级别的不同区域按气流流向应保持一定的压差。
高效过滤器的检漏大于99.97%照度:>300lx-600lx噪音:≤75db(动态测试)D级洁净区洁净操作区的空气温度应为18-26℃洁净操作区的空气相对湿度应为45%-60%房间换气次数:≥15次/h压差:100,000级区相对室外≥10Pa,高效过滤器的检漏大于99.97%照度:>300lx-600lx噪音:≤75db(动态测试)文章为作者独立观点,不代表阿里巴巴以商会友立场。
转载此文章须经作者同意,并附上出处及文章链接。
2010新版GMP附录—无菌药品

无菌药品第一章范围第一条无菌药品是指法定药品标准中列有无菌检查工程的制剂和原料药,包括无菌制剂和无菌原料药。
第二条本附录适用于无菌制剂生产全过程以及无菌原料药的灭菌和无菌生产过程。
第二章原则第三条无菌药品的生产须满足其质量和预定用途的要求,应当最大限度降低微生物、各种微粒和热原的污染。
生产人员的技能、所接受的培训及其工作态度是达到上述目标的关键因素,无菌药品的生产必须严格按照精心设计并经验证的方法及规程进行,产品的无菌或其它质量特性绝不能只依赖于任何形式的最终处理或成品检验(包括无菌检查)。
第四条无菌药品按生产工艺可分为两类:采用最终灭菌工艺的为最终灭菌产品;部分或全部工序采用无菌生产工艺的为非最终灭菌产品。
第五条无菌药品生产的人员、设备和物料应通过气锁间进入洁净区,采用机械连续传输物料的,应当用正压气流保护并监测压差。
第六条物料准备、产品配制和灌装或分装等操作必须在洁净区内分区域(室)进行。
第七条应当根据产品特性、工艺和设备等因素,确定无菌药品生产用洁净区的级别。
每一步生产操作的环境都应当达到适当的动态洁净度标准,尽可能降低产品或所处理的物料被微粒或微生物污染的风险。
第三章洁净度级别及监测第八条洁净区的设计必须符合相应的洁净度要求,包括达到“静态”和“动态”的标准。
第九条无菌药品生产所需的洁净区可分为以下4个级别:A级:高风险操作区,如灌装区、放置胶塞桶和与无菌制剂直接接触的敞口包装容器的区域及无菌装配或连接操作的区域,应当用单向流操作台(罩)维持该区的环境状态。
单向流系统在其工作区域必须均匀送风,风速为0.36-0.54m/s(指导值)。
应当有数据证明单向流的状态并经在密闭的隔离操作器或手套箱内,可使用较低的风速。
B级:指无菌配制和灌装等高风险操作A级洁净区所处的背景区域。
C级和D级:指无菌药品生产过程中重要程度较低操作步骤的洁净区。
以上各级别空气悬浮粒子的标准规定如下表:注:(1)为确认A级洁净区的级别,每个采样点的采样量不得少于1立方M。
国家局2010版GMP实施疑难问题解答(二)

国家局2010版GMP实施疑难问题解答(二)1.非最终灭菌小容量注射剂的洗瓶、灌封、配料的洁净级别如何划分?它们的辅助功能间与其生产操作间的洁净级别一定要相同吗?如操作间是B级背景下的A级,它的辅助间是B级可以吗?答:对于非最终灭菌小容量注射剂各工艺步骤应处于何种洁净级别,药品GMP附录1第十三条给出了示例,非最终灭菌小容量注射剂洗瓶可设在D级,灌封在B级背景下的A级,可除菌过滤的药液或产品的配制在C级,无菌配料应在B级背景下的A级。
无菌药品的生产操作环境可参照该示例进行选择。
应当注意的是,核心区域的布局应合理,尽量减少辅助功能间的设置,如必须设置辅助间,应尽量减少其对核心区域的影响。
辅助间的具体洁净级别应根据在该房间内进行的操作或所存储物料和器具的特性确定。
2.我公司将小容量注射剂与大容量注射剂的浓配与稀配放在C级区,提高了浓配的洁净级别,这是否可行?答:是否可行,需要考虑浓配工序对稀配工序造成的影响是否可被接受,能否可以采取措施降低污染和交叉污染的可能性。
例如,浓配过程中可能使用大量物料,有粉尘产生,可造成污染或交叉污染(活性炭的称量、配制等)。
企业应考虑能否采取相关措施,确保将粉尘污染或交叉污染的风险降低到可以接受的水平。
3.规范要求洁净区与非洁净区之间、不同级别洁净区之间的压差应当不低于10帕斯卡,如果生产核心区域为A级,那么从核心生产区A级到非洁净区是否至少会有40帕斯卡的压差?如何达到?答:是的。
可由专业的设计院对空气净化系统进行设计,在此基础上,通过送风量与回风量的合理配置以及不同洁净级别的换气次数的差异来达到这一要求。
4.相同洁净区不同功能区域之间的压差应当多少合适?无压差可以吗?答:药品GMP第四十八条规定:洁净区与非洁净区之间、不同级别洁净区之间的压差应当不低于10帕斯卡。
必要时,相同洁净度级别的不同功能区域(操作间)之间也应当保持适当的压差梯度。
在相同级别的洁净区内不同功能区域内进行的操作有产生交叉污染潜在风险或储存的物料或器具有受到其他功能区域的污染的潜在风险时,应保持一定的压差,以防止污染和交叉污染的发生。
新版(2010)GMP中对洁净等级的规定(无菌药品附录)

附录1:无菌药品第一章范围第一条无菌药品是指法定药品标准中列有无菌检查项目的制剂和原料药,包括注射剂、眼用制剂、无菌软膏剂、无菌混悬剂等。
第二条本附录适用于无菌制剂生产全过程以及无菌原料药的灭菌和无菌生产过程。
第三条悬浮粒子、浮游菌、沉降菌和表面微生物等测试方法应按照相关标准执行。
第二章原则第四条无菌药品的生产须满足其质量和预定用途的要求,应最大限度降低微生物、各种微粒和热原的污染。
生产人员的技能、所接受的培训及其工作态度是达到上述目标的关键因素,无菌药品的生产必须严格按照精心设计并经验证的方法及规程进行,产品的无菌或其它质量特性绝不能只依赖于任何形式的最终处理或成品检验。
第五条无菌药品按生产工艺可分为两类:采用最终灭菌工艺的为最终灭菌产品;部分或全部工序采用无菌生产工艺的为非最终灭菌产品。
第六条无菌药品生产的人员、设备和物料应通过气锁间进入洁净区,如采用机械连续传输物料时,应采用正压气流保护并监测压差。
物料准备、产品配制和灌装或分装等操作必须在洁净区内分区(室)进行。
第七条应按所需环境的特点确定无菌药品洁净生产区的级别。
每一步生产操作的环境都应达到适当的动态洁净度标准,以尽可能降低产品或所处理的物料被微粒或微生物污染的风险。
第三章洁净度级别及监测第八条洁净区的设计必须符合相应的洁净度要求,包括达到“静态”和“动态”的标准。
第九条无菌药品生产所需的洁净区可分为以下4个级别:A级高风险操作区,如:灌装区、放置胶塞桶、敞口安瓿瓶、敞口西林瓶的区域及无菌装配或连接操作的区域。
通常用层流操作台(罩)来维持该区的环境状态。
层流系统在其工作区域必须均匀送风,风速为0.36-0.54m/s(指导值)。
应有数据证明层流的状态并须验证。
在密闭的隔离操作器或手套箱内,可使用单向流或较低的风速。
B级指无菌配制和灌装等高风险操作A级区所处的背景区域。
C级和D级指生产无菌药品过程中重要程度较低的洁净操作区。
以上各级别空气悬浮粒子的标准规定如下表:注:(1)为了确定A级区的级别,每个采样点的采样量不得少于1m3。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
09版GMP无菌及非无菌要求的制剂生产洁净度要求
无菌药品生产所需的洁净区可分为以下4个级别:
A级:相当于100级(层流)
高风险操作区,如:灌装区、放置胶塞桶、敞口安瓿瓶、敞口西林瓶的区域及无菌装配或连接操作的区域。
通常用层流操作台(罩)来维持该区的环境状态。
层流系统在其工作区域必须均匀送风,风速为0.36-0.54m/s。
应有数据证明层流的状态并须验证。
在密闭的隔离操作器或手套箱内,可使用单向流或较低的风速。
B级:相当于100级(动态)
指无菌配制和灌装等高风险操作A级区所处的背景区域。
C级(相当于10,000级)和D级(相当于100,000级)
指生产无菌药品过程中重要程度较次的洁净操作区。
以上各级别空气悬浮粒子的标准规定如下表:
注:
(a)指根据光散射悬浮粒子测试法,在指定点测得等于和/或大于粒径标准的空气悬浮粒子浓度。
应对A级区“动态”的悬浮粒子进行频繁测定,并建议对B级区“动态”也进行频繁测定。
A级区和B级区空气总的采样量不得少于1米3,C级区也宜达到此标准。
(b)生产操作全部结束,操作人员撤离生产现场并经15~20分钟自净后,洁净区的悬浮粒子应达到表中的“静态”标准。
药品或敞口容器直接暴露环境的悬浮粒子动态测试结果应达到表中A级的标准。
灌装时,产品的粒子或微小液珠会干扰灌装点的测试结果,可允许这种情况下的测试结果并不始终符合标准。
(c)为了达到B、C、D级区的要求,空气换气次数应根据房间的功能、室内的设备和操作人员数决定。
空调净化系统应当配有适当的终端过滤器,如:A、B和C级区应采用不同过滤效率的高效过滤器(HEPA)。
(d)本附录中“静态”及“动态”条件下悬浮粒子最大允许数基本上对应于ISO14644-1
0.5μm悬浮粒子的洁净度级别。
(e)这些区域应完全没有大于或等于5μm的悬浮粒子,由于无法从统计意义上证明不存在任何悬浮粒子,因此将标准设成1个/米3,但考虑到电子噪声、光散射及二者并发所致的误报因素,可采用20个/米3的限度标准。
在进行洁净区确认时,应达到规定的标准。
(f)须根据生产操作的性质来决定洁净区的要求和限度。
温度、相对湿度等其它指标取决于产品及生产操作的性质,这些参数不应对规定的洁净度造成不良影响。
洁净区微生物监控的动态标准(a)如下:
注:
(a)表中各数值均为平均值。
(b)可使用多个沉降碟连续进行监控,但单个沉降碟的暴露时间可以少于4小时。
第十三条无菌药品的生产操作应在符合下表中规定的相应级别的洁净区内进行,未列出的操作可参照下表在适当级别的洁净区内进行:
注:
(a)此处的高污染风险是指产品容易长菌、灌装速度很慢、灌装用容器为广口瓶、容器须暴露数秒后方可密闭等状况;
(b)此处的高污染风险是指产品容易长菌、配制后需等待较长时间方可灭菌或不在密闭容器中配制等状况。
非无菌操作:
口服液体、固体、腔道用药(含直肠用药)、表皮外用药品、非无菌的眼用制剂暴露工序及其直接接触药品的包装材料最终处理的暴露工序区域,应参照“无菌药品”附录中D级洁净区的要求设置与管理。
