热力学基础习题课
热力学习题课超经典 共24页PPT资料
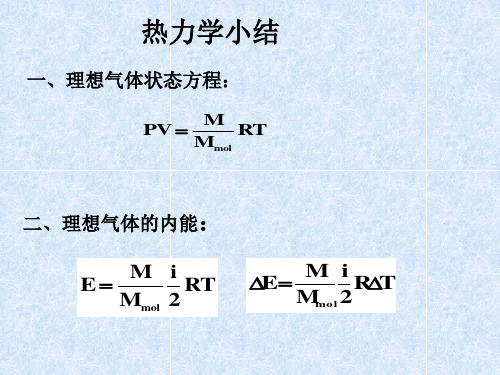
1、求Ta、Tb、Tc。 2、求气体在ab和bc 过程中吸收的热量, 气体内能的变化各如 何? 3、气体在abc过程中 最高温度如何?
P(105Pa)
1.5 b
1a
0.5
c
0 1 2 3 V(10-3m3)
P(105Pa)
1.5 b
1、由 PV M RT 1 a
Mmol
0.5
求出求Ta、Tb、Tc。 0 1
T
Skn (玻氏熵公式)
热力学第二定律的实质:一切与热现象有 关的实际宏观过程都是不可逆的。
无摩擦的准静态过程才是可逆的
熵增加原理:孤立系统内部所发生的过程 总是向着状态几率增大的方向进行
= 可逆过程
孤立系统 dS0 > 不可逆过程
例:0.1mol的单原子理想气体,经历一准 静态过程abc,ab、bc均为直线。
(A) (1)过程中吸热,(2) 过程中放热.
√(B) (1)过程中放热,(2) 过程p中吸热.
(C) 两种过程中都吸热. (D) 两种过程中都放热.
a
(2)
分析: 作一循环a(1)ba, 这是逆循环.
(1)
b
W<0, △E=0, Q<0,
O
V
(1)过程中放热;
同理可得(2) 过程中吸热。
练习13 第四题 容积为10L的盒子以速度 v=200m/s匀速运动,容器中充有质量为50g 温度为18C的氢气,设盒子突然停止,气体 的全部定向运动动能都变为气体分子热运动 动能,容器与外界没有热交换,则达到热平 衡后,氢气的温度将增加——K;氢气的压强将 增加 —— Pa
c
2 3 V(10-3m3)
2、a
b,
M QabMmoC lV(TbTa) E
热力学基础习题课共35页

66、节制使快乐增加并使享受加强。 ——德 谟克利 特 67、今天应做的事没有做,明天再早也 是耽误 了。——裴斯 泰洛齐 68、决定一个人的一生,以及整个命运 的,只 是一瞬 之间。 ——歌 德 69、懒人无法享受休息之乐。——拉布 克 70、浪费时间是一桩大罪过。——卢梭
热力学基础习题课
16、自己选择的路、跪着也要把它走 完。 17、一般情况下)不想三年以后的事, 只想现 在的事 。现在 有成就 ,以后 才能更 辉煌。
18、敢于向ห้องสมุดไป่ตู้暗宣战的人,心里必须 充满光 明。 19、学习的关键--重复。
20、懦弱的人只会裹足不前,莽撞的 人只能 引为烧 身,只 有真正 勇敢的 人才能 所向披 靡。
第13章 热力学基础习题及答案

第十三章习题热力学第一定律及其应用1、关于可逆过程和不可逆过程的判断:(1) 可逆热力学过程一定是准静态过程.(2) 准静态过程一定是可逆过程.(3) 不可逆过程就是不能向相反方向进行的过程.(4) 凡有摩擦的过程,一定是不可逆过程.以上四种判断,其中正确的是。
2、如图所示,一定量理想气体从体积V1,膨胀到体积V2分别经历的过程是:A→B等压过程,A→C等温过程;A→D绝热过程,其中吸热量最多的过程。
3、一定量的理想气体,分别经历如图(1) 所示的abc过程,(图中虚线ac为等温线),和图(2) 所示的def过程(图中虚线df为绝热线).判断这两种过程是吸热还是放热.abc过程热,def过程热.4、如图所示,一绝热密闭的容器,用隔板分成相等的两部分,左边盛有一定量的理想气体,压强为p0,右边为真空.今将隔板抽去,气体自由膨胀,当气体达到平衡时,气体的压强是。
(=γC p/C V)5、一定量理想气体,从同一状态开始使其体积由V1膨胀到2V1,分别经历以下三种过程:(1) 等压过程;(2) 等温过程;(3)绝热过程.其中:__________过程气体对外作功最多;____________过程气体内能增加最多;__________过程气体吸收的热量最多.VV答案1、(1)(4)是正确的。
2、是A-B 吸热最多。
3、abc 过程吸热,def 过程放热。
4、P 0/2。
5、等压, 等压, 等压理想气体的功、内能、热量1、有两个相同的容器,容积固定不变,一个盛有氦气,另一个盛有氢气(看成刚性分子的理想气体),它们的压强和温度都相等,现将5J 的热量传给氢气,使氢气温度升高,如果使氦气也升高同样的温度,则应向氨气传递热量是 。
2、 一定量的理想气体经历acb 过程时吸热500 J .则经历acbda 过程时,吸热为 。
3、一气缸内贮有10 mol 的单原子分子理想气体,在压缩过程中外界作功209J ,气体升温1 K ,此过程中气体内能增量为 _____ ,外界传给气体的热量为___________________. (普适气体常量 R = 8.31 J/mol· K)4、一定量的某种理想气体在等压过程中对外作功为 200 J .若此种气体为单 原子分子气体,则该过程中需吸热_____________ J ;若为双原子分子气体,则 需吸热______________ J.p (×105 Pa)3 m 3)5、 1 mol 双原子分子理想气体从状态A (p 1,V 1)沿p -V 图所示直线变化到状态B (p 2,V 2),试求:(1) 气体的内能增量. (2) 气体对外界所作的功. (3) 气体吸收的热量. (4) 此过程的摩尔热容.(摩尔热容C =T Q ∆∆/,其中Q ∆表示1 mol 物质在过程中升高温度T ∆时所吸收的热量.)答案1、3J2、-700J3、124.7 J ,-84.3 J4、500J ;700J5、解:)(25)(112212V p V p T T C E V -=-=∆ (2) ))((211221V V p p W -+=, W 为梯形面积,根据相似三角形有p 1V 2= p 2V 1,则)(211122V p V p W -=. (3) Q =ΔE +W =3( p 2V 2-p 1V 1 ).(4) 以上计算对于A →B 过程中任一微小状态变化均成立,故过程中ΔQ =3Δ(pV ). 由状态方程得 Δ(pV ) =R ΔT , 故 ΔQ =3R ΔT ,摩尔热容 C =ΔQ /ΔT =3R .p p p 12循环过程1、 如图表示的两个卡诺循环,第一个沿ABCDA 进行,第二个沿A D C AB ''进行,这两个循环的效率1η和2η的关系及这两个循环所作的净功W 1和W 2的关系是 η1 η2 ,W 1 W 22、 理想气体卡诺循环过程的两条绝热线下的面积大小(图中阴影部分)分别为S 1和S 2,则二者的大小关系是:3、一卡诺热机(可逆的),低温热源的温度为27℃,热机效率为40%,其高温热源温度为_______ K .今欲将该热机效率提高到50%,若低温热源保持不变,则高温热源的温度应增加________ K .4、如图,温度为T 0,2 T 0,3 T 0三条等温线与两条绝热线围成三个卡诺循环:(1) abcda ,(2) dcefd ,(3) abefa ,其效率分别为η1_________,η2__________,η 3 __________.5、一卡诺热机(可逆的),当高温热源的温度为 127℃、低温热源温度为27℃时,其每次循环对外作净功8000 J .今维持低温热源的温度不变,提高高温热源温度,使其每次循环对外作净功 10000 J .若两个卡诺循环都工作在相同的两条绝热线之间,试求: (1) 第二个循环的热机效率; (2) 第二个循环的高温热源的温度.6、 1 mol 单原子分子理想气体的循环过程如T -V 图所示,其中c 点的温度为T c =600 K .试求:(1) ab 、bc 、c a 各个过程系统吸收的热量; (2) 经一循环系统所作的净功; (3) 循环的效率. BAC DC 'D 'p p-3m 3)p O 3T 0 2T 0 T 0fad b c e(注:循环效率η=W /Q 1,W 为循环过程系统对外作的净功,Q 1为循环过程系统从外界吸收的热量ln2=0.693)答案 1、=;<2、S 1 = S 2.3、500 ; 1004、33.3% ; 50%; 66.7%5、解:(1) 1211211T T T Q Q Q Q W -=-==η 2111T T T W Q -= 且 1212T TQ Q =∴ Q 2 = T 2 Q 1 /T 1即 212122112T T T W T T T T T Q -=⋅-==24000 J 由于第二循环吸热 221Q W Q W Q +'='+'=' ( ∵ 22Q Q =') =''='1/Q W η29.4% (2) ='-='η121T T 425 K6、解:单原子分子的自由度i =3.从图可知,ab 是等压过程,V a /T a = V b /T b ,T a =T c =600 KT b = (V b /V a )T a =300 K (1) )()12()(c b c b p ab T T R i T T C Q -+=-= =-6.23×103 J (放热) )(2)(b c b c V bc T T R iT T C Q -=-= =3.74×103 J (吸热) Q ca =RT c ln(V a /V c ) =3.46×103 J (吸热) (2) W =( Q bc +Q ca )-|Q ab |=0.97×103 J (3) Q 1=Q bc +Q ca , η=W / Q 1=13.4%热力学第二定律1、根据热力学第二定律判断下列说法的正误: (A) 功可以全部转换为热,但热不能全部转换为功. ( ) (B) 热可以从高温物体传到低温物体,但不能从低温物体传到高温物体 ( )(C) 不可逆过程就是不能向相反方向进行的过程.()(D) 一切自发过程都是不可逆的.()2、热力学第二定律的开尔文表述和克劳修斯表述是等价的,表明在自然界中与热现象有关的实际宏观过程都是不可逆的,开尔文表述指出了___________________________的过程是不可逆的,而克劳修斯表述指出了________________的过程是不可逆的.3、所谓第二类永动机是指________________________________________,它不可能制成是因为违背了________________________________________.答案1、⨯,⨯,⨯,√2、功变热;热传导3、从单一热源吸热,在循环中不断对外作功的热机;热力学第二定律。
热力学基础习题课-田浩.ppt

V C T
CP dT
பைடு நூலகம்
M
CV dT
PV C1 绝 Q 0 1 P T C2 热 TV 1 C3
0
M
CV dT
CV dT
0
题 型
1、理想气体各种等值、绝热过程的功、热 量和内能变化的计算。(5道) 2、热机效率及制冷机制冷系数的计算。 (3道) 3、热力学第二定律,及熵变的计算。 (2道)
A
B
VB
(2)B气体对外做功为 A U CV ,m (TB T0 ) 0.55T0
所以A气体对外做功0.55RT0.
(3)对A气体应用热力学第一定律,有
Q U A CV ,m (TA T0 ) A 2.5R(2.78T0 T0 ) 0.55RT 5RT0
热力学基础
一、热力学基本概念:热力学系统、热力学过程、
内能、功、热量、热容
U M
定压摩尔:C p dT p
i 对于理想气体: CV R 2
Q
CV T
A pdV
V1
V2
Q dU 定容摩尔:CV dT dT V V
Q0 A 解:(2)a到b过程,
B
b到c过程,等容降压,放热 Qbc CV ,m (Tc Tb ), CV ,m 2.5R
1 所以 Tb 2 Ta , Tc Ta 273K
V V 1Ta ( ) 1Tb , 1.4 2
所以 Qbc CV ,m (Ta 2 1Ta )
C A B
D
解:(1)由题意可知,A,B两室中气体的变化过程为准静 态过程。且 vA vB v 对于A室气体,经历等容过程,有 QA vCV ,m (TA T0 ) 对于B室气体,经历等压过程,有 QB vC p,m (TB T0 ) 因为 QA QB Q ,所以 C p,m TB T0 7 CV ,m TA T0 5 根据迈耶公式: Cp,m CV ,m R ,所以 CV ,m 5R / 2, Cp,m 7R / 2 (2)B室中气体的做功为 A pV vR(TB T0 ) 所以
大学物理热学习题课

dN m 32 4 ( ) e Ndv 2kT
v2
对于刚性分子自由度 单原子 双原子 多原子
i tr
(1)最概然速率
2kT 2 RT RT vp 1.41 m
(2)平均速率
i=t=3 i = t+r = 3+2 = 5 i = t+r = 3+3 =6
6、能均分定理
8kT 8 RT RT v 1.60 m
M V RT ln 2 M mol V1
QA
绝热过程
PV 常量
M E CV T M mol
(2)由两条等温线和两条绝热线 组成的循环叫做 卡诺循环。 •卡诺热机的效率
Q0
Q2 T2 卡诺 1 1 Q1 T1
M P1V1 P2V2 A CV T M mol 1
E 0
•热机效率
A Q1 Q2
M E CV T M mol M Q C P T M mol
A Q1 Q2 Q2 1 Q1 Q1 Q1
A=P(V2-V1) 等温过程
A
E 0
Q1 Q2 •致冷系数 e W Q1 Q2
热机效率总是小于1的, 而致冷系数e可以大于1。
定压摩尔热容
比热容比
CP ( dQ )P dT i2 i
8、平均碰撞次数 平均自由程
z
2d v n
2
CV •对于理想气体:
Cp
v z
1.热力学第一定律
1 2 2d n
二、热 力 学 基 础
Q ( E2 E1 ) A dQ dE dA
准静态过程的情况下
4. 摩尔数相同的两种理想气体 一种是氦气,一种是氢气,都从 相同的初态开始经等压膨胀为原 来体积的2倍,则两种气体( A ) (A) 对外做功相同,吸收的热量 不同. (B) 对外做功不同,吸收的热量 相同. (C) 对外做功和吸收的热量都不 同. (D) 对外做功和吸收的热量都相 同. A=P(V2-V1)
热力学第一定律习题课 (1)全

= 1.3%
(5)
P
qm ws
220 t/h103 kg/t 3600 s/h
1.1361 03
kJ/kg
=
6.94 104
kW
讨论
(1)本题的数据有实际意义,从计算中可以看到,忽略进出 口的动、位能差,对输轴功影响很小,均不超过3%,因此在实 际计算中可以忽略。 (2)蒸汽轮机散热损失相对于其他项很小,因此可以认为一 般叶轮机械是绝热系统。
m2u2 m1u1 m2 m1 h 0
u2
m2
m1 h
m2
m1u1
方法三 取充入气罐的m2-m1空气为闭口系
Q U W
Q 0 ? W ? U ?
U m2 m1 u2 u
W W1 W2 m2 m1 pv W2
2
则 Q23 U23 W23 U3 U2 87.5 kJ175 kJ 87.5 kJ
U1 U3 U123 87.5 kJ (77.5 kJ) 165 kJ
讨论
热力学能是状态参数,其变化只决定于初 终状态,于变化所经历的途径无关。
而热与功则不同,它们都是过程量,其变 化不仅与初终态有关,而且还决定于变化所 经历的途径。
1 2
(cf23
c22 )
ws
因为w3 0,所以
燃烧室 压 气 机
cf 3' 2 q (h3' h2 ) cf22
2 670103 J/kg- (800 - 580) 103 J/kg + (20 m/s)2 = 949 m/s
( 4 ) 燃气轮机的效率
取燃气轮机作为热力系,因为燃气在
( 5 ) 燃气轮机装置的总功率 装置的总功率=燃气轮机产生的功率-压气机消耗的功率
统计热力学基础习题课

统计热力学基础习题课一、内容提要1、微观粒子的运动形式和能级公式n e r t εεεεεε++++=v式中,ε:粒子的总能量,t ε:粒子整体的平动能,r ε:转动能,v ε:振动能,e ε:电子运动能,n ε:核运动能。
(1)三维平动子)(82222222cn b n a n m h z y xt ++=ε式中,h :普朗克常数;m :粒子的质量;a ,b ,c :容器的三个边长,n x ,n y ,n z 分别为x ,y ,z 轴方向的平动量子数,取值1,2,3……。
对立方容器)(8222322z y x t n n n mVh ++=ε基态n x = 1,n y = 1,n z = 1,简并度10,=t g ,而其他能级的简并度要具体情况具体分析,如32286mVh t =ε的能级,其简并度g = 3。
(2)刚性转子双原子分子 )1(822+=J J Ih r πε式中,J :转动量子数,取值0,1,2……,I :转动惯量,20R I μ=,μ:分子的折合质量,2121m m m m +=μ,0R :分子的平衡键长,能级r ε的简并度 g r = 2J+1(3)一维谐振子νυεh )21(v +=式中,ν:分子的振动频率,υ:振动量子数,取值0,1,2……,各能级都是非简并的,g v = 1对三维谐振子, νυυυεh z y x )23(v +++=2)2)(1(v ++=s s g , 其中s=υx + υy + υz(4)运动自由度:描述粒子的空间位置所必须的独立坐标的数目。
2、能级分布的微态数和Boltzmann 分布 (1)能级分布的微态数能级分布:N 个粒子分布在各个能级上的粒子数,叫做能级分布数,每一套能级分布数称为一种分布。
微态数:实现一种分布的方式数。
定域子系统能级分布微态数 ∏=i i n i D n g N W i!!离域子系统能级分布微态数 ∏=i i n i D n g W i!系统总的微态数 ∑=ΩDD W(2)最概然分布等概率定理:对N ,U ,V 确定的系统,每个可能的微态出现的概率相等。
热力学基础习题课PPT学习教案

解:Q E W E 350130 220J Q 40 220 260J Q 60 220 280J
第11页/共20页
5.设在某一过程P中,系统由状态A变为状态B,如果 沿相反方 向进行,可以经过与原来一样的那些中间过程,而重新回到初 态,外界未发生任何变化,则过程P称为可逆过程;如果沿相 反方向进行,不能重复与原来一样的那些中间过程回到初态, 或回到初态而外界不能完全恢复,则过程P称为不可逆过程。 6. 一卡诺制冷机,低温热源的温度为300K,高温热源的温度 为450K,每一循环过程从低温热源吸热400J,则每一循环过
Wab
P(Vb
Va )
1.25105 5
(20) 103
2.5103
J
Qab CP (Tb Ta ) 2 8.31 (300) 6232.5 J
b c 等体过程
3 Wbc 0 Qbc CV (Tc Tb ) 2 8.31 300 3739.5 J
c a 等温过程
Wca
WQcWa aRbTlWnbVVacc
程外界必须做功为200 J 。
解: Q2 T2 W T1 T2
第12页/共20页
三、计算题
1. 一定质量的单原子分子理想气体,开始时处于状态a,体积 为1升,压强为3atm,先作等压膨胀至b态,体积为2升,再作 等温膨胀至c态,体积为3升,最后等体降压到1atm的压强, 求:(1)气体在全过程中内能的改变;(2)气体在全过程 中所作的功和吸收的热量。
J
Wadb Qadb 4.54103 J E 0
第16页/共20页
4.如图示,为1摩尔理想气体(其 )。ln 2 0.69
C p 5 )的循环过程(
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
解:(1) E 0
2
a
d
Wab
Qab
M
7 RT 2
700
J Q E W
W 200 J
E
M
CV T
M
5 RT 2
500
J
7.设高温热源的热力学温度是低温热源的热力学温度的n倍,
则理想气体在一次卡诺循环中,传给低温热源的热量是从高
温热源吸取的热量的 [ (A) n倍 (B) n-1倍
]C
(C)
1倍
n
(D) n 1 倍
n
解:卡诺循环 1 Q2 1 T2
第7章 热力学基础 习题课
一、选择题 答案:1、B;2、B;3、B;4、D;5、D;6、D;7、C。
二、填空题
答案:1、等温 ;2、 绝热 ;3、 0.758 105 Pa 60.5 J
4、260 J -280J ; 5、沿反方向进行,可以经过和原来一 样的那些状态,而又重新回到初态,外界未发生任何变化 沿过程反方向进行,不能重复原来所有状态或重新回到初 态而外界不能完全恢复 ; 6、200J 。
6. 一卡诺制冷机,低温热源的温度为300K,高温热源的温度 为450K,每一循环过程从低温热源吸热400J,则每一循环过
程外界必须做功为200 J 。
解: Q2 T2 W T1 T2
三、计算题
1. 一定质量的单原子分子理想气体,开始时处于状态a,体积 为1升,压强为3atm,先作等压膨胀至b态,体积为2升,再作 等温膨胀至c态,体积为3升,最后等体降压到1atm的压强, 求:(1)气体在全过程中内能的改变;(2)气体在全过程 中所作的功和吸收的热量。
A:1/3 B:1/4
C:2/5 D:2/7
解:W PV M RT
M
Q CPT
W R 2 Q CP 7
6.双原子的理想气体做等压膨胀,若气体在膨胀过程中,从
外界吸收的热量为700J,则该气体对外做功为 [ D ]
A:350J B:300J C:250J D:200Jcbda
[ B]
(A) -1200J (B) -1000 J (C) -700J (D) 1000J
解:
PV T
C Ta Tb Ea Eb
Q E W
其中:Q 200 J E 0 J WACB Q 200 J
WDA P(VA VD ) 1200 J Q WACB WBD WDA 1000 J
作功40J,传入系统的热量Q= 260 J (2)当系统由状态b
沿曲线ba返回状态a时,外界对系统作功60J,则系统吸收的
热量Q= 280 J 。
解:Q E W E 350 130 220 J
Q 40 220 260 J
Q 60 220 280 J
5.设在某一过程P中,系统由状态A变为状态B,如果 沿相反方 向进行,可以经过与原来一样的那些中间过程,而重新回到初 态,外界未发生任何变化,则过程P称为可逆过程;如果沿相 反方向进行,不能重复与原来一样的那些中间过程回到初态, 或回到初态而外界不能完全恢复,则过程P称为不可逆过程。
一、选择题
1. 理想气体经历如图所示的abc平衡过程,则该系统对外做功
W,从外界吸收热量Q和内能的增量△E的正负情况 [ B ]
A:△E>0,Q>0,W<0 B:△E>0,Q>0,W>0
C:△E>0,Q<0,W<0 D:△E<0,Q<0,W>0
P
解:Q=△E+W
bc
a
V
2.如图,一定量的理想气体经历acb过程时吸热200J,则经
a
c
a cb Q2 QacQcb Eac QcbEab Qcb
a’ ②
c b 等温压缩 Qcb< 0 Q2 < Q1 O
T
4.根据热力学第二定律可知:
[ D]
A:功可以全部转换为热,但热不能全部转换为功。
B:热可以从高温物体传到低温物体 但不能从低温物体传到高温物体
C:不可逆过程就是不能向相反方向进行的过程
3. 右图,一定量的理想气体分别由初态a经①过程ab和由初态a
经②过程acb到达相同的终态b,则两个过程中气体从外界吸收
的热量Q1,Q2的关系为: [ B ]
A:Q1<0, Q1>Q2 B:Q1>0, Q1>Q2
p
C:Q1<0, Q1>Q2 D:Q1>0, Q1<Q2
b ①
解: a b 等体降压 Q1 Eab
解: (1)等压 Va Vb Ta Tb
Tb
Vb Va
Ta
2Ta
Pa Pb 3 atm
等温 等体
PbVb PcVc
Pc Pd Tc Td
Td
Pc
Vb
Pd Pc
Vc Tc
Pa Ta
2 3
Pb
2
atm
E 0
(2)W
Q
Wab
Wbc
P(Vb
Va ) PV
ln Vc Vb
550
J
2.如图示,1mol氧气,由状态a变化到状态b,试求下列三种情 况下,气体内能的改变、所作的功和吸收的热量:
D:一切自发过程都是不可逆的
解:A不正确,热可以全部转化为功,只是会引起其他变化。 例如等温膨胀时气体吸热全部转化成功,不过体积改变了。
B不正确,热量可以从低温物体传到高温物体,不过外界会有 变化,要有外界做功。
5.对于室温下的双原子分子理想气体,在等压膨胀的情况下,
系统对外所作的功与从外界吸收的热量之比W/Q等于 [ D ]
绝热膨胀到体积增大一倍时,气体压强为0.758105 Pa,此过
程中所作的功为 60.5 J 。
解: P P 0.714 5 7
VV P1V1 P2V2
7 P2
P1V1 5 V2
W P1V1 P2V2
1
4.如图,一理想气体系统由状态a沿acb到达状态b,有350J的 热量传入系统,而系统做功130J,(1)经过adb过程,系统
Q1
T1
Q2 T2 1 Q1 T1 n
二、填空题
1.理想气体 等温 过程中,系统吸收的热量可用P-V上过程曲 线下的面积表示。
2.一定质量的理想气体经压缩后,体积减小为原来的一半,这 个过程可能是绝热、等温或等压过程,如果要使外界做的功最 大,那么,这个过程应该是 绝热 过程。
3.某理想气体在P——V图上其等温线的斜率与绝热线的斜率 之比为0.714,当此理想气体由压强 2105 帕,体积0.5升之状态
