(完整版)食品化学(知识点)
食品化学主要知识点

第一章水1、水结冰时体积增大;0℃下冰的导热值约为同温度下水的4倍;冰的热扩散速率是水的9倍;温差相等时,生物组织的冷冻速率比解冻速率更快。
(P11)2、分子的缔合:水分子在三维空间形成多重氢键键合,每个水分子具有相等数目的氢键给体和受体,能够在三维空间形成氢键网络结构。
(P13)3、水分子缔合的原因:①H-O键间电荷的非对称分布使H-O键具有极性,这种极性使分子之间产生引力;②由于每个水分子具有数目相等的氢键供体和受体,因此可以在三维空间形成多重氢键;③静电效应。
(P13)4、持水容量:通常用来描述基质分子(一般指大分子化合物)截留大量水的能力。
(P20)5、食品中水的存在形式:体相水(自由水、截留水)和结合水(化合水、邻近水、多分子层水)(P19)6、水与离子和离子基团的相互作用:①由于水中添加可解离的溶质,使纯水考氢键键合形成的四面体排列的正常结构遭到破坏②由于既不具有氢键受体又没有给体的简单无机离子,它们与水相互作用时仅仅是离子-偶极的极性结合③在稀水溶液中一些离子具有净结构破坏效应,这些离子大多为负离子和大的正离子,如:K+,Rb+,NH4+,Cl-,Br-,I-,NO3-,BrO3-,IO3-,ClO4-等④另外一些离子具有净结构形成效应,这些离子大多是电场强度大,离子半径小的离子。
如:Li+,Na+,Ca2+,Ba2+,Mg2+,Al3+,F-,OH-等(P23)7、水具有氢键键合能力的中性基团的相互作用:①水与溶质之间的氢键键合比水与离子之间的相互作用弱②氢键作用的强度与水分子之间的氢键相近③水能与某些基团,例如羟基、氨基、羰基、酰氨基和亚氨基等极性基团,发生氢键键合。
④结晶大分子的亲水基团间的距离是与纯水中最邻近两个氧原子间的距离相等⑤如果在水合大分子中这种间隔占优势,这将会促进第一层水和第二层水之间相互形成氢键⑥在生物大分子的两个部位或两个大分子之间可形成由几个水分子所构成的“水桥”8、水与非极性物质的相互作用:①水中加入疏水性物质,疏水基团与水分子产生斥力,从而使疏水基团附近的水分子之间的氢键键合增强,结构更为有序②疏水基团之间相互聚集,从而使它们与水的接触面积减小,结果导致自由水分子增多③非极性物质具有两种特殊的性质,蛋白质分子产生的疏水相互作用,极性物质能和水形成笼形水合物9、疏水水合:向水中添加疏水物质时,由于它们与水分子产生斥力,从而使疏水基团附近的水分子之间的氢键键合增强,使得熵减小,此过程成为疏水水合。
食品化学的知识点总结

食品化学的知识点总结一、食品成分食品的化学成分是指食品中含有的各种化学物质。
食品成分主要包括水分、蛋白质、脂肪、碳水化合物、维生素和矿物质等。
这些成分对于食品的营养价值和风味都有很大的影响。
1. 水分水是食品中最主要的成分之一,对于食品的质地、口感和营养价值都有着重要的影响。
食品中的水分含量是影响食品贮存以及微生物、酶、氧化、酶解等变质的主要因素之一。
2. 蛋白质蛋白质是食品中的主要营养成分,它是由氨基酸组成的,对于维持人体正常的生理功能和机体的发育都有重要的意义。
蛋白质在食品中的作用主要有增加食品的营养价值、影响食品的质地和口感等。
3. 脂肪脂肪是食品中的主要能量来源,也是体内沉积物和传导器,对于维持人的正常生理功能有重要的作用。
食品中的脂肪含量会影响食品的口感、香味和营养价值。
4. 碳水化合物碳水化合物是人体的主要能量来源,是构成膳食纤维的主要成分,对于维持人体生命活动和保持体能都有着重要的意义。
食品中的碳水化合物含量会影响食品的甜度、质地和口感。
5. 维生素维生素是对人体的新陈代谢活动和细胞分裂具有重要作用的微量营养素。
食品中的维生素种类繁多,对于维持人体的正常生理功能和增强人体的抵抗力都有着重要的作用。
6. 矿物质矿物质是人体必需的微量元素,对于人体的生理功能具有重要的作用。
食品中的矿物质种类繁多,对于人体的正常生长和发育都有着重要的意义。
二、食品的味道和香味的形成食品的味道和香味的形成是由于食品中的各种化学成分对人的感官器官产生的感觉。
食品的味道主要来自于咸、甜、酸、苦、鲜等味道,食品的香味主要来自于食品中的挥发性物质。
1. 咸味很多食品中都含有盐分,食品中的盐分会使食品呈现出咸味。
人的舌头上具有咸味感受器,当含有盐分的食品进入口腔时,就会产生咸味的感觉。
2. 甜味食品中含有碳水化合物会使食品呈现出甜味,当含有碳水化合物的食品进入口腔时,就会产生甜味的感觉。
3. 酸味食品中含有有机酸或无机酸会使食品呈现出酸味,当含有酸性物质的食品进入口腔时,就会产生酸味的感觉。
食品化学复习知识点

食品化学复习知识点一、名词解释1、食品化学:是从化学角度和分子水平上研究食品的化学组成、结构、理化性质、营养和安全性质以及它们在生产、加工、储存和运销过程中的变化及其对食品品质和安全性影响的科学。
2、构型:一个分子各原子在空间的相对分布或排列,即各原子特有的固定的空间排列,使该分子所具有的特定的立体结构形式。
3、变旋现象:当单糖溶解在水中的时候,由于开链结构和环状结构直接的相互转化,出现的一种现象。
4、间苯二酚反应:5、膨润现象:淀粉颗粒因吸水,体积膨胀到数十倍,生淀粉的胶束结构即行消失的现象。
6、糊化:生淀粉在水中加热至胶束结构全部崩溃,淀粉分子形成单分子,并为水所包围而成凝胶状态,由于淀粉分子是链状或分支状,彼此牵扯,结果形成具有粘性的糊状黏稠体系的现象。
7、淀粉老化:经过糊化后的淀粉在室温或低于室温的条件下放置后,溶液变得不透明甚至凝结而沉淀的现象。
8、多糖(淀粉)的改性:指在一定条件下通过物理或化学的方法使多糖的形态或结构发生变化,从而改变多糖的理化性能的过程。
(如胶原淀粉)9、同质多晶现象:同一种物质具有不同固体形态的现象。
10、油脂塑性:指在一定压力下表现固体脂肪具有的抗应变能力。
11、油脂的精炼:采用不同的物理或化学方法,将粗油(直接由油料中经压榨、有机溶剂提取到的油脂)中影响产品外观(如色素等)、气味、品质、的杂质去除,提高油脂品质,延长储藏期的过程。
(碱炼:NaOH去除游离脂肪酸)12、氨基酸的等电点:当氨基酸在某一pH值时,氨基酸所带正电荷和负电荷相等,即净电荷为零,此时的pH值成为氨基酸的等电点。
13、蛋白石四级结构:由多条各自具有三级结构的肽链通过非共价键连接起来的结构形式。
14、蛋白质的变性:把蛋白质二级及其以上的高级结构在一定条件下(如加热、酸、碱、有机溶剂、重金属离子等)遭到破坏而一级结构并未发生变化的过程。
15、水合性质:由于蛋白质与水的相互作用,使蛋白质内一部分水的物理化学性质不同于正常水。
食品化学复习知识点

水1.冰:是水分子通过氢键有序排列成巨大且长的晶体。
2.冷冻食品中常见的4种冰晶体结构:六方形、不规则树枝状、粗糙的球形和易消失的球晶。
3.冰的特性——过冷(1)过冷是由于无晶核存在,当液体水冷却到冰点(0℃)以下仍不析出固体的现象(常常先被冷却成过冷状态,只有当温度降低到开始出现稳定性晶核时,或在震动促进下才会立即向冰晶体转化并促使温度回升到0℃,开始出现稳定性晶核的温度叫过冷温度)(2)若向冷水中投入一粒冰晶或摩擦器壁产生冰晶,过冷现象立即消失(3)过冷溶液中加入晶核,晶核逐渐形成长大的结晶,这种现象称之为异相成核(4)冰晶体的大小和结晶速度受溶质、温度、温度降低速度、溶质的种类和数量等因素影响4.水在食品中的存在状态:自由水、结合水(1)结合水特点:呈现低的流动性,在-40℃不会结冰,不能作为所加入溶质的溶剂,在质子核磁共振实验中使氢的谱线变宽(2)结合水分类:化合水——单层水——多层水——(自由水)(3)游离水分类:滞化水、毛细管水、自由流动水5.水与溶质的相互作用(1)水与离子或离子基团的相互作用:水合作用(2)水与极性基团的相互作用:各种有机分子与水之间的作用以氢键为主要方式(3)水与非极性基团的相互作用:主要为疏水水合作用疏水水合:含有非极性基团的烃类、脂肪酸、氨基酸以及蛋白质加入水中,由于极性的差异使疏水基尽可能聚集在一起以减少它们与水的接触,此过程称为疏水水合6.水分活度(Aw):在一定温度下,食品中水的蒸气压和该温度下纯水的饱和蒸气压的比值Aw与温度的关系:温度升高时,Aw随之升高,这对密封在袋中或罐内食品的稳定性有很大影响7.水的吸湿等温线:在一定温度条件下,用来联系食品的含水量(用每单位干物质中的水含量表示)与其水活度的关系图(MSI)【结合食品的吸湿等温线,解释各区间水的存在形式】区间Ⅰ:化合水,水与溶质结合最紧密区间Ⅰ与区间Ⅱ之间:化合水+单层水区间Ⅱ:化合水+单层水+多层水区间Ⅱ与区间Ⅲ之间:出现游离水区间Ⅲ:游离水,既可以作为溶剂,又有利于微生物生长8.滞后现象:食品的脱附曲线与吸湿曲线理论上应该一致,但实际不能重叠的现象【简述Aw与食品保存性的关系】1.Aw与微生物生命活动的关系:不同类群微生物生长繁殖的最低Aw范围是:大多数细菌为0.94-0.99,大多数霉菌为0.8.-0.94,大多数耐盐细菌为0.75,耐干燥霉菌和耐高渗透压酵母为0.60-0.65,、在Aw低于0.60时,绝大多数微生物就无法生长。
食品化学知识点
食品化学知识点第一章水1、在冷冻食品中存在4中主要的冰晶体结构:六方形、不规则树枝状、粗糙的球形和易消失的球晶以及各种中间状态的晶体。
2、冰的特性—过冷A】食品中水的蒸汽压和该温度下纯水的饱和蒸汽压的比值。
3、【水分活度W4、水在食品中以游离水和结合水两种状态存在的。
5、结合水的特性:①在-40℃不会结冰;②不能作为所加入溶质的溶剂;③在质子核磁共振试验中使氢的谱线变宽。
6、各种有机分子与水之间的作用以氢键为主要方式。
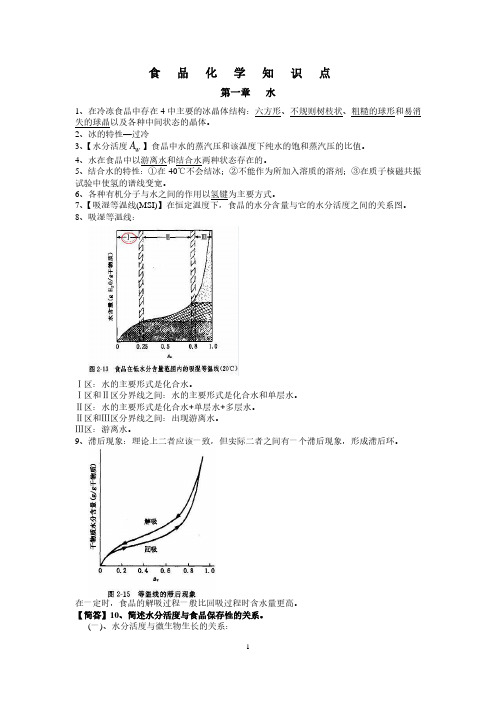
7、【吸湿等温线(MSI)】在恒定温度下,食品的水分含量与它的水分活度之间的关系图。
8、吸湿等温线:Ⅰ区:水的主要形式是化合水。
Ⅰ区和Ⅱ区分界线之间:水的主要形式是化合水和单层水。
Ⅱ区:水的主要形式是化合水+单层水+多层水。
Ⅱ区和Ⅲ区分界线之间:出现游离水。
Ⅲ区:游离水。
9、滞后现象:理论上二者应该一致,但实际二者之间有一个滞后现象,形成滞后环。
在一定时,食品的解吸过程一般比回吸过程时含水量更高。
【简答】10、简述水分活度与食品保存性的关系。
(一)、水分活度与微生物生长的关系:不同类群微生物生长繁殖的W A 最低范围是:大多数细菌为0.94~0.99,大多数霉菌为0.80~0.94,大多数耐盐细菌为0.75,耐干燥霉菌和耐高渗透压酵母为0.60~0.65。
在低于0.60时。
绝大多数微生物就无法生长。
细菌形成芽孢时的W A 阈值比繁殖生长时要高。
(二)、水分活度与酶水解的关系:当降低到0.25~0.30的范围,就能有效地减慢或阻止酶促褐变的进行。
(三)、水分活度与化学反应的关系:① 大多数化学反应都必须在水溶液中才能进行。
降低水分活度,食品中许多化学反应受到抑制,反应速率下降。
② 发生离子化学反应的条件是反应物首先必须进行离子的水合作用,所以要有足够的游离水。
③ 化学反应和生物反应都必须有水分子参与。
降低水分活度,减少了参加反应的水的有效数量,反应速率下降。
④ 当W A <0.8时,大多数酶活力受抑制;当W A 在0.25~0.30之间时,淀粉酶、多酚氧化酶和过氧化物酶就会丧失活力或受到强烈的抑制。
食品化学知识点

食品化学知识点一、食品组成及相关知识食品是指提供营养和能量,并满足人体生理和心理需求的物质。
食品大致可分为五大类:谷类、肉类、蔬菜类、水果类和奶类。
1.1 营养素营养素是指人体必须吸收的物质,包括碳水化合物、脂肪、蛋白质、维生素和矿物质等。
碳水化合物是人体能量的主要来源,包括单糖、双糖和多糖。
单糖包括葡萄糖、果糖和半乳糖等;双糖包括蔗糖、乳糖和麦芽糖等;多糖包括淀粉和纤维素等。
脂肪是人体必须吸收的营养素,包括不饱和脂肪酸和饱和脂肪酸等。
不饱和脂肪酸包括单不饱和脂肪酸和多不饱和脂肪酸等,可降低胆固醇水平,预防心血管疾病。
蛋白质是组成人体组织的重要成分,包括必需氨基酸和非必需氨基酸等。
维生素是维持人体生理功能的重要物质,包括水溶性维生素(如维生素B1、维生素B2、维生素B6、维生素C等)和脂溶性维生素(如维生素A、维生素D、维生素E、维生素K 等)等。
矿物质是人体必须吸收的元素,包括铁、钙、钾、镁、锌等。
1.2 食品添加剂食品添加剂是指在食品加工中添加的具有特定功能的物质,可分为色素、防腐剂、甜味剂、增味剂、膨松剂、酸味剂、稳定剂和乳化剂等。
色素可增加食品的色泽,使其更具吸引力;防腐剂可延长食品的保质期,防止细菌滋生;甜味剂可增加食品的甜度;增味剂可增强食品的香味和口感;膨松剂可增加食品的松软度;酸味剂可增加食品的酸味;稳定剂可提高食品的稳定性;乳化剂可使油水混合物更加均匀。
1.3 食品中的化学成分食品中含有多种化学成分,包括糖类、蛋白质、脂肪、矿物质、维生素、酸碱度等。
其中,糖类是食品中含量最高的成分之一,可分为单糖、双糖和多糖。
同时,食品中还含有不同种类的酸,如有机酸和脂肪酸等。
二、食品加工及相关知识2.1 食品生产加工食品生产加工包括原材料处理、加工制备、成品包装和贮存等环节。
其中,原材料处理包括采集、分级、分选、清洗、翻晒等步骤;加工制备包括切割、研磨、混合、腌制、烘干等步骤;成品包装包括采购包装材料、包装机械调试、包装等步骤;贮存包括成品的仓储、保管、配送、销售等步骤。
食品化学(知识点)

10、引起滞后现象的原因 1、解吸过程中一些吸水与非水溶液成分作用而无法释放。 2、样品中不规则形状产生的毛细管现象的部位,欲填满或抽空水分需要不同的蒸汽压
(要抽出需要 P 内>P 外,要填满即吸着时需 P 外>P 内)。 3、解吸时,因组织改变,无法紧密结合水分,因此回吸相同水分含量时其水分活度较
从水的正常结构来看,所有离子对水的结构都起到破坏作用,因为它们都能阻止水在 0℃
下
结冰。
对全部高中资料试卷电气设备,在安装过程中以及安装结束后进行高中资料试卷调整试验;通电检查所有设备高中资料电试力卷保相护互装作置用调与试相技互术关,系电,通力根1保过据护管生高线产中敷工资设艺料技高试术中卷0资不配料仅置试可技卷以术要解是求决指,吊机对顶组电层在气配进设置行备不继进规电行范保空高护载中高与资中带料资负试料荷卷试下问卷高题总中2体2资,配料而置试且时卷可,调保需控障要试各在验类最;管大对路限设习度备题内进到来行位确调。保整在机使管组其路高在敷中正设资常过料工程试况1卷中下安,与全要过,加度并强工且看作尽护下可1都关能可于地以管缩正路小常高故工中障作资高;料中对试资于卷料继连试电接卷保管破护口坏进处范行理围整高,核中或对资者定料对值试某,卷些审弯异核扁常与度高校固中对定资图盒料纸位试,置卷编.工保写况护复进层杂行防设自腐备动跨与处接装理地置,线高尤弯中其曲资要半料避径试免标卷错高调误等试高,方中要案资求,料技编试术写5、卷交重电保底要气护。设设装管备备置线4高、调动敷中电试作设资气高,技料课中并3术试、件资且中卷管中料拒包试路调试绝含验敷试卷动线方设技作槽案技术,、以术来管及避架系免等统不多启必项动要方高式案中,;资为对料解整试决套卷高启突中动然语过停文程机电中。气高因课中此件资,中料电管试力壁卷高薄电中、气资接设料口备试不进卷严行保等调护问试装题工置,作调合并试理且技利进术用行,管过要线关求敷运电设行力技高保术中护。资装线料置缆试做敷卷到设技准原术确则指灵:导活在。。分对对线于于盒调差处试动,过保当程护不中装同高置电中高压资中回料资路试料交卷试叉技卷时术调,问试应题技采,术用作是金为指属调发隔试电板人机进员一行,变隔需压开要器处在组理事在;前发同掌生一握内线图部槽 纸故内资障,料时强、,电设需回备要路制进须造行同厂外时家部切出电断具源习高高题中中电资资源料料,试试线卷卷缆试切敷验除设报从完告而毕与采,相用要关高进技中行术资检资料查料试和,卷检并主测且要处了保理解护。现装场置设。备高中资料试卷布置情况与有关高中资料试卷电气系统接线等情况,然后根据规范与规程规定,制定设备调试高中资料试卷方案。
食品化学复习知识点(二)

食品化学复习知识点(一)引言概述:食品化学是研究食品的组成、结构、性质和变化规律的学科,了解食品化学的知识对于提高食品的品质、安全和营养价值具有重要意义。
本文将介绍食品化学的复习知识点,以帮助读者更好地理解和掌握相关内容。
正文:一、食物的化学组成1.1 主要食物成分:碳水化合物、脂类、蛋白质、维生素和矿物质等。
1.2 食物的营养价值:了解食物中不同成分的营养作用和重要性。
1.3 食物的能量价值:计算食物的热量含量及其在人体中的利用。
二、食物的化学反应2.1 激素和酶的作用:了解激素和酶在食物化学反应中的作用机制。
2.2 食品的变质过程:细菌、酵母菌和霉菌的作用以及氧化和褐变等反应的原因和机制。
2.3 食品储存的化学原理:掌握食品储存中的化学反应和控制措施。
三、食品的添加剂3.1 食品添加剂的分类:了解食品添加剂的种类及其用途。
3.2 食品添加剂的作用原理:理解食品添加剂的功能和作用机制。
3.3 食品添加剂的安全性评价:了解食品添加剂的安全性评价标准和方法。
四、食品的鉴别与分析4.1 食品鉴别的方法:介绍常用的食品鉴别方法,如感官评价、化学分析和生物检测等。
4.2 食品中有害物质的检测:了解食品中常见有害物质的检测方法及其危害。
4.3 食品分析技术:介绍常用的食品分析技术,如色谱分析和质谱分析等。
五、食品加工与营养保持5.1 食品加工的化学原理:了解常用食品加工方法的化学原理和影响因素。
5.2 食品贮藏与保鲜技术:介绍常用的食品贮藏与保鲜技术,如冷冻、真空包装和辐照等。
5.3 食品的营养保持:了解食品加工对营养物质的影响以及保持营养物质的方法。
总结:本文介绍了食品化学的复习知识点,包括食物的化学组成、化学反应、添加剂、鉴别与分析以及食品加工与营养保持。
通过深入了解和掌握这些知识点,读者可以更好地理解和应用食品化学的原理,提高食品的质量和卫生安全水平,保障食品的营养价值。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
注意:1)RVP是样品的内在性质,而ERH是当样品中的水蒸气平衡时的大气性质;
2)仅当样品与环境达到平衡时,方程的关系才成立。
6、水分活度与温度的关系:
水分活度与温度的函数可用克劳修斯-克拉贝龙方程来表示:
dlnaw/d(1/T)=-ΔH/R
lnaw=-ΔH/RT+C
图:马铃薯淀粉的水分活度和温度的克劳修斯-克拉贝龙关系
7、食品在冰点上下水分活度的比较:
①在冰点以上,食品的水分活度是食品组成和温度的函数,并且主要与食品的组成有关;而在冰点以下,水分活度仅与食品的温度有关。
②就食品而言,冰点以上和冰点以下的水分活度的意义不一样。如在-15℃、水分活度为0.80时微生物不会生长且化学反应缓慢,然而在20℃、水分活度为0.80时,化学反应快速进行且微生物能较快地生长。
不能作溶剂,-40℃以上不结冰,对固体没有显著地增塑作用,与腐败无关
Ⅱ区:Aw=0.25~0.8(加Ⅰ区,0.07g水/g干物质至0.14~0.33g水/g干物质)
作用力:氢键、H2O—H2O、H2O—溶质
属多分子层水,加上Ⅰ区约占高水食品的5%不作溶剂,-40℃以上不结冰,但接近0.8(Aw)的食品,可能有变质现象,起增塑剂的作用,并且使固体骨架开始溶胀
第一章绪论
1、食品化学:是从化学角度和分子水平上研究食品的化学组成、结构、理化性质、营养和安全性质以及它们在生产、加工、贮存和运销过程中的变化及其对食品品质和食品安全性影响的科学,是为改善食品食结构、改进食品包装、加强食品质量控制及提高食品原料加工和综合利用水平奠定理论基础的学科。
③不能用食品在冰点以下的水分活度来预测食品在冰点以上的水分活度,同样也不能用食品冰点以上的水分活度来预测食品冰点以下的水分活度。
8、水分吸附等温线
在恒定温度下,用来联系食品中的水分含量(以每单位干物质中的含水量表示)与其水分活度的图,称为水分吸附等温线曲线(moisture sorption isotherm,MSI)。
意义:
(1)测定什么样的水分含量能够抑制微生物的生长;
(2)预测食品的化学和物理稳定性与水分含量的关系;
(3)了解浓缩和干燥过程中样品脱水的难易程度与相对蒸气压(RVP)的关系;
(4)配制混合食品必须避免水分在配料之间的转移;
(5)对于要求脱水的产品的干燥过程、工艺、货架期和包装要求都有很重要的作用。
2、食品化学的研究范畴
第二章水
3、在温差相等的情况下,为什么生物组织的冷冻速率比解冻速率更快?
4、净结构破坏效应:一些离子具有净结构破坏效应(net structure-breaking effect),如:K+、Rb+、Cs+、NH4+、Cl-、I-、Br-、NO3-、BrO3-、IO3-、ClO4-等。这些大的正离子和负离子能阻碍水形成网状结构,这类盐溶液的流动性比纯水更大。
Ⅲ区:Aw=0.80~0.99(新增的水为自由水,(截留+流动),最低0.14~0.33g水/g干物质,多者可达20g H2O/g干物质,体相水)
可结冰,可作溶剂,有利于化学反应的进行和微生物的生长
9、滞后现象
向干燥样品中添加水,所得到的吸附等温线与将水从样品中移出所得到的解吸等温线并不相互重叠,这种不重叠性称为滞后现象(hysteresis)。滞后作用的大小、滞后曲线的形状、滞后曲线的起始点和终止点取决于食品的性质、食品除去或添加水分时所发生的物理变化,以及温度、解吸速度和解吸时的脱水程度等多种因素。在Aw一定时食品的解吸过程一般比吸附过程水分含量更高。
9、MSI图形形态
大多数食品的水分吸附等温线呈S型,而水果、糖制品、含有大量糖的其他可溶性小分子的咖啡提取物以及多聚物含量不高的食品的等温线为J型。
图:低水分含量范围食品的水分吸附等温线
Ⅰ区:Aw=0~0.25约0~0.07g水/g干物质
作用力:H2O—离子,H2O—偶极,配位键
属单分子层水(含水合离子内层水)
从水的正常结构来看,所有离子对水的结构都起到破坏作用,因为它们都能阻止水在0℃下结冰。
5、水分活度
目前一般采用水分活度表示水与食品成分之间的结合程度。
aw=f/f0其中:f为溶剂逸度(溶剂从溶液中逸出的趋势);f0为纯溶剂逸度。
相对蒸气压(Relative Vapor Pressure,RVP)是p/p0的另一名称。RVP与产品环境的平衡相对湿度(Equilibrium Relative Humidity,ERH)有关,如下:
图12:核桃仁的水分吸附等温线的滞后现象(25℃)
10、引起滞后现象的原因
1、解吸过程中一些吸水与非水溶液成分作用而无法释放。
2、样品中不规则形状产生的毛细管现象的部位,欲填满或抽空水分需要不同的蒸汽压(要抽出需要P内>P外,要填满即吸着时需P外>P内)。
3、解吸时,因组织改变,无法紧密结合水分,因此回吸相同水分含量时其水分活度较高
净结构形成效应:另外一些离子具有净结构形成效应(net structure-forming effect),这些离子大多是电场强度大、离子半径小的离子或多价离子。它们有助于形成网状结构,因此这类离子的水溶液的流动性比纯水的小,如:Li+、Na+、Ca2+、Ba2+、Mg2+、Al3+、F-、OH-等。
11、脂类氧化反应与Aw的关系
影响脂肪品质的化学反应主要为酸败,而酸败过程的化学本质是空气中氧的自动化。脂类氧化反应与Aw的关系:在Ⅰ区中,氧化反应的速度随水分的增加而降低;在Ⅱ区中,反应的速度随水分的增加而加快;在Ⅲ区中,反应的速度随水分的增加呈下降趋势。其原因是脂类氧化反应的本质是水与脂肪自动氧化中形成的氢过氧化合物通过氢键结合,降低了氢过氧化合物分解的活性,从而降低了脂肪的氧化反应的速度。从没有水开始,随着水量的增加,保护作用增强,因此氧化过程有一个降低的过程。除了水对氢过氧化物的保护作用外,水与金属的结合还可使金属离子对脂肪氧化反应的催化作用降低。当含水量超过Ⅰ、Ⅱ区交界时,较大量的通过溶解作用可以有效的增加氧的含量,还可使脂肪分子通过溶胀而更加暴露,氧化速度加快。当含水量到达Ⅲ区时,大量的水降低了反应物和催化剂的浓度,氧化速度又有所降低。
