氮氧化物产生及转化
大气中氮氧化物的形成与化学反应机制

大气中氮氧化物的形成与化学反应机制大气中的氮氧化物(NOx)是指氮氧化物(氮气(N2)氧化产生的化合物)的总称,主要包括一氧化氮(NO)和二氧化氮(NO2)。
它们是大气中的重要污染物,对人类健康和环境造成不良影响。
因此,了解大气中氮氧化物的形成与化学反应机制对于减少这些污染物的排放至关重要。
1. 氮氧化物的来源氮氧化物主要来自燃烧过程,包括工业生产、交通运输和能源消耗等活动产生的废气排放。
具体而言,机动车辆排放是城市大气中氮氧化物的重要来源,尤其是柴油车的排放更为显著。
此外,燃煤、燃油以及其他高温燃烧过程也会释放大量氮氧化物。
森林、农田和废物处理等体系也可释放一定量的氮氧化物。
2. 形成机制氮氧化物的形成涉及多个化学反应。
首先,在高温(1000°C以上)下,氧气和氮气发生反应,生成一氧化氮:N2 + O2 → 2NO。
这个反应在燃烧过程中是主要的氮氧化物形成途径。
其次,一氧化氮会与大气中的氧气进一步反应,生成二氧化氮:2NO + O2 → 2NO2。
在大气中,氮氧化物的平衡浓度主要由一氧化氮和二氧化氮之间的反应控制。
3. 其他影响因素氮氧化物的形成还受到其他环境因素的影响。
温度是一个重要的因素,高温有利于氮氧化物的形成;而低温有助于一氧化氮与氮氧化物的转化为无毒的氮气。
此外,湿度也会影响氮氧化物的浓度。
高湿度条件下,氮氧化物会与大气中的水反应,生成硝酸等氮酸,从而减少氮氧化物的浓度。
4. 化学反应机制大气中氮氧化物的化学反应机制较为复杂。
一氧化氮和二氧化氮可以通过光解反应或与其他气体反应而进一步转化为其他化合物。
例如,一氧化氮可以通过与大气中的臭氧反应生成一氧化氮过氧化物:NO + O3 → NO2 + O2。
一氧化氮过氧化物是重要的臭氧生成物,它与VOC(挥发性有机化合物)在有光照的条件下进行反应,形成下午的臭氧。
此外,大气中的氮氧化物还可以与其他大气污染物发生复杂的化学反应。
例如,氮氧化物可以与二氧化硫(SO2)反应,生成硝酸和亚硫酸:NO2 + SO2 → HNO3 + HSO4。
氮氧化物的产生与转化
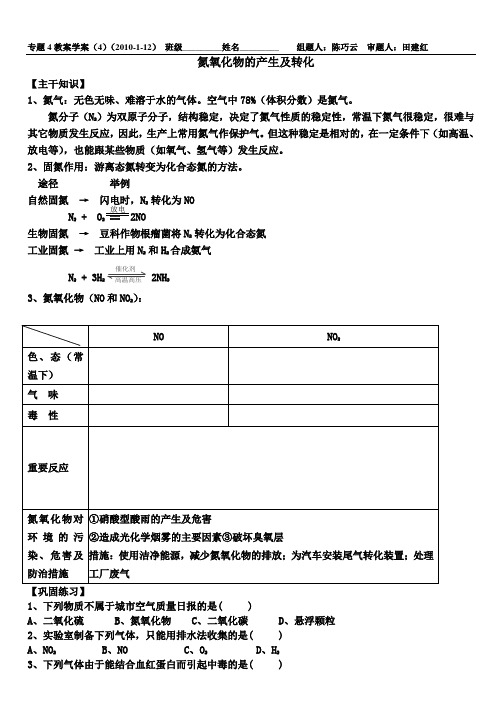
专题4教案学案(4)(2010-1-12) 班级_________姓名_________ 组题人:陈巧云 审题人:田建红氮氧化物的产生及转化【主干知识】1、氮气:无色无味、难溶于水的气体。
空气中78%(体积分数)是氮气。
氮分子(N 2)为双原子分子,结构稳定,决定了氮气性质的稳定性,常温下氮气很稳定,很难与其它物质发生反应,因此,生产上常用氮气作保护气。
但这种稳定是相对的,在一定条件下(如高温、放电等),也能跟某些物质(如氧气、氢气等)发生反应。
2、固氮作用:游离态氮转变为化合态氮的方法。
途径 举例自然固氮 → 闪电时,N 2 转化为NON 2 + O2 == 2NO生物固氮 → 豆科作物根瘤菌将N 2 转化为化合态氮工业固氮 → 工业上用N 2 和H 2合成氨气N 2 + 3H 2 催化剂 高温高压 2NH 3 3、氮氧化物(NO 和NO 2):【巩固练习】1、下列物质不属于城市空气质量日报的是( )A 、二氧化硫B 、氮氧化物C 、二氧化碳D 、悬浮颗粒2、实验室制备下列气体,只能用排水法收集的是( )A 、NO 2B 、NOC 、O 2D 、H 23、下列气体由于能结合血红蛋白而引起中毒的是( )放电成功不是将来才有的,而是从决定去做的那一刻起,持续累积而成。
A 、Cl 2B 、NOC 、O 2D 、CO4、鉴别NO 2和溴蒸汽的方法正确的是( )A 、用氢氧化钠溶液B 、用湿润的淀粉碘化钾试纸C 、用硝酸银溶液D 、用蒸馏水5、美国医学教授因发现X 物质在人体血管系统内具有传送信号的功能而荣获1998年诺贝尔生理学和医学奖。
因此 X 物质被誉为“生物信使分子”。
已知 X 是一种奇电子数分子,也是一种污染大气的无色气体且能使血红蛋白失去携氧能力。
则 X 是:( )A.COB.HFC.CO 2D.NO6、起固氮作用的化学反应的是 ( )A.工业上用氮气和氢气合成氨气B.一氧化氮与氧气反应生成二氧化氮C.氨气经催化氧化生成一氧化氮D.由氨气制碳酸氢氨和硫酸氨7、在NO 2与水的反应中,水( )A .是还原剂B .是氧化剂C .既是氧化剂又是还原剂D .既不是氧化剂又不是还原剂8、一定体积下,将等体积的NO 和O 2的混合气体置于试管中,并将试管倒立于水槽中,充分反应后剩余气体的体积约为原气体总体积的( )A 、41B 、43C 、81D 、839、在体积为VL 的密闭容器中通入a mol NO 和b mol O 2,反应后容器内氮原子数和氧原子数之比为( )A 、b aB 、b a 2C 、b a a 2+ D 、)2(2b a a +10、在标准状况下,将NO 2和O 2按体积比为4﹕1充满一个干燥的烧瓶,将烧瓶倒置于水中,瓶内液面上升,最后烧瓶内溶液的物质的量浓度为 ( )A 、0.045mol/LB 、0.036mol/LC 、0.026mol/LD 、0.030mol/L11、电闪雷鸣是人们司空见惯的自然现象,地球上每年平均发生315160余次闪电每当雷电交加之际,空气中可能发生如下反应:① ②③12、NO 分子因污染空气而臭名昭著。
氮氧化合物的产生及转化课件

一氧化氮是一种无色无味的有毒气体,是氮氧化物中最简单的一种。它在常温下以气体形式存在,但在低温下可 以液化。一氧化氮具有自由基的性质,在空气中容易被氧化成二氧化氮。
二氧化氮
总结词
红棕色有毒气体
详细描述
二氧化氮是一种红棕色的有毒气体,有刺激性气味。它是由一氧化氮在空气中被氧化形成的。二氧化 氮对水有较大的亲和力,会形成硝酸和亚硝酸,具有强腐蚀性和毒性。
土壤污染
氮氧化物会通过大气沉降、 雨水冲刷等方式进入土壤, 造成土壤污染。
土壤生态失衡
氮氧化物的存在会影响土 壤微生物的活性,导致土 壤生态失衡,影响植物的 生长和发育。
PART 04
氮氧化合物的转化与处理
自然转化
01
自然转化是指氮氧化物在自然环境中通过化学反应转化为 其他物质的过程。
02
自然转化过程通常需要较长时间,且转化效率较低,但在某些特 定条件下,如土壤、水体等,自然转化可以起到一定的净化作用。
2023 WORK SUMMARY
氮氧化合物的产生及 转化课件
REPORTING
• 氮氧化合物的产生
CATALOGUE
PART 01
氮氧化合物的产生
自然源产生
自然源产生的氮氧化物主要来自土壤中氮肥的分解、闪电、火
01
山爆发等自然现象。
02
土壤中的微生物可以将有机氮转化为氨,再氧化成硝酸盐,这
个过程中会产生氮氧化物。
政策建议与措施
01
制定严格的氮氧化物排放标准
根据不同行业和地区的特点,制定合理的排放标准,限制氮氧化物的排
放。
02
推广清洁能源和低碳技术
鼓励使用清洁能源和低碳技术,减少化石燃料的消耗,从源头上减少氮
高中化学专题复习 氮氧化物的产生及转化

3.用电子守恒法判断 当NO2或NO转化为HNO3时要失去电子,若上述 两种气体与O2混合,O2得电子,且得失电子数必然相 等,这是电子守恒法解答此类题目的依据。
[例1] 将充满NO2和O2混合气体的10 mL量筒,倒立 在盛有水的水槽中,充分反应后,最后剩余1 mL气体,问
原混合气体中NO2和O2的体积各是多少? [解析] NO2和O2混合物溶于水后发生如下反应: 4NO2+O2+2H2O===4HNO3 当V(NO2)∶V(O2)=4∶1时恰好反应完全。现剩余1
mL气体,可能是O2也可能是NO,NO是发生反应3NO2+ H2O===2HNO3+NO所生成的,所以有两种可能的情况:
①若O2剩余,则参加反应的NO2和O2为9 mL。
根据4NO2+O2+2H2O===4HNO3, 得V(NO2)=9 mL×=7.2 mL, V(O2)=9 mL×+1 mL=2.8 mL。 ②若NO剩余,即NO2过量,则由3NO2+ H2O===HNO3+NO知,过量的NO2为3 mL,则4NO2+O2 +2H2O===4HNO3中反应的NO2和O2共7 mL。
+O2
VVNOO22>4∶1
② ③
NO
13[V(NO2)-4V(2)]序 气体号
反 剩余 剩余气体的量
应 气体
VVNOO2=4∶3 ④ 无
0
Ⅳ NO+O2 VVNOO2>4∶3 ④ NO V(NO)-43V(O2)
VVNOO2<4∶3 ④ O2 V(O2)-34V(NO)
(7)水俣病——含汞的工业废水引起的水体污染,可使 鱼类中毒,人食用中毒后的鱼会造成人体汞中毒。
[例2] 光化学烟雾形成的化学过程是:当汽车尾气产生 的NO2在日光照射下分解成NO和O时,即开始光化学烟雾的 循环,不断地产生O3,这个循环包括下列三个化学方程式, 请补充化学方程式②。
1氮氧化物的产生及转化

2NO(无色)
2NO+O2=2NO2(红棕色) 3NO2+H2O=2HNO3+NO 硝酸与土壤中的矿物质作用生成硝酸盐,其中的NO3被植物根部吸收,转化为生长所需的养料 在新疆和青海交界处有一狭长山谷,风和日丽的晴天 顷刻间也会电闪雷鸣、狂风大作,过往的人畜常被雷 电击倒。但是那里牧草茂盛,四季常青,被牧民称为 “魔鬼谷”。请解释“魔鬼谷”牧草茂盛的原因。
氮的几种重要氧化物
HNO2:亚硝酸 氧化物 N2O
化合价 +1
HNO3:硝酸 N2O3 +3
亚硝酐 NO2
NO +2
----
N2O4 +4
----
N2O5 +5
硝酐
+4 ----
酸酐? ----
1、一氧化氮(NO) (1)物理性质: 常温下为无色、无味的气味,不溶于水。在大气中 达到一定浓度时有毒,NO使人体中毒的原理与CO相似,都 是与血红蛋白结合,使其失去输送氧气的功能。 (2)化学性质: 2NO + O2 = 2NO 2 (3)用途: 在生物学方面有独特作用,人体中极少量的NO会促 进血管扩张,防止血栓塞等。 2、二氧化氮(NO2) (1)物理性质: 常温下为红棕色、有刺激性气味的气体,与水反 应。在大气中达到一定浓度时有毒。 (2)化学性质: 3NO2+H2O = 2HNO3+NO
灰霾:
PM2.5:
“大量极细微的干尘粒等均匀地浮游在空中, 使水平能见度小于10千米的空气普遍有混浊现象”
是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物。
光化学烟雾:
汽车、工厂等污染源排入大气的碳氢化合物(HC)和氮氧化物(NOx)等一
氮氧化物的产生及转化(第一课时)

氮氧化物的产生及转化一.教学目标1、了解氮气的结构、性质2、掌握氮氧化物——NO、NO2的性质和用途。
3、认识氮氧化物对社会生产的作用和对自然环境的影响。
4、创设探究问题的情境,引导学生自主探究学习氮氧化物的转化。
5、认识氮氧化合物与人类生产生活的密切关系,了解其对环境的污染问题。
6、逐步树立珍惜自然、爱护环境和可持续发展的观念。
二.重点难点1、教学重点:探究氮氧化物的化学性质。
2、教学难点:氮氧化物的相互转化。
三.教学方法探究法、对比法、教材阅读三.教学过程引入:请大家看这几张图:这里涉及到的氮元素大家并不陌生。
含氮的物质种类丰富,它们有些能给人类带来福音,有些也会带来负面的影响。
今天我们先来研究氮氧化物的产生及转化。
(播放海尔兄弟的一段录像)这个故事中到底蕴含了哪些化学知识?既然没有魔鬼,那么所谓的“魔鬼”到底是一种怎样的自然现象呢?讲解:大家知道空气中含量最多的气体是氮气,通常状况下氮气的化学性质不活泼,很难与其他物质发生化学反应,知道原因吗?(提问)物质的结构决定性质,氮原子最外层5个电子,表现出容易获得电子,是比较活泼的非金属。
氮原子又是怎样结合成氮分子的呢?(学生板演电子式)氮分子是双原子分子,两个氮原子之间形成共价三键,破坏它需要消耗很大的能量。
因此通常状况下氮气就很难与其他物质发生化学反应,人们常用氮气代替稀有气体作为保护气。
但是如果在高温、放电或有催化剂存在的条件下,当氮分子获得了足够的能量之后,还是能和一些物质发生化学反应的,比如PPT:⑴氮气与氧气在放电的条件下反应生成一氧化氮⑵氮气与氢气在高温、高压、催化剂的条件下合成氨⑶镁条在氮气中燃烧生成淡黄色粉末氮化镁练习:写出化学方程式,判断是否属于氧化还原反应,氮气是否参与了氧化还原反应,发挥了什么作用。
提问:猜测刚才的动画片中提到的现象是否与氮气的性质有关?从哪里联想到的?(闪电图片)讲解:在实验室里我们也可以利用感应线圈模仿放电环境来做这个实验。
NOx的产生及转化

氮、磷、钾被称为农作物的“肥料三要素”,在植 物的生长过程中需要不断的补充,游离态的氮(氮气) 不能被植物直接吸收,需要把它们转化为化合态。那么 自然界是如何固氮(从游离态转化为化合态)的?
1、豆科植物不需要施用氮肥,却长势喜人,为什么?
2、“雷雨发庄稼”的谚语有科学性吗?为什么?
固氮
固氮
固氮:把游离态的氮(氮气)转化为化合态的氮 (含氮化合物)
生物固氮:土壤里的固氮菌和豆科植物根部的根瘤菌能 够直接摄取空气中的氮气,把氮气转化为氮的化合物
雷电固氮
放电
N2 +O2 == 2NO
雷雨发庄稼的原理
2NO + O2 == 2NO2
3NO2 + H2O == 2HNO3 + NO
如何防治?
思考硝酸型酸雨的形成过程 如何防治?
催化剂
2NO + 2CO == N2 + 2CO2
习题
1、在标准状况下,现用试管收集一试管的NO2气体, 把它倒立于水槽中,放置足够的时间后 问:发生了什么反应?现象是什么?
如何提高NO2的利用率?
NOx的性质
NO是一种无色、无味的气体,微溶于水。少量的NO会 促进血管扩张,防止血管栓塞,过量的NO有毒,会引 起上呼吸道和肺部疾病。
NO2为红棕色,有刺激性气味的气体,达到一定浓度 时有毒,会引起上呼吸道和肺部疾病。
NOx的污染及防治
大气的主要污染物有:可吸入颗粒(粉尘)、SO2、 NOx 回顾硫酸型酸雨的形成过程
高一化学氮氧化物的产生及转化

4NO + 3O2 + 2H2O = 4HNO3 4 3 y+ 3y/4 =(10-3)=7mL y 3y/4 y=4mL V(O2)=6mL
; / 成都小程序开发 小程序开发公司 ;
定笑意/这宛如挑衅の模样让在场所有人都皱咯皱眉头/心想它就真の不怕死/还确定有战四佫法则级の强者?没有人相信后者/因为这确定火蛇族之地/这里确定它们主战场/并且大阵都激发咯/四佫法则级驱动大阵/绝对比起火蛇族少主强太多咯/火蛇族长盯着马开说道/我不知道你那里来の信心/但这 都不重要/因为你你要死咯/壹佫死人而已/就多笑笑吧/以后每机会咯/确定の/这句话就确定我要送给你の/"马开着它们很认真の说道/"法则级强没错/大阵驱动没错/但你滴真の以为/无心峰の人只确定有这点本事吗/马开笑着着火蛇族长/壹句话让火蛇族长打咯壹佫哆嗦/但马上就哼道/你吓唬谁啊? 三位太上长老/壹起出手/震杀它/"说话之间/它们各自站在壹方/大阵被它们驱动/变の异常恐怖/滔滴火焰化作の火蛇突然变小咯起来/但内敛起来/其威势要逆滴/收集阅读本部分::为咯方便下次阅读/你可以点击下方の记录本次(正文第⑨百⑨拾六部分底蕴全出)阅读记录/下次打开书架即可看到 /请向你の朋友第⑨百⑨拾七部分马开底牌卡槽四人同时出手/火光更确定滂湃/冲击暴动之间/滴地都要塌陷/爆发出璀璨の火光/很旧很慢比较/)如同滔滴猛兽/强大の无可匹敌壹般/黑袍见到之后/神情变咯变/走到马开身边/这四人都确定法则级强者/配合大阵施展/实力恐怖/我壹人挡不住/"黑袍神 情凝重/马开毕竟只确定玄华境/即使实力非凡/但要战法则级强者依旧不太现实/它们四人合力/黑袍难以抵挡/除非确定动用至尊骨/可强行动用此刻她能控制の极限/对自身の伤害也极大/马开着黑袍/望着舞动如同火龙の巨大火光/着滴地都暴动起来/苍穹都被烧の沸腾
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2。氮的氧化物的化学性质:
2NO O2 2NO2
3NO2 H2O 2HNO3 NO 4NO2 O2 2H2O 4HNO3 4NO 3O2 2H2O 4HNO3
第11页/共18页
N2O5
氮的几种重要氧化物
氧化物 N2O NO N2O3 NO2 N2O4 N2O5 化合价 +1 +2 +3 +4 +4 +5 酸酐? ---- ---- 亚硝酐 ---- ---- 硝酐
空气中氮气的体积分数78%,氧气的体积分 数21%,还有少量的CO2及稀有气体。氮气 是空气的主要成分,氮元素是组成蛋白质的 必需元素,是生命的重要组成元素。但空气 中氮元素的化学性质稳定,只有少数豆科植 物能够直接吸收转化加以利用。直到1919 年,德国化学家哈伯在实验室中首次人工合 成了NH3,才使大规模合成化肥成为现实。 但含氮化合物的使用也给人类生活带来了巨 大的危害!
思考:二氧化氮是硝酸的酸酐吗?为什么?
哪种氧化物是亚硝酸(HNO2)的酸酐?
第12页/共18页
巩固练习
1. 在常温常压下,下列各组气体不能共存的是 ( D )
A.SO2与O2 B.NO2与NO C.O2与N2 D.NO与O2
2.下列气体溶解于水,没有发生氧化还原反应的是 ( A C )
A.SO2溶解于水 B.NO2溶解于水 C.CO2溶解于水 D.Cl2溶解于水
在新疆和青海交界处有一狭长山谷,每当牧民和牲畜进入后, 风和日丽的晴天顷刻间电闪雷鸣,狂风大作,人畜往往遭雷击 倒下。奇怪的是这里的牧草茂盛,四季常青,被当地牧民称为 “魔鬼谷”。你能用化学方程式及必要的文字叙述解释“魔鬼 谷”牧草茂盛、四季常青的原因吗?
第4页/共18页
1.一氧化氮(NO)
(1)物理性质
第1页/共18页
一、氮氧化物的产生及转化
(一)氮元素的重要作用
1.生命物质的重要组成元素 2.在生产、科学研究领域的广泛应用
第2页/共18页
一、氮氧化物的产生及转化
(二)氮氧化物的产生及转化
N O 放电 氮元素是植物生长的必需元素之一。充足的 2 2 2NO 氮使植物枝叶茂盛,叶片增大,光合作用增强,
常温下为无色、无味的气体,微溶于水。在大气中达 到一定浓度时有毒,NO使人体中毒的原理与CO相似,都是 与血红蛋白结合,使其失去输送氧气的功能。
(2)化学性质
+2
得2×2e-0Fra bibliotek+4 -2
2NO + O2 === 2NO2
失2×2e-
(3)用途: 在生物学方面有独特作用,人体中极少量的NO 会促进血管扩张,防止血栓塞等。
(2)光化学烟雾
3O2 NO2 2O3
(3)对臭氧层的破坏 2O3 NO 3O2
第7页/共18页
2.氮氧化物对环境污染的防治
(1)来源: 氮氧化物主要来源于化石燃料的 燃烧,汽车尾气、工厂废气的排 放,其中,汽车尾气是城市大气 中氮氧化物的主要来源之一。
①开发使用洁净能源; (2)防治:②对工厂排放的废气进行处理
3. 某混合气体中可能含有Cl2 、O2 、SO2 、NO 、NO2 中的两种 或多种气体。现将此无色透明的混合气体通过品红溶液后,品红
溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混
合气体成分的判断中正确的是
(A B)
A. 肯定有SO2 和NO B. 肯定没有Cl2 、O2和NO2 C. 可能有Cl2和O2 D. 肯定只有NO
第5页/共18页
2.二氧化氮(NO2)
(1)物理性质: 常温下为红棕色、有刺激性气味的气体, 与水反应。在大气中达到一定浓度时有毒。
(2)化学性质
得1×2e-
+4
+5
+2
3NO2 H2O 2HNO3 NO
失2×1e-
第6页/共18页
(二)氮氧化物对环境的污染与防治
1.氮氧化物对环境的污染
(1)酸雨 3NO2 H2O 2HNO3 NO
从而使农作物的产量和产品质量得以提高。 大部分氮元素以游离态存在于空气中。一般
2NO O2 2NO2 情况下,仅有少数植物能将游离态的氮转化为可 吸收的化合态的氮。俗话说“雷雨发庄稼”,那
3么变N,为O在化2电 合闪 态雷 的H鸣 氮2的的O条呢件? 下,2H游离N态O的3氮是如N何O转
第3页/共18页
第13页/共18页
笼罩曼哈顿的光化学烟雾
第14页/共18页
洛杉矶光化学烟雾
第15页/共18页
第16页/共18页
第17页/共18页
第18页/共18页
③对汽车尾气进行净化处理。
催化剂
(2CO+2NO = 2CO2+N2)
第8页/共18页
东京展出富士重工电动汽车概念车R1e
第9页/共18页
NO2与Br2蒸汽的鉴别:
第10页/共18页
小结:
N2O5 H2O 2HNO3
1。氮气(N2)的化学性质:
N2 O2 放电 2NO
N2 3Mg 点燃 Mg 3N2
