蛋白质化学1(3.3)
蛋白质的化学全合成

蛋白质的化学全合成1. 前言蛋白质是生命体中最为重要的大分子之一,在生命体的生存中发挥着至关重要的作用。
其结构多样性和复杂性使其成为生命科学中最为具有挑战性的研究领域之一。
在过去的几十年里,生物技术和化学技术等领域的不断发展和进步,使得蛋白质的化学全合成成为可能。
2. 蛋白质的化学全合成的原理蛋白质化学全合成指的是通过化学合成方法在旁路反应和选择性修饰的控制下一步步地合成出完整、具有生物活性的蛋白质的技术。
其原理主要是将氨基酸依次加入至聚合物上,以在无水条件下形成肽键,并不断组装连接,得到具有完整空间结构和功能的蛋白质分子。
3. 蛋白质化学全合成的步骤蛋白质化学全合成一般可以分为以下几个步骤:3.1. 保护群的引入和去除在化学合成肽链的过程中,为了防止氨基酸发生旁路反应,需要引入“保护群”。
保护群的引入方式包括固相合成和液相合成。
保护群去除环节也是必不可少的步骤。
3.2. 氨基酸的活化在成品肽的合成中,通常采用氨基酸二元法,首先要将氨基酸与活化剂(如DCC)反应生成氨基酸酰尿素中间体,再与下一个氨基酸进行缩合。
3.3. 肽链的组装和延伸通过将氨基酸分子依次组装连结,构建所需的蛋白质分子。
3.4. 连接和删除保护群氨基酸分子之间需要用活化剂和缩合剂反应,使它们形成新的肽键;之后需要在一定的条件下去除引入的保护基,使肽链不断延伸。
3.5. 溶液法和固相法的应用在蛋白质化学全合成中,通常会采用固相合成法和溶液相合成法两种方法来合成肽链。
4. 蛋白质化学全合成的限制因素蛋白质化学全合成虽然有其自身的优势,但同时也存在着各种限制因素。
例如,由于蛋白质复杂结构的存在,化学合成方法往往会受到质量控制、时间效率、中间体的制造和纯化等多种因素的限制;此外,缩合的情况还受到侧链和残基的种类、组合方式等角度的限制。
5. 结语蛋白质化学合成是现代化学和生物学交叉领域的研究热点之一。
虽然该技术受到了多种限制因素的制约,但在不断的技术创新和实现中,也为化学家和生物学家们提供了更广阔的切入点和研究空间,为相关理论的建树和实践应用的提升都提供了重要催化作用。
鲁科版(2019)必修第二册《3.3.3 糖类、油脂和蛋白质 》练习卷(3)

鲁科版(2019)必修第二册《3.3.3 糖类、油脂和蛋白质》练习卷(3)一、单选题(本大题共10小题,共30.0分)1.东汉蔡伦总结前人经验,用树皮、破渔网、破布、麻头等作为原料,制造成较低成本的书写纸,史称“蔡侯纸”。
“蔡侯纸”的主要成分可能是()A. 淀粉B. 天然纤维C. 聚氯乙烯D. 二氧化硅2.下列物质属于酯的是()A. HCOOHB. HCOOCH3C. CH3COOHD. HOCH2CHO3.下列物质属于油脂的是()A. B.C. D.4.植物油厂为了提取大豆中丰富的油脂,下列实验方案设计合理的是()A. 将大豆用水浸泡,使其中的油脂溶于水,然后再分馏B. 先将大豆压成颗粒状,再用无毒的有机溶剂浸泡,然后对浸出液进行蒸馏分离C. 将大豆用碱溶液处理,使其中的油脂溶解下来,然后再蒸馏出来D. 将大豆粉碎,然后隔绝空气加热,使其中的油脂蒸发出来5.下列关于油脂的结构的说法正确的是()A. 油脂是高级脂肪酸与甘油生成的酯B. 若R1、R2、R3都是饱和烃基,称为简单甘油酯C. 若R1、R2、R3都是不饱和烃基,称为混合甘油酯D. 某油脂分子中,所含烃基有三种,但每一个油脂分子中所含这三种烃基都相同,而且排列结构也相同,则该油脂为混合物6.糖类、油脂、蛋白质都是与生命息息相关的物质,下列有关说法正确的是()A. 葡萄糖和蔗糖是同系物,淀粉和纤维素是同分异构体B. 淀粉、纤维素、油脂、蛋白质都是高分子化合物,都能发生水解反应C. 葡萄糖和蔗糖都能与新制Cu(OH)2悬浊液共热,产生砖红色沉淀D. 天然油脂没有固定的熔点和沸点,所以天然油脂是混合物7.下列物质属于油脂的是()A. B.C. D. 润滑油8.有机化合物A的分子量为100,其中碳的质量分数为60%,氢的质量分数为8%,其余为氧,那么A的分子式是()A. C7H16B. C5H8O2C. C4H4O3D. C6H12O9.中国文化中的“文房四宝”所用材料的主要成分为单质的是A笔B墨C纸D砚A. AB. BC. CD. D10.农业上用的杀菌剂波尔多液由硫酸铜和石灰乳按一定比例配制而成,它能防治植物病毒的原因是A. 硫酸铜使菌体蛋白质盐析B. 石灰乳使菌体蛋白质水解C. 菌体蛋白质溶解于波尔多液D. 铜离子和石灰乳使菌体蛋白质变性二、实验题(本大题共1小题,共10.0分)11.乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。
蛋白质结构
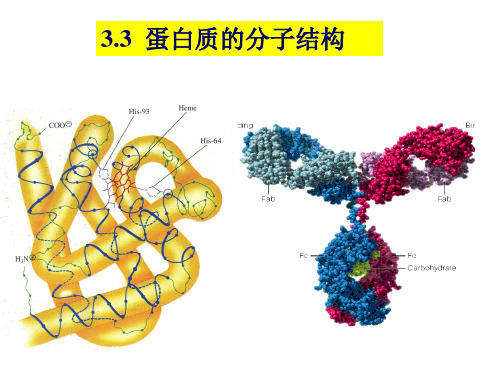
c. 链由141AA残基组成, 链由146AA残基组成。
3.3.2 蛋白质的二级结构
• 指蛋白质分子中多肽链本身的折叠和盘绕的方式,它仅涉及肽 链中主链的构象,并不涉及侧链的构象。 • 蛋白质分子中某一段肽链的局部空间结构,即该段肽链主链骨 架原子的相对空间位置。
酰胺平面是构成主链构象的基本单元.
酰胺平面
多肽链可以看成由Cα串联起来的无数个酰胺平面组成
a .一条多肽链,153个氨基酸残基,一个血红素辅基,分子
量17600。 折叠成8段较直的-螺旋体(A-H),最长的有23个氨基酸残基, 最短的有7个氨基酸残基。拐弯处多由Pro、Ser、Ile、Thr等组 成。
b.肌红蛋白的整个分子具有外圆中空的不对称结构,肽链共
c.具有极性侧链的氨基酸残基分布于分子表面,而带非极性
5
βββ
5
回形拓扑结构
2 3 4 1 回形拓扑结构
平行-折叠的结构比较
卵溶菌酶
黄素蛋白 丙糖磷酸异构酶 乳酸脱氢酶结构域1
丙酮酸激酶结构域4
羧肽酶
腺苷酸激酶
(a)
(b)
next
木瓜蛋白酶
ห้องสมุดไป่ตู้
3.3.5.蛋白质的三级结构(Tertiary Structure)
是指多肽链在二级结构、超二级结构、结构域的基础上,进 一步盘绕、折叠形成的包括主链和侧链构象在内的特征三维 结构。即多肽链上的所有原子(包括主链和侧链)在三维空 间的分布。
蛋白质中相邻的二级结构单位(即单个α -螺旋或β -折叠或β -转角)组合 在一起,形成有规则的、在空间上能辩认的二级结构组合体称为蛋白质的超二 级结构. 基本组合方式:α α ;β
αβ ; β β β
食品化学第3章蛋白质

• 对于阴离子,它们对蛋白质结构稳定性影 响的大小程度为:F-<SO4-<Cl-<Br-<I<ClO4-<SCN- <Cl3CCOO-。 • 在高浓度时阴离子对蛋白质结构的影响比 阳离子更强 – 一般Cl- 、F- 、SO4-稳定蛋白质; – SCN- 、Cl3CCOO-是蛋白质去稳定剂。
• 导致蛋白质冻结变性的原因可能是: – 由于导致蛋白质的水合环境变化,破坏 了维持蛋白质构象的力 – 因为一些基团的水化层被破坏,基团之 间的相互作用引起蛋白质的聚集或亚基 重排; – 也可能是由于结冰后,剩余水中无机盐 浓度大大提高,这种高盐浓度导致蛋白 质变性。
(3)机械处理
• 有些机械处理如揉捏、搅打等,由于剪切 力的作用使蛋白质分子伸展,破坏了其中 的-螺旋,导致蛋白质变性。 • 剪切的速度越大,蛋白质变性程度越大
(2)盐类
• 碱土金属Ca2+、Mg2+离子可能是蛋白质 中的组成部分,对蛋白质构象起着重要作 用,所以除去会降低蛋白质分子对热、酶 等的稳定性。 • 例如,液化淀粉酶需要用Ca2+提高其稳定 性。
• 而对于一些重金属离子如Cu2+、Fe2+、 Hg2+、Pb2+、Ag+等,由于易与蛋白质分 子中的-SH 形成稳定的化合物,因而导致 蛋白质的变性。 • 二巯基丙醇为什么能治疗重金属中毒? • 此外由于Hg2+、Pb2+等还能够与组氨酸、 色氨酸残基等反应,它们也能导致蛋白质 的变性。
结合蛋白根据结合物不同分为六类
• 核蛋白类:与 核酸 结合。 • 糖蛋白类:与 糖类 结合。 • 脂蛋白类:与 脂类 结合。 • 色蛋白类:与 色素 结合。 • 磷蛋白类:与 磷酸 结合。 • 金属蛋白类:与 金属 结合。
生物化学课件3_蛋白质的共价结构

★DNFB法:Sanger试剂,DNP-多肽,酸水解,黄色DNP氨基酸,有机溶剂(乙酸乙酯)抽提分离,纸层析、薄 层层析、液相等
★ PITC法:Edman法,逐步切下。无色PTH-氨基酸,
有机溶剂抽提,层析。
2020/5/8
29
§3.4 蛋白质一级结构测序
3、 测序前的准备工作
§3.3 肽
1、 肽和肽键的结构
2020/5/8
14
§3.3 肽
1、 肽和肽键的结构
★多肽链可以看成由Cα 串联起来的无数个酰胺平 面组成
2020/5/8
15
§3.3 肽
2、 肽的物理和化学性质
(1)、 旋光性 一般短肽的旋光度等于其各个氨基酸的旋光度的总和。 (2)、 酸碱性质 短肽在晶体和水溶液中也是以偶极离子形式存在。 肽的酸碱性质主要取决于N端α-NH2和C端α- COOH以及侧链R上可解离的基团。
Leu+ Pro0 Val-
此肽除Glx外,净电荷为0,可根据此肽的电
泳行为确定是Glu或是Gln。
2020/5/8
38
§3.4 蛋白质一级结构测序
5、 二硫键、酰胺及其他修饰基团的确定
(3)、 糖、脂、磷酸基位置的确定
糖类通过Asn、Ser与蛋白质连接,-N-糖苷 -0-糖 苷
脂类:Ser、 Thr、Cys 磷酸:Ser、 Thr、His 经验性序列:
§3.4 蛋白质一级结构测序
1、蛋白质测序的基本策略 对于一个纯蛋白质,理想方法是从N端直接测至 C端,目前能测100多个N端氨基酸。
(1)、 直接法(测蛋白质的序列) 两种以上特异性裂解法
N A 法裂解 A1 A2 B 法裂解 B1 B2
生物化学蛋白质教案

生物化学蛋白质教案
引言:
生物化学蛋白质是生命体内不可或缺的重要分子,在维持生命活动中具有重要的功能和作用。
了解蛋白质的基本结构、合成和功能对于学习生物化学至关重要。
本教案将介绍生物化学蛋白质的基本知识和相关实验技术,帮助学生更好地理解和掌握这一领域的知识。
一、蛋白质的基本概念和结构
1.1 蛋白质的定义和重要性
1.2 蛋白质的组成和结构层次
1.3 氨基酸的基本结构和分类
二、蛋白质的合成和调控
2.1 蛋白质的合成和转录
2.2 翻译的过程和机制
2.3 蛋白质的修饰和折叠
三、蛋白质的功能和作用
3.1 酶的作用和催化机制
3.2 结构蛋白的功能和作用
3.3 运输蛋白和信号蛋白的作用
四、常见的蛋白质实验技术
4.1 SDS-PAGE凝胶电泳
4.2 Western blotting
4.3 免疫共沉淀实验
4.4 质谱分析技术
五、蛋白质相关疾病和药物研发
5.1 蛋白质相关疾病的发生机制
5.2 药物研发中的蛋白质靶点
结语:通过学习生物化学蛋白质的基本知识和实验技术,学生将能够更好地理解蛋白质在生命活动中的重要性和作用。
掌握这些。
2020-2021鲁科版化学第二册课时3.3.3糖类、油脂和蛋白质含解析

2020-2021学年新教材鲁科版化学必修第二册课时分层作业:3.3.3糖类、油脂和蛋白质含解析课时分层作业(十九)(建议用时:40分钟)[合格过关练]1.糖类、油脂和蛋白质的共同特点是()A.均是高分子化合物B.常温下,遇碘水均会显蓝色C.均只含有C、H、O三种元素D.均是生命活动必不可少的物质D[蛋白质不仅含有C、H、O,还含有N、S等元素,糖类是人体的主要供能物质,油脂是人体主要的储能物质,蛋白质是人体细胞的构成物质,故都是生命活动必不可少的物质。
] 2.现有下列物质:①纤维素、②甲酸甲酯(HCOOCH3)、③淀粉、④甲醛(HCHO)、⑤丙酸、⑥乙酸,其中符合C n(H2O)m的组成且不属于糖类的是()A.①②④B.②④⑥C.①⑤⑥D.①③⑤B[①纤维素、③淀粉都为多糖,不符合题意;②甲酸甲酯分子式为C2H4O2,可写作C2(H2O)2,但不属于糖类,符合题意;④甲醛分子式为CH2O,可写作C(H2O),但不属于糖类,符合题意;⑤丙酸分子式为C3H6O2,不符合C n(H2O)m组成,不符合题意;⑥乙酸分子式为C2H4O2,可写作C2(H2O)2,但不属于糖类,符合题意;所以②④⑥符合,B正确。
]3.下列说法正确的是()A.凡符合C n(H2O)m通式的化合物一定属于糖类,不符合此通式的不属于糖类B.凡能溶于水且具有甜味的化合物都属于糖类C.葡萄糖是能水解的最简单糖类D.淀粉是绿色植物光合作用的产物,是动植物所需能量的重要来源D[如HCHO、CH3COOH等都符合C n(H2O)m的通式,但不是糖类,不符合此通式的也可能是糖类,如鼠李糖(C6H12O5),A不正确;能溶于水且具有甜味的化合物不一定是糖类,糖类物质不一定具有甜味,如淀粉,B不正确;葡萄糖是一种单糖,它不能再水解为更简单的糖,C不正确.]4.某糕点的营养成分如下表所示:A.淀粉和纤维素属于糖类,且互为同分异构体B.维生素是一种基本营养物质C.淀粉、油脂、蛋白质都由碳、氢、氧三种元素组成D.淀粉、油脂、蛋白质都为有机高分子化合物B[淀粉和纤维素的聚合度不同,因此不互为同分异构体,A错误;维生素是一种基本营养物质,B正确;淀粉、油脂都由碳、氢、氧三种元素组成,而蛋白质至少含有碳、氢、氧、氮四种元素,C 错误;油脂的相对分子质量较小,不是有机高分子化合物,D错误.]5.下列关于油和脂肪的比较,错误的说法是()A.油的熔点低,脂肪的熔点高B.油含不饱和烃基的相对量比脂肪少C.油和脂肪都不易溶于水,易溶于汽油、酒精、苯等有机溶剂D.油和脂肪都能发生水解反应B[油脂是高级脂肪酸的甘油酯,根据常温下的状态分为固态的脂肪和液态的油,其中脂肪中烃基饱和程度高,熔点高,油含不饱和烃基的相对量较多,熔点低,在一定条件下,油和脂肪都能水解。
2011版高中化学全程学习方略课件:3.3.4《蛋白质》(鲁科版必修2)
蛋白质
脂肪
—COOH、—NH2
实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组
成。取W g该种氨基酸放在纯氧中充分燃烧,生成CO2、
H2O和N2。现按如图所示装置进行实验(铁架台、铁夹、 酒精灯等未画出)。
请回答下列有关问题: (1)实验开始时,首先要通入一段时间的氧气,其理 由是______________。
1.(2010·郑州高二检测)下列过程涉及化学变化的是 ( A.升华 B.分馏 C.盐析 D.变性 )
【解析】选D。盐析、变性都是蛋白质的性质,盐析是
物理变化,是可逆过程;变性是化学变化,是不可逆过
程;升华、分馏是物理变化。
2.欲将蛋白质从水中析出而又不改变它的性质,应加入 ( )
A.福尔马林溶液
3.蛋白质是一切生命的物质基础,是维持人体健康和促
进身体发育的先决条件,补充优质蛋白质更可帮助体弱 者直接增强抵抗力,维护身体健康。下列关于蛋白质的 叙述不正确的是( )
A.所有蛋白质遇到浓硝酸后都会变黄 B.蛋白质溶液中加入硫酸铵饱和溶液,蛋白质析出,加 水又溶解
C.蛋白质能透过滤纸,但不能透过半透膜
)
C.乙酸、油脂都能与NaOH溶液反应
D.乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯 中的少量乙酸可用饱和Na2CO3溶液除去
【解析】选A。乙烯使溴水退色的原理是加成反应,苯 使溴水退色的原理是萃取,故A错;淀粉水解的最终产 物是葡萄糖 ,蛋白质水解的最终产物是氨基酸,故B正 确;乙酸与NaOH发生酸碱中和,油脂在碱性条件下能水
A.生成二氧化碳气体的质量
B.生成水的质量 C.通入氧气的体积 D.氨基酸的相对分子质量
【解析】观察装置图可知,该实验是通过测定氨基酸在 纯氧中燃烧后生成H2O的质量(被B中浓H2SO4吸收), CO2的质量(被C中碱石灰吸收),及N2的体积(即F中排
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
ACTH、α-MSH和β-MSH一级结构比较
13
类阿片活性肽:
一组有吗啡样作用的内源肽类物质,包 括脑啡肽(5肽),内啡肽和强啡肽 甲硫脑啡肽 N-tyr.gly.gly.phe.met-OH bLPH61-65
亮脑啡肽
a内啡肽
N-tyr.gly.gly.phe. leu -OH
N-tyr.gly.gly.phe.met.thr. bLPH61-77 ser.gln.thr.pro.leu.val.thr-OH N-tyr.gly.gly.phe.met.thr. bLPH61-77 ser.glu.lys.ser.gln.thr.pro.leu. val.thr.leu-OH
3
多肽举例: 3肽 9肽 红细胞谷胱甘肽
下丘脑促甲状腺素释放素 垂体催产素,加压素 10肽 促黄体生成素释放素
39肽 促肾上腺皮质激素
53肽 表皮生长因子
4
蛋白质:一般50~100个以上氨基酸组成,
分子大,具有严密和稳定的三维空间
结构。 结构层次包括一,二,三及四级 结构。另外尚有超二级结构及结构域
S
S
*活性中心2位Tyr -C=O 与5位Asn –NH 间形成氢键, Tyr 的苯环位于环状结构内部 3位Ile 与8位Leu是其活性与作用专一性的关键位置
8
血管加压素: NCys. Tyr. Phe. Gln. Asn. Cys. Pro. Arg. GlyC * 2位Tyr与3位Phe间由范德华力引起堆积效应,
4. 链中Ser和GlyLeabharlann 链小,利于活性区域形成16
功能:
增加毛细血管通透性,血管扩张 平滑肌收缩或松弛
引起疼痛
17
胰岛素: 不同物种提取的胰岛素含51个氨基
酸,A,B 两条肽链, A链和B链通过两条
二硫键互相连接成胰岛素分子,分子量
约为6000。
18
胰岛素的一级结构
19
A链含有11种共21个氨基酸残基,N端为甘氨酸,C-端为天冬酰胺; B-链含有16种共30个氨基酸残基, N-端为苯丙氨酸,C-端为丙氨酸。
Tyr与5位Asn 间不能形成氢键,Tyr的酚羟基被
排于环状结构外
9
功能:
催产素为增强子宫平滑肌收缩和泌乳
血管加压素为增强血管平滑肌收缩,升高血压 及利尿
10
ACTH, MSH, LPH, POMC 等多肽
促肾上腺皮质激素ACTH :39肽 1-18区为生物活性区,活性中心位于N端14肽区 15-18区为加强对受体结合的部位 25-39区增强分子稳定性,免受酶破坏。与 生物活性关系不大,切去仍保留活性 人工合成的1-24肽具有ACTH相同活性,可用于临床 功能:促进肾上腺皮质激素合成分泌
24
•细胞色素C与生物进化
•细胞色素C是一种比较古老的蛋白质,从酵 母菌到人,各种生物都具有细胞色素,这种
蛋白质已进化了15亿年。
•目前已测定了近百种生物的细胞色素C的氨 基酸顺序,由于种属遗传差异,其一级结构 有较大的不同。
25
N-
-C
细胞色素C结构示意图
26
与铁原子结合的氨基酸 18: His 和 80: Met 35个氨基酸残基(约1/3)保持不变,称保守部位 赖氨酸的集中存在,在空间集结成由一负电荷区 相隔的两个正电荷区域,为其功能必不可少 82: Phe, 对电子传递起作用
β
g内啡肽
14
功能特点: 类阿片活性肽, 能与吗啡受体结合, 产生吗啡 样作用。完成生物活性功能的基本结构单位是脑啡 肽。结构完整性是生理功能必需, 两个gly.gly是功能 所必需。N端不可缺少, 取代或延伸, C端不可缺少, 但可延伸
15
激肽(kinin):来源于血浆和组织的一组蛋白质
舒缓激肽(BK):9肽 NArg-Pro-Gly-Phe-Ser-Pro-Phe-ArgC 1. 结构完整性是生理功能必需 2. N,C端的Arg及两个Phe为生物活性必不可少 3. 链中Pro对维持肽链走向,分子构象稳定起关 键作用
22
蛋白质一级结构与分子进化 同源蛋白质:不同种属中执行同一功能的蛋白质。 对其一级结构的比较, 可以反映物种种属的进化 举例: 细胞色素C 近百种属 35个氨基酸残基完全不变
23
细胞色素C与物种进化
•细胞色素C的基本知识 本质:细胞色素C=一条肽链(含104个氨基 酸残基)+铁卟啉 (说明:不同生物其多肽链的氨基酸残基数不同, 如昆虫有108个氨基酸残基,植物有112个) 作用:传递电子,即Fe3++e--------Fe2+
20
一级结构存在种属变异:
A链 8 人 狗 猪 牛 Thr Thr Thr Ala 9 Ser Ser Ser Ser 10 Ile Ile Ile Val B链 30 Thr Ala Ala Ala
21
特点: 肽链中可变氨基酸不是胰岛素的活性部位 维持空间结构的关键部位保守性强, 对功能无明显干扰 牛,猪胰岛素在临床上被用于治疗糖 尿病,而猪胰岛素 更易于被人接受
5
多肽,蛋白质 一级结构:
一级结构与功能
指氨基酸在蛋白质分子中的排列顺序。 表示法:从左到右表示从多肽链的氨基末端到 羧基末端。 现用单字母代表一种氨基酸
甘:Gly G
丝:Ser S
6
几种多肽,蛋白质一级结构与功能的关系
7
催产素和血管加压素(九肽)
牛催产素结构: NCys. Tyr. Ile. Gln. Asn. Cys. Pro. Leu. GlyC
本章内容
多肽,蛋白质一级结构与功能 蛋白质一级结构与分子进化 蛋白质一级结构与分子病 蛋白质一级结构的测定
蛋白质的空间结构
免疫球蛋白与补体 纤维状蛋白质胶原
1
本章要点: 基本概念 多肽,蛋白质结构层次
举例说明一级结构,空间结构与功能的关系
分子病
2
多肽和蛋白质
在蛋白质分子中,氨基酸之间以肽键 相连 氨基酸之间通过肽键联结起来的化合物称为肽。 两个氨基酸形成的肽叫二肽,三个氨基酸形成的 肽叫三肽……, 一般将十肽以下称为寡肽,十肽以上者称多肽。 分子相对小,没有严密和相对稳定的空间结构
11
阿黑皮素原(POMC): 结构上为ACTH,促黑素细胞激素(MSH),内啡肽, 脂酸动员激素(LPH)的前体
ACTH 1-13区,同a-MSH分子结构,但无N端乙酰化 功能特点:一级结构决定其功能, His-Phe-Arg-Trp-Gly 有MSH活性 a,β –MSH中有此结构
12
图1-12
