(完整版)初中化学物质转化关系图.doc
九级化学物质转化关系图

一、初中化学物质的转化关系1、氧气、氧化物、酸、氢气、水H2OKMnO4↘↓↑↗CO、CO2↗SO2H2SO4H2O2→→P2O5+ Mg Al Zn Fe→ H2→H2O ↘MgO HClKClO3↗↓↘Al2O3 Fe3O42、碳与碳的化合物3、氢氧化钠、碳酸钠、氯化钠+ CO2↗ Na2SO4 → BaSO4↓(白)NaOH → Na2CO3 → CaCO3↓(白)(变质)↘ NaCl → AgCl↓(白)4、含钙化合物的关系:↙↗―――――――↘↖CaCO3→CaO→Ca(OH)2→CaCl2↖CO2↙5、氧化钡、氢氧化钡与硫酸钡1 / 32 /3 ↗BaCl 2 → BaSO 4↓(白)BaO → Ba(OH)2 ↗↘ + CuS O 4↘Cu(OH)2↓(蓝)6、硫酸铜、碳酸氢钙、碳酸氢钠、碳酸氢铵CuO ↗ CO 2↙ ↘ Ca(HCO 3)2 → CaCO 3→CaOCuSO 4.5H 2O →CuSO 4→ Cu ↘ H 2O↗Na 2CO 3 ↗ NH 3 → NH 3.H 2O NaHCO 3 →CO 2 NH 4HCO 3 → H 2O↘H 2O → H 2CO 3 ↘ CO 2 → H 2CO 37、铝、镁、锌、铁、铜及其化合物↗ZnSO 4↖ ↗ AlCl 3↖Zn → ZnO Al → Al 2O 3 ↘ZnCl 2↙ ↘Al 2(SO 4)3↙Fe Al↗MgCl 2↖ ↙﹉﹉﹉﹉↗ CuCl 2↘↖Mg → MgO Cu ←→CuO Cu(OH)2 ↘MgSO 4↙ ↖____↘ CuSO 4↗↙ Fe Al↙ FeCl 3 ↖ C CO H 2 Mg Al ↗FeSO 4Fe(OH)3 Fe 2O 3 ←――――→ Fe↖Fe 2(SO 4)3↙ O 2 H 2O ↘ FeCl 2 8、常见物质的相互转化关系(即注明必要的反应物、反应条件)CO 2 CO C 或O 2 O 2 H 2O H 2O 2Al 2O 3 AlCl 3 Al CuO CuSO 4 Cu ⑴ ⑵ ⑶ ⑷ MgO MgSO 4 Mg Cu H 2 Fe CaO Ca(OH)2 CaCO 3 CaCl 2 Ca(OH)2CaCO 3 ⑸ ⑹ ⑺ ⑻CaCO3Na2CO3CO2CO2NaOHNa2CO3CO2O2H2ONaOH NH4ClNH3⑼⑽⑾⑿3 / 3。
第2课时 物质的转化

1.根据物质的性质分类,CH3COOH属于
A.碱
B.四元酸
( C)
C.一元酸
D.盐
解析:CH3COOH在水溶液中电离出一个H+,属于一元酸。
2.酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和
所得到的盐,常见的有NaHCO3、NaHSO4、KH2PO4、K2HPO4等。已
知H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2,则下列
D.与碱性氧化物反应生成盐和水
解析:酸使紫色石蕊溶液变红色,故A错误;酸能和碱反应生成盐 和水,属于酸的通性,故B正确;酸与活泼金属反应生成盐和氢气,属 于酸的通性,故C正确;酸可以和碱性氧化物反应生成盐和水,属于酸 的通性,故D正确。
4.碱溶液中都含有OH-,因此不同的碱表现出一些共同的性质。
基本反应类型
__复__分__解__反__应__ 复分解反应 复分解反应
现象或化学方程式
基本反应类型
盐的 主要 化学 性质
与酸反应 与碱反应
Na2CO3 + 2HCl=== 2_N_a_C__l+___H_2_O_ __+__C__O_2_↑___
Ca(OH)2 + Na2CO3===CaCO3↓ + 2NaOH
写出下列有关序号的化学方程式并注明反应类型:
化学方程式
①_____2_C__a_+__O__2=__=_=_2_C__a_O_____ ②______C_a_O__+__H__2O__=_=__=_C_a_(_O__H__)2_____ ③_C__a_(_O_H__)_2+___N_a_2_C_O__3_=_=_=_C__a_C__O_3_↓_+__2_N__a_O__H_
2.根据酸的通性,说出将盐酸加入含有酚酞的NaOH溶液(红色)的 现象。
浙教版初中科学九上2.5《物质的转化》(共21张PPT)

一、金属单质
Ca
O2
CaO
H2O
Ca(OH)2
HCl
CaCl2
盐的转变关系:
金属 碱性 氧化物
碱 盐
二、非金属单质
C O2
CO2 H2O
H2CO3
Ca(OH)2
CaCO3
盐的转变关系:
非金属
酸性 氧化物
酸
盐
加热
Fe + S == FeS
• 金属 + 非金属
盐 (无氧酸盐)
一、单质、氧化物、酸、碱、盐各类物质的相互关系
1.自然界没有风风雨雨,大地就不会春华秋实。2.瀑布跨过险峻陡壁时,才显得格外雄伟壮观。3.诽谤,同时造了无数的罪业,这是嫉妒;自己欢喜4.在茫茫沙漠,唯有前时进的脚步才是希望的象征。5.只会幻想而不行动的 人,永远也体会不到收获果实时的喜悦。6.我们只要每天睁开眼睛,看到自己还活着,就该庆幸自己多么的幸运7.赞叹,同时积累了同样的功德利益,这是随喜。怎么做,完全在于自己。8.盲目的上进,就像在死胡同里打转。 你浪费的人生,原本可以有更多的精彩。9.其他烦心的事,想开点,看开点,再苦再难的日子,熬着熬着也就挨过来了。10.这个世界到处充满着不公平,我们能做的不仅仅是接受,还要试着做一些反抗。11.懦弱的人只会裹 足不前,莽撞的人只能引为烧身,只有真正敢的人才能所向披靡。12.精神健康的人,总是努力地工作及爱人,只要能做到这两件事,其它的事就没有什么困难。13.命,是失败者的借口;运,是成功者的谦词。带着青春的印 记,我们这代人,慢慢的随着时间的流淌,渐渐老去。晚安!14.努力不是为了做给谁看,无论什么结果都能问心无愧;努力是因为你可以不接受命运的框定,靠自己来场漂亮的反击。15.美国人口普查局的“世界人口时钟” 显示,全世界每秒钟有1.8人死亡,一小时就是6,360人,一天就有152,640人死亡。16.当你觉得老天对你不公的时候,别急着红眼,别急着抱怨,因为这样只会削弱你的意志,消磨你的斗志,最后让你变得平庸,一事无成。 17.昨天,再值得留恋,也不会为你的留恋停留;明天,再艰辛,也不会因为你的脆弱而怜悯;优雅之人心如止水,波谰不惊,不以物喜,不以己悲。做一个优雅从容的人,只有先稳下来,静下心,学会宽容,仁爱,温和。 18.无论你正经历着什么,过得是否开心,世界不会因为你的疲惫,而停下它的脚步。那些你不能释怀的人与事,总有一天会在你念念不忘之中遗忘。无论黑夜多么漫长不堪,黎明始终会如期而至。睡一觉,愿美梦治愈你的 难过。晚安!19.凡事顺其自然,凡事不可强求。人生,错过太多,我们都在重复,所以,我们不必为自己错过的悲哀,而应该为自己拥有的而喜悦。错过了漂亮,你还拥有健康;错过了健康,你还拥有智慧;错过了智慧,你还 拥有善良;错过了财富,你还拥有安逸;错过了安逸,你还拥有自由20.人生,总有乌云密布的低沉的时刻,但也会有蓦然抬头,拨云见日的一天。而最重要的是在低潮时要忍耐得住,不要放弃对光明的追求,永远不要以为走
专题二物质的相互转化

专题二物质的相互转化教学目标1.掌握单质、氧化物、酸、碱、盐等物质间的转化关系。
2.构建酸、碱、盐与单质、氧化物的关系网络。
3.能应用所学的酸碱盐的知识合理解释或解决一些生产、生活的实际问题。
重点无机物相互转化规律根底回归一、物质的分类(一)纯洁物和混合物工程纯洁物混合物概念由同一种物质组成由两种或两种以上的物质混合而成,彼此间不发生化学反响区别①一种物质②对于由分子构成的物质而言,由一种分子构成③有固定的组成④有固定的性质①两种或两种以上物质②由不同种分子构成③没有固定的组成④没有固定的性质联系(二)单质和化合物工程单质化合物概念由同种元素组成的纯洁物由不同种元素组成的纯洁物一样点均为纯洁物均为纯洁物不同点①由一种元素组成②单质的分子由同种原子构成①由不同种元素组成②化合物分子由不同种原子构成联系(三)氧化物工程酸性氧化物碱性氧化物概念凡能跟起反响生成盐和水的氧化物凡能跟起反响而生成盐和水的氧化物组成大多数是非金属氧化物(穿插关系) 都是金属氧化物(附属关系)性质①与水反响生成对应的含氧酸(SiO2除外)②与可溶性碱反响生成盐和水①与水反响生成可溶性碱②与酸反响生成盐和水(四)酸、碱、盐工程酸碱盐概念电离时生成的阳离子全部是氢离子的化合物电离时生成的阴离子全部是氢氧根离子的化合物电离时生成金属离子和酸根离子的化合物一样点均为化合物,其水溶液都能导电(电离)不同点酸=H++酸根离子碱=金属离子+OH-盐=金属离子+酸根离子组成特点一定含氢元素一定含氢、氧两种元素一定含有非金属元素联系酸+碱→盐+水(中和反响)二、物质的相互转化转化的文字表达式化学方程式〔举例〕①金属+ 氧气→②非金属 + 氧气→③金属氧化物 +水→④非金属氧化物+ 水→⑤金属 + 非金属→盐Mg +Cl2 = MgCl2⑥金属氧化物 + 非金属氧化物→盐CaO + SiO2 = CaSiO32、金属、非金属、金属氧化物、非金属氧化物、酸、碱、盐的相互关系转化的文字表达式化学方程式〔举例〕①金属+ 酸→②非金属+ 碱→③金属氧化物 + 酸→④非金属氧化物 + 碱→⑤酸 + 碱→⑥酸 + 盐→⑦碱 + 盐→⑧盐 + 盐→典型例题1.以下各组变化中,每一转化在一定条件下均能一步实现的是A.①和② B.②和③ C.①和③ D.①②③2.在①单质、②氧化物、③酸、④碱等四类物质中,经一步反响可以生成盐的是〔〕A.只有①②③B.只有②③④C.只有①②④D.①②③④3.甲、乙、丙是初中化学中常见的物质,其转化关系如右图所示:〔1〕假设甲、乙组成元素一样,甲、乙、丙中有一种物质为水,那么甲为〔填化学式〕,实验室制丙的化学方程式为:〔写出一种〕。
中考化学推断题三角关系图
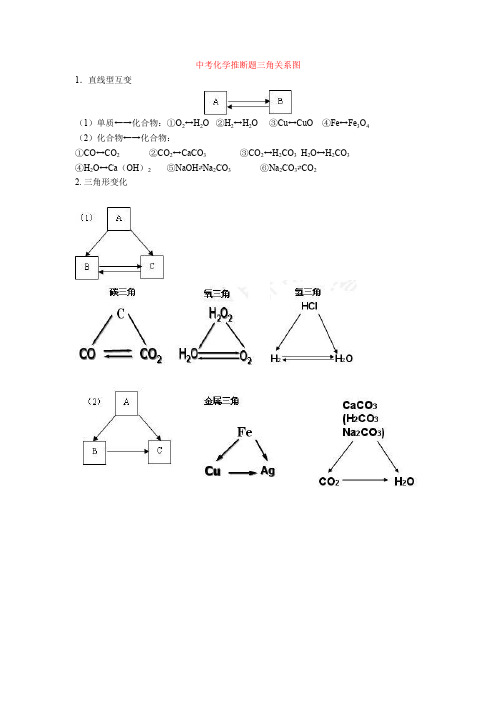
中考化学推断题三角关系图1.直线型互变(1)单质←→化合物:①O2↔H2O ②H2↔H2O ③Cu↔CuO④Fe↔Fe3O4(2)化合物←→化合物:①CO↔CO2 ②CO2↔CaCO3 ③CO2↔H2CO3 H2O↔H2CO3④H2O↔Ca(OH)2 ⑤NaOH⇄Na2CO3 ⑥Na2CO3⇄CO22. 三角形变化(4)其它:3. 四边形关系:二、中考化学推断题2.甲、乙、丙是初中常见物质,它们之间的转化关系如下图所示,其中部分反应物、生成物及反应条件已略去。
(1)若甲、乙、丙都是气体,丙是灭火剂,则乙是________。
(2)若甲、乙、丙都为金属,反应皆是在溶液中进行的置换反应,甲、乙、丙三种金属的化学式依次是________(写一组)。
(3)若甲、乙、丙含相同的金属元素。
甲是可用于改良酸性土壤的碱,乙转化为丙的化学方程式是________(写一个)。
(4)下列三组物质中,符合上述转化关系的是________ (填标号)。
【答案】一氧化碳(或CO ) Zn 、Fe 、Cu 2233CaCl + Na CO =CaCO + 2NaCl ↓ a b 【解析】 【分析】根据甲、乙、丙是初中常见物质,若甲、乙、丙都是气体,丙是灭火剂,所以丙是二氧化碳,甲转化成的乙会转化成二氧化碳,所以甲是氧气,乙是一氧化碳;若甲、乙、丙都为金属,反应皆是在溶液中进行的置换反应,排在前面的金属可以将排在后面的金属从其盐溶液中置换出来;若甲、乙、丙含相同的金属元素,甲是可用于改良酸性土壤的碱,所以甲是氢氧化钙,甲、乙都会转化成丙,所以乙是氯化钙,氢氧化钙、氯化钙都会生成丙,所以丙是碳酸钙,然后将推出的物质进行验证即可。
【详解】(1)若甲、乙、丙都是气体,丙是灭火剂,所以丙是二氧化碳,甲转化成的乙会转化成二氧化碳,所以甲是氧气,乙是一氧化碳;(2)若甲、乙、丙都为金属,反应皆是在溶液中进行的置换反应,排在前面的金属可以将排在后面的金属从其盐溶液中置换出来,所以甲、乙、丙三种金属的化学式依次是:Zn 、Fe 、Cu ;(3)若甲、乙、丙含相同的金属元素,甲是可用于改良酸性土壤的碱,所以甲是氢氧化钙,甲、乙都会转化成丙,所以乙是氯化钙,氢氧化钙、氯化钙都会生成丙,所以丙是碳酸钙,乙转化为丙的反应是氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,化学方程式是:2233CaCl + Na CO =CaCO + 2NaCl ↓;(4)a 、过氧化氢分解会生成水和氧气,水通电会生成氢气和氧气,故正确;b 、碳酸钠会转化成氢氧化钠,氢氧化钠会转化成硫酸钠,碳酸钠也会转化成硫酸钠,故正确;c 、硝酸钾不会转化成碳酸钾,故错误。
中考化学第二轮复习物质的转化与推断精品课件

3. (2021烟台模拟)A~F为初中化学常见物质,固体A在空气中易潮解,B 和C能参与光合作用,B和D组成元素相同。它们相互转化的关系如图所 示(“→”表示反应能一步实现,“——”表示相连物质间能发生反应,部分 反应物、生成物和反应条件已省略)。下列说法错误的是( D) A. C和F组成元素可能相同 B. 固体B可用于人工降雨 C. D和E在一定条件下反应生成B D. A~F属于酸、碱、盐、氧化物、 单质中的四类物质
烧产生的二氧化硫少很多,因此燃煤更容易导致酸雨,对环境影响比较大;煤和天然气燃烧都生成二氧化碳,所以都有温室气体产生。
A. C→CO B. H O →O 设计实验 根据氧化亚铜和稀硫酸发生反应的化学方程式可知,若该红色粉末中含Cu2O,则反应生成物一定有溶于水形成蓝色溶液的CuSO4和不溶于水的红色固体Cu,因此可观察到的现
(1)写出化学式:D_H__C_l_,E__F_e_。 (2)物质G所属的物质类别是_氧__化__物__(_或__金__属__氧__化__物__)_;物质C与物质D反 应的基本类型是__复__分__解__反__应__。 (3)物质A和物质D反应的化学方程式是 _K__2C__O_3_+__2_H__C_l_=_=_=__2_K_C__l+__H__2O__+__C_O__2_↑_。 (4)古代常将草木灰与C溶液混合,滤取反 应后清液作漂洗的洗涤剂。写出此反应的 化学方程式_C_a_(_O__H_)_2+__K__2_C_O__3=_=__=_C__a_C_O__3↓_+__2_K__O__H_。
选项
甲
乙
丙
A
H2SO4
H2
H2O
B
NaOH
NaCl NaNO3
(1)写出化学式:B_H__2_S_O_4__,E__C_u_S_O__4_。 (2)物质C所属的物质类别是氧__化__物__(_或__金__属__ _氧__化__物__)_,选择C作为食品干燥剂的原因有 安__全__无__毒__,__价__格__低__廉__(_或__吸__水__性__强__或__不__与__食___ 品__反__应__(答两条即可)。 (3)写出D转化为F的化学方程式__C_a_(O__H_)_2_+__N_a_2_C_O_3_=_=_=__C_a_C_O__3↓_+__2_N__a_O_H__。 (4)B在生产上的用途有_金__属__除__锈__(_或__化__工__原__料__、__气__体__干__燥__剂__等__)_,上述反 应没有包含的基本反应类型是_分__解__反__应__。
初中化学重点复习系列7-化学转换三角及推断

初中化学重点复习系列7-化学转换三角及推断一、三角转换1、氧三角2H 2O 2MnO22H 2O+O 2↑ 2H 2O通电2H 2↑+O 2↑2H 2+O 点燃2H 2O 2、碳三角2C+O 2点燃2CO 2CO+O 2点燃2CO 2C+O 2点燃CO 2 C+CO 2高温2CO3、钙(石灰)三角及转化:石灰石、生石灰、熟石灰 CaCO 3高温CaO+CO 2↑CaO+H 2O==Ca(OH)2 Ca(OH)2+CO 2==CaCO 3↓+H 2O 4、铁三角1 2H 2O+4Fe+3O 2缓慢氧化2Fe 2O 3·H 2OFe 2O 3+6HCl==2FeCl 3+3H 2O Fe 2O 3+3CO高温2Fe+3CO 2Al+FeCl 3==AlCl 3+Fe2Fe+3Cl 2点燃2FeCl 35、铁三角2(Fe 3O 4可以写成Fe 3O 4 •Fe 3O 4)3Fe+2O 2点燃Fe 3O 4 Fe 3O 4+4CO高温3Fe+4CO 2Fe 3O 4+8HCl==2FeCl 3+FeCl 2+4H 2O Zn+FeCl 2==ZnCl 2+Fe Fe+2HCl==FeCl 2+H 2↑ 6、铜三角2Cu+O 2 △2CuO H 2+CuO△Cu+H 2OCuO+H 2SO 4==CuSO 4+H 2O Fe+CuSO 4==FeSO 4+Cu Cu+Ag 2SO 4==CuSO 4+2Ag 7、酸三角H 2SO 4+BaCl 2==BaSO 4↓+2HClCCOCO 2H 2OH 2O 2O 2FeFe 2O 3FeCl 3CuCuOCuSO 4H 2SO 4CaOCa(OH)2 CaCO 3FeFe 3O 4FeCl 2HCl+AgNO 3==AgCl ↓+HNO 3 H 2SO 4+Ba(NO 3)2==BaSO 4↓+2HNO 3 Na 2CO 3+H 2SO 4==Na 2SO 4+H 2O+CO 2↑ 8、碱三角Ca(OH)2+Na 2CO 3==CaCO 3↓+2NaOH 2NaOH+CuSO 4==Cu(OH)2↓+Na 2SO 4 Ca(OH)2+CuSO 4==Cu(OH)2↓+CaSO 4 Ca(OH)2+(NH 4)2SO 4==CaSO 4+2H 2O+2NH 3↑ 9、盐三角1Na 2CO 3+H 2SO 4==Na 2SO 4+H 2O+CO 2↑ Na 2SO 4+BaCl 2==BaSO 4↓+2NaCl Na 2CO 3+2HCl==2NaCl+H 2O+CO 2↑ Na 2CO 3+2HNO==2NaNO 3+H 2O+CO 2↑ 10、盐三角2CaCO 3+2HCl==CaCl 2+H 2O+CO 2↑ CaCl 2+2AgNO 3==2AgCl ↓+Ca(NO 3)2CaCO 3+2HNO 3==Ca(NO 3)2+H 2O+CO 2↑ 外一:我们身边的物质总转变 ② ① ⑧ ⑨ ⑥ ⒀⒁③④ ⑦ ⒂⑤ ⑩ ⑾⑿①2KMnO 4 △ K 2MnO 4+MnO 2+O 2↑ ②2H 2O 2MnO22H 2O+O 2↑ ③2H 2O通电2H 2↑+O 2↑ ④2H 2+O 2点燃2H 2O⑤3Fe+2O 2点燃Fe 3O 4⑥C+O 2点燃CO 2⑦6CO 2+6H 2O 叶绿素光照C 6H 12O 6+6O 2⑧H 2CO 3△H 2O+CO 2↑ ⑨CO 2+H 2O==H 2CO 3⑩Ca(OH)2+CO 2=CaCO 3↓+H 2O⑾CaCO 3高温CaO+CO 2↑⑿CaCO 3+2HCl=CaCl 2+H 2O+CO 2↑⒀3CO+Fe 2O 3高温2Fe+3CO 2 ⒁2CO+O 2点燃2CO 2⒂C+CO 2高温2CO二、推断题解题思路1、 阅读题目:要求通阅全题,统领大局。
初中化学 化学转换三角及推断

初中化学化学转换三角及推断化学转换三角是一种直观的化学反应表示方法,它用不同的物质或元素符号来表示化学反应中物质的转换关系。
这个三角形可以清晰地展示出化学反应中各物质之间的相互转化关系。
推断题是初中化学考试中常见的一种题型,它通过给出一些化学反应的条件和结果,让考生推断出未知的反应物或生成物。
这种题型需要考生对化学反应有深入的理解和掌握,同时具备分析问题和解决问题的能力。
化学转换三角可以帮助考生在推断题中快速找到突破口。
例如,对于一个包含多种物质的推断题,我们可以通过分析化学转换三角来确定哪些物质之间可能发生反应,从而缩小可能的答案范围。
我们还可以通过观察化学转换三角中物质的分布情况,推断出反应的类型和反应条件等重要信息。
熟练掌握常见的化学反应类型和反应条件,以便在解题时能够迅速联想到相关的反应。
注意题目中给出的反应条件和结果,从中提取关键信息,如颜色变化、沉淀生成等。
尝试从已知的反应中找出规律,以便在未知的反应中找到对应的规律。
对于一些难以确定的物质,可以通过化学转换三角来分析其可能的性质和反应类型。
已知A、B、C、D、E五种物质,它们之间存在如下的化学转换关系:现知A是一种碱,B是一种盐,C是一种金属单质,D是一种非金属单质,E是一种酸。
根据上述信息,推断出A、B、C、D、E、F、G、H、I、J分别是什么物质。
A与B反应生成C和D,由于A是一种碱,B是一种盐,因此可以推断出这是一个碱与盐之间的复分解反应。
结合给出的反应条件和结果,可以推断出C可能是沉淀物或气体,D是非金属单质。
C与E反应生成A和F,由于E是一种酸,可以推断出这是一个金属与酸之间的反应。
结合给出的反应条件和结果,可以推断出F是一种盐。
B与E反应生成G和H,由于E是一种酸,可以推断出这是一个盐与酸之间的反应。
结合给出的反应条件和结果,可以推断出G和H可能是沉淀物或气体。
F与H反应生成I和J,由于F是一种盐,H是一种非金属单质,可以推断出这是一个盐与非金属单质之间的反应。
