新药研究开发与上市流程图
新药的开发流程及周期
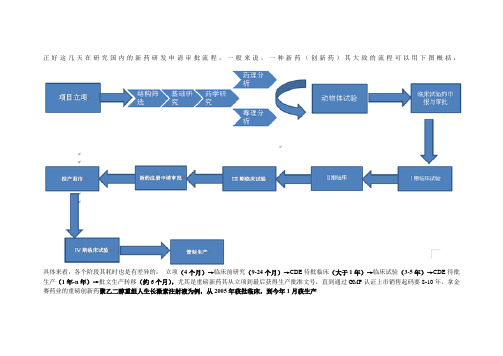
正好这几天在研究国内的新药研发申请审批流程,一般来说,一种新药(创新药)其大致的流程可以用下图概括:具体来看,各个阶段其耗时也是有差异的:立项(4个月)→临床前研究(9-24个月)→CDE待批临床(大于1年)→临床试验(3-5年)→CDE待批生产(1年-n年)→批文生产转移(约6个月),尤其是重磅新药其从立项到最后获得生产批准文号,直到通过GMP认证上市销售起码要8-10年。
拿金赛药业的重磅创新药聚乙二醇重组人生长激素注射液为例,从2005年获批临床,到今年1月获生产这份流程图和这篇文章给出了药物研发的成功率以及每个步骤所花费的时间。
总体来看,每5种进入临床的药物中只有1种能进行所有的试验和批准过程。
新药开发阶段如下:临床前试验:由制药公司进行的实验室和动物研究,以观察化合物针对目标疾病的生物活性,同时对化合物进行安全性评估。
这些试验大概需要3.5年的时间。
研发中新药申请(Investigational New Application, IND):在临床前试验完成后,公司要向FDA提请一份IND,之后才能开始进行药物的人体试验。
如果30天内FDA没有发出不予批准的申明,此IND即为有效。
提出的IND需包括以下内容:先期的试验结果,后续研究的方式、地点以及研究对象;化合物的化学结构;在体内的作用机制;动物研究中发现的任何毒副作用以及化合物的生产工艺。
另外,IND必须得到制度审核部门(the Institutional Review Board)的审核和批准。
同时,后续的临床研究需至少每年向F DA提交一份进展报告并得到准许。
临床试验,Ⅰ期:此阶段大概需要1年时间,由20~80例正常健康志愿者参加。
这些试验研究了药物的安全性方面,包括安全剂量范围。
此阶段的研究同时确定了药物在体内的吸收、分布、代谢和排泄、以及药物的作用持续时间等项目。
临床试验,Ⅱ期:此阶段需要约100到300名志愿患者参与进行一些控制研究,以评价药物的疗效。
中药新药研发流程基础知识PPT

但是过多的剂量则是致命的;同 样的道理,吗啡可以缓解疼痛, 过量服用药理学是研究药物与机体相互作 用及其规律的机制。
药理学的方法是实验性的,即在 严格控制的条件下观察药物对机 体或其组成部分的作用规律并分 析其客观作用原理。
一、中药新药研发过程
药材辅料
中药研发流程图
药学提取 工艺
小试3
药学成型
批
摸索质量
工艺
标准
大生产一批 主要药效学
中试3批
建立质量标 准草案
稳定性三因素 试验
包 装
稳定性加速及 长期实验
急毒
长毒
临床
临床批件
生产批件
1、调研
2、立项
3、实验室研究
工艺制备研究 提取工艺设计 提取工艺实验 成型工艺设计 成型工艺实验 三批小样实验 放大处方量实验 试制三批小样,确定工艺
中药研发基础知识
中药新药分类:
1、未在国内外上市销售的药品. 2、改变给药途径且尚未在国内外上市销售的制剂 3、已在国外上市销售但尚未在国内上市销售的药品 4、改变已上市销售盐类药物的酸根、碱基(或者金属元素),但不
改变其药理作用的原料药及其制剂 5、改变国内已上市销售药品的剂型,但不改变给药途径的制剂 6、已有国家药品标准的原料药或者制剂
的反应,开始确定 其副作用。
Ⅱ期:对药品或治 疗的研究扩大到规 模较大的患者人群 (100-300人),取得 效果的初步证据, 对其安全性展开进 一步的评估。如果 获得效果证据并且 风险可以接受,则 进入下一阶段。
6、临床研究
Ⅲ期:在此阶段,将候 选药物扩大到大规模的 患者人群(1,000-3,000人 ),进一步测试其效果, 监测其副作用。在某些 情况下,如可行,将与 治疗标准进行对比。
中药新药研发流程图
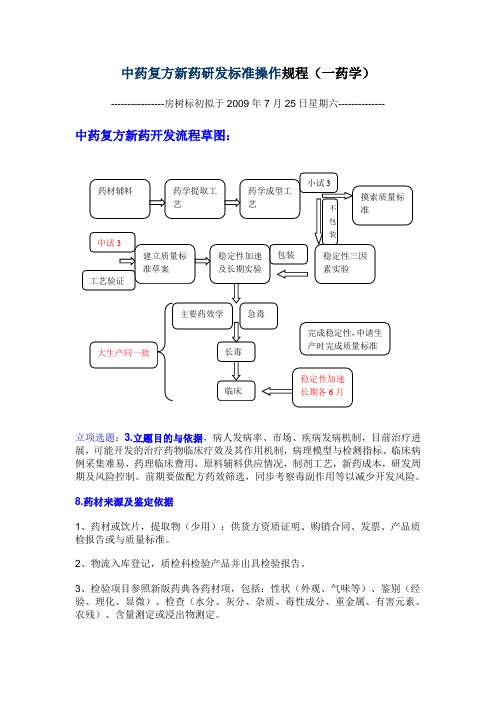
中药复方新药研发标准操作规程(一药学)----------------房树标初拟于2009年7月25日星期六--------------中药复方新药开发流程草图:立项选题:3.立题目的与依据,病人发病率、市场、疾病发病机制,目前治疗进展,可能开发的治疗药物临床疗效及其作用机制,病理模型与检测指标、临床病例采集难易,药理临床费用,原料辅料供应情况,制剂工艺,新药成本,研发周期及风险控制。
前期要做配方药效筛选,同步考察毒副作用等以减少开发风险。
8.药材来源及鉴定依据1、药材或饮片,提取物(少用):供货方资质证明、购销合同、发票、产品质检报告或与质量标准。
2、物流入库登记,质检科检验产品并出具检验报告。
3、检验项目参照新版药典各药材项,包括:性状(外观、气味等)、鉴别(经验、理化、显微)、检查(水分、灰分、杂质、毒性成分、重金属、有害元素、农残)、含量测定或浸出物测定。
9、10、11三项原料药材符合法定标准的可不提供。
12.生产工艺研究资料,工艺验证资料及文献资料,辅料来源及质量标准。
1.(12与13文献资料):文献检索包括复方中各位药材的成分、理化性质、含量测定方法、药理、药代、临床,新药制剂工艺等全面信息,为以后的药学工艺、质量标准的制定,药理模型的建立、临床方案的设计奠定科研基础。
2.辅料来源及质量标准:供货方资质证明、购销合同、发票、产品质检报告与质量标准。
物流入库登记,质检检验产品并出具检验报告。
检验项目参照新版药典各辅料项。
3.生产工艺研究资料,工艺验证资料:购进原料后,现通过实验室摸索(正交设计等摸索提取及制剂工艺)再通过实验室小试建立工艺。
注意:工艺指标选择要有意义(有效成分或指标成分),小试工艺参数最好是个范围,以便于生产条件的实现,同时也要有一个最佳工艺参数。
如提取工艺参数:溶剂量,时间、温度;直接浓缩至一定密度的浸膏,考察出膏量及有效成分含量。
可进一步考察浓缩参数:温度、压力、时间;指标可选膏的浓度。
新药研发流程 PPT .ppt

很多动物实验
三、新药研究申请 (Investigational New Drug Application, IND)
新药研发流程
药物从最初的实验室研究到最终摆 放到药柜销售平均需要花费12年的 时间。进行临床前试验的5000种 化合物中只有5种能进入到后续的 临床试验,而仅其中的1种化合物 可以得到最终的上市批准。总的来 说新药的研发分为两个阶段:研究 和开发。这两个阶段是相继发生有 互相联系的。区分两个阶段的标志 是候选药物的确定,即在确定候选 药物之前为研究阶段,确定之后的 工作为开发阶段。所谓候选药物是 指拟进行系统的临床前试验并进入 临床研究的活性化合物。
提取 长春花——长春碱,长春新碱 太平洋红豆杉树——紫杉醇 动物——胰岛素、激素、天花疫苗 有机 分子设计——合成——体外活性 合成 筛选——特异性疾病动物模型筛
选
分改 造子
头孢菌素——从第一代发展到第四代其 抗菌范围和抗菌活性不断增强和扩大
临床前研究
化学或生物实体的工艺研发及产品制备
开发出符合新药申报要求的化合物实体制备工艺研发,并按照该工的 发现。所谓先导化合物 (leading compound),也称新 化学实体(new chemical entity, NCE),是指通过各种途径和方法 得到的具有某种生物活性或药理活 性的化合物。
进活先 以性导 及物化 药质合 物的物 合挖主 成掘要 心、有 中现如 间有下 体药几 的物个 筛不来 选良源 等作: 。用对 的天 改然
新药从研发到上市需经过哪些流程?

新药从研发到上市需经过哪些流程?10 年时间,花费10亿美元,研发一款新药,无论是利益的驱动,还是拯救万千患者的成就感,药企的这一行为都值得我们尊敬。
一款新药从研发到上市都需要经过哪些流程?每一步又有哪些经验可以借鉴?本文以小分子药物为例,试着做了一个梳理,希望能对你有所帮助。
一、临床前研究1、研究开发(一般2-3年)实验室研究,寻找治疗特定疾病的具有潜力的新化合物(1)药物靶点的发现及确认这是所有工作的起点,只有确定了靶点,后续所有的工作才有展开的依据。
(2)化合物的筛选与合成根据靶点的空间结构,从虚拟化合物库中筛选一系列可匹配的分子结构,合成这些化合物,它们被称为先导化合物。
(3)活性化合物的验证与优化不是所有先导化合物都能符合要求,在这个阶段需要通过体外细胞试验验证,初步筛选出活性高、毒性低的化合物,并根据构效关系进行结构优化,这些化合物称为药物候选物。
同时也存在一个化合物对目标A 靶点没有作用,却有可能对其他的B 靶点、C 靶点有非常好活性的情况,暂且不表。
2、临床前实验(一般2-4年)这一阶段目的,一是评估药物的药理和毒理作用,药物的吸收、分布、代谢和排泄情况(ADME)。
二是进行生产工艺、质量控制、稳定性等研究(CMC)。
第一部分的实验需要在动物层面展开,细胞实验的结果和活体动物实验的结果有时候会有很大的差异。
这一步的目的是确定药物的有效性与安全性。
第二部分需要在符合GMP要求的车间完成。
(1)药理学研究包括:药效学、药动学(2)毒理学研究急毒、长毒、生殖毒性,致癌、致畸、致突变情况(3)制剂的开发总不能弄点化合物就直接往嘴里倒吧,制剂开发是药物应用的一个重要环节。
比如有的药口服吸收很差,就需要开发为注射剂。
有的药在胃酸里面会失去活性,就需要开发为肠溶制剂。
有的化合物溶解性不好,这也可以通过制剂来部分解决这个问题。
还有的需要局部给药,就需要通过制剂开发成雾化剂、膏剂等。
二、临床试验审批 Investigational New Drug(IND)三、临床试验(一般3-7年)人体试验共分三期:•Ⅰ期临床20-100例,正常人,主要进行安全性评价。
中药新药研发流程ppt课件

中药新药研发流程
9
2 正式临床前实验阶段
药效学、毒理学实验
中药新药研发流程
10
2 正式临床前实验阶段
药效学、毒理学实验
主要药效学研究及文献资料生产工艺的研究 毒理学试验:急性毒性实验 长期毒性试验
中药新药研发流程
11
3 研究资料整理与申报阶段
资料整理
蓝韵研发部资料详细整理:
药物名称 证明性资料 立题依据与目的 主要研究成果的总结与评价 药学研究资料综述 药理毒理研究资料综述 临床试验资料 临床试验方案 临床研究者手册 药品注册申请-境内申请人用表
如对一些方案有异议或无法把握,进一步咨询国家食品药品监督管理局审评中心相关专家,如药 理毒理咨询朱飞鹏博士、临床及功能主治等咨询张磊博士。
中药新药研发流程
6
1 准备及预实验阶段
立项后基础实验
蓝韵实验中心按初步工艺进行摸索,工艺标准等初步试验, 提取部分样品进行临床试验,确定组方临床疗效。
中药新药研发流程
中药新药研发流程
13
THANKS
中药新药研发流程
14
期待您的关注,下载文档可以自由编辑!
中药新药临床前研究流程
中药新药研发流程
1
中药新药临床前研究的阶段性工作
1
准备及预实验阶段
2
正式临床前实验阶段
3
研究资料整理与申报阶段
中药新药研发流程
2
1 准备及预实验阶段
适应症确定
是否适应中医中药的优势和特点? 是否是现代医学难以解决的疾病? 同类品种情况如何? 疾病发病情况如何? 市场需求如何? 现代医学疾病适应症确定 与现代疾病适应症对应的中医功能主治的确定
研发部
创新药从研发到上市流程教材课件(PPT82页)

这个阶段也称为靶标发现和靶标选择。 常用的方法是以靶标为基础或以生理为基础
靶标可以是单个基因、蛋白质或与许多不同疾病相关的蛋白质相互作 用的通路。科学家通过各种方法来分离和识别特定的靶标,从而更好 地理解靶标的功能以及与疾病之间的关系。然后设计或分离出与靶标 相互作用的化合物。人类基因组测序是基于靶标方法的主要驱动力。 用细胞测试和动物模型观察与疾病有关的生理反应,如血液测试或心 脏功能。化合物的测试和评价也是基于这些生理反应。如果化合物能 够影响或改变生理反应,则继续研究下去。靶标和作用机制的鉴别会 在先导化合物(lead compound)研究到一定阶段后再进行。
5 Compounds 5 个化合物
100 – 500名 志愿者
6年
1,000 – 5,000 名志愿者
1 个FDA 审批药
物
2年
2年
$323.5MM
$414.7MM
$858.8MM
$120.6MM
*PhRMA 2003研发费用;根据34名成员数据得出的平均值;不包括IV费用和“非分类”费用 ( $MM )
—Science Translational Medicine 5 (171)
新药研发不同阶段成功的机率
基础研究 或药物发 现前研究
发现
100%
临床前
临床I期
临床II期
临床III期
FDA 批准 上市
7%
<1%
药物发现前研究(Pre-discovery)
➢疾病的选择和认识
(Understanding the disease)
➢生物靶标的识别
(Target identification)
新药研发的流程优选演示

用辅料的胶囊剂。II期临床试验的处方通常含少量有药用辅料。在II期临 床试验期间,最终的剂型被选择和开发作III期临床使用并代表了提交 FDA上市申请的处方。
3、新药研究申请 (Investigational New Drug
生物学特性——毒理学2
致癌性研究——当一个化合物具有足够的前景 进入人体临床试验时才进行。 生殖研究——包括:抚养和交配行为、胚胎早 期、早产和产后发育、多代影响和致畸性。 基因毒性或诱导研究——测定试验化合物是否 引起基因突变或引起微粒体或DNA的损伤。
2.3 处方前研究
物化性质 溶解度 分配系数 溶解速率 物理形态 稳定性
有机合成
分子设计 合成 物模型筛选
体外活性筛选
分子改造
特异性疾病动
头孢菌素:从第一代发展到第四代,其抗菌范围和抗菌活性 也不断扩大和增强。
2、临床前研究
2.1 化学合成 提供足够量的化合物(药物)作为临床前试验、临床研究、小
规模和大规模制剂制备,每一步必须进行质量控制和验证。 2.2 生物学特性
药理学 药物代谢 毒理学 2.3 处方前研究 物化性质 最初的处方设计
Application, IND)
递交申请(临床研究方案)
FDA审核
4、临床试验
临床试验的分期
病例数为主
成功完成比 例(%)
45
II期临床 III期临床
几百 几百~几千
几个月到2年 1~4年
某些短期安全性,主 要是有效性
安全性、有效性和剂 量
30 5~10
生物学特性——毒理学1
急性毒性研究——单剂量和/或多剂量短期给药。给药剂 量向一定范围增加,以确定试验化合物不产生毒性的最 大剂量、发生严重毒性的剂量水平及中等毒性剂量水平。 亚急性或亚慢性毒性研究——最少为2个星期给药、3个 或更多剂量水平和2个物种。 慢性毒性研究——用于人体一周或以上的药物,必须要 有90~180天的动物试验表明其安全性;若是用于慢性疾 病治疗,必须进行一年或更长的动物试验。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
新药研究开发与上市流程图
人们生活水平提高要求更多更好的新药,药物科学的发展为新药开发提供了理论基础和技术,市场经济竞争也促进了新药快速发展。
美国食品与药物管理局(FDA)近十年来每年批准上市的新药都在20种以上。
我国近年来引进新药品种很多,但需要加快创新。
新药开发是一个非常严格而复杂的过程,各药虽然不尽相同,药理研究却是必不可少的关键步骤。
临床有效的药物都具有相应的药理效应,但具有肯定药理效应的药物却不一定都是临床有效的药物。
例如抗高血压药都能降低血压,但降压药并不都是抗高血压药,更不一定是能减少并发症、延长寿命的好药。
因此新药开发研究必需有一个逐步选择与淘汰的过程。
为了确保药物对病人的疗效和安全,新药开发不仅需要可靠的科学实验结果,各国还对新药生产上市的审批与管理制定了法规,对人民健康及工商业经济权益予以法律保障。
新药来源包括天然产物、半合成及全合成化学物质。
过去选药主要方法是依靠实践经验,现在可以根据有效药物的植物分类学找寻近亲品种进行筛选或从有效药物化学结构与药理活性关系推断,定向合成系列产品,然后进行药理筛选。
近年来对于机体内在抗病物质(蛋白成分)利用DNA基因重组技术,即将DNA 的特异基因区段分离并植入能够迅速生长的细菌或酵母细胞,以获得大量所需蛋白药物。
此外,还可对现有药物进行化学结构改造(半合成)或改变剂型,也可获得疗效更好,毒性更小或应用更方便的药物。
医学教育网搜集整理新药研究过程大致可分三步,即临床前研究、临床研究和售后调研。
临床前研究包括用动物进行的系统药理研究及急慢性毒性观察。
对于具有选择性药理效应的药物,在进行临床试验前还需要测定该药物在动物体内的吸收、分布及消除消除过程。
临床前研究是要弄清新药的作用谱及可能发生的毒性反应。
在经过药物管理部门的初步审批后才能进行临床试验。
目的在于保证用药安全。
临床研究首先在10~30例正常成年志愿者观察新药耐受性,找出安全剂量。
再选择有特异指征的病人按随机分组、设立已知有效药物及空白安慰剂双重对照(对急重病人不得采用有损病人健康的空白对照),并尽量采用双盲法(病人及医护人员均不能分辨治疗药品或对照药品)观察,然后进行治疗结果统计分析,客观地判断疗效。
与其同时还需进行血药浓度监测计算药动学数据。
受试病例数一般不应少于300例,先在一个医院以后可扩大至三个以上医疗单位进行多中心合作研究。
对那些需要长期用药的新药,应有50~100例病人累积用药半年至一年的观察记录。
由此制定适应证、禁忌证、剂量疗程及说明可能发生的不良反应后,再经过药政部门的审批才能生产上市。
售后调研是指新药问市后进行的社会性考查与评价,在广泛的推广应用中重点了解长期使用后出现的不良反应和远期疗效(包括无效病例)。
药物只能依靠广大用药者(医生及病人)才能作出正确的历史性评价。
一种药物从最初的实验室研究到最终摆放到药柜销售平均需要花费12年的时间。
进行临床前试验的5000种化合物中只有5种能进入到后续的临床试验,
这份报告真实再现了药物的发明和发展进程。
美国的新药批准体系也许是世界上最严格的体系。
根据国会的技术评估部在1993年2月所作的报告来看,一种药物从实验室到上柜销售平均将花去公司3.59亿美元。
这份流程图和这篇文章给出了药物研发的成功率以及每个步骤所花费的时间。
总体来看,每5种进入临床的药物中只有1种能进行所有的试验和批准过程。
新药开发阶段如下:
临床前试验:由制药公司进行的实验室和动物研究,以观察化合物针对目标疾病的生物活性,同时对化合物进行安全性评估。
这些试验大概需要3.5年的时间。
研发中新药申请(Investigational New Application, IND):在临床前试验完成后,公司要向FDA提请一份IND,之后才能开始进行药物的人体试验。
如果30天内FDA没有发出不予批准的申明,此IND即为有效。
提出的IND需包括以下内容:先期的试验结果,后续研究的方式、地点以及研究对象;化合物的化学结构;在体内的作用机制;动物研究中发现的任何毒副作用以及化合物的生产工艺。
另外,IND必须得到制度审核部门(the Institutional Review Board)的审核和批准。
同时,后续的临床研究需至少每年向FDA提交一份进展报告并得到准许。
临床试验,Ⅰ期:此阶段大概需要1年时间,由20~80例正常健康志愿者参加。
这些试验研究了药物的安全性方面,包括安全剂量范围。
此阶段的研究同时确定了药物在体内的吸收、分布、代谢和排泄、以及药物的作用持续时间等项目。
临床试验,Ⅱ期:此阶段需要约100到300名志愿患者参与进行一些控制研究,以评价药物的疗效。
这个阶段大约需要2年时间。
临床研究,Ⅲ期:此阶段持续约3年时间,通常需要诊所和医院的1000~300名患者参与。
医师通过对病患的监测以确定疗效和不良反应。
新药申请(New Drug Application, NDA):通过三个阶段的临床试验,公司将分析所有的试验数据。
如果数据能够成功证明药物的安全性和有效性,公司将向FDA提出新药申请。
新药申请必须包括公司所掌握的一切相关科学信息。
典型的新药申请有10万页甚至更多。
根据法律,FDA审核一份NDA的时限应该为6个月。
但是几乎所有案例中的新药申请从首次提交到最终获得FDA批准的过程都超过了这个时限;在1992年对于新分子实体的新药申请平均审核时间为29.9个月。
批准:一旦FDA批准了一份新药申请,此种新药就可以被医师用于处方。
公司必须继续向FDA提交阶段性报告,包括所有的不良反应报告和一些质量控制记录。
FDA还可能对一些药物要求做进一步的研究(Ⅳ期),以评价药物的长期疗效。
发明和研究安全有效的新药是一个长期、艰难和昂贵的进程。
今年,以研究为基础的制药公司将在研发方面投资126亿美元,这种投资将每五年翻一倍。
开发流程:大致如下
专业范本可能没有涵盖全面,最好找专业人士审核后使用,感谢您的下载!。
