化学无机物思维导图
高一化学思维导图归纳总结

高一化学思维导图归纳总结化学作为一门自然科学,研究了物质的组成、性质、结构、转化以及与能量的关系。
在高中化学的学习中,形成思维导图可以帮助学生将知识点归纳总结,并提高对知识点之间的联系和脉络的把握。
本文将从无机化学、有机化学和化学实验三个方面,对高一化学的思维导图归纳总结进行探讨。
一、无机化学思维导图归纳总结1. 元素的分类思维导图中可以将元素分为金属、非金属和过渡金属三大类,然后再进一步归纳每一类元素的特性和周期表中的排列规律。
2. 化学键的形成化学键的形成包括离子键、共价键和金属键。
我们可以用思维导图将这三种化学键的特点、形成过程以及应用进行总结。
3. 化学反应化学反应可以分为氧化还原反应、酸碱中和反应、置换反应、分解反应等。
可以用思维导图将每种反应的条件、实例以及反应方程式归纳总结起来。
4. 高一无机化学实验总结通过实验,我们可以更好地理解无机化学的知识点。
思维导图可以帮助我们将实验的目的、步骤、结果以及实验操作技巧进行归纳总结。
二、有机化学思维导图归纳总结1. 有机化合物的命名有机化合物的命名包括根据官能团进行命名、以及根据碳链进行命名等。
思维导图可以将不同的命名规则、常见的官能团和碳链进行整理和总结。
2. 有机化合物的反应有机化合物的反应种类繁多,可以归纳总结为取代反应、加成反应、消除反应等。
思维导图可以将每种反应的条件、实例以及反应机理进行细致的归纳总结。
3. 高一有机化学实验总结有机化学实验可以加深对有机化合物的理解,帮助学生掌握有机化学的基本操作技巧。
思维导图可以将实验的目的、步骤、结果以及实验注意事项进行总结归纳。
三、化学实验思维导图归纳总结1. 化学实验常用仪器和玻璃器皿思维导图可以将实验中常用的仪器和玻璃器皿进行分类和整理,包括容量瓶、烧杯、试管、滴定管等,并记录其使用方法和注意事项。
2. 化学实验中的操作技巧化学实验过程中常用的操作技巧包括称量、加热、过滤、取样等。
思维导图可以将每种操作技巧的步骤和注意事项进行清晰的归纳总结。
普通无机化学

这本书也让我对未来的化学研究充满了期待。作者们在书中展示了无机化学 的巨大潜力,以及未来可能的发展方向。这让我看到了化学的无限可能性,也激 发了我对未来的探索欲望。
《普通无机化学》这本书是一本非常值得一读的书。它既是一本教科书,也 是一本科学探索的导引。通过阅读这本书,我不仅学到了很多无机化学的知识, 更重要的是,我收获了对化学的热爱和对未来的期待。我相信,这本书对我未来 的学习和工作都会产生深远的影响。
这本书的写作风格非常清晰易懂。虽然其中涉及到的化学概念和理论不少, 但作者们都用简洁明了的语言进行解释,没有过多的专业术语,使得我可以轻松 理解并掌握这些知识。这让我更加确信,无论我在什么领域工作,化学都是我必 须掌握的重要工具。
再者,通过阅读这本书,我深深地感受到了化学的无处不在。从日常生活中 的各种材料和能源,到高科技中的关键技术,化学都发挥着不可或缺的作用。这 让我更加明白,化学是一门对人类社会有着重大影响的科学,我能够参与其中, 是一种莫大的荣幸。
目录分析
《普通无机化学》是一本广泛被全球化学专业学生使用的教材,它涵盖了无 机化学的各个主要领域,从基础知识到高级应用,为读者提供了一个全面的学习 路径。以下是对这本书目录的深入分析。
这本书的目录结构清晰,层次分明,便于学生和理解。全书共分为十章,以 无机化学的基础理论为第一章,全面介绍了无机化学的基本概念和原理,如原子 结构、分子结构、化学键、化学反应动力学等。这些内容对于理解后续章节的内 容起到了重要的铺垫作用。
第二章到第九章,本书转向了各个具体的无机化学领域,包括氧化还原反应、 电化学、配位化学、主族元素化学、副族元素化学、金属有机化学和非金属元素 化学等。这些章节的内容不仅详细介绍了各个领域的核心概念和原理,而且列举 了大量的实例和应用,帮助学生理解和应用这些知识。
九年级化学知识点归纳 思维导图

九年级化学知识点归纳思维导图化学作为一门自然科学,研究的是物质的组成、性质以及它们之间的变化。
在九年级学习化学的过程中,我们接触到了许多重要的知识点。
为了更好地理解和记忆这些知识,我们可以使用思维导图的方法整理归纳,将复杂的概念和关系以图形化的方式呈现,提升学习效果。
以下是九年级化学知识点的思维导图。
1. 物质的分类- 纯物质和混合物- 纯物质:由同一种组分构成,具有一定的固定化学组成和独特的性质。
分为元素和化合物。
- 元素:由相同类型的原子组成,不能分解为其他物质。
- 化合物:由两种以上不同类型的原子按照一定比例结合而成,可以分解为其他物质。
- 混合物:由两种或两种以上的物质按照一定比例混合而成,可以根据混合的均匀程度分为均质混合物和非均质混合物。
2. 常见物质的性质和变化- 物质的性质:可以分为物理性质和化学性质。
- 物理性质:物质在不改变化学组成的情况下表现出来的性质,如颜色、硬度、熔点、沸点等。
- 化学性质:物质在发生化学反应时表现出来的性质,如燃烧性、氧化性等。
- 物质的变化:可以分为物理变化和化学变化。
- 物理变化:物质在不改变化学组成的情况下改变外观或状态的变化,如溶解、凝固、融化等。
- 化学变化:物质在与其他物质发生反应时改变化学组成和性质的变化,如燃烧、酸碱中和等。
3. 原子和分子- 原子:是物质的基本粒子,由质子、中子和电子组成。
- 质子:带有正电荷的基本粒子,质量约为1个原子质量单位。
- 中子:不带电荷的基本粒子,质量约为1个原子质量单位。
- 电子:带有负电荷的基本粒子,质量很轻,约为1/1836个原子质量单位。
- 分子:是原子的组合形式,是能保持化学性质的最小粒子。
4. 元素周期表- 元素周期表:是按照原子序数的大小和元素性质进行排列的表格。
元素周期表按照一定的规律分为周期和族。
- 周期:是指元素周期表中横向的行,代表了元素的原子轨道。
周期越往下,电子层越多。
- 族:是指元素周期表中纵向的列,代表了元素的化学性质。
高中化学基础知识网络图完整版

高中化学基础知识网络图完整版Revised on November 25, 2020高中化学识网络图第一部分:物质的组成、分类、性质和变化第二部分:基本理论(物质结构、化学反应速率、化学平衡、电解质溶液)和化学平衡第三部分:元素化合物转化关系有机抓住官能团的性质烃烃的衍生物糖蛋白质:多肽、氨基酸(官能团:—NH 2和—COOH )高分子化合物链烃(脂肪烃)环烃饱和链烃 烷烃:C n H 2n+2(n ≥1)R —CH 3 不饱和链烃 烯烃:C n H 2n (n ≥2) R —CH=CH 2二烯烃:C n H 2n-2(n ≥4)R —CH=CH —CH=CH 2 炔烃:C n H 2n-2(n ≥2) R —C ≡CH环烷烃C n H 2n (n ≥3)芳香烃(苯和苯的同系物)C n H 2n-6(n ≥6)天然高分子:橡胶(聚异戊二烯)、多糖、蛋白质R卤代烃(官能团:—X ):饱和一卤代烃C n H 2n+1X(n ≥1)R —X 醇 (官能团:—OH ):饱和一元醇C n H 2n+1OH(n ≥1)R —OH 醚 C n H 2n+2O (n ≥2)R —O —R 酚(苯酚)(官能团:—OH )C n H 2n-6O (n ≥2)OH羧酸 (官能团:—COOH ):饱和一元羧酸 C n H 2n+1O 2 (n ≥1)R —COOH醛 (官能团:—CHO )C n H 2n O (n ≥1)R —CHO 酮 (官能团:—CO —)C n H 2n O (n ≥3)R —CO —R ’酯 (官能团:—COO —R ):饱和一元羧酸和饱和一元醇形成的酯 C n H 2n O 2 (n ≥2)R —COOR ’ 硝基化合物(官能团—NO 2)R —NO 2 胺(官能团—NH 2)R —NH 2单糖:葡萄糖、果糖C 6H 12O 6(互为同分异构)二糖:蔗糖、麦芽糖C 12H 22O 11(互为同分异构) 多糖:淀粉、纤维素(C 6H 12O 6)n (n 值不同)合成高分子合成塑料 合成橡胶 合成纤维有机化合物。
高一化学必修一思维导图,全册知识点分享

高一化学必修一思维导图,全册知识点分享发布时间: 2022-9-20 | 标签:化学必修一思维导图高一化学必修一思维导图高中化学必修一应该如何画好高一化学必修一思维导图呢?刚刚进入高一的同学们,面对难度倍增的化学知识可真是头大。
高中化学确实不简单,因此知犀为大家整理了一份高一化学必修一思维导图,同学们可以借助导图,从宏观上理清必修一整本书的脉络结构以及一些重难点知识。
知识点再多再杂,也能完全理顺!现在就一起来看一下高一化学必修一思维导图吧~高一化学必修一思维导图(1)大纲高一化学必修书共分六章。
分别是:第一章关于实验化学,第二章关于化学物质及其变化,第三章关于金属及其化合物,第四章关于非金属及其化合物。
高一化学必修一思维导图(2)第一章:从实验学化学第一章是化学实验的入门知识。
学生应了解常用仪器的识别和使用,掌握基本的实验操作,防止实验事故的发生。
高一化学必修一思维导图(3)第二章:物质的分类本节要求学生简单地根据物质的成分进行分类,并掌握常用的分类方法。
高一化学必修一思维导图(4)第二章:离子反应本节内容主要是掌握离子方程式的书写。
高一化学必修一思维导图(5)第二章:氧化还原反应本节要求掌握氧化还原反应的概念,从化学价态变化的分类标准理解氧化还原反应的特点。
高一化学必修一思维导图(6)第三章:金属的化学性质在这一节中,首先给出金属的简要概述,其次已知钠和铝与氧的反应,最后了解金属与酸和水的反应。
高一化学必修一思维导图(7)第三章:钠及其化合物这部分的内容是重点内容。
学生需要认识到钠是一种典型的活性金属元素,从钠的物理性质、化学性质、化合物及相关计算等方面综合控制钠。
高一化学必修一思维导图(8)第三章:铝及其化合物学习铝也是从它的物理性质,化学性质,化合物以及相关的计算。
高一化学必修一思维导图(9)第三章:铁及其化合物学习铁,首先需要对铁的物理化学性质有一个初步的了解,其次是了解铁的氧化物和氢氧化物,最后通过实验学会区分铁盐和盐铁盐。
化学必修一思维导图

化学必修一思维导图一、物质及其变化1. 物质的结构原子结构:由原子核和核外电子组成,原子核由质子和中子组成。
分子结构:由原子通过化学键连接而成。
晶体结构:由原子、分子或离子按照一定的规律排列而成。
2. 物质的分类纯净物:由同种元素或化合物组成,具有固定的组成和性质。
3. 物质的性质物理性质:不涉及物质组成和结构变化的性质,如颜色、状态、密度等。
化学性质:涉及物质组成和结构变化的性质,如可燃性、氧化性等。
二、化学键与化学反应1. 化学键离子键:由正负离子之间的静电作用力形成。
共价键:由原子间共享电子对形成。
金属键:由金属原子间的自由电子云形成。
2. 化学反应化学反应类型:合成反应、分解反应、置换反应、复分解反应等。
化学反应条件:温度、压力、催化剂等。
化学反应速率:反应物浓度、温度、催化剂等。
三、元素周期表1. 元素周期律元素周期表按照原子序数排列,具有周期性变化的规律。
元素周期表中,同一周期的元素具有相似的化学性质,同一族的元素具有相似的物理性质。
2. 元素周期表的应用元素周期表可以用于预测元素的化学性质和物理性质。
元素周期表可以用于解释元素的电子结构和化学键的形成。
四、化学计量学1. 物质的量物质的量:表示物质中含有的基本粒子数,单位为摩尔。
摩尔质量:表示1摩尔物质的质量,单位为克/摩尔。
2. 化学反应的计量关系化学方程式:表示化学反应的物质及其量的关系。
化学方程式的平衡:反应物和物的物质的量保持一定的比例。
3. 化学反应的热力学焓变:表示化学反应中能量的变化,单位为焦耳。
反应热:表示化学反应中吸收或释放的热量,单位为焦耳。
五、溶液与胶体1. 溶液溶液的定义:由溶质和溶剂组成的均匀混合物。
溶液的浓度:表示溶液中溶质的含量,单位为摩尔/升。
2. 胶体胶体的定义:由分散相和分散介质组成的混合物,分散相粒子的大小介于分子和宏观粒子之间。
胶体的性质:具有丁达尔效应、布朗运动等特性。
六、酸碱反应1. 酸碱理论酸碱质子理论:酸是质子(H+)的供体,碱是质子的受体。
九年级全册化学总复习思维导图
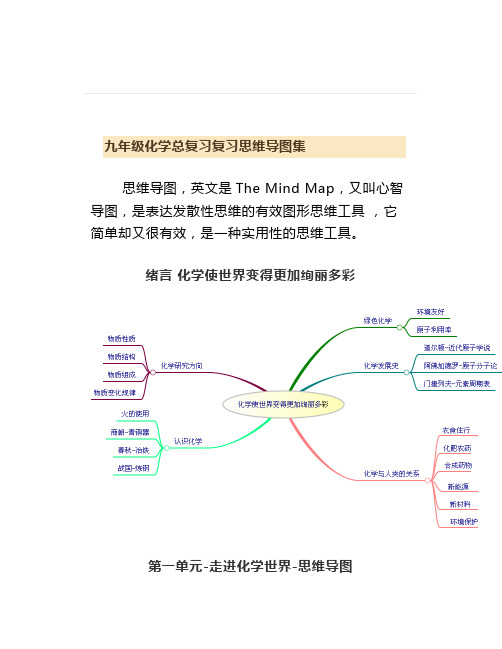
九年级化学总复习复习思维导图集思维导图,英文是The Mind Map,又叫心智导图,是表达发散性思维的有效图形思维工具,它简单却又很有效,是一种实用性的思维工具。
绪言化学使世界变得更加绚丽多彩第一单元-走进化学世界-思维导图第二单元-我们周围的空气-思维导图思维导图运用图文并重的技巧,把各级主题的关系用相互隶属与相关的层级图表现出来,把主题关键词与图像、颜色等建立记忆链接。
思维导图充分运用左右脑的机能,利用记忆、阅读、思维的规律,协助人们在科学与艺术、逻辑与想象之间平衡发展,从而开启人类大脑的无限潜能。
思维导图因此具有人类思维的强大功能。
第三单元-物质构成的奥秘-思维导图第四单元-自然界的水-思维导图第五单元-化学方程式-思维导图思维导图是一种将思维形象化的方法。
我们知道放射性思考是人类大脑的自然思考方式,每一种进入大脑的资料,不论是感觉、记忆或是想法——包括文字、数字、符码、香气、食物、线条、颜色、意象、节奏、音符等,都可以成为一个思考中心,并由此中心向外发散出成千上万的关节点,每一个关节点代表与中心主题的一个连结,而每一个连结又可以成为另一个中心主题,再向外发散出成千上万的关节点,呈现出放射性立体结构,而这些关节的连结可以视为您的记忆,就如同大脑中的神经元一样互相连接,也就是您的个人数据库。
第六单元-碳和碳的化合物-思维导图第七单元-燃料及其利用-思维导图第八单元-金属和金属材料-思维导图思维导图是有效的思维模式,应用于记忆、学习、思考等的思维“地图”,有利于人脑的扩散思维的展开。
思维导图已经在全球范围得到广泛应用,新加坡教育部将思维导图列为小学必修科目,大量的500强企业也在学习思维导图,中国应用思维导图也有20多年时间了。
第九单元-溶液-思维导图第十单元-酸和碱-思维导图第十一单元-盐化肥-思维导图自上世纪八十年代思维导图传入中国内地。
最初是用来帮助“学习困难学生”克服学习障碍的,但后来主要被工商界(特别是企业培训领域)用来提升个人及组织的学习效能及创新思维能力,在学科教学方面,历经52年的发展,也没在学校广泛应用,后经华东师大刘濯源带领的思维可视化研究团队十五年的研究及实践,得出的结论是“思维导图”并不适合直接应用于学科教学,因为“思维导图”过于强调“图像记忆”和“自由发散联想”而非“理解性记忆”和“结构化思考”。
高中生物第一册 2 2 细胞中的无机物 课件 (思维导图)

在
形
式
•自由水 •结合水
•定义 •绝大部分的水呈游离状态,可以自由流动 生
物
•特点 •可流动、易蒸发、易散失
体
•1.是细胞内的良好溶剂
的 一
•2.参与细胞内的生化反应
切
•功能 •3.运输营养和代谢废物
生 命
•4.为细胞提供液体生活环境
活
•定义 •与细胞内其他化合物相结合的水
动 都
离
•特点 •不流动、不易散失、含量较稳定
含量较多的阳离子: Na+、K+、 Ca2+、Mg2+、Fe2+、Fe3+等。 含量较多的阴离子: Cl-、SO42-、PO43-、HCO3-等。
思考&讨论
资料2 植物在缺乏N、P、K等营养物质时会 出现各种症状,因此生产过程中常要给植物 施肥。玉米在生长过程中缺乏P,植株就
资料1 下图是一种叶绿素分子 和血红素分子局部结构简图。
影响生物组织细胞的代谢速率。 自由水/结合水比值高,代谢快
自由水/结合水比值低,代谢慢 •抗逆性高
观察一下,你有什么发现?
将种子放在 阳光下2天
重量 减轻
自由水大 量散失
晒干的种子 用水浸泡
仍能 萌发
失去大部分自由 水的种子仍保持 其生理活性
晒干的种 子不浸泡
不萌发
自由水少,代谢弱
将种子放在酒精 灯中用试管加热
不同生物的含水量不同
藻类90%
水母97%
鱼类80-85%
蛙类78%
高等植物60-80%
哺乳动物65%
同一生物在不同的生长发育时期含水量不同
幼儿和成人体内的含水量
幼儿>成人>老年 男性>女性
