ChP 2020年版变化
《中国药典》2020年版第四部通用技术要求主要特点和增修订内容

《中国药典》2020年版第四部通⽤技术要求主要特点和增修订内容主要特点和增修订内容2.1制剂通则论述框架和技术要求进⼀步完善2.1.1系统修订制剂通则整体框架0100制剂通则旨在通过对药物制剂的总体论述来指导医药⼯作者对不同剂型、亚剂型进⾏合理的应⽤。
《中国药典》2015年版制剂通则是《中国药典》2010年版中药、化学药和⽣物制品制剂通则的简单整合,缺少关键考察项的汇总和归纳。
为进⼀步引导⽣产企业全⾯关注制剂⽣产质量控制和整体要求,对0100制剂通则进⾏修订,主要修改包括两个⽅⾯:⾸先完善了叙述结构。
从药物制剂制备的原则“安全、有效、可控、依从性”的⾓度出发,增加对剂量单位均匀性、稳定性、安全性与有效性、剂型与给药途径、包装与贮藏和标签与说明书等部分的分论述;强调中药制剂在整个⽣产过程中的关键质量属性,关注每个关键环节的量值传递规律。
其次,完善了具体内容。
提出剂量单位均匀性的要求,保障制剂⽣产质量的批间和批内药物含量等的⼀致性,体现制剂全过程控制的理念;在稳定性中提出复检期概念,促进⽣产企业根据产品⾃⾝的稳定性特性进⾏前瞻性的质量考察;在安全性与有效性中提出“通过⼈体临床试验证明药物的安全有效性后,药物才能最终获得上市与临床应⽤”,提⽰上市制剂的处⽅和⼯艺不得随意变更。
2.1.2系统修订各制剂通则的框架和表述《中国药典》2020年版制剂通则统⼀了各剂型论述框架及主要制备技术的简单论述。
除0110糊剂及0186膏剂外,其他36个剂型均不同程度修订了体例格式。
为进⼀步统⼀⽬前各剂型的表述问题,规范统⼀“⽣产与贮藏期间应符合下列规定”项下内容,按照原辅料→⼯艺与技术→质量与控制→包装与使⽤→贮存与运输等五⽅⾯的技术要点,着重补充⼤多数剂型缺少的⼯艺与技术⽅⾯的阐述。
增加特殊亚剂型临床使⽤关注点,如泡腾⽚不得直接吞服等,指导临床合理⽤药。
2.1.3收载和整合临床成熟剂型和亚剂型收载和整合临床成熟剂型和亚剂型,体现《中国药典》的先进性和对我国临床成熟新制剂技术的⽀持。
浅谈Incoterms2020的一些改进和建议

浅谈Incoterms2020的一些改进和建议Incoterms是指国际贸易术语通则(International Commercial Terms),是国际贸易中用于明确买卖双方在交货、付款以及运输方面的权利和义务的规则,由国际商会(ICC)制订和推广。
2020年的Incoterms中对一些条款进行了修改和调整,旨在更好地适应当前的国际贸易形势和市场需求。
第一,FCA条款的加强。
FCA条款在2020年的新版Incoterms中得到了加强,强调了交交货物的责任由卖方进行,使用FCA条款的买方不必再早些时间抵达卸货地点。
同时,新版FCA还加强了对承运人的要求,明确了卖方有责任安排运输,但不要求其为承运人操作。
第二,CIP和CIF条款的细化。
CIP和CIF条款是指卖方有责任负担货物运往目的地港口以及购买保险。
2020年版本的Incoterms中,在CIP和CIF条款中,卖方需要购买适当的保险,以保证货物在运输过程中不受损失。
此外,CIP和CIF条款还强调了卖方应当在货物到达目的地之前向买方提供一些必要的文件,比如承运单据等。
第三,DAT和DAP条款的改进。
DAT和DAP条款是指卖方有责任将货物运往目的地,并担负清关手续的义务。
2020年版本的Incoterms中,DAT条款被修改为DPU条款,卖方需要在目的地货场交货,而不是仅在港口交货。
DAP条款也得到了修改,强调了卖方有责任将货物送到购买方方便交货的地点,而不是仅在目的地港口交货。
综上所述,无论是针对人员竞争力还是国际贸易的市场竞争力,经过这次的改进,2020年版的Incoterms已经更好地适应当代商业需要。
此外,在实际运用中,大家也需要注意各种条款之间的区别和细节,避免引发不必要的纠纷。
GMP规范新版2020版与2002版区别
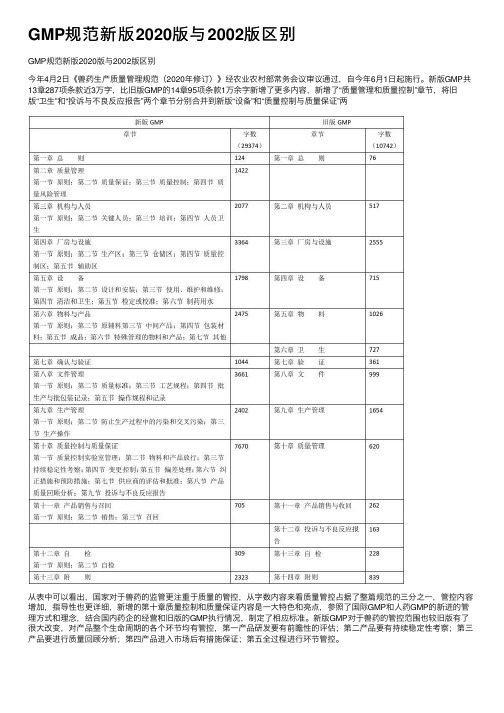
GMP规范新版2020版与2002版区别GMP规范新版2020版与2002版区别今年4⽉2⽇《兽药⽣产质量管理规范(2020年修订)》经农业农村部常务会议审议通过,⾃今年6⽉1⽇起施⾏。
新版GMP共13章287项条款近3万字,⽐旧版GMP的14章95项条款1万余字新增了更多内容,新增了“质量管理和质量控制”章节,将旧版“卫⽣”和“投诉与不良反应报告”两个章节分别合并到新版“设备”和“质量控制与质量保证”两从表中可以看出,国家对于兽药的监管更注重于质量的管控,从字数内容来看质量管控占据了整篇规范的三分之⼀,管控内容增加,指导性也更详细,新增的第⼗章质量控制和质量保证内容是⼀⼤特⾊和亮点,参照了国际GMP和⼈药GMP的新进的管理⽅式和理念,结合国内药企的经营和旧版的GMP执⾏情况,制定了相应标准。
新版GMP对于兽药的管控范围也较旧版有了很⼤改变,对产品整个⽣命周期的各个环节均有管控,第⼀产品研发要有前瞻性的评估;第⼆产品要有持续稳定性考察;第三产品要进⾏质量回顾分析;第四产品进⼊市场后有措施保证;第五全过程进⾏环节管控。
2002年农业部第11号令的第⼀版规范实⾏,到2020年农业农村部的第3号令,历经18年时间中国兽药⽣产管理从⽆到有、从粗到细、从国内到国际的发展阶段,这18年是⼀座桥梁,连接着过去和未来,过去的粗放式管理和⽣产模式,关注的只是产品的有效性,仅处于国内局限性的兽药市场和国内养殖现状及思维模式。
从有兽药GMP规范的18中,国内兽药发展更注重了规范⽣产,保障了畜禽和⼈民群众的健康。
中国的兽药伴随中国国家快速发展的浪潮,也搭载着国家发展、开放、包容、共荣的巨轮向远⽅的梦想前⾏。
发展的浪潮起伏向前,⼀刻不停,药品安全、⽣物安全、⾷品安全时时刻刻在影响着畜禽健康和百姓的健康,⼈们和社会物质和精神⽂明的进步,对于安全和健康有了更⼤的需求。
兽药从最根本上影响着的⾁蛋奶安全,影响着百姓“菜篮⼦”的绿⾊和安全。
2020年CTPAT及SCAN反恐安全标准新版变化和标准要求培训教材

CONTENTS主要内容
1 CTPAT背景介绍 2 CTPAT最低安全要求的框架结构变化 3 各章节主要变化和要点解析 4 CTPAT 审核服务介绍
最新安全要求(MSC)框架结构变 化
关注区域
Corporate Security
Transportation Security
People and Physical Security
美国海关的真实案 例
在这个伪装的墙面后面是6939磅大麻
真实案例
2019年3月19日, CBP在来自菲律 宾的集装箱中查获的1185磅可卡因 。
用黑色胶带捆绑的现金藏在卡车 车厢后挡板的夹层里
C-TPAT是什麽
C-TPAT(反恐)是美国国土安全部海关边境保护局(即US Customs and Border Protection,简称“CBP”)在9·11事件发生后所倡议成立的自愿性 计划。 C-TPAT全名为“Customs-Trade Partnership Against Terrorism” ,即“海关-商贸反恐怖联盟”。透过C-TPAT(反恐)的安全建议,CBP希望 能与相关业界合作建立供应链安全管理系统,以确保供应链从起点到终点的 运输安全、安全讯息及货况的流通,从而阻止恐怖份子的渗入。
1更.S新ec的uri最ty 低Vis安ion全a要nd求Responsibility (NEW)
2.Risk Assessment (REVISED)
3.Business Partners
4.Cybersecurity (NEW + REVISED)
5.Conveyance and Instruments of International Traffic (ITT) Security
2020药典凡例变化解读(一)
2020药典凡例变化解读(一)写在前面:原则上,无变化内容不做解读,除非在实践中存在某些认知误区或者教训,需要进行必要的提醒。
请正确对待凡例中的一类排版错误,举一反三,以便即将到来的文件修订中避免类似错误。
凡例总则一、《中华人民共和国药典》简称《中国药典》,依据《中华人民共和国药品管理法》组织制定和颁布实施。
《中国药典》一经颁布实施,其所载同品种或相关内容的上版药典标准或原国家药品标准即停止使用。
解读:这里的“相关内容”主要指通用技术要求部分,以及新版药典未收载品种的检验通则等内容。
《中国药典》……现行版。
本部为《中国药典》四部。
二、《中国药典》主要由凡例、通用技术要求和品种正文构成。
凡例是为正确使用《中国药典》,对品种正文、通用技术要求以及药品质量检验和检定中有关共性问题的统一规定和基本要求。
通用技术要求包括《中国药典》收载的通则、指导原则以及生物制品通则和相关总论等。
解读:明确指出生物制品分册保留自己特有的部分通则。
注意“总论”。
《中国药典》各品种项下收载的内容为品种正文。
解读:对于标准体系的描述具备了高度的概括性,将“通则、指导原则以及生物制品通则和相关总论等”内容统一收入“通用技术要求”。
和其它国家家药典的表述趋向一致了。
三、药品标准由品种正文及其引用的凡例、通用技术要求共同构成。
本版药典收载的凡例、通则/生物制品通则、总论的要求对未载入本版药典的其他药品标准具同等效力。
解读:由上一版的“国家药品标准由凡例与正文及其引用的通则共同构成。
”的描述修订为上述描述。
突出了药品标准的“正文”的重要性。
当然,正文也有配合相应的凡例、通用技术要求产能完整使用。
四、凡例和通用技术要求中采用“除另有规定外”这一用语,……并据此执行。
无变化。
五、品种正文所设各项规定是针对符合《药品生产质最管理规范》……亦不能认为其符合规定。
无变化。
六、《中国药典》……英文缩写为ChP 。
无变化。
通用技术要求解读:调整了行文顺序,将“通用技术要求”放在了“品种正文”的章节前面,突出药典作为技术标准、技术法规的特殊性。
Incoterms2020的改变问题解析及贸易术语选用与应用

Incoterms2020的改变问题解析及贸易术语选用与应用随着国际贸易的不断发展,Incoterms(国际贸易术语)作为国际贸易中最常用的标准贸易术语之一,对于贸易双方的权利和责任分配起着至关重要的作用。
自1936年首次发布以来,Incoterms已经经历了多次修改和更新,以适应不断变化的国际贸易环境和法律法规的变化。
最新版本的Incoterms2020于2019年发布,相比于之前的版本,Incoterms2020增加和修改了一些贸易术语,同时对于部分术语的解释和规定也有所变化。
本文将对Incoterms2020的改变问题进行解析,以及对贸易术语的选用与应用进行深入探讨。
1. 新增贸易术语相比于之前的版本,Incoterms2020新增了贸易术语“DPU”(Delivered at Place Unloaded,交货地卸货),这个术语弥补了之前版本中的一些不足,使得在国际贸易中更加清晰地规定了卸货地点。
这对于国际贸易中常见的多式联运(即货物在不同的交通工具上运输)情况下具有重要的意义,有助于贸易双方在交货地点的选择和责任分配上做出更清晰的约定。
2. 修改和调整部分术语的规定除了新增贸易术语外,Incoterms2020还对部分原有的贸易术语的规定进行了修改和调整。
对于“FCA”(Free Carrier,装运港交货),在Incoterms2020版本中增加了一个选项,即在卖方的场所交货。
这一变化使得买卖双方可以更加灵活地选择交货地点,更好地适应具体的贸易情况和需求。
3. 修订了解释和规定二、贸易术语选用与应用在国际贸易中,正确选择和应用适合的贸易术语对于贸易双方的权利和责任分配至关重要。
在选择贸易术语时,需要根据具体的贸易情况和需求进行具体分析和考虑。
在应用贸易术语时,需要严格按照相关的规定和约定进行执行,以确保贸易双方的权益不受损害。
下面我们将针对贸易术语的选用与应用进行深入探讨。
1. 根据具体情况选择适合的贸易术语在选择贸易术语时,需要充分考虑具体的贸易情况和需求,以确保选择的贸易术语能够最大程度地满足贸易双方的实际需求。
浅谈Incoterms2020的一些改进和建议

浅谈Incoterms2020的一些改进和建议Incoterms2020是国际商会发布的最新一版全球贸易术语,于2019年正式生效,取代了之前的Incoterms2010版本。
新版的Incoterms2020在许多方面进行了一些改进和调整,以适应国际贸易中的新需求和挑战。
本文将就其中一些改进和建议进行浅谈。
Incoterms2020增加了一些新的贸易术语,以更好地反映现实情况和市场需求。
增加了DPU(目的地支付不清关)和DDP(目的地支付清关)两个术语,这在一些情况下为买卖双方提供了更多的选择和灵活性。
Incoterms2020强调了风险转移的概念,对卖方和买方在货物交付过程中的责任和义务进行了更加详细和明确的规定。
通过明确界定每个贸易术语下的责任分配,可以减少争议和纠纷的发生,提高贸易的效率和可预测性。
Incoterms2020还强调了合同条款的重要性,并建议贸易双方在合同中明确指定所使用的贸易术语。
这有助于确保双方对交易条件的理解一致,并防止不必要的误解和纠纷。
尽管Incoterms2020在许多方面进行了改进,但也有一些可以进一步完善的地方。
尽管新版中增加了一些新的贸易术语,但对于一些特殊情况仍然存在一定的空白。
在涉及多种运输方式和多个国家的复杂交易中,可能需要更多的明确规定和指导。
虽然Incoterms2020着重强调了风险转移的概念,但并没有对风险管理和保险责任进行详细的规定。
在一些高风险行业,如石油和化工等,可能需要更加具体和细致的规定,以保护双方的权益和减轻潜在的风险。
尽管Incoterms2020强调了合同条款的重要性,但对于一些中小企业来说,了解和使用贸易术语仍然存在一定的困难。
建议在推广和宣传Incoterms2020时,加强对中小企业的培训和指导,帮助他们更好地理解和应用这些贸易术语。
Incoterms2020在全球贸易中起着重要的指导作用,对于减少争议和纠纷,提高贸易效率和可预测性具有重要意义。
浅谈Incoterms2020的一些改进和建议

浅谈Incoterms2020的一些改进和建议国际商业贸易中,Incoterms(国际贸易术语解释通则)是一种重要的贸易工具,它规定了买卖双方在货物交付和风险转移方面的责任和义务。
自1936年首次发布以来,Incoterms已经经历了多次修改和更新,以适应不断变化的国际贸易环境。
最新版本的Incoterms2020于2019年发布,对比前一版的Incoterms2010进行了一些改进和调整,以适应全球贸易的新变化和特点。
Incoterms2020在内容上做了一些改进和增加,同时也提出了一些新的建议。
以下将从改进和建议两方面对Incoterms2020进行浅谈。
一、改进1. 清晰的语言和规定Incoterms2020在语言和规定上更加清晰,易于理解和执行。
它删除了一些含糊不清的条款,进一步减少了误解和争议的可能性。
在规定上,Incoterms2020对于货物的风险和责任转移做了更加明确的规定,使得买卖双方更容易理解各自的义务和责任。
2. 考虑安全和责任Incoterms2020更加关注货物运输过程中的安全和责任问题。
在新版中,特别增加了对于安全合规方面的规定,强调了卖方和买方在货物运输中应该遵守的相关规定和要求,以确保货物的安全和完好交付。
3. 增加了新的条款Incoterms2020在原有的条款基础上,增加了一个新的条款DAT(交付地点-船运和空运)。
DAT条款适用于货物的船运和空运,明确了卖方将货物交付给买方的责任和义务,进一步丰富了Incoterms的内容,使得其更加全面和完善。
4. 考虑数字化贸易Incoterms2020考虑到了数字化贸易的趋势和特点,对于货物交付方式和相关规定做了相应的调整和适应,使得Incoterms更加符合当今国际贸易的新要求和实际情况。
二、建议1. 进一步减少歧义和争议2. 更加注重可操作性和灵活性尽管Incoterms2020已经适应了大部分国际贸易的需求和实际情况,但是在未来的更新中,可以更加注重可操作性和灵活性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
ChP 2020年版变化
一、聚山梨酯80
1、乙二醇、二甘醇和三甘醇
供试品溶液和对照品溶液配制方法修订,色谱条件修订,增加灵敏度溶液。
2、环氧乙烷和二氧六环
环氧乙烷对照品溶液配制方法修订,二氧六环对照品溶液配制浓度修订,系统实用性溶液增加信噪比要求。
删除二氧六环峰高要求。
稀释剂聚乙二醇400修订为水。
3、脂肪酸组成
供试品处理过程,加热回流修订为65℃水浴加热回流,上层溶液增加无水硫酸钠干燥过程。
分离度溶液浓度由0.01mg/mL修订为0.1mg/mL。
4、无菌
删去无菌要求。
二、依地酸二钠
1、新增干燥失重、氨基三乙酸(HPLC法)检项。
2、其他项目检验操作规程有变化。
三、乳糖
1、删除了鉴别1及颜色。
2、其他项目检验操作过程有变化。
★ ChP2020年版涉及到的部分变化,是否需要进行验证或确认,请评估。
★新要求
另外基于风险控制,根据最新法规及研发注册RA要求,辅料额外增加以下质量标准。
1、依地酸二钠增加细菌内毒素和微生物限度,标准如下:
微生物限度:每1g供试品中需氧菌总数不得过1000cfu,霉菌和酵母菌总数不得过100cfu。
细菌内毒素:每1g依地酸二钠中含内毒素的量应小于17EU。
2、乳糖增加细菌内毒素,标准如下:
细菌内毒素:每1g乳糖中含内毒素的量应小于5EU。
3、聚山梨酯80增加微生物限度,标准如下:
微生物限度:每1g供试品中需氧菌总数不得过1000cfu,霉菌和酵母菌总数不得过100cfu。
微生物限度检验方法和细菌内毒素检验方法,麻烦根据验证的方法进行检验。
