染料的颜色与结构的关系
树脂颜色染料颜色和发色基团助色基团理论
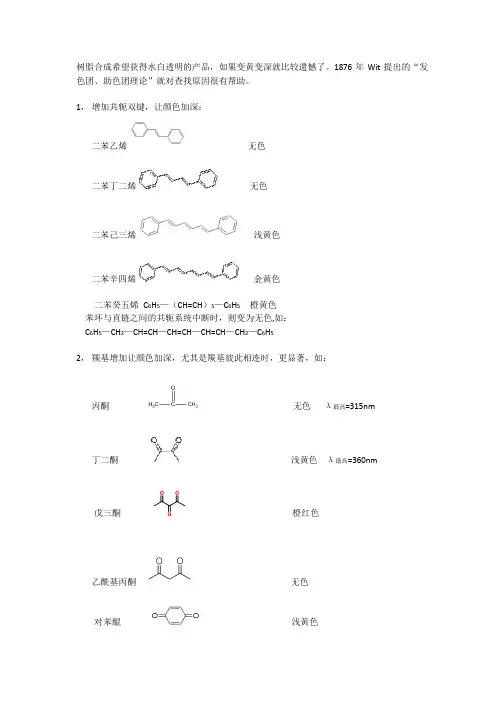
2, 羰基增加让颜色加深,尤其是羰基彼此相连时,更显著,如:
丙酮
无色 λ最高=315nm
丁二酮 戊三酮
浅黄色 λ最高=360nm 橙红色
乙酰基丙酮 对苯醌
无色 浅黄色
邻苯醌 3, 有苯环变为稠环时,颜色加深,如:
苯 萘 蒽
红色
无色 λ最高=255nm 无色 λ最高=275nm 无色 λ最高=370nm
树脂合成希望获得水白透明的产品,如果变黄变深就比较遗憾了。1876 年 Wit 提出的“发 色团、助色团理论”就对查找原因很有帮助。
1, 增加共轭双键,让颜色加深:
二苯乙烯
无色
二苯丁二烯
无色
二苯己三烯
浅黄色
二苯辛四烯
金黄色
二苯癸五烯 C6H5—(CH=CH)5—C6H5 橙黄色 苯环与直链之间的共轭系统中断时,则变为无色,如: C6H5—CH2—CH=CH—CH=CH—CH=CH—CH2—C6H5
主要内容来自《高等精细化学品化学》 沙洲步兵
丁省
橙色 λ最高=460nm
4, 引入助色基团让发色体颜色加深,且强度增加,如:
蒽醌(浅黄色)
1-氨基蒽醌(红色)
1,4-二羟基蒽醌(红色)
助色基团对发色的影响顺序:—NR2>—NHR>—NH2>—OH>—OR
Witt 的理论是经验的总结,有ቤተ መጻሕፍቲ ባይዱ用价值,但此 19 世纪的理论不是建立在有机物发色的本质 上,有许多例外现象,而且只能做定型的判断。 也就是说对于树脂生产时的大体推测判断是有帮助的。
第2章 染料的颜色与结构的关系

分子的左边是供电子基,右边是吸电子基,激发时电子发生转移。变成:
(CH3)2N N O
激发态在极性溶剂中比较稳定,因而产生深色效应。 同理,染料在纤维上的颜色也会因纤维极性不同而不同,一般来说,同一染料上 染不同的纤维时,在极性高的纤维上呈深色效应,在极性低的纤维上呈浅色效应。如 阳离子染料在涤纶上得色较在腈纶上浅。
返回第2章目录
第二章 染料的颜色与结构的关系
第四节 外界条件对吸收光谱的影响
二、溶液的浓度的影响 当染料溶液浓度很小时,染料在溶液中以单分子状态存在。如果加大溶液的浓 度,会使溶质分子聚集成为二聚体或多聚体,一般情况下,聚集态的分子π电子流动 性较低,会产生浅色效应。 三、温度的影响 溶液中溶质的聚集倾向一般随温度的升高而降低,因此,提高温度会产生深色 效应。某些有机化合物能随温度变化改变其分子结构,具有热变色性。例如:热敏变 色染料。 四、pH值的影响
第一节 光和色的基本概念
一、光的概念
可见光:波长范围大约在380~780nm的电磁波
电磁波:无线电波 60000
混色光:太阳光
红外线 780
可见光 380
紫外线 100
X射线 0.1
γ射线 nm
红外线
可 见 光
紫外线
返回第2章目录
第二章 染料的颜色与结构的关系
第一节 光和色的基本概念 不同波长的可见光的颜色及其互补色关系表: 波长 nm 380~435 435~480 480~490 490~500 500~560 560~580 580~595 595~605 605~780 光谱色 紫 蓝 蓝绿 绿蓝 绿 黄绿 黄 橙 红 互补色 黄绿 黄 橙 红 红紫 紫 蓝 蓝绿 绿蓝
染料的颜色与结构及功能染料简介解读

第 1 章染料的颜色与结构及功能染料简介学习目标 :①以量子概念,,分子激发理论阐述染料对光的选择吸收的原因。
②掌握染料颜色与染料分子结构的关系以及外界因素的影响。
③理解功能染料的概念,并熟悉荧光染料、夜光染料及变色染料的颜色产生机理。
④了解荧光染料、夜光染料及变色染料在纺织染整方面的应用,思考染料发展方向。
导言:早在 19 世纪 60 年代 W.H.Perkin 发明合成染料以后,人们对染料的颜色和结构的关系进行了深入的研究,并提出了各种理论。
量子力学的发展使人们对物质的结构的认识有了一个新的突破,此后人们开始从量子力学的角度来对染料的颜色和结构的关系进行研究。
在早期的颜色理论中,发色团及助色团理论的影响很大。
染料的颜色除了与染料本身结构有关外,还受到外界条件的影响。
随着科技的发展,功能染料在当今的社会发展中起到了越来越重要的作用。
荧光染料、夜光染料及变色染料在纺织染整方面的应用也得到很重要的发展。
1.1 光与色颜色是光线刺激了眼睛而在大脑中反映出来的一种主观感受。
它需要考虑到物理学和生理学两方面的因素。
光具有波粒二象性。
很早以前,麦克斯韦就提出了光具有电磁波的特性。
它由相互垂直的电场和磁场组成,其振幅以波动方式分别随时间和距离而变化。
1905 年,普朗克和爱因斯坦建立了一种与电磁辐射模型显然不同的微粒子理论。
这种理论把光看成是一束不连续的能量微粒或光子流,但它按麦克斯韦波动理论的波阵面速度传播。
现在我们知道,光既是一种波又是一种微粒,它具有波粒二象性。
光是一种电磁波,波长不同的光会使光的性质不同,从而引起不同的色觉。
波长为400nm-800nm的光按适当比例的混合后,照射到眼睛的视网膜上呈现的是白色。
使一束这样的混合光通过一个适当的棱镜或光栅,我们会看到连续的有色光谱,其色调主要以此为红、橙、黄、绿、蓝和紫。
这些有色光的波长从红到紫以依次递减。
因此,低能量的光子产生红色的感觉,高能量的光子产生紫色的感觉。
第03章 染料的颜色和结构

435nm
580nm
560nm 500nm
480nm 490nm
4
二、吸收定律
Lambert-Beer定律:
l
I0
入射光 C
Iλ 透射光
在稀溶液(理想溶液)中,若不计溶质分子之间 的和溶质与溶剂分子之间的相互作用,透射光强 Iλ与入射光强I0 之间成自然对数关系。 Iλ=I0 ℮ -k'c l (1)——这是光谱学的基本定律之一。
吸收能级ΔE——等于染料吸收带宽的曲线积分(激化度)。 吸收带的宽度和颜色的鲜艳度有关。谱带越宽,颜色越灰暗。
7
1、 A-λ曲线:
A
1.20
0.90 0.60 0.30
λmax=530nm
0.00 380
480
580
680
780 λ(nm)
活性红X-3B的吸光度曲线
(l=1cm,c=50mg∕L)
1、稠环数越多,颜色越深越浓; 2、芳烃的直向稠合比角向稠合易于产生深浓色效应。 3、交替键越长,颜色越深越浓;
二、判断取代基与颜色的关系
1、供电子基一般产生深色和浓色效应; 如-NH2、-NHR、-NH2、-OH、-OR等 2、吸电子基一般产生深色和浓色效应; 如-NO2、-X、-CN、>C=O、—SO3H等 3、供吸电子基的协同作用,使深浓色效应增强,形成氢键,则更强; 4、隔离基可构成混色效应。 如均三嗪基、酰胺基、间次苯基、亚甲基等。
分子轨道理论着眼于处理电子在整个分子中的运动状态和能量的关系, 根据量子力学原理,由薛定谔(Schrö dionger)方程式算出可能出现
的分子轨道,再由各分子轨道能级间隔来确定吸收的量子能级,从而 与λ形成定量关系。
第三章 染料的颜色和结构

§3.1 引言 §3.2 吸收现象与吸收光谱曲线 §3.3 吸收光谱曲线的量子概念 §3.4 染料颜色与结构的关系 §3.5 外界条件对吸收光谱的影响
本章教学要求
1.了解染料对光吸收现象的关系 2.了解光谱色的性质,吸收光谱曲线的量子 概念。 3.掌握染料分子结构与染料颜色之间的关系 (重点) 4.了解外界条件对吸收光谱的影响。
注: 重氮组分 引入吸电 子基有利 于深色效 应.
② 在染料分子的共轭系统中引入取代基之间能形成 氢键,有利于深色效应。
三、染料分子的吸收各向异性和空间阻碍
染料分子对光的吸收是有方向性的,使染料显示不 同颜色。例如:
λmax= 603 nm
λmax= 420 nm λmax= 623 nm
结论 染料的结构与颜色的关系:
普通发色体的颜色,一般并不很深,对各类纤维也不一定有亲和力, 但当另外引入一些基团时,会使整个分子的颜色加深、加浓,并且对纤维 有 亲 和 力 , 维 特 把 这 些 基 团 称 为 助 色 团 。 主 要 的 助 色 团 有 : —OH 、 — OR、—NHR、—NR2、—Cl、—Br等。
此外,像—SO3Na、—COONa等较特殊的助色团,它们对颜色无显 著的影响,但可使染料具有水溶性,并使染料在水溶液里带负电荷,从而 对某些纤维产生亲和力。
橙
蓝
5955n8m0nm 黄
480nm
蓝 绿-蓝
580nm 黄-绿 绿 -绿 490nm
560nm
500nm
4. 颜色的拼配 三原色: 红 黄 蓝 红 黄
二次色: 橙
绿紫 橙
三次色:
橙
黄灰 蓝灰 红灰
绿
紫
颜色拼配举例
刚果红染料的原理

刚果红染料的原理
刚果红染料是一种常用的染料,具有鲜艳的红色。
它是由刚果红染料分子组成的,这些染料分子具有特定的结构和成分。
刚果红染料的原理主要涉及以下几个方面:
1. 分子结构:刚果红染料是一类大分子化合物,其化学结构中含有多个芳香环和杂环结构,其中一个重要的成分是刚果红A。
这些结构与刚果红染料的颜色有关。
2. 吸收光谱:刚果红染料能够吸收可见光范围内的光线,主要吸收绿色和蓝色光波。
在吸收光谱中,刚果红染料分子能够吸收特定波长的光,使得其他波长的光能够被反射或透过,从而呈现红色。
这种吸收光谱特性是刚果红染料呈现红色的主要原因。
3. 共轭体系:刚果红染料分子内的芳香环和杂环结构形成了共轭体系。
共轭体系的存在使得刚果红染料能够吸收和释放电子的能量,并在分子内部进行共振结构变化。
这种共轭体系的运动使得刚果红染料能够对吸收的光能进行有效的转换和排放,从而呈现出鲜艳的红色。
4. 反射与透射:当光线照射到刚果红染料时,一部分光线会被染料分子所吸收,其中的能量会激发染料分子进入激发态。
激发态的染料分子会重新释放能量,其
中一部分通过发光的方式逃逸出来,另一部分则通过非辐射跃迁的方式回到基态。
这些逃逸出来的光线具有红色的波长,形成了刚果红染料显现红色的原因。
总结起来,刚果红染料能呈现红色的主要原理是它具有特定的分子结构和化学成分,能够吸收绿色和蓝色光波,通过共轭体系的共振结构变化将吸收的光能有效转换并发射出来,从而呈现出鲜艳的红色。
这些原理使得刚果红染料成为了一种常用的红色染料。
精细化学品课件染料和颜料(化工精细方向)PPT课件
• 称为朗伯特-比尔(Lambert-Beer)定律。 • 最色调大就吸改收变波。长一λm般ax的黄增、长橙或、减红短称,浅染色;料绿的、
青、蓝称深色。所以染料最大吸收波长增 大,色调就加深;反之染料最大吸收波长 减短,色调就变浅。
(三)染料的结构和颜色的关系
1 、染料的发色理论概述
染料的颜色和染料分子结构有关。
Eh hC
当吸收光的能量与ΔE相等时,有机分子才会显示出颜色。ΔE 越大,所需吸收光的波长越短;反之,ΔE越小,所需吸收光 的波长越长。作为染料,它们的主要吸收波长应在400~760 nm 波段的可见光范围内。
★2、 结构和颜色的关系
(1)共轭双键长度与颜色的关系
• 共轭双键的数目越多,π→π*跃迁所需的能量越低,选择吸收光的波长 移向长波方向,产生不同程度的深色效应。分子结构中萘环代替苯环 或偶氮基个数增加,颜色加深。共轭双键系统愈长颜色愈深。芳环越 多,共轭系统也越长;电子叠合轨道越多,越易激发;激化能降低, 颜色加深。
(2) 醌构理论
• 醌构理论是英国人阿姆斯特朗(Armstrong) 于1888年提出的,认为分子中由于醌构的 存在而产生颜色。如对苯醌是有色的,在 解释芳甲烷染料和醌亚胺染料的颜色时, 得到应用。
(3) 发色理论的量子化概念
• 根据量子力学,可以准确计算出物质分子中电 子云分布情况,定量地研究分子结构与发色的 关系,认为染料分子的颜色是基于染料分子吸 收光能后,分子内能发生变化而引起价电子跃 迁的结果。1927年提出了染料发色的价键理论 和分子轨道理论。
NaO3S
NN
OH
酸性橙
•蒽醌染料
结构特征:含有 O
O 基团或多环酮 。
茜素
有机着色化合物
有机着色化合物
有机着色化合物通常指的是有机颜料,它们是一种不溶性的有机物,用于为各种底物提供颜色。
以下是一些关于有机着色化合物的详细信息:
1. 化学结构:有机颜料与染料在化学结构上可能是一致的,但它们的使用方法不同。
某些还原染料和硫化还原染料可以通过还原成隐色体作为纤维染料使用,而不经还原则可以作为颜料使用。
2. 应用领域:有机颜料广泛应用于油墨、油漆、涂料、合成纤维的原浆着色,以及织物的涂料印花、塑料、橡胶和皮革的着色等。
其中,油墨制造业是有机颜料使用量最大的领域。
3. 物理性质:有机颜料是不溶于水或一般有机溶剂的有色化合物。
它们通过与高分子化合物结合,黏附在纤维或基质上实现着色效果。
4. 分子结构:有机化合物中π轨道和n轨道的数量越多,化合物呈现颜色的可能性就越大。
共轭双键的存在会导致吸收光谱发生红移,因此许多染料化合物含有苯环结构或大量共轭双键。
5. 分类:有机颜料可以根据化学结构进行分类,包括偶氮颜料、酞菁颜料、蒽醌、靛族、喹吖啶酮、二恶嗪等。
6. 特性:作为颜料使用的有机化合物需要具备一系列的特性,如耐日晒、耐水浸、耐酸碱、耐热以及在应用介质中的易分散性等。
综上所述,有机着色化合物即有机颜料,它们是一类具有特定化学结构和物理性质的有机化合物,广泛应用于各种着色领域。
染料的颜色与结构的关系
求:染色上染百分率、上染速率,研究染色动力学
精品课件
三、吸收光谱曲线
???由染料的吸收光谱曲线,可以得到一些重要的分析数据
精品课件
最大吸收波长λmax——曲线的峰值,它决定了染
精品课件
精品课件
最大共轭效应只有在分子的整个共轭 系统中的原子和原子团处在同一平面上时,才 能显示出来;
因为这样,整个共轭系统中各π电子 云,才能得到最大限度的叠合。
如果分子平面受到程度不等的破坏, 则π电子云叠合程度就会降低,π电子离域程 度低,使激化能增高,吸收光谱向短波方向移 动,产生浅色效应,同时吸光系数也往往降低。
精品课件
色环图
精品课件
K/S
16
14
12
10
8
6
4
2
0
400
450
500
550
600
650
700
波长
几种不同颜色染料的吸收光谱图
精品课件
二、吸收定律
染料的理想溶液对单色光(单色光是波长间隔很小的 光,严格地说是由单一波长的光波组成的光)的吸收强度和 溶液浓度、液层厚度间的关系服从朗伯特-比尔 (Lambert-Beer)定律:
②染料分子基态极性大于激发态
由于基态极性大于激发态,在极性较大的水 中,使基态偶极距增加,即极性增加而基态更 趋稳定,跃迁到激发态所需激发能更大,发生 浅色效应。
①
②
精品课件
(CH3)2N
N
O
“苯酚蓝” 的分子右边是吸电 (CH3)2N
N
O
染整复习题N
染整复习题N1、影响上染百分率的因素有哪些?染料浓度浴温度pH时间其他添加剂2、影响染料颜色的结构因素有哪些?它们是怎样影响的?染料结构中共轭双键的数量,连接到共轭体系的基团的极性,以及染料络合物的形成及染料的离子化等,均含影响染料的颜色。
①、共轭双键数目的影响染料结构中的共轭双键越多,共轭体系越长,染料吸收的光能越低,染料吸收的光波长越长,染料的颜色越深。
随着偶氮染料数量的增加,共轭体系增长,染料颜色变深。
在染料的分子结构中,由于某些基团之间的势能,共轭体系的共面性受到影响,电子跃迁能增加,吸收光波的波长减小,染料的颜色变浅,如间隔基。
②、共轭体系上的极性基团的影响。
在染料分子的共轭体系中,当极性基团连接时,染料分子的偏振效应一般会增强,共轭体系中π电子的共轭度会提高,从而使电子的跃迁能降低,吸收光的波长会变大,染料的颜色会更深③、染料在介质的影响下发生离子化,产生的电荷若加强了染料分子的极化效应,则电子的跃迁能降低,吸收光波的波长变大,染料的颜色变深。
④ 染料与金属络合后,颜色通常会越来越深。
3.酸性染料分为哪些种类,并说明其染色性能特点?可分为强酸、弱酸和中性浴染色:强酸性:匀染性好,分子结构简单,对羊毛亲和力较低,湿牢度较差。
弱酸性:结构稍微复杂,对羊毛亲和力较高,湿牢度较好,匀染性较差。
中性:分子结构更复杂,对羊毛亲和力更高,湿牢度好,匀染性差。
分散染料染色涤纶纤维的常用方法有高温高压染色和热熔染色。
4.举例说明染料和纤维之间的作用力类型范德华力,染料分子的他子量越大,共轭系统大,则其对纤维的这种作用力就越大,如直接染料。
氢键,任何染料在纤维之间都有大小氢键,如还原染料。
离子键,如强酸染料,染色蛋白质纤维。
共价键,如活性染料和纤维之间的共价键。
配位键,如酸性含媒染料与蛋白质纤维间。
5.用阴离子染料染色纤维素纤维时,在染色溶液中加入硫酸钠或食盐等中性盐会产生什么影响,为什么?答:无机的中性盐类如食盐、元明粉等,在水中发生电离,无机的阳离子体质小,因此在水溶液中活泼性大,容易吸附在纤维分子周围从而降低纤维分子表面的阴电荷,相对地增加了染料阴离子与纤维素分子间的吸附量,达到促染的效果,故食盐与硫酸钠起促染剂的作用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
更多染料的共轭双键系统是由偶氮基联接芳环构成的。例如
吸收波长为:
=hc/E 由上可知,激化态和基态的能级间隔越小,吸 收光波的波长越大,而吸收频率则与此成反比。 作为染料,它们的主要吸收波长应在380- 780nm波段范围内。染料激化态和基态之间的能 级间隔E必须与此相适应。
价电子跃迁类型
一般有机物分子中的 价电子有σ键的σ电子, π键的π电子以及未共 用电子对的n电子。
助色团:指的是那些接在 共轭系统上的-NH2、- NHR、-NR2、-OH、-OR等供电子基团。
第二节 吸收现象和吸收光谱曲线
一、颜色和吸收
染料的颜色是它们所吸收的光波颜色(光谱色)的补色, 是它们对光的吸收特性在人们视觉上产生的反映。染料分 子的颜色和结构的关系,实质上就是染料分子对光的吸收 特性和它们的结构之间的关系。
吸收光谱曲线的位移
颜色变浅
黄、橙、红、紫、蓝、青、绿
颜色加深
第三节 吸收光谱曲线的量子概念
一、光的量子理论
光是一种电磁波,具有波和微粒两象性质。它的波 动频率和光速c成正比,和波长成反比。
=c/ (波) 光又具有微粒性质。它的能量发射、传播和转移都 不是连续,而是量子化的,以能量微粒光子为最小 单元的。光子的能量和光的频率成正比。
最大摩尔吸光度εmax——对应于Amax,它决定 了染料颜色的浓淡;
吸收带宽Δṽ——对应于Δλ,它决定了染料颜色的 鲜艳度(纯度);
在有关吸收光谱的术语中,颜色的深浅是如下描述 的:被吸收光的波长越长,则该颜色越深,被吸收光的 波长越短,颜色越浅。
而光波从长到短的顺序为红、橙、黄、绿、青、蓝、 紫,其对应的补色顺序为绿(蓝光绿)、青、蓝、紫、 红、橙、黄,这就是颜色从深到浅的顺序。
1.共轭双键系统
一般而言,在共轭双键体系中,共轭双键愈长,π→π*跃 迁所需能量较低,则选择吸收的光线波长也愈长,在同系 物中,产生不同程度的深色、浓色效应。
图 偶数交替烃分子轨道的能级
例如:
苯
萘
蒽
λ max (nm)
ε lg max
200 3.65 无色
285 3.75 无色
384 3.8 无色
A=lgI0/I =cl 式中:A为光密度,I0为入射光强度,I为透射光 强度,c为溶液浓度,l为光程,为摩尔吸光系数。
求:染色上染百分率、上染速率,研究染色动力学
三、吸收光谱曲线
???由染料的吸收光谱曲线,可以得到一些重要的分析数据
最大吸收波长λmax——曲线的峰值,它决定了染 料颜色的深浅(色相);
Ee Ev Er
➢各能级都是量子化的,分子能量为各运动状态能量之和:
E Ee Ev Er ➢分子的能量状态称为分子能级。
v'=2
v'=1
E
v'=0 E1 激发态
v"=2 v"=1 v'=0
E0
分子能级示意图
基态
激发 E=E1-E0
E=Ee+Ev+Er
这个能级间隔的大小虽然包含着振动能量和转动能量的变 化,但主要是由价电子激化所需的能量决定的。
图 各状态的电子自旋方向
第四节 染料的颜色和结构的关系
作为染料,它们的主要吸收波长要在可见光范围内, 吸收强度max一般为104~105;
染料对可见光的吸收特性主要是由它们分子中π电子 运动状态所决定的。要具有上述吸收特性,染料分子结构 中须有一个发色体系。这个发色体系一般是由共轭双健系 统和在一定位置上的供电子共轭基,即所谓助色团所构成 的。有许多除了供电子共轭基外,还同时具有吸电子基团。 也有一些染料(为数不多)的发色体系中是没有所谓助色 团的。
就有机化合物而言, 对可见光吸收的能级 间隔是由它们分子中 电子运动状态所决定 的。
三、吸收强度和选律
瞬间偶极矩
在光谱学中,人们用跃迁矩来估算吸收强度。据估 算,许多具有共轭结构的有机化合物的电子跃迁,吸收强 的max可达105 数量级。人们把 max 很小的跃迁称为“禁 戒”的,而把max 大的跃迁称为“允许”的。max 小于 102的就算是“禁戒”的了。
染料的颜色与结构的关系
张晓莉
本章主要内容
第一节 引 言 第二节 吸收现象和吸收光谱曲线 第三节 吸收光谱曲线的量子概念 第四节 染料的颜色和结构的关系 第五节 外界条件对吸收光谱的影响
本章的任务在于说明:染料对光的吸收现象、 吸收现象的量子概念以及染料的颜色和结构的一 般关系。这里所谓染料的颜色一般是指染料的稀 溶液吸收特性,也就是指染料成分子分散状态时 的吸收特性而言的。同一染料由于聚集状态或晶 体结构的不同,表现的颜色就会有差异。
E=h (粒子)
式中E为一个光子的能量,h为普朗克常数(6.6256×10-27尔格·秒,l尔格=1×10-7J)。
二、分子能级
➢根据量子理论,原子和分子的能量是量子化的。 ➢物质分子中,存在电子相对于原子核的运动,以及
原子核间的相对振动和整个分子所存在的一定的转 动。各运动状态都有相应的能量,分别为电子能 级、振动能级、转动能级。
色环图
K/S
16
14
12
10
8
6
4
2
0
400
450
500
550
600
6吸收光谱图
二、吸收定律
染料的理想溶液对单色光(单色光是波长间隔很小的 光,严格地说是由单一波长的光波组成的光)的吸收强度和 溶液浓度、液层厚度间的关系服从朗伯特-比尔 (Lambert-Beer)定律:
问题
1、物体为何有颜色?染料为何有颜色? 2、染料的共轭体系与颜色关系如何? 3、哪些基团将使颜色加深?哪些基团消色?哪
些基团辅助发色? 4、如何解释染料的吸光现象?从吸收光谱曲线
可得到染料的哪些颜色信息?
第一节 引 言
发色团:一般指的是那些能对波长为200~1000nm 的 电磁波发生吸收的基团。实际上,染料要求结构中能吸收 可见光波(380~780nm)的基团。它们的分子结构里要 有一个由若干共轭双键构成的共轭系统。
要发生具有一定跃迁矩的所谓“允许”的跃迁,要有 一定的条件,这些条件称为选律。
1、对称选律 电子在对称性相同的分子轨道间的跃迁是 禁止的,在对称性相反的轨道间的跃迁是 允许的。
图 1,3-丁二烯的分子轨道
2、自旋选律 在没有外磁场等因素的作用下,伴有态数改变的 跃迁是禁止的,态数不变的跃迁是允许的。
