(整理)Chemkin模型学习读书笔记.
读书笔记(一)
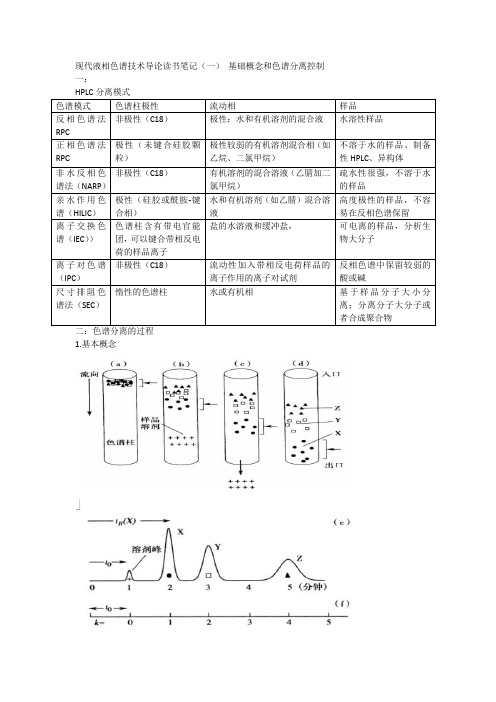
现代液相色谱技术导论读书笔记(一)基础概念和色谱分离控制一:1.基本概念假定含有三种不同化合物分离,●代表化合物X,▲代表化合物Y,□代表化合物Z。
如图中没有显示流动相分析,溶解样品的溶剂分子用+代替。
当样品进样到图a的色谱柱上,有流动相带动,在不同阶段内留个色谱柱,然后离开色谱柱进入检测器如图e ,并生成一个检测器响应对应时间作图的结果(色谱图)。
当样品在色谱柱中(图a~d),样品XYZ分子展现出两种行为:差异移动和分子扩散。
当一个给定的溶质分子通过色谱柱时,这些分子迅速扩散,占据色谱柱中大部分体积。
给定溶质分子在色谱柱里所占的体积定义为色谱带。
当色谱带离开色谱柱时,它就在色谱图中被记录下来,为色谱峰。
每个色谱峰的身份可以由他们通过色谱柱的时间来定义(保留时间)。
保留时间是指样品进样后到出现色谱峰顶端时的时间段。
溶剂峰的保留时间是色谱柱的死时间。
保留因子k:固定相中的溶质分子总量除以流动相中溶质分子总量。
k=(tR−t0)/t0)−1或者k=(tRt0保留时间其中:tR:死时间t0:=Vm/F,F为流速ml/min,Vm为色谱柱内流动相总和。
其中:tVm≈5*10-4Ld2 L:柱长mm;d:内径mm2.分离条件和样品组成的角色反相色谱法中使用非极性的色谱柱和极性的含水的流动相。
极性的溶质分子喜欢极性的流动相(物以类聚)而保留程度较低(较大的R值,较小的K值),而非极性的溶质分子会倾向和非极性的固定相相互作用并能保持更久。
反相色谱柱的流动相通常是由水或水性缓冲盐(A相)和有机溶剂(B相)组成。
当有机溶剂增加时,所有样品化合物的保留都会减少。
%B值改变+10%,K值一般会减少到原来的1/2或1/3.3.分离度和方法建立HPLC方法的建立:选择合适的分离条件,以便为一个给定的样品提供可靠的分离结果。
当需要分离多个色谱峰时,对于分离程度最差的一对色谱峰来说,分离度的最低要求是Rs≥2,这样的色谱峰对称为决定性的色谱峰,分离度为决定性的分离度。
CHEMKIN4.0.1入门指南讲诉

CHEMKIN入门指南《燃烧学》辅助教程上篇基础知识、核心程序、化学平衡(EQUIL)、全混反应(AURORA)如果文中有任何错误,请不吝指出,以便不断改进2004.3第一章CHEMKIN简介本章介绍CHEMKIN的主要功能和求解过程。
第一节安装CHEMKINChemkin最早的版本始于1980,由美国Sandia实验室的Kee RJ等人编写,经过多年的不断发展日趋完善。
后来由Reaction Design公司收购并继续开发,目前最新版为3.7.1。
由于学习和科研需要,我们花费2000$向ReactionDesign公司订购了一套最新版本的CHEMKIN 3.7.1,其中包括20个网络教学许可证,用于《燃烧学》课程的学习。
[安装] 请从ftp://combustion:combustion@166.111.56.202的“CHEMKIN软件”目录内下载安装程序chemkin371_pc_setup.exe,执行安装程序。
安装完后会自动在桌面及开始菜单建立快捷方式。
[运行许可证书] 教学用的CHEMKIN采用网络认证,故电脑必须联网(校内)。
当程序计算(Run)时,系统会提示选择license,选择“Specify license server”,然后next,在下一画面填入“166.111.56.202”即可。
第二节CHEMKIN介绍CHEMKIN是一种非常强大的求解复杂化学反应问题的软件包,常用于对燃烧过程、催化过程、化学气相沉积、等离子体及其他化学反应的模拟。
CHEMKIN包括“核心程序(Core Utilities)”和“应用程序(Application)”两级程序包。
以气相反应、表面反应、传递过程这三个核心软件包为基础,CHEMKIN提供了对12种常见化学过程模拟的软件包及后处理程序。
CHEMKIN的三个核心程序模块:1) 气相动力学(Gas-PhaseKinetics):是所有程序计算的基础,提供气相成分组成、热力学数据、化学反应等信息。
CHEMKIN tutorials2.1-2.3

2.气相燃烧过程2.1 平衡2.1.1绝热火焰温度2.1.1.1项目简述这个用户指南提出了使用气相平衡计算确定绝热火焰温度的氢气/空气系统。
绝热火焰温度是指在某一特定条件下测量的混合气体燃烧可以达到的最高温度。
在一个包含热损失,化学动力学和质量传输局限在内的实际系统中,火焰温度可能低于绝热火焰温度。
2.1.1.2项目设置项目文件可以命名为equilibrium__gas.ckprj。
用于此样品的数据文件可以在samples\equilibrium\gas directory中查询。
该反应堆图包含有一个单一的平衡反应堆。
平衡计算仅需要知道物质种类和它们的热力学数据,而没必要知道参加反应的名单。
对于此示例问题,化学输入的文件只包括3个元素:H,O,N和H2, H, O2, O, OH, HO2, H2O,N2, and H2O2等9种物质。
为了获得准确的火焰温度,产品列表中的基础种类和稳定物种是同等重要的。
对于一般的平衡计算来说,包含一些不重要的物种比忽略一些被证明是重要的物种要好得多。
解决这个问题首先需要涉及C1平衡板。
这个问题类型(恒压和焓),初始温度(300 K)和压力(1 atm)进入反应堆物理性质上的标签。
溶液估温2000 K 用于帮助确保获得该解决方案是点燃的气体,而不是未燃的状态。
对于平衡模拟的时候溶液估温不是必要的,但是当涉及辅助解决方案时可能会用到。
在反应物二级的特异性数据选项卡上输入起始组成数据。
反应物混合规定了包括提供初始摩尔元素及初始能量系统的初始状态。
随着初始温度的增加,补遗集面板用来指定两个额外的模拟。
2.1.1.3项目结果图2-1表示的是这些模拟的平衡温度,它代表H/O为2.0的氢气/空气混合物的绝热火焰温度。
这些温度都在2400以上,因此与对应燃烧气体相符合。
正如人们所料的那样,这些绝热火焰温度随着初始气体温度增长而升高。
图2-1氢气/空气混合的绝热火焰温度2.2利用当量比燃烧过程的很多属性强烈依赖于燃烧混合物的化学计量。
电沉积纳米金的读书笔记

[1]吉玉兰, 王广凤, 方宾. 纳米金/单壁碳管修饰玻碳电极对黄芩苷的电催化作用及快速检测[J].2010, 6(6): 11-12.NG/GCE电极的制备将l mg酸化的SWNT分散在5 mL DMF中,超声振荡至溶液均一。
玻碳电极先在0.05 μm A2O3上抛光,然后分别在无水乙醇和二次蒸馏水中各超声清洗l min,晾干后,用微量进样器取10.0μL上述SWNT分散液滴加在玻碳电极表面,晾干,即得SWNT/GCE。
将SWNT/GCE用二次水冲净置于0.1 mg/mL HAuCl4中,以扫速50 mV/s,于1.2~-0.6 V范围连续扫描5圈,取出用水反复冲净,晾干得NG/SWNT/GCE。
[2]张英,袁若,柴雅琴等. 纳米金修饰玻碳电极测定对苯二酚[J]. 西南师范大学学报,2002, 6(31):87-90.NG/GCE电极的制备将玻碳电极分别用0.1 μm和0.03 μm A12O3。
粉末抛光成镜面,二次水冲洗,依次用(1+1) HNO3,无水乙醇和二次水超声清洗5 min,取出后用二次水冲净置于1 mg/mL HAuCl4中,以饱和甘汞电极(SCE)为参比,铂丝为对电极,于-0.2 V下保持60 s,取出后用二次水反复冲洗,得NG/GCE修饰电极,悬在pH为7.0的PBS上方保存备用。
NG/GCE修饰电极的性能图1(a)是裸GCE和NG/GCE修饰电极在 5.0 mmol/L Fe(CN)63-/4- + 0.1 mol/L PBS(pH=7.0)中的循环伏安图.从图中可以看出,Fe(CN)63-/4-在NG/GCE修饰电极上峰电流明显增加,并且氧化还原峰电位差值减小,这主要是因为:NG使GCE电极的表面粗糙度和有效面积增加以及带正电荷的NG叫同带负电荷Fe(CN)63-/4-有较强的静电作用,使氧化还原发应更容易发生.图l(b)是裸GCE和NG/GCE修饰电极在5.0 mmol/L Fe(CN)63-/4-+0.1 mol/L PBS(pH=7.0)中的交流阻抗图,由图可知,NG/GCE电极膜的阻抗比裸GCE小很多,这说明NG能很好地增强电子的传输.[3]朱强,袁若,柴雅琴等.以纳米金为介质的无标记电流型甲胎蛋白免疫传感器的研究[J]. 西南师范大学学报, 2002, 2(32):82-90.将玻碳(GC)电极经金相砂纸打磨,Al2O3粉抛光打磨后,用超声清洗5 min,纳米金在玻碳电极上的修饰按参照文献,将抛光洗净的GC电极置于粒径为16 nm的金溶胶中于+1.5 V的电位下沉积750 s,完成后再静置于金溶胶中5 min,取出冲洗掉电极表面吸附不牢固的纳米金,再将其放入anti—AFP溶液中静置吸附7 h即可,取出冲洗,置于PBS(磷酸缓冲溶液,pH=7.0)中备用,电极修饰过程如图1所示.图2为金溶胶在GC电极表面沉积不同时间的循环伏安曲线.从图2可以看出,峰电流随着带负电的纳米金的沉积量的增加逐渐降低,在750 s以后变化很小,说明此时玻碳电极上的纳米金沉积基本达到最大,所以选择750s作为沉积优化时间.图3为纳米金修饰后的玻碳电极在anti-AFP中吸附不同时间的循环伏安曲线.Anti-AFP中的-NH4能与纳米金稳固的结合,由于抗体是非导电性物质,随着抗体在电极表面的增加对电流的阻碍作用增大,[Fe(CN)6]3-/4-电对的峰电流随之降低.由图3可知结合7 h后,峰电流不再明显变化,说明抗体固载达到最大值,因此选用7 h为优化的抗体结合时间.曲线a,[Fe (CN)6]3-/4-在裸GC电极氧化还原峰分别为:E pa=0.26 V,E pc=0.15V,i pa/i pc=1,为[Fe (CN)6]3-/4-的可逆氧化还原电对.曲线b,裸GC电极上沉积纳米金后,电流值明显降低,表明纳米金已经修饰在电极表面并与同样带负电的[Fe (CN)6]3-/4-相排斥,从而阻碍了电子的传输.曲线c,修饰了纳米金的电极在吸附AFP抗体后,由于抗体是非导电性物质,电流响应值仍是降低.曲线d,AFP抗原和AFP抗体结合成复合物进一步阻碍了电子的传输.图4(b)交流阻抗图进一步表征了电极的修饰过程.曲线a为裸GC电极的阻抗图,近似一条直线,表明电子传递到电极表面只受扩散控制;当电极表面沉积了纳米金(曲线b),出现高的膜本体阻抗(Ret=2500Ω);曲线c,当电极修饰了抗体和纳米金,抗体的覆盖使阻抗值增加(Ret=3300Ω);当电极表面抗体与抗原反应结合成复合物后,其阻抗进一步增大(Ret=3500Ω(曲线d).由以上结果表明,修饰电极的CV 图与交流阻抗图结果一致,anti—AFP被成功的固定在电极表面.[4]闵丽根, 袁若, 柴雅琴. 基于纳米金与碳纳米管-纳米铂-壳聚糖纳米复合物固定癌胚抗原免疫传感器的研究[J]. 化学学报, 2008, 66(14): 1676-1680.玻碳电极(GCE,直径4mm)经0.3, 0.05μm Al2O3悬浊液抛光成镜面后,依次用蒸馏水、无水乙醇、蒸馏水超声5min,清洗后将电极置于室温下晾干,备用.将一定量的碳纳米管-纳米铂-壳聚糖的纳米复合物滴加于电极表面,于室温下晾干.用水清洗后滴加硫堇,于室温下晾干8 h,浸泡在pH 6.0 PBS中30min以除去电极表面物理吸附的硫堇分子.用水冲洗,然后依次于纳米金和癌胚抗体中于4℃浸泡8 h.最后,将上步制好的电极浸在HRP(2mg/mL,pH6.0的PBS)中4h以封闭非特异性结合位点,然后用PBS(pH 6.0)和水洗涤,晾干,即得免疫电极.置于4℃的冰箱中保存待用.免疫传感器的制作过程见图1.检测方法(桃花)利用循环伏安法进行电极制备过程的表征及对CEA的检测.该方法采用三电极体系,修饰电极为工作电极,甘汞电极为参比电极,铂丝电极为对电极.整个实验在0.1 mol/L PBS(磷酸缓冲溶液,pH 6.0)中进行,电位区间为-0.6~+0.2 V,扫描速率l00mV/s.进行免疫测定时.测试底液为5 mL 0.1 mol/L PBS(pH 6.0)+3.5 mmol/L H2O2,以循环伏安法检测CEA的浓度.实验温度均控制为(25±0.5)℃.电极修饰过程的电化学表征(桃花)用循环伏安法研究了电极在自组装过程中的电化学特性.图3中曲线a为玻碳电极上修饰MWNT-Pt-CS复合物的循环伏安图,图中在E=0 V附近出现一对峰值较小的氧化还原峰,是由碳纳米管上的羧基引起的.曲线b为滴加硫堇后的循环伏安图,在-0.2 V左右出现一对明显的氧化还原峰,此为硫堇的特征峰.曲线c为MWCNT-Pt-CS复合物修饰电极依次吸附纳米金、抗体和辣根过氧化物酶后的循环伏安图,由于大分子抗体和辣根过氧化物酶是非导电性物质,氧化还原峰较曲线b明显下降.曲线d为制备好的免疫电极在PBS中加入3.5 mmol/L H2O2后的循环伏安图,由于HRP催化H2O2,使得循环伏安曲线的氧化峰减小,还原峰明显增大.曲线e是免疫反应后的循环伏安图,由于抗原抗体结合形成的复合物阻碍了电子的传递,与d比较e的氧化还原峰明显降低.缓冲液酸度的选择(桃花)pH对免疫传感器的影响主要有两个方面:一方面影响抗原、抗体及HRP的活性;另一方面对亲和性的影响。
CHEMKIN基础培训资料

近壁面低温区 (CO和烟灰生成区)
反应路径分析
机理简化的有效工具 图形化研究反应机理的瓶颈 识别主要物质和反应 查看潜在的化学机理 可以与敏感性分析联用 适用所有反应器
Reaction Design 介绍 CHEMKIN介绍 CHEMKIN安装 CHEMKIN用户界面 CHEMKIN化学设置 CHEMKIN模型 CHEMKIN后处理 CHEMKIN算例
等人于1980年开发的用于解决燃烧过程中的 气相化学反应动力学问题的软件包 CHEMKIN不是一个应用软件,它只是一个 子程序库,目的在于为解决带有流动的燃烧 过程中的化学问题提供一个计算工具
CHEMKIN-I的缺点
CHEMKIN-I的缺点是其源程序代码中对字 符串常量使用了Fortran66标准的Hollerith 码进行处理,这与目前使用的大多数 Fortran编译器不相容,因此已很少使用
打开防火墙的两个端口:例外—添加端口 reaction design license server port ½ 28850/28851
License tools—manage reaction design license中的path to license:28850@ip
Reaction Design 介绍 CHEMKIN介绍 CHEMKIN安装 CHEMKIN用户界面 CHEMKIN化学设置 CHEMKIN模型 CHEMKIN后处理 CHEMKIN算例
分析复杂气相和表面化学反应装置中的传质 系数、热化学速率以及动力学
CHEMKIN 3.7
Start界面 徽标
CHEMKIN 3.7
CHEMKIN 3.7的后处理
ChemKin 操作入门

ChemKin4.0 操作入门安装:运行setup.exe。
然后把carck文件夹中的chemkin.lic文件拷到安装目录下的licenses文件夹中。
一、新算例设置的基本操作1、建立新工程2、设定反应器模型在左侧models面板双击所需反应器模型,如PSR模型,则反应器模型出现在右边的Diagram View面板,下角Update project按钮变成黄色。
当设定好模型后,点击该黄色按钮确定,按键变成灰色,方可进入下一步反应机理设定。
3、设定反应机理在左侧,Open Projects面板,双击Pre-Processing。
进入机理设置界面。
Working Dir 是所有计算结果,包括工程文件的存储位置,自行设定。
点击New Chemistry Set,设定机理文件,必须设定Gas Phase Kinetic File—后缀为.inp;Thermodynamic Data File――后缀为.dat,都通过设定路径来设定。
设好后Save As…,确定,就变成下面的样子,点Run Pre Processor。
运行成功则View Results….变成黑色,Cluster变成黑色,没有跳出任何消息框。
运行成功方可进行计算的初始参数设定。
在cluster中,●properties选求解Gas Energy Equation,●C1表示反应器,在reactor physical properties中设置停留时间、温度、压力、体积、热损失等项。
注意单位。
表面项和传输项设置留待诸位研究设置方法。
在species specific data 中设置反应器中原有的物质组分,要各组分的fraction加起来=1。
这一项我的计算中不需要设置。
注意,此处设置的温度为牛顿迭代计算的初值,默认条件下等于入流温度。
●R1表示入流。
入流可以有多个,比如我的先进再燃就有5个入流,入流再多也应该没有关系,进去就都一样了,看设置参数的方便而定。
吸附动力学和热力学各模型公式及特点
分配系数吸附量LangmiurKL 是个常数与吸附剂结合位点的亲和力有关,该模型只对均匀表面有效FreundlichCe 反应达到平衡时溶液中残留溶质的浓度KF 和n 是Freundlich 常数,其中KF 与吸附剂的吸附亲和力大小有关,n 指示吸附过程的支持力。
1/n 越小吸附性能越好一般认为其在0.1~0.5时,吸附比较容易;大于2时,难以吸附。
应用最普遍,但是它适用于高度不均匀表面,而且仅对限制浓度范围(低浓度)的吸附数据有效一级动力学1(1)k t t e q q e -=-线性二级动力学 2221e t e k q t q k q t =+线性初始吸附速度Elovich 动力学模型Webber-Morris动力学模型Boyd kinetic plot令F=Q t/Q e,K B t=-0.498-ln(1-F)准一级模型基于假定吸附受扩散步骤控制;准二级动力学模型假设吸附速率由吸附剂表面未被占有的吸附空位数目的平方值决定,吸附过程受化学吸附机理的控制,这种化学吸附涉及到吸附剂与吸附质之间的电子共用或电子转移;Webber-Morris动力学模型粒子内扩散模型中,qt与t1/2进行线性拟合,如果直线通过原点,说明颗粒内扩散是控制吸附过程的限速步骤;如果不通过原点,吸附过程受其它吸附阶段的共同控制;该模型能够描述大多数吸附过程,但是,由于吸附初期和末期物质传递的差异,试验结果往往不能完全符合拟合直线通过原点的理想情况。
粒子内扩散模型最适合描述物质在颗粒内部扩散过程的动力学,而对于颗粒表面、液体膜内扩散的过程往往不适合Elovich 方程为一经验式,描述的是包括一系列反应机制的过程,如溶质在溶液体相或界面处的扩散、表面的活化与去活化作用等,它非常适用于反应过程中活化能变化较大的过程,如土壤和沉积物界面上的过程。
此外,Elovich 方程还能够揭示其他动力学方程所忽视的数据的不规则性。
Elovich和双常数模型适合于复非均相的扩散过程。
顶好的Chemkin学习资料
大型气相化学反应动力学软件CHEMKIN学习报告作者:范志林1 总体介绍CHEMKIN软件是美国Sandia国家实验室开发的大型气相化学反应动力学软件,可以用来解决带有化学反应的流动问题,是燃烧领域中普遍使用的一个模拟计算工具。
CHEMKIN3.7版本有多种针对不同模型的应用程序,包括AURORA、CRESLAF、EQUIL、OPPDIF、PASR、PLUG、PREMIX、SHOCK、SPIN、SURFTHERM、OVEND、TWAFER 12个应用程序,分别用来模拟充分搅拌反应器(AURORA)、圆柱形或平面形通道内的层流化学反应(CRESLAF)、化学平衡相平衡(EQUIL)、对流扩散火焰(OPPDIF)、部分搅拌反应器(PASR)、柱塞流反应器(PLUG)、一维稳态层流预混火焰(PREMIX)、冲击波化学动力学(SHOCK)、化学气相沉积滞留反应器(SPIN)、气相和表面化学系统的热化学传质及动力学(SURFTHERM)、多晶片低压化学沉淀反应器(OVEND)、用来确定多晶片低压化学沉淀反应中的温度(TWAFER)。
对大多数CHEMKIN应用程序而言,在应用之前需事先准备好三个输入文件:气相输入文件(gas chemistry input file)、表面反应输入文件(surface chemistry input file)和程序应用输入文件(application input file)。
输入文件默认为采用文本文档的形式给出,其中气相输入文件(gas chemistry input file)中指定了反应中元素组成、组分组成、各组分热力学参数、包括基元反应式、Arrhenius系数(pre-exponential factor、temperature exponent和activation energy)的反应机理;而程序应用输入文件(application input file)中则要根据实际情况来指定反应器的几何参数、问题类型、初始条件以及解文件控制参数等等。
Chemkin模型学习读书笔记
Chemkin模型学习读书笔记一、模型总体介绍大型气相动力学计算软件包Chemkin(chemical kinetics)可以用来解决带有化学反应的流动问题,是燃烧领域中普遍使用的一个模拟计算工具。
该软件是1980 年美国Sandia 国家实验室Kee R. J. 等人开发并推出的,经几次完善发展,至今已开发出了第6个版本CHEMKIN 4.0.2。
chemkin有多种针对不同模型的应用程序,在4.0版本中共有23种计算模型,分6大类:○1封闭的0维反应器:包括封闭的内燃发动机模型(closed internal combustion engine simulator),封闭的同质反应器(closed homogeneous batch reactor), 封闭的部分搅拌反应器(closed partially stirred reactor)和封闭的等离子反应器(closed plasma reactor)。
顾名思义,此类模型没有出入反应流,只根据反应器的初状态计算其末状态的参数。
○2开放的0维反应器:包括良搅拌反应器PSR(perfectly stirred reactor),等离子良搅拌反应器(plasma PSR)和部分搅拌反应器(partially stirred reactor)。
此类模型需要定义入流的流量、种类和温度等信息,计算后会给出出口的状态参数。
○3流动反应器:包括栓塞流反应器(plug-flow reactor)、等离子栓塞流反应器(plasma plug-flow reactor)、平面层流反应器(planar shear flow reactor)、圆柱形通道内的层流反应器(cylindrical shear flow reactor)和蜂窝整料反应器(honeycomb monolith reactor)。
此类模型考虑流动中的化学反应,主要是表面反应。
○4火焰模拟反应器:包括预混层流燃烧器-稳定的火焰(premixed laminar burner-stabilized flame)、预混层流火焰-火焰速度计算(premixed laminar flame-speed calculation)、和扩散/预混对撞火焰(diffuseion or premixed opposed-flow flame)。
(整理)科研读书笔记
一、派尔斯(Peierls)相变1、聚乙炔的结构(1)聚乙炔是由CH单体聚合而成的平面型线型共轭高分子。
(2)聚乙炔的常见同分异构体:反式:两个CH单体组成一个原胞,双键两端的两个氢原子位于双键的两侧,反式异构体是热力学的稳定状态。
顺式:四个CH单体组成一个原胞,双键两端的两个氢原子位于双键的同侧。
在温度升高时,顺式会转变成为反式。
在保持相领两键之间的夹角是120度的情况下,有四种同分异构体:(3)聚乙炔薄膜的结构在电子显微镜下,聚乙炔薄膜是由混乱取向的细丝所组成,细丝的直径随着不同的聚合条件而定,每根细丝由千万个碳链组成,薄膜中细丝之间的空隙很大。
细丝中碳链上碳原子间的耦合性很强,碳链之间的耦合性很低,所以碳链基本上只能在单链上运动。
由于细丝之间的空隙很大,所以容易参杂,因为是插隙式的,所以能保持碳链的完整性。
2、一维体系的电导和派尔斯相变(1)价电子在聚乙炔中,每个碳原子有四个价电子,其中三个是sp2杂化轨道,第四个是2p轨道。
在sp2杂化轨道上的一个电子与z氢原子相连,另外两个分别与左右的碳原子相连形成σ键,σ键构成了聚乙炔的主链。
第四个电子是π电子,π电子可以在相邻碳原子之间跳跃,因此π电子可以导电。
(2)相变过程:一维体系物质的电导率随温度变化而变化的过程。
(3)派尔斯相变:当温度升高时,一维体系由绝缘体或半导体转变为导体的相变过程。
3、费米面(1)波数K:波长的倒数;(K=1/入=p/h)表示在1cm的长度中有多少波长。
(2) K 空间(动量空间):以K 为坐标轴的空间。
(3) 对于动量为p 的电子,取电子的运动方向为x 轴,则其波函数是平面波:px i P eL x1)(=ψ(4) 电子在长度为L 的直链中运动时,其波函数要满足周期性的边界条件(在边界上波函数值相等→Lmk =(m=0,1,2------)) (5) 费米动量:设一维体系的长度为L ,其中有N 个可以自由移动的电子,体系中的N 个电子按其能量的大小依次从K 小的状态向K 大的状态逐一填充在动量空间,N 个电子填充后,最大的动量为P F ,P F 就是费米动量。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Chemkin模型学习读书笔记一、模型总体介绍大型气相动力学计算软件包Chemkin(chemical kinetics)可以用来解决带有化学反应的流动问题,是燃烧领域中普遍使用的一个模拟计算工具。
该软件是1980 年美国Sandia 国家实验室Kee R. J. 等人开发并推出的,经几次完善发展,至今已开发出了第6个版本CHEMKIN 4.0.2。
chemkin有多种针对不同模型的应用程序,在4.0版本中共有23种计算模型,分6大类:○1封闭的0维反应器:包括封闭的内燃发动机模型(closed internal combustion engine simulator),封闭的同质反应器(closed homogeneous batch reactor),封闭的部分搅拌反应器(closed partially stirred reactor)和封闭的等离子反应器(closed plasma reactor)。
顾名思义,此类模型没有出入反应流,只根据反应器的初状态计算其末状态的参数。
○2开放的0维反应器:包括良搅拌反应器PSR(perfectly stirred reactor),等离子良搅拌反应器(plasma PSR)和部分搅拌反应器(partially stirred reactor)。
此类模型需要定义入流的流量、种类和温度等信息,计算后会给出出口的状态参数。
○3流动反应器:包括栓塞流反应器(plug-flow reactor)、等离子栓塞流反应器(plasma plug-flow reactor)、平面层流反应器(planar shear flow reactor)、圆柱形通道内的层流反应器(cylindrical shear flow reactor)和蜂窝整料反应器(honeycomb monolith reactor)。
此类模型考虑流动中的化学反应,主要是表面反应。
○4火焰模拟反应器:包括预混层流燃烧器-稳定的火焰(premixed laminar burner-stabilized flame)、预混层流火焰-火焰速度计算(premixed laminarflame-speed calculation)、和扩散/预混对撞火焰(diffuseion or premixedopposed-flow flame)。
○5多晶片沉积滞留CVD反应器:停滞流CVD反应器(stagnation flow reactor)和旋转盘CVD反应器(rotating disk CVD reactor。
○6爆管反应器:通用瞬间爆轰反应器(normal incident shock)和通用反射爆轰反应器(normal reflected shock)。
此外还可独立进行化学平衡和相平衡的计算及对反应机理模型进行分析。
下面就其中一部分模型进行详细介绍。
二、部分模型的详细介绍1、PSR模型良搅拌反应器(Perfectly Stirred Reactor,PSR)计算模型常应用于化学反应基础研究中。
PSR是连续理想混合流动模型的理想混合反应器,物料以稳定的流量进入反应器后,瞬间就在整个反应器内分散均匀并与器内原存留的物料完全混合,因此反应物转化为生成物的速率由化学反应速率控制而不是混合过程。
这样的假设减小了计算强度,容器内的燃烧过程能够用详细化学反应机理来描述。
理想混合流动的特点是:(1)器内以及出口物料的组成和温度等参数均匀一致,且不随时间、空间而变化;(2)各物料微元在器内的停留时间不尽相同,存在停留时间分布。
如图1所示。
图1 理想混合式流动质量控制方程为:()*0(1,2,,)k k k k m Y Y VW k K ω--== (1-1)能量控制方程为: ()**10Kk k k k k m Y h Y h Q =-+=∑ (1-2)在上述方程中,m表示反应气体的质量流率(g/s);k ω 表示第k 种组分的摩尔生成速率(mol/(cm 3s));Y k 表示第k 种组分的质量分数;W k 表示第k 种组分的摩尔质量(g/mol);V 是搅拌器的容积(cm 3);h k 是第k 种组分的比焓(J/g);Q 是反应器的散热速率(J/s)。
上标*表示进口参数。
滞留时间(Residence time )τ由搅拌器的体积和气体的质量流速确定:V mρτ= (s) (1-3) 其中质量密度ρ通过理想气体状态方程计算得到:PW RTρ= (1-4) 上述公式中P 表示压力;R 是通用气体常数(J/mol ⋅K);T 是温度(K);W 是混合物的平均摩尔质量(g/mol)。
2、Plug-flow 模型Plug-flow 是连续理想排挤流动模型,理想排挤反应器,物料以稳定的流量由反应器的一端流入反应器后,各物料微元沿流动方向齐头并进,完全没有轴向混合与扩散,就好像活塞在气缸里向前平推一样,如图2所示。
图2 理想排挤式流动活塞流模型的特点是:(1)在与流动方向垂直的任意截面上各点,物料的流速、浓度、温度及停留时间等完全一样;(2)物料的浓度、温度等各参数沿流动方向递变;(3)在每一截面上物料各参数都不随时间而变化。
在管段流中,已被接受的理想模型是PFR ,其假设没有混合在轴向方向但在横向混合充分。
它也被展示成没有轴向可实现的反应物转化最大。
同样地,缺少横向梯度意味着没有质传递限度,再一次加强反应器性能。
除了这些实用的优点外,PFR 反应器计算非常快捷,因为它是使用初命令ODE ’s 模型,不需要传递其他特性。
调节PFR 反应器性能方程式就是简化质传递、能量传递、动量传递的一半模式。
他们可以衍生出很多在流向中微元段的平衡,规定在横向上没有变量,任何质量的轴向扩散相比于相关对流项都被忽略。
这样,所有的气体质平衡(连续性方程)可表达为:质量连续方程:∑∑===++g Kk k m k Mm m i W s a dx d uA dx du A dx dA u 1,1, ρρρ (2-1) 这里ρ是质浓度,u 是轴向气流速,包括K g ;W k 是k 的摩尔重量,S k 表示所有的表观方应器中这种物质的摩尔产率,质量A 和a i,m 是截面面积和材料单位长度的有效内表面积。
A 和a i,m 可作为x 的随机函数。
式2-1简单描述了气体质流速在反应器中可以作为生成或者消耗结果反应所有物质。
相似方程也可以独立列出。
气相转化方程:⎪⎪⎭⎫ ⎝⎛+=+∑∑∑===g g K k k m i m k k K k k m k M m m i k k A a s W W s a Y dx dY uA 1,,1,1,ωρ (2-2) 这里Y k 是物质k 质量分数,ωk 是同类气体反应的摩尔产率。
这些反应不能改变总的气体质量,但可改变组分。
能量平衡:k K K k k m k M m m i e e K k k m k M m m i K k k k P K k k k h W s a q a W s a u Y h dx du u dx dT C dx dY h uA g b g g g ∑∑∑∑∑∑======-=⎪⎪⎭⎫ ⎝⎛++⎪⎪⎭⎫ ⎝⎛++',1,1,1,12121 ρ(2-3)h K 是物质k 的比热焓,是单位气体质量的平均热容,T 是相对气体温度。
在正确的求和中s k,m 是固体物质k 在物质临界面的体积摩尔产率。
大量的与临界的物质区别在1.1章和第4章被讨论。
式2-3描述了流动气体总能量变化引发从外墙环境的热通量变化Qe ,和散落固体的焓聚集。
如果式2-3没包含临界面物质的焓,那么这个公式就无任何意义。
气体的动量方程表示压力、惯性的、粘滞力和临界反应动量之间的平衡。
因而,动量方程:01,1,=+++∑∑==g K k k m k M m m i W s a u dx dF dx du uA dx dP A ρ (2-4) P 是绝对压力,F 是管壁作用在气体上的压力,将在下面被讨论。
压力与密度理想气体状态方程有关,如式2-4所示。
由于不均匀物质产率一般来说取决于临界面的组分和气体的组分,现在需要方程确定的临界面物质位置分数。
假设这些物质是固定的,固态转化方程简写成式2-5。
临界面物质守恒方程可应用于每种表面材料临界相中的每一种物质。
表面节点物质转化方程:0=k sl s f s K K k ,...,= (2-5) 微分/代数的联系包括了相互依赖的变量p 、u 、T 、P 、t 、Y k 以及Z k 。
函数W ,h k ,P C ,k ω,m k s , 都可以用这些变量表达,并且可以通过访问气态动力学和表面动力学子程序库得到。
数值A (x )、a i ,m (x )以及a e (x )由反应器的几何条件来确定。
这样就只剩下Q e 和F 有待确定。
对于活塞流以及相关的反应模型,有几种不同的选择可以处理反应器的能量平衡:1.限制温度。
反应器可以看作是等温的,或者轴向温度曲线可以指定为用户定义的分段线性曲线,或者可以通过用户子程序指定任意的温度曲线;在所有限制温度的情况下,方程10-3是不能得到解决的。
2.绝热反应器或者Qe =0。
在这种状态下能量方程就可以解决了。
3.指定热损失。
可以是恒定的热流量,或者是用户指定的热流量关于距离的分段线性函数,定义为Qe (x )。
4.特殊的热传递效率。
每种优化Qe (x )是按照周围温度和总体热传递效率而定的。
(2-8)和U 都需由用户提供。
粘滞力按照如下摩擦因素书写。
(2-9)摩擦系数可以按局部雷诺数表示。
(2-10)D 是管段直径,μ是气体粘度。
对层流来说(雷诺数=2100)圆管的分析结果是:(2-11)对于湍流可以使用近似的Blasius 公式(2-12)这种方法仅仅只是近似的,尤其是对于非圆形导管,但是通常在气态反应器中粘滞力是非常次要的。
为了保持这种状态,同时也为了避免不得不计算传输特性,气体粘性的计算通过按(T/T in)0..5的比例缩放进口处数(由用户提供)值来确定,同时还要忽略成分间的相互依赖性。
还必须指定反应器的初始(进口)条件。
显然,当x=0时,p、u、T、P和Y k的值应该是已知的,或者可以很容易的从问题的描述、理想气体定律、反应器几何条件中得到,当然,此时t=0。
由于控制方程中没有Z k的派生,似乎对于他们来说不需要初始条件。
然而,在反应器的入口,所使用的瞬时解决者需要变量Z k的一系列一致的派生。
对于活塞流的模拟,这可以在单独的初步计算中完成,在这个过程中解决了一套虚拟的瞬时方程,即联立解方程2-6与方程2-13,直到达到稳定状态。
(2-13)这里是物质k的占有率,是题目中总的相浓度。
式2-13的初值一般选取很随意(除非是复合稳态的),尽管更好的猜测可能使得其会更好的收敛。
