配位化学练习题5
配位化学习题

二、简答题 1.八面体型配合物[Cr(en)3]3+ 和[Ni(en)3]2+ 的中心原子分别为d3和d8电子构型,它们CFSE 都是–1.2∆O,能否说二者稳定性相同?为什么? 2.请画出[CoCl3(NH3)3]+ 的所有几何异构体。 3.[Fe(H2O)6]2+为顺磁性, 而[Fe(CN)6]4–为反 磁性, 请分别用价键理论和晶体场理论解释该 现象。
将化学组成为cocl34nh3的紫色固体配制成溶液向其中加入足量的agno3溶液后只有13的氯从沉淀析出
习题
一.选择题 1.在配合物 .在配合物[(RuCl5)2O]4– 和[PtCl3(C2H4)]– 中, 中心原子的配位数分别是 A、5.5,5; B、 5.5,4; C、6,5; D、6, 、 , ; 、 , ; 、 , ; 、 , 4。 。 2.将化学组成为 .将化学组成为CoCl3·4NH3的紫色固体配制成 的紫色固体配制成 溶液,向其中加入足量的AgNO3溶液后,只有 溶液后, 溶液,向其中加入足量的 溶液后 1/3的氯从沉淀析出。该配合物的内界含有 的氯从沉淀析出。 的氯从沉淀析出 A、2个Cl–和1个NH3; B、2个Cl–和2个NH3; 、 个 和 个 ; 、 个 和 个 ; C、2个Cl–和3个NH3; D、2个Cl–和4个NH3。 、 个 和 个 ; 、 个 和 个 。
4.(1)欲使0.10molAgCl溶解在1升氨水中,的浓 度至少应多大? (2)欲使0.10molAgI溶解在1升氨水中,的浓度 至少应多大? Ksp(AgCl)=1.56x10-10; Ksp(AgI)=1.5x10-16;K不稳=6.2x10-8
5.已知: Co3++e→ Co2+ Eθ=1.82V 已知: 已知 → O2+4H++4e→ 2H2O Eθ =1.23V → NH3·H2O→ NH4++OHKb=1.8×10-5 → × Co3++6NH3→ [Co(NH3)6]3+ K稳 稳 =1.6×1035 × Co2+ +6NH3→ [Co(NH3)6]2+ K稳=1.6×105 稳 × 判断: 判断: (1)溶液中 溶液中[H+]=1.0mol·l-1,空气 2=20.26kPa, 空气Po 溶液中 空气 能够将氧化Co 能够将氧化 2+ → Co3+. (2)设NH3·H2O浓度为 浓度为1.0mol·l-1,空气能否将 设 浓度为 [Co(NH3)6]2+ → [Co(NH3)6]3+
配位化合物练习题配位键配位数与配位化合物的命名

配位化合物练习题配位键配位数与配位化合物的命名配位键是指形成配位化合物的中心金属离子与配体之间的化学键。
配位数是指配位化合物中金属离子与配体之间的键的数量。
命名配位化合物的规则根据配体中的原子数、电荷和官能团等因素来确定。
以下是一些配位化合物练习题,以及配位键、配位数和命名的相关内容。
练习题一:以下配位化合物中,指出配位键的类型和配位数:1. [Co(NH3)6]Cl32. [Fe(CN)6]4-3. [Cu(NH3)4(H2O)2]2+练习题二:请根据以下配位化合物的配位数,给出它们的命名:1. [PtCl4]2-2. [Cu(NH3)2(H2O)2]2+3. [Fe(CO)5]练习题三:请给出以下配位化合物的化学式和它们的命名:1. Tetrachloridocobaltate(II)2. Hexaamminecobalt(III) chloride3. Potassium hexacyanidoferrate(III)解析:练习题一:1. [Co(NH3)6]Cl3配位键类型:配位键类型是金属离子和配体之间的键,此处是配体是氨(NH3),氨和钴(Co)之间形成了配位键。
配位数:配位数是指金属离子与配体之间键的数量,这里配位数为六,因此配位复合物的名称是六配位配合物。
2. [Fe(CN)6]4-配位键类型:配体是氰化物(CN),氰化物和铁(Fe)之间形成了配位键。
配位数:配位数为六,因此配位复合物的名称是六配位配合物。
3. [Cu(NH3)4(H2O)2]2+配位键类型:配体是氨和水,氨和铜(Cu)以及水和铜之间形成了配位键。
配位数:配位数为六,因此配位复合物的名称是六配位配合物。
练习题二:1. [PtCl4]2-配位数为四的配位化合物命名为四氯金(II)。
2. [Cu(NH3)2(H2O)2]2+配位数为六的配位化合物命名为二氨二水铜(II)。
3. [Fe(CO)5]配位数为五的配位化合物命名为五羰基铁。
配位化学试题及答案

配位化学试题及答案一、选择题(每题2分,共10分)1. 配位化学中,配体与中心原子通过什么键结合?A. 离子键B. 共价键C. 配位键D. 氢键答案:C2. 以下哪个不是配位化合物的特点?A. 含有配位键B. 含有金属离子C. 含有非金属离子D. 含有配体答案:C3. 配位化学中,配位数指的是什么?A. 配体的数量B. 中心原子的电荷数C. 配体的电荷数D. 配体的价电子数答案:A4. 以下哪种配位化合物的几何构型是八面体?A. [Co(NH3)6]3+B. [Fe(CN)6]4-C. [Ni(CO)4]D. [PtCl6]2-答案:B5. 配位化学中,内球络合物与外球络合物的区别是什么?A. 配体的种类不同B. 配位键的数目不同C. 配位键的强度不同D. 配位键的类型不同答案:C二、填空题(每题2分,共10分)1. 在配位化学中,中心原子与配体之间的键被称为________。
答案:配位键2. 配位化合物的化学式中,通常用方括号表示________。
答案:配位离子3. 配位化学中,配体与中心原子之间的键角通常小于________。
答案:180度4. 配位化合物的命名中,配体的名称通常放在中心原子的名称________。
答案:之前5. 配位化学中,配体的配位能力与其________有关。
答案:电子密度三、简答题(每题5分,共10分)1. 简述配位化学中的配位键形成机制。
答案:配位键的形成机制是指配体向中心原子提供孤对电子,而中心原子提供空轨道,两者通过共享电子对形成配位键。
2. 描述一下配位化学中的几何异构现象。
答案:在配位化学中,几何异构是指具有相同化学式但不同空间排列的配位化合物。
例如,[Co(NH3)4Cl2]Cl·H2O可以存在两种不同的几何异构体:顺式和反式。
四、计算题(每题10分,共20分)1. 已知一个配位化合物的化学式为[Cu(NH3)4]SO4,计算其中心原子Cu的氧化态。
化学配位键练习题

化学配位键练习题化学配位键是指金属离子与周围配体之间的化学键。
配位键的形成是由于配体中的一个或多个可以提供一个或多个电子对的位点与金属离子形成了稳定的化学键。
掌握化学配位键的概念以及常见的结构类型对于理解化学反应、催化剂的设计和金属材料的性质等方面都具有重要意义。
下面是几个化学配位键的练习题,通过回答这些问题可以检验你对该知识点的掌握程度。
1. 以下哪种物质中存在着金属配位键?a) 氯气 (Cl2)b) 氧气 (O2)c) 硫酸 (H2SO4)d) 硝酸 (HNO3)2. 以下哪种配体可以形成多个配位键?a) 水 (H2O)b) 氨 (NH3)c) 碳一氧化物 (CO)d) 乙醇 (C2H5OH)3. 配位键中,金属离子通常作为[ ]提供电子对。
a) 电子受体c) 电荷中心d) 键的中心4. 以下哪个配体是经典的两电子供体?a) 水 (H2O)b) 氨 (NH3)c) 乙醇 (C2H5OH)d) 二氧化硫 (SO2)5. 以下哪个金属离子可形成八配位数的配合物?a) 铁 (Fe2+)b) 锌 (Zn2+)c) 铜 (Cu+)d) 铝 (Al3+)6. 对于配位化合物Na[Ag(CN)2],配位键中的氰离子作为什么类型的配体?a) 单电子供体b) 双电子供体c) 三电子供体7. 哪种配体是Lewis碱?a) 水 (H2O)b) 氰化物 (CN-)c) 溴离子 (Br-)d) 铵离子 (NH4+)8. 已知配合物[Co(Cl)4]2-的配位键类型是:a) 构成离子键b) 构成金属键c) 构成共价键d) 构成氢键9. 根据VSEPR理论,以下哪个配合物具有线性形状?a) [Ni(CO)4]b) [CuCl4]2-c) [Pt(NH3)4]2+d) [Fe(CN)6]4-10. 下面哪个化学反应是指通过配位键断裂或形成,从而改变配合物的化学性质?a) 氧化反应b) 还原反应c) 配位置换反应d) 加成反应以上是化学配位键练习题,希望能够帮助你巩固和深化对这一知识点的理解。
配位化学试题
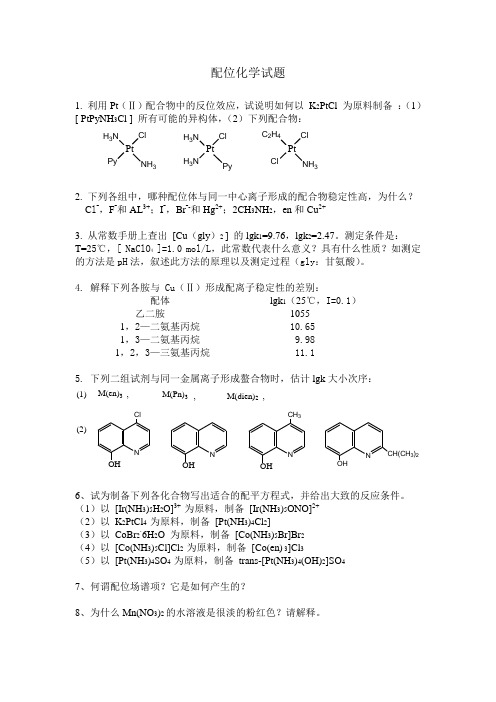
配位化学试题1. 利用Pt (Ⅱ)配合物中的反位效应,试说明如何以 K 2PtCl 为原料制备 :(1)[ PtPyNH 3Cl ] 所有可能的异构体,(2)下列配合物: PtCl NH 3H 3N Py Pt Cl Py H 3N H 3N Pt ClNH 3C 2H 4Cl2. 下列各组中,哪种配位体与同一中心离子形成的配合物稳定性高,为什么? C l -,F -和AL 3+;I -,Br --和Hg 2+;2CH 3NH 2,en 和Cu 2+3. 从常数手册上查出 [Cu (gly )2 ] 的lgk 1=9.76,lgk 2=2.47。
测定条件是: T=25℃,[ NaClO 4 ]=1.0 mol/L ,此常数代表什么意义?具有什么性质?如测定的方法是pH 法,叙述此方法的原理以及测定过程(gly :甘氨酸)。
4. 解释下列各胺与 Cu (Ⅱ)形成配离子稳定性的差别:配体 lgk 1(25℃,I=0.1) 乙二胺 10551,2—二氨基丙烷 10.651,3—二氨基丙烷 9.981,2,3—三氨基丙烷 11.15. 下列二组试剂与同一金属离子形成螯合物时,估计lgk 大小次序:M(en)3M(Pn)3M(dien)2(1),,,(2)N OH Cl N OH N OH CH 3NOH CH(CH 3)26、试为制备下列各化合物写出适合的配平方程式,并给出大致的反应条件。
(1)以 [Ir(NH 3)5H 2O]3+ 为原料,制备 [Ir(NH 3)5ONO]2+(2)以 K 2PtCl 4 为原料,制备 [Pt(NH 3)4Cl 2](3)以 CoBr 2·6H 2O 为原料,制备 [Co(NH 3)5Br]Br 2(4)以 [Co(NH 3)5Cl]Cl 2 为原料,制备 [Co(en) 3]Cl 3(5)以 [Pt(NH 3)4SO 4 为原料,制备 trans-[Pt(NH 3)4(OH)2]SO 47、何谓配位场谱项?它是如何产生的?8、为什么Mn(NO 3)2的水溶液是很淡的粉红色?请解释。
普通化学-配位化合物章节题

第5章配位化合物一、单项选择题5.1 下列分子或离子能做螯合剂的是( )。
A.H 2N—NH 2B.CH 3COO —C.HO -OHD.H 2NCH 2CH 2NH 2 5.2利用生成配合物而使难溶电解质溶解时,下面哪一种情况最有利于沉淀的溶解( )。
A. f K θ愈大,sp K θ愈小B. f K θ愈小,sp K θ 愈大 C. f K θ愈大,sp K θ也愈大 D. f K θ≥sp K θ5.3 加下列哪种物质能增加AgCl 在水中的溶解度( )。
A.NaClB.AgNO 3C.NH 3·H 2OD.CaCl 2 5.4 摄影时用Na 2S 2O 3洗未曝光AgBr ,再用Na 2S 回收洗出的银,涉及到的两种反应分别是( )A.氧化还原、沉淀B. 氧化还原、配位C.配位、沉淀D. 配位、氧化还原5.5 若用NH 4SCN 测定Co 2+时,为了防止Fe 3+干扰,最好是加( )。
A.NaFB.NaBrC.NaClD.NaI 5.6在-(en)])O [Co(C 242中,中心离子的配位数为( )。
A.2B.4C.5D.65.7 下列各物质能在强酸性介质中稳定存在的是( )。
A.[HgI 4] 2-B. [Zn(NH 3)4]2+C.[Fe(C 2O 4)3]3-D.[Ag(S 2O 3)2]3- 5.8 FeCl 3和KSCN 的混合溶液中,加入足够的NaF ,其现象是( ) A.变成无色 B.颜色加深 C.产生沉淀 D.颜色变浅5.9 设[HgI 4]2-的f K θ=K 1θ,[HgCl 4]2-的f K θ=2K θ,则下列反应:[HgCl 4]2-+4I -=[HgI 4]2-+4Cl -的平衡常数为( )A. K 1θ+2K θB. K 1θ/2K θC. 2K θ/ K 1θD. K 1θ×2K θ5.10 向[Cu(NH 3)4]2+水溶液中通人氨气,则( )A.K +234f,Cu(NH)θ增大 B. K +234f,Cu(NH )θ减小 C.c (Cu2+)增大 D.c (Cu 2+)减小二、填空题5.1氯化二氯·三氨·一水合钴(Ⅲ)的化学式为 , 配体是 ,配位原子是 ,配位数是 。
配位化学练习题

配位化学练习题配位化学是无机化学的重要分支,研究的对象是配位化合物和配位反应。
配位化学主要研究金属离子与配体之间的相互作用,以及在配位化合物中金属离子的周围有哪些配体。
以下是一些配位化学的练习题,用以帮助读者巩固相关知识。
题目一:给定以下化学方程式,请推导出反应类型,并写出反应物和生成物的化学式。
1. AgNO3 + NaCl →2. CuSO4 + NH3 →3. FeCl3 + KOH →题目二:根据以下配位化合物的谱系图,请回答以下问题。
1. 对于配位数为4的配合物,属于以下哪种晶体场理论?2. 高自旋和低自旋的配合物分别具有什么样的差异?3. 配体场强度增加,配体键长和配位键数会发生什么变化?4. 对于给定的配合物,如果配位键数为6,那么该配合物的中心离子是什么?题目三:结合以下反应机理,请写出反应的平衡常数表达式。
1. Co(H2O)6 2+ + 6NH3 ⇌ Co(NH3)6 2+ + 6H2O2. NH3 + H2O ⇌ NH4+ + OH-3. Cu(H2O)6 2+ + 4Cl- ⇌ [CuCl4]2- + 6H2O题目四:以下是一些配位化合物的常见名称,请根据化学式给出其对应的名称。
1. Fe2(SO4)32. K3[Fe(CN)6]3. [Co(NH3)4Cl2]Cl题目五:给定以下化学方程式,请写出反应的电子方程式和平衡常数表达式。
1. Co(H2O)6 2+ + [Cr(CN)6]4- → Co(CN)6 4- + [Cr(H2O)6]2+2. [Cu(NH3)4]2+ + 4Br- → [CuBr4]2- + 4NH3题目六:结合以下反应,回答以下问题。
1. 配位化合物的颜色与什么因素有关?2. 过渡金属配合物为什么可以具有催化性质?3. 配合物中的中心离子的电荷数会如何影响配合物的稳定性?4. 配体的选择如何影响配位化合物的形状?这些练习题覆盖了配位化学的不同方面,包括反应类型、配位反应机理、命名和电子结构等。
配位化学试题及答案

配位化学试题及答案一、选择题(每题2分,共10分)1. 下列哪项不是配位化合物的特点?A. 含有中心原子或离子B. 含有配位键C. 含有离子键D. 含有配体答案:C2. 配位化合物的几何构型通常由什么决定?A. 配体的电荷B. 配体的数目C. 配体的电子排布D. 中心原子的氧化态答案:B3. 配位化学中,路易斯碱是指什么?A. 能够提供电子的分子或离子B. 能够接受电子的分子或离子C. 能够提供空轨道的分子或离子D. 能够接受空轨道的分子或离子答案:B4. 下列哪种配体是单齿配体?A. 乙二胺(en)B. 1,3-丙二胺(pn)C. 环己二胺(cn)D. 四齿配体答案:A5. 配位化合物的命名中,配体的名称通常放在什么位置?A. 中心原子的前面B. 中心原子的后面C. 配位化合物的前面D. 配位化合物的后面答案:A二、填空题(每题2分,共10分)1. 配位化学中,中心原子或离子与配体之间形成的化学键称为______。
答案:配位键2. 一个中心原子或离子最多可以与______个配体形成配位键。
答案:63. 配位化合物的配位数是指______。
答案:中心原子或离子周围配体的数量4. 配位化合物的命名中,配体的数目通常用希腊数字表示,其中“二”表示______。
答案:二5. 配位化合物的命名中,配体的电荷通常用罗马数字表示,其中“Ⅱ”表示______。
答案:+2三、简答题(每题5分,共20分)1. 简述什么是内界和外界,并举例说明。
答案:内界是指配位化合物中中心原子或离子与配体形成的配位单元,外界是指配位单元以外的部分。
例如,在[Co(NH3)6]Cl3中,[Co(NH3)6]是内界,Cl3是外界。
2. 什么是螯合配体?请举例说明。
答案:螯合配体是指能够通过多个配位点与中心原子或离子形成配位键的配体。
例如,乙二胺(en)可以与金属离子形成螯合配位化合物。
3. 配位化合物的稳定性与哪些因素有关?答案:配位化合物的稳定性与中心原子或离子的电荷、配体的类型、配位数以及配体与中心原子或离子之间的配位键强度等因素有关。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
配位化学练习题
1.对于配合物中心体的配位数,说法不正确的是()
(A) 直接与中心体键合的配位体的数目(B) 直接与中心体键合的配位原子的数目
(C) 中心体接受配位体的孤对电子的对数(D) 中心体与配位体所形成的配价键数2.在[Co(En)(C2O4)2]-络离子中,中心离子的配位数为()。
A.2;B.4;C.6;D.5;E.3 3.CoCl3·4NH3用H2SO4溶液处理再结晶,SO 2
可以取代化合物中部分Cl-,但NH3的
4
物质的量不变,用过量AgNO3处理该化合物溶液,每摩尔钴可得1摩尔AgCl沉淀,这化合物是()
A、[Co(NH3)4]Cl3
B、[Co(NH3)4Cl]Cl2
C、[Co(NH3)4Cl2]Cl
D、[Co(NH3)4Cl3]
4.下列关于螯合物的叙述正确的是( )
A、有两个以上配位原子的配体均生成螯合物
B、螯合物通常比具有相同配位原子的非螯合配合物稳定得多
C、螯合物的稳定性与环的大小有关,与环的多少无关
D、起螯合作用的配体为多齿配体称为螯合剂
5.CoCl3·4NH3用H2SO4溶液处理再结晶,SO2-4可以取代化合物中部分Cl-,但NH3的物质的量不变,用过量AgNO3处理该化合物溶液,每摩尔钴可得1摩尔AgCl沉淀,这化合物是( )
A、〔Co(NH3) 2〕Cl3
B、〔Co(NH3) 2Cl〕Cl2
C、〔Co(NH3) 2Cl2〕Cl
D、〔Co(NH3) 2Cl3〕
6.下列化合物中,能作为有效螯合剂的是( )
A、H2N—NH2
B、H2O2
C、乙二胺
D、
7.在FeCl3与KSCN的混合液中加入过量NaF,其现象是()
(A) 产生沉淀(B) 变为无色(C) 颜色加深(D) 无变化
8.下列物质呈抗磁性的是()
(A) O2(B) O3(C) NO (D)Cr(H O)
3
26
二.填空题
1.命名:K[PtCl3NH3] K4[Fe(CN)6]
中心原子的电荷数,配位数。
2.Mn(acac)3的磁矩为4.90 B.M.,试指出:
(1) 中心原子氧化态,(2) 中心原子的配位数,
(3) 中心原子未成对电子数,(4) 配合物的空间构型,
(5) 中心原子的杂化轨道类型。
注:acac-为乙酰丙酮根CH3C CH C CH3
O O-
3. 用氰化物试剂做实验,废液应该用、、等处理,如未经预处理便倒入废酸缸中,则会有剧毒产生。
4.某中心离子(或原子)的配位数,就是直接同该中心离子(或原子)。
5.当分裂能Δ>电子成对能P时,易形成自旋配合物。
6.配位共价键形成的时候,中心原子提供,配位原子提供
7.若中心原子分别采用SP3和dSP2杂化与配体中的配位原子成键,则中心原子的配位数均为,所形成的配离子类型为和,配离子的空间构型为和。
8.磁矩的测量证明,〔Co(NH3)6〕2+有3个未成对电子,而[Co(CN)6〕3-离子已没有未成对电子,由此说明,其中属内轨型配合物,其空间构型为;
这也说明,两者比较其中更稳定。
9.配合物CrCl3·6H2O的水溶液加入溶液,只能沉淀出1/3的离子,所以该配合物化学式应写成,中心离子的配位数为,其分子空间构型为。
10.已知CoCl3·x NH3的配合物有两种同分异构体。
若用AgNO3沉淀0.05 mol CoCl3·x NH3
中的氯离子,其中一种同分异构体消耗了0.15 mol的AgNO3;另一种则消耗了0.10 mol的AgNO3,这两种配合物的化学式分别是和。
11.实验测得Fe(CN)64-和Co(NH3)63+均为反磁性(磁矩等于0)它们的空间构型为,其杂化轨道类型为,。
12.实验测得Fe(H2O)63+和Fe(CN)63-的磁矩差别极大,其中CN-为强场配体,它们的空间构型为,其杂化轨道类型为,。
13.在水溶液中Fe3+易和K2C2O4生成K3[Fe(C2O4)3],此化合物应命名为。
Fe3+的配位数为,配离子的空间构型为。
此配合物具有很强的顺磁性,中心离子磁矩为5.9 B.M.,按晶体场理论,中心原子d电子排布为。
14.配合物[Co(NH3)4(H2O)2](SO4)3的内界是,外界是,配位体是,配位原子是,中心原子的配位数是。
15.配合物PtCl4.2NH3的水溶液不导电,加入硝酸银溶液也不产生沉淀,滴加强碱也无氨气放出,所以它的化学式是命名为。
16.Cu(NH3)42+的K稳_ 于Cu(En)22+的K稳,是由于后者具有效应。
三、计算讨论题
1. 根据实测磁矩,推断下列螯合物的空间构型并指出是内轨还是外
轨型配合物;并说明在晶体场中的高低自旋状态。
[Co(CN)6] 3-(μ=1.8) 和[Co(en)3] 2+(μ=3.82)
2.试用价键理论和晶体场理论阐述配合物的稳定性。
已知[Fe(CN)6]3-(μ=2.3)和[FeF6]3-(μ=5.9)
3.利用配合物的稳定常数,判断下列配体取代反应的方向和进行的
程度。
HgCl42-+ 4I-……→HgI42-+ 4Cl-
已知:Ks[HgCl4]2-=1.6×1015 ,Ks[HgI4]2-= 7.21×1029。
