初三化学20道计算题
九年级化学化学计算题题20套(带答案)及解析
九年级化学化学计算题题20套(带答案)及解析一、中考化学计算题1.小王同学为了测定某Na2CO3溶液中溶质的质量分数,取10g该溶液于烧杯中,然后将400g澄清石灰水分四次加入,烧杯中沉淀的质量与每次加入澄清石灰水的质量关系如表。
请计算:第一次第二次第三次第四次加入澄清石灰水100100100100的质量/g生成沉淀的质量0.4m 1.0 1.0/g(1)表中m的值为_____。
(2)Na2CO3溶液中溶质的质量分数_____(写出计算过程)。
【答案】0.8 10.6%【解析】【分析】第一次生成沉淀0.4g,而第三次不到0.4g的3倍,则第二次应该为0.4g的二倍,所以m=0.4g×2=0.8g,根据碳酸钙的质量和对应的化学方程式求算碳酸钠溶液中溶质的质量分数。
【详解】由分析可知,m=0.4g×2=0.8g设原Na2CO3溶液中溶质的质量分数为x。
106100=10g?x 1.0gx=10.6%答:(1)表中的m的值为 0.8。
(2)原Na2CO3溶液中溶质的质量分数是10.6%。
2.将含有杂质(不溶于水)的氯化钡样品12.5g放入39.6g水中充分搅拌,完全溶解后过滤。
取20g滤液与足量的稀硫酸完全反应,得到4.66g沉淀。
请计算:①配制的氯化钡溶液中溶质的质量分数。
②样品中氯化钡的质量分数。
【答案】20.8%;83.2%【解析】【详解】①设参加反应的氯化钡的质量为x 。
2244BaCl +H SO =BaSO +2H 208233x4Cl.66g208233=x 4.66gx= 4.16g则配制的氯化钡溶液中溶质的质量分数为 :4.16g20g×100%=20.8% ②由于20g 溶液中含有4.16g 氯化钡,则可设样品中氯化钡的质量为y 。
则4.16g y=20g-4.16g 39.6gy=10.4g样品中氯化钡的质量分数为:10.4g12.5g×100%=83.2%答:①氯化钡溶液中溶质的质量分数为20.8% ②样品中氯化钡的质量分数为83.2%。
中考化学化学计算题题20套(带答案)

中考化学化学计算题题20套(带答案)一、中考化学计算题1.某粗盐样品仅含NaCl和MgCl2,为探究粗盐中NaCl的质量分数,某研究性小组取了10g样品,加适量水使其完全溶解后,加入20g 5%的氢氧化钠溶液,测得相关数据如图。
(1)请列式计算该粗盐样品中NaCl的质量分数为____________。
(2)当加入氢氧化钠溶液至ag时,此时所得溶液中溶质的质量是____________?【答案】90.5% 10.22g【解析】(1)根据氯化镁与氢氧化钠反应的化学方程式,由氢氧化镁的质量求出氯化镁的质量即可求出氯化钠的质量,再计算出粗盐样品中NaCl的质量分数;(2)根据图像分析解答。
(1)设样品中氯化镁的质量为x,反应生成氯化钠的质量为y。
MgCl2+ 2NaOH=Mg(OH) 2↓+2NaCl95 58 117x 0.58g y95581170.58x g y==x=0.95gy=1.17g样品中氯化钠的质量为10g-0.95g=9.05g该粗盐样品中NaCl的质量分数为9.0510gg×100%=90.5%(2)当加入氢氧化钠溶液至ag时,此时所得溶液中溶质的质量为10g-0.95g+1.17g=10.22g 答:(1)该粗盐样品中NaCl的质量分数90.5%;(2)当加入氢氧化钠溶液至ag时,此时所得溶液中溶质的质量10.22g。
2.现有碳酸钠和氯化钠的固体混合物12.6g,其中含氧元素4.8g,将该混合物加入到一定质量的稀盐酸中,恰好完全反应,得到137g氯化钠溶液。
计算:(l)原固体混合物中碳酸钠的质量分数(结果保留至0.1%)______;(2)所用稀盐酸中溶质的质量分数(结果保留至0.1%)______。
【答案】84.1% 5.7%【解析】【分析】【详解】(l)原固体混合物中碳酸钠的质量分数4.8g÷=10.6g;混合物中碳酸钠的质量分数为10.6g÷12.6g×100%≈84.1%;(2)设盐酸中溶质的质量为x,生成二氧化碳质量为y2322Na CO+2HCl=2NaCl+H O+CO106734410.6g x y↑1067344==10.6g x yx=7.3gy=4.4g所用稀盐酸中溶质的质量分数7.3g÷(137g+4.4g-12.6g)×100%≈5.7%3.为测定某大理石样品中碳酸钙(杂质不溶于水也不参与反应)的质量分数,某小组的同学进行了如下实验(水和氯化氢的挥发忽略不计):取12.5g样品研碎放入烧杯中,每次加入20.8 g稀盐酸后并用电子天平称量,记录实验数据如下。
初中化学计算题集锦

初中化学计算题集锦1. 已知24g镁完全反应,生成氧化镁的质量是多少克?(Mg + O₂→ MgO)2. 计算16g硫与足量氧气完全燃烧生成二氧化硫的质量。
(S + O₂→ SO₂)3. 若有3.01×10²³个水分子,求这些水的质量。
(H₂O)4. 98%的硫酸溶液500mL中含有多少摩尔的H₂SO₄?(密度为1.84g/cm³)5. 配制500mL 0.1mol/L的NaCl溶液,需要称取NaCl多少克?6. 现有20%的氢氧化钠溶液100g,稀释至5%的溶液,最终溶液的体积是多少毫升?7. 20g碳酸钙高温分解,理论上可以得到多少克二氧化碳气体?(CaCO₃→ CaO + CO₂)8. 已知锌与盐酸反应产生氢气0.2g,求参加反应的锌的质量。
(Zn + 2HCl → ZnCl₂ + H₂)9. 计算标准状况下,11.2L氧气的质量。
(O₂)10. 若将20g氢氧化钾(KOH)溶于水中配制成250mL溶液,该溶液的物质的量浓度是多少?11. 硫酸铜晶体CuSO₄·5H₂O中结晶水的质量分数是多少?12. 用含杂质20%的铁矿石500吨,最多能炼得纯铁多少吨?(杂质不参与反应)13. 将一定量的锌投入含有100g硫酸的溶液中,完全反应后剩余硫酸的质量为20g,求参加反应的锌的质量。
(Zn + H₂SO₄→ ZnSO₄+ H₂)14. 若有2mol氢气与足量氧气完全燃烧,理论上需要多少升氧气(标准状况下)?(2H₂ + O₂→ 2H₂O)15. 用20%的盐酸(HCl)溶液配制500mL 5%的盐酸溶液,需要多少毫升的20%盐酸溶液和多少毫升的水?16. 若10g镁条在空气中完全燃烧生成氧化镁,同时消耗了氧气的质量是多少克?17. 计算100mL 0.2mol/L的硝酸银溶液与足量氯化钠反应理论上可产生的沉淀AgCl的质量。
(AgNO₃ + NaCl → AgCl + NaNO₃)18. 有一未知浓度的盐酸溶液20mL,需用20mL 0.1mol/L的氢氧化钠溶液恰好完全中和,求该盐酸的物质的量浓度。
初三化学化学计算题题20套(带答案)

初三化学化学计算题题20套(带答案)1. 假设有一块铁块,其质量为56克。
求该铁块中含有的铁原子数。
解答:我们需要知道铁的摩尔质量。
铁的摩尔质量约为56克/摩尔。
因此,该铁块中含有的铁原子数为56克 / 56克/摩尔 = 1摩尔。
由于1摩尔物质中含有6.022 x 10²³个原子,所以该铁块中含有的铁原子数为1摩尔x 6.022 x 10²³个/摩尔= 6.022 x 10²³个。
2. 某化学反应中,反应物A和反应物B的化学计量比为2:3。
如果反应物A的质量为24克,求反应物B的质量。
解答:我们需要根据化学计量比计算出反应物B的质量。
由于反应物A和反应物B的化学计量比为2:3,所以反应物B的质量为24克x (3/2) = 36克。
3. 在一定条件下,一定量的氧气与一定量的氢气完全反应,了36克水。
求反应中消耗的氧气和氢气的质量。
解答:我们需要根据水的化学式H₂O计算出水的摩尔质量。
水的摩尔质量为2 x 1.008克/摩尔 + 16.00克/摩尔 = 18.016克/摩尔。
因此,36克水的物质的量为36克 / 18.016克/摩尔 = 2摩尔。
由于水的化学计量比为2:1,所以反应中消耗的氢气的物质的量为2摩尔,质量为2摩尔 x 2.016克/摩尔 = 4.032克。
同样,消耗的氧气的物质的量为1摩尔,质量为1摩尔 x 32.00克/摩尔 = 32.00克。
4. 某溶液中,溶质的质量分数为10%。
如果该溶液的质量为500克,求溶质的质量。
数为10%,即溶质的质量占溶液总质量的10%。
因此,溶质的质量为500克 x 10% = 50克。
5. 在一定条件下,一定量的氢气和一定量的氧气完全反应,了水。
如果反应中消耗的氢气的质量为2克,求反应中消耗的氧气的质量。
解答:我们需要根据水的化学式H₂O计算出水的摩尔质量。
水的摩尔质量为2 x 1.008克/摩尔 + 16.00克/摩尔 = 18.016克/摩尔。
初三化学考试 计算题25道(附答案)

25基础计算1.在一个实验室中发现一橡胶球可以漂浮在0.5mol/L的NaCl溶液表面,求该NaCl溶液的密度。
答案:1.018g/mL。
解析:根据阿威休斯定律得到:Fb=FgρVg=m*gρ=m/V=(Vg*g)/V=(Fg/Ag*g)/V=(4πr^3/3*g)/[(4/3)*π*r^3]=3/4*r*g=7.35*10^-5*g其中,Ag为橡胶球跟水接触的面积,r为橡胶球半径,g为重力加速度。
因此,NaCl溶液的密度为:ρNaCl=ρwater+ρball=1.000g/mL+7.35*10^-5*g/mL=1.018g/mL。
2.一种饱和食盐水的密度为1.20g/mL,问在哪个温度下它的浓度为26%。
答案:56.8°C。
解析:首先,要知道饱和食盐水在不同温度下的密度变化情况,参考表格得出如下数据:温度(°C)密度(g/mL)01.091101.078201.064301.049401.033501.015600.996700.975800.951900.9241000.895然后,根据浓度的定义可知:浓度=质量/总质量总质量=质量/浓度因为食盐水是饱和的,所以其浓度为100%。
设实验时食盐水的质量为m,则总质量为m/1.20,其中1.20为食盐水的密度。
根据题意,浓度为26%,所以食盐的质量为0.26*(m/1.20)。
由此0.26*(m/1.20)=m/(1.20+Δρ)其中Δρ为实验时食盐水的密度与需要求的密度的差值。
将参考表格中的数据代入上式计算,得到Δρ为0.325g/mL。
解方程得出:Δρ=0.325=0.26*m/(1.20+Δρ)m=68.45g因此,实验时食盐水的质量为68.45g。
而在哪个温度下其密度为1.20*0.26=0.312g/mL呢?查表可得,在56.8°C时,食盐水的密度约为0.312g/mL,因此答案为56.8°C。
初三化学化学方程式的计算题20套(带答案)含解析

初三化学化学方程式的计算题20套(带答案)含解析一、中考化学方程式的计算1.欲测得某块大理石中所含碳酸钙的含量,现取该大理石加入到足量稀盐酸中(杂质不与稀盐酸反应),产生CO 2的质量与稀盐酸的质量关系如图所示,请计算。
(1)该实验中最多制得CO 2的质量为_____。
(2)该大理石中所含碳酸钙的质量_____(写出计算过程)。
【答案】8.8g 20g【解析】【分析】碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳。
【详解】(1)由图像可知,该实验中最多制得CO 2的质量为8. 8g 。
(2)设该大理石中碳酸钙的质量为x3222CaCO +2HCl =CaCl +H O +CO 10044x 8.8g↑100x =448.8gx=20g答:大理石中所含碳酸钙的质量为20g 。
2.氯酸钾24.5g 加热完全反应后,制得氧气的质量是___________?【答案】9.6g【解析】【分析】【详解】解:设制得氧气的质量是x 。
232MnO 2KClO 2KCl +3O 2459624Δ.5g x ↑2459624.5g x=x=9.6g答:制得氧气的质量是9.6g。
【点睛】根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整。
3.过氧化钙(CaO2)常用于活鱼运输时的增氧剂,过氧化钙与水反应方程式为:2CaO2+2H2O═2Ca(OH)2+O2↑.某过氧化钙样品中含有少量不溶于水且不与水反应杂质,取该样品15.0g投入盛有108.0g水的烧杯中,缓慢搅拌,充分反应,最终收集到氧气质量为3.20g,计算该样品中过氧化钙的质量分数____(写出计算过程)。
【答案】96%【解析】【分析】【详解】解:设过氧化钙质量为x,22222CaO2H O=2Ca(OH)O14432x 3.2g14432=x 3.2g++↑x=14.4g,该样品中过氧化钙的质量分数是:14.4g15.0g×100%=96%,答:该样品中过氧化钙的质量分数是96%。
【化学】 中考化学化学计算题20篇(附带答案解析)

【化学】 中考化学化学计算题20篇(附带答案解析)一、中考化学计算题1.(1)若用98%的浓硫酸(密度为1.84g/mL )配制500g19.6%的稀硫酸,需要浓硫酸_____mL(结果精确到0.1)。
(2)向100g 碳酸钠溶液中慢慢滴加(1)中配制的稀硫酸,并用玻璃棒不断搅拌,测得pH 的变化情况如图。
玻璃棒的作用是_____,B 处溶液中的溶质有_____。
当稀硫酸和碳酸钠溶液恰好完全反应时,求所得溶液中溶质的质量分数。
_____(写出详细计算过程,结果精确到0.1%)【答案】54.3 使反应物充分接触并反应;使反应更充分;使反应更快(合理即可) Na 2SO 4、H 2SO 4 14.9% 【解析】 【分析】 【详解】(1)溶液稀释过程中溶质的质量相等,用98%的浓硫酸(密度为1.84g/mL )配制500g19.6%的稀硫酸,设需要浓硫酸的体积是x ,则x ×1.84g/mL ×98%=500g ×19.6%,解得x ≈54.3mL(2)向100g 碳酸钠溶液中慢慢滴加(1)中配制的稀硫酸,并用玻璃棒不断搅拌,测得pH 的变化情况如图。
玻璃棒的作用是使反应物充分接触并反应,B 处溶液显酸性,则稀硫酸有剩余,溶液中的溶质有生成的Na 2SO 4、剩余的H 2SO 4。
当稀硫酸和碳酸钠溶液恰好完全反应时,所得溶液是硫酸钠溶液,设所得溶液中溶质的质量是y ,生成二氧化碳的质量是z 。
23242422Na CO +H SO =Na SO +H O +981424410CO 19.0g yz6%⨯↑9810019.6%=142g y⨯,解得y=28.4g 9810019.6%=44g z⨯,解得z=8.8g 反应后所得溶液的质量为:100g+100g-8.8g=191.2g所得溶液中溶质的质量分数为:19282.41.g g×100%≈14.9%【点睛】溶液稀释过程中溶质的质量相等;化学方程式的计算,关键是根据化学反应方程式找出相关物质的质量关系,利用反应中物质的质量比不变进行列比例式计算,易错点是由质量比算数错误,所以这一步要仔细检查。
九年级化学化学计算题题20套(带答案)含解析
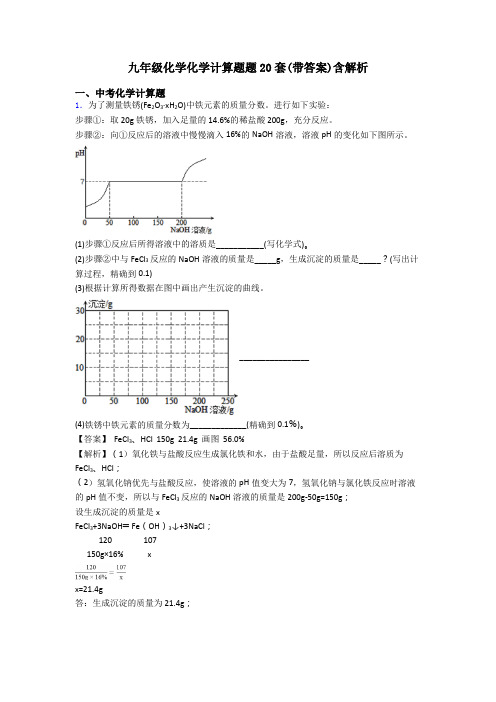
九年级化学化学计算题题20套(带答案)含解析一、中考化学计算题1.为了测量铁锈(Fe2O3·xH2O)中铁元素的质量分数。
进行如下实验:步骤①:取20g铁锈,加入足量的14.6%的稀盐酸200g,充分反应。
步骤②:向①反应后的溶液中慢慢滴入16%的NaOH溶液,溶液pH的变化如下图所示。
(1)步骤①反应后所得溶液中的溶质是___________(写化学式)。
(2)步骤②中与FeCl3反应的NaOH溶液的质量是_____g,生成沉淀的质量是_____?(写出计算过程,精确到0.1)(3)根据计算所得数据在图中画出产生沉淀的曲线。
________________(4)铁锈中铁元素的质量分数为_____________(精确到0.1%)。
【答案】 FeCl3、HCl 150g 21.4g 画图 56.0%【解析】(1)氧化铁与盐酸反应生成氯化铁和水,由于盐酸足量,所以反应后溶质为FeCl3、HCl;(2)氢氧化钠优先与盐酸反应,使溶液的pH值变大为7,氢氧化钠与氯化铁反应时溶液的pH值不变,所以与FeCl3反应的NaOH溶液的质量是200g-50g=150g;设生成沉淀的质量是xFeCl3+3NaOH═Fe(OH)3↓+3NaCl;120 107150g×16% xx=21.4g答:生成沉淀的质量为21.4g;(3)所以产生沉淀的曲线为;(4)所以铁锈中铁的质量分数为 =56%。
2.某化学兴趣小组对某铜锌合金样品进行探究实验,称取样品10.0 g,再用100.0 g稀硫酸溶液逐滴滴入,实验情况如图所示。
求:(1)铜锌合金中,Zn的质量分数是________。
(2)所用稀硫酸溶液中溶质的质量分数是__________?【答案】65% 19.6%【解析】试题分析:(1)铜锌合金与稀硫酸反应,其中只有锌与硫酸反应,故固体减少的量即为锌的质量=10g-3.5g=6.5g,则Zn%=6.5g/10g×100%=65%(2)解:设所用稀硫酸中溶质的质量分数为xZn+H2SO4=ZnSO4+H2↑65 986.5g 50gx65/98=6.5g/50gxx=19.6%答:锌的质量是65%;所用稀硫酸中溶质的质量分数为19.6%考点:合金、化学方程式计算3.某炼铝工厂想测定铝土矿中A12O3的含量,将矿石粉碎(其中杂质不溶于水,不与酸反应,且不含铝元素),进行如下实验,第一步反应的物质质量关系如坐标图所示:(1)上述实验过程中发生反应的化学方程式是_____;(2)根据已知条件列出求解第一步实验铝土矿中参加反应的A12O 3质量(x)的比例式_____ (3)铝土矿样品中A12O 3的含量_____;(4)坐标图中B 点所示溶液中溶质的化学式是_____;(5)在第二步实验结束后所得溶液中溶质的质量分数是_____(6)用1700t 此铝土矿冶炼得到540t 的铝,则在冶炼中,铝土矿的利用率是_____。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初三化学20道计算题
20道计算题,这可不是一件简单的事情啊!尤其对于初三的学生来说,学习化学可谓艰苦。
以下就是20道计算题,让我们一起来探索化学带来的乐趣吧!
1. 一定体积的氧气中含有多少分子?
根据摩尔定律可以得出:一定体积的氧气中含有大约 6.02 * 10^23子。
2.果把12克碳和32克氢结合在一起,可以得到多少克氢气?
根据化学知识,12克碳和32克氢可以结合组成CH4,在标准温度和压力下,可以得到16克氢气。
3. 一定体积的液态水中含有多少分子?
根据摩尔定律,一定体积的液态水中含有大约 3.02 * 10^23子。
4.果把24克铝和32克氧结合在一起,可以得到多少克Al2O3?
根据化学知识,24克铝和32克氧可以结合组成Al2O3,可以得到56克Al2O3。
5.果把3克氢,1克锂和2克氧结合在一起,可以得到多少克LiH2O?
根据化学知识,3克氢,1克锂和2克氧可以结合组成LiH2O,可以得到6克LiH2O。
6.度和体积之间是怎样的关系?
密度和体积之间是一种反比例关系,即体积增大,密度就会减小,反之亦然。
7.果把8克铀和16克氧结合在一起,可以得到多少克U3O8?
根据化学知识,8克铀和16克氧可以结合组成U3O8,可以得到24克U3O8。
8.果把6克氢,2克氯和1克氧结合在一起,可以得到多少克HClO?
根据化学知识,6克氢,2克氯和1克氧可以结合组成HClO,可以得到3克HClO。
9.的熔点是多少?
水的熔点是0°C,即32°F(华氏度)。
10.的沸点是多少?
水的沸点是100°C,即212°F(华氏度)。
11. 一定体积的金属中含有多少原子?
根据摩尔定律,一定体积的金属中含有大约 6.02 * 10^23子。
12. 一定体积的汽油中含有多少分子?
根据摩尔定律,一定体积的汽油中含有大约 6.02 * 10^23子。
13.果把6克氢,6克氮和6克氧结合在一起,可以得到多少克NH3?
根据化学知识,6克氢,6克氮和6克氧可以结合组成NH3,可以得到18克NH3。
14. 一定体积的空气中含有多少分子?
根据摩尔定律,一定体积的空气中含有大约 6.02 * 10^23子。
15.度是指什么?
密度是指某种物质单位体积所含质量的大小,它是一个基本物理量,用单位质量/单位体积来表示。
16.果把8克铝和16克氯结合在一起,可以得到多少克AlCl3?
根据化学知识,8克铝和16克氯可以结合组成AlCl3,可以得到24克AlCl3。
17.果把3克氢,2克氧和4克锂结合在一起,可以得到多少克Li2O?
根据化学知识,3克氢,2克氧和4克锂可以结合组成Li2O,可以得到6克Li2O。
18.果把10克碳和20克氧结合在一起,可以得到多少克CO2?
根据化学知识,10克碳和20克氧可以结合组成CO2,可以得到30克CO2。
19.气和空气之间是怎样的关系?
氧气和空气之间是一种混合物,即空气中含有大约21%的氧气,79%的氮气。
20.果把6克氢,1克氯和2克氧结合在一起,可以得到多少克H2O2?
根据化学知识,6克氢,1克氯和2克氧可以结合组成H2O2,可以得到3克H2O2。
以上就是20道计算题,我们可以看到,计算题是掌握化学知识的一个重要方面,学习化学不仅要学习理论知识,还要把这些理论知识运用到实际的应用中。
因此,我们在学习化学时,要时刻牢记它的
三大要素:1、理解化学原理;2、掌握必要的实验技能;3、熟悉计算题的解答方法。
只有这样,才能更好的掌握化学知识,更好地掌握这门科目。
