硅铁12.30
硅铁基本知识

硅铁基本知识国内硅铁、工业生产现状及用途[我的钢铁] 2009-08-31 11:46:32一、什么是硅产品含硅量达14%以上至99%之间,其余为杂质或另一种(个别两种)主要元素,通过冶炼所得的合金俗称硅产品。
通常包括工业硅、硅铁、硅钡、碳化硅、硅钙等,最常用的为工业硅、硅铁两种。
冶炼任一种硅产品必须涉及到矿石(含SiO2)这一原料,采矿会破坏森林、植被,同时冶炼过程也会产生大量的污染(如CO、粉尘过量等),属于消耗资源、高污染、技术含量低的冶金行业。
所以,发达国家一般不予生产,主要依赖进口。
由于硅产品的广泛用途(汽车工业、信息工业)又决定了它的最大消费方为发达国家地区,所以发展中国家生产的硅产品,除自身消耗外,大部分用于出口换取外汇。
冶炼硅产品必须具备以下两个最基本的条件:①自身环境净化能力强的地方(亦允许产生轻度污染源的地方);②丰富的低价电源,因为硅冶为高耗能行业,以工业硅为例,每吨成品耗电平均12000度,通常只能以低廉的水电(每度从元不等)作为生产能源。
由于污染重,能耗高硅冶企业只能分布在边远、水电丰富(个别火电丰富)的地区,并且受电力紧张的缘故,在枯水季节常因限电而减产或停产。
二、我国硅冶炼行业状况福建三明地区是中国最早生产工业硅等硅产品的地方,由于近年水电的缺乏及资源的过度开采。
目前福建的硅冶规模大部分偏小,近五六年来,贵州、云南利用自身丰富的水电资源,已成为中国最大的硅生产基地,特别是贵州产量约占全国的50%以上,生产硅产品的地方还有四川、湖南、江西(个别)、西宁、内蒙、东北等地。
除个别小厂外,现在硅铁炉一般都在6300KVA以上,随着国家对铁合金行业的整顿,以及受环保要求,各地小容量电炉及达不到环保要求的炉子必然被淘汰。
三、硅系产品用途。
1、工业硅,俗称金属硅或结晶硅,严格来讲工业硅不属于铁合金行业,在习惯上由于工业硅的冶炼采用矿热炉进行,就把工业硅划分到铁合金行业中。
工业硅是指含硅量大于等于%的纯硅产品,其中以铁、铝、钙(按顺序排列)的三种杂质含量分成各小类,如553、441、331、2202等。
硅铁理化特性表
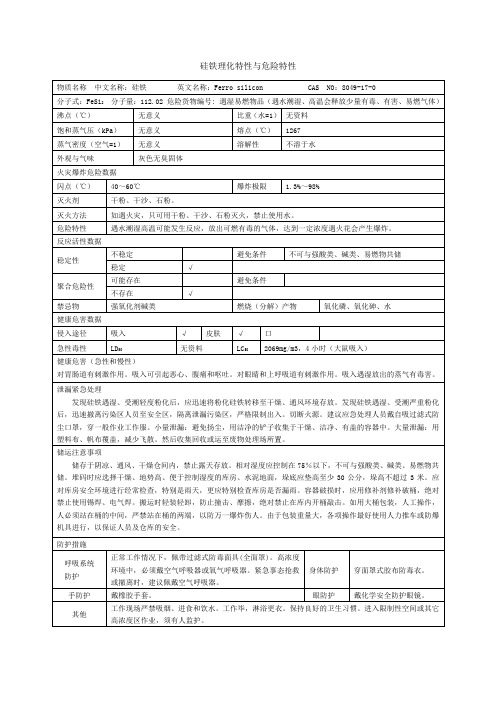
发现硅铁遇湿、受潮轻度粉化后,应迅速将粉化硅铁转移至干燥、通风环境存放。发现硅铁遇湿、受潮严重粉化后,迅速撤离污染区人员至安全区,隔离泄漏污染区,严格限制出入。切断火源。建议应急处理人员戴自吸过滤式防尘口罩,穿一般作业工作服。小量泄漏:避免扬尘,用洁净的铲子收集于干燥、洁净、有盖的容器中。大量泄漏:用塑料布、帆布覆盖,减少飞散。然后收集回收或运至废物处理场所置。
稳定性
不稳定
避免条件
不可与强酸类、碱类、易燃物共储Fra bibliotek稳定√
聚合危险性
可能存在
避免条件
不存在
√
禁忌物
强氧化剂碱类
燃烧(分解)产物
氧化磷、氧化砷、水
健康危害数据
侵入途径
吸入
√
皮肤
√
口
急性毒性
LD50
无资料
LC50
2069mg/m3,4小时(大鼠吸入)
健康危害(急性和慢性)
对胃肠道有刺激作用。吸入可引起恶心、腹痛和呕吐。对眼睛和上呼吸道有刺激作用。吸入遇湿放出的蒸气有毒害。
硅铁理化特性与危险特性
物质名称 中文名称:硅铁 英文名称:Ferro silicon CAS NO:8049-17-0
分子式:FeSi2分子量:112.02危险货物编号:遇湿易燃物品(遇水潮湿、高温会释放少量有毒、有害、易燃气体)
沸点(℃)
无意义
比重(水=1)
无资料
饱和蒸气压(kPa)
无意义
熔点(℃)
防护措施
呼吸系统
防护
正常工作情况下,佩带过滤式防毒面具(全面罩)。高浓度环境中,必须戴空气呼吸器或氧气呼吸器。紧急事态抢救或撤离时,建议佩戴空气呼吸器。
硅铁含量表

硅铁含量表
硅铁含量表是一份用于记录硅铁化合物中硅铁含量的表格。
硅铁是一种常见的铁合金,由铁和硅组成。
硅铁含量表可以记录不同硅铁样品的硅铁含量,通常以百分比或重量分数表示。
硅铁含量表通常包括以下信息:
1. 样品编号:用于标识每个硅铁样品的唯一编号。
2. 硅铁含量:样品中硅铁的含量,通常以百分比或重量分数表示。
3. 采样日期:记录样品采集的日期,用于追溯样品来源和检测时间。
硅铁含量表在炼钢和冶金工业中广泛使用,用于确定不同硅铁样品的质量和纯度。
它也是研究硅铁化合物性质和应用的重要工具。
- 1 -。
硅铁规格型号表

硅铁规格型号表硅铁是一种重要的铁合金,广泛应用于钢铁冶炼、铸造等领域。
其主要成分为硅和铁,同时含有少量的碳、锰、硫、磷等元素。
硅铁的规格型号表如下:规格型号硅含量(%)铁含量(%)碳含量(%)锰含量(%)硫含量(%)磷含量(%)75# 74.0-80.0 余量≤24.0 ≤0.04 ≤0.4 ≤0.02 ≤0.0472# 72.0-78.0 余量≤25.0 ≤0.04 ≤0.4 ≤0.02 ≤0.0470# 70.0-76.0 余量≤26.0 ≤0.04 ≤0.5 ≤0.02 ≤0.0465# 65.0-72.0 余量≤30.0 ≤0.04 ≤0.5 ≤0.02 ≤0.0460# 60.0-68.0 余量≤34.0 ≤0.04 ≤0.5 ≤0.02 ≤0.0455# 55.0-65.0 余量≤38.0 ≤0.04 ≤0.5 ≤0.02 ≤0.04硅铁的主要用途是作为钢铁冶炼中的脱氧剂和合金添加剂。
在钢铁冶炼过程中,加入适量的硅铁可以降低钢中的氧含量,提高钢的纯度和强度。
同时,硅铁中的硅还可以与钢中的其他元素形成合金,改善钢的物理和化学性能,例如提高耐磨性、耐蚀性、抗拉强度等。
硅铁还广泛应用于铸造领域。
在铸造过程中,硅铁可以作为脱氧剂和合金添加剂,改善铸件的组织和性能,例如减少气孔、夹杂和缩孔等缺陷,提高铸件的强度和韧性。
同时,硅铁还可以作为耐火材料的原料,制造高温炉料和耐火砖等。
根据不同的用途和要求,硅铁的规格型号也有所不同。
例如,在钢铁冶炼中,要求硅铁的硅含量高,铁含量低;而在铸造中,要求硅铁的硅含量和铁含量都在一定范围内。
因此,在选择硅铁的规格型号时,需要根据实际需求进行选择,以达到最佳的效果。
硅铁是一种重要的铁合金,具有广泛的应用前景。
通过选择合适的规格型号,可以满足不同领域的需求,提高产品的质量和性能。
高纯硅铁指标范文

高纯硅铁指标范文高纯硅铁是指含硅量大于99%的硅铁合金。
硅铁是一种用于钢铁冶炼中的铁合金,通过向炼钢炉中加入硅铁,可以改善钢的质量和性能。
高纯硅铁是硅铁中硅含量最高的一种合金,具有一定的特殊用途和特殊生产工艺。
高纯硅铁的主要指标包括硅含量、碳含量、铝含量、铁含量以及杂质含量等。
其中,硅含量是高纯硅铁最重要的指标之一,硅含量越高,合金的质量和性能越好。
高纯硅铁中的硅含量一般在99%-99.9%之间。
高纯硅铁的硅含量的高低对硅铁合金的性能有着明显的影响。
高纯硅铁中的硅含量越高,合金的熔点越低,热膨胀系数越低,热延性越好。
此外,高纯硅铁还具有良好的导电性能,可以提高钢材的热传导率和电导率。
高纯硅铁中的碳含量也是一个重要指标。
碳是硅铁合金中的另一个主要元素,它对硅铁合金的物理和化学性能有着重要影响。
高纯硅铁通常都是低碳合金,碳含量一般在0.02%-0.05%之间。
低碳硅铁可以显著提高硅铁合金的塑性和可焊性,同时减少合金中的热裂纹和气孔等缺陷。
除了硅和碳之外,高纯硅铁中的铝含量也是一个重要的指标。
铝是硅铁合金中的一种常见杂质元素,会对硅铁合金的性能产生不利影响。
高纯硅铁中的铝含量一般应小于0.07%,以保证合金的质量和性能。
此外,高纯硅铁中的杂质含量也是需要关注的指标之一、高纯硅铁的制备过程中,杂质元素的含量很容易受到外界环境的影响,因此需要进行严格的控制和监测。
常见的杂质元素包括铜、镍、锰等,这些元素对合金的质量和性能有着不同程度的影响。
总而言之,高纯硅铁是一种硅铁合金,具有较高的硅含量和低的碳含量。
其硅含量、碳含量、铝含量、铁含量以及杂质含量等指标是评价合金质量和性能的关键因素。
通过控制这些指标,可以生产出性能稳定、质量优良的高纯硅铁合金,满足不同领域的需求。
硅铁

硅铁(Ferro Silicon)硅铁被广泛地应用于铸造熔炼钢水的脱氧剂。
由于脱氧时放出大量的热,所以在脱氧同时,钢水温度提高从而降底熔炼钢水的能源消耗。
硅铁还作为合金添加剂用于炼钢中。
钢中添加一定数量的硅,能显著提高钢的强度、硬度和弹性。
金属硅(Silicon Metal)金属硅广泛用于铝业,其他冶金、铸造和化工、有机硅工业。
特别在特种钢的铸造中作为脱氧剂而被广泛使用。
铬铁(Ferro Chrome)铬铁合金作为钢的添加剂生产多种高强度、抗腐蚀、耐磨、耐高温、耐氧化的特种钢,如不锈钢、耐酸钢、耐热钢、滚珠轴承钢、弹簧钢、工具钢等。
金属铬主要用于与钴、镍、钨等元素冶炼特种合金锰铁(Ferro Manganese )锰铁主要是由锰、铁两种元素组成的合金,熔点接近1300℃,密度7.2-7.3g/cm 3;按照其含碳量的不同,中低碳锰铁可分为含碳量小于0.7%的低碳锰铁和含碳量0.7%-2.0%的中碳锰铁。
中低碳锰铁广泛应用于特殊钢铸造生产,是铸造工业的重要的添加剂.硅硅(台湾、香港称矽)是一种化学元素,它的化学符号是Si ,旧称矽。
原子序数14,相对原子质量28.09,有无定形和晶体两种同素异形体,同素异形体有无定形硅和结晶硅。
属于元素周期表上IVA 族的类金属元素。
晶体硅为钢灰色,无定形硅为黑色,密度2.4g /cm3,熔点1420℃,沸点2355℃,晶体硅属于原子晶体,硬而有光泽,有半导体性质。
硅的化学性质比较活泼,在高温下能与氧气等多种元素化合,不溶于水、硝酸和盐酸,溶于氢氟酸和碱液,用于造制合金如硅铁、硅钢等,单晶硅是一种重要的半导体材料,用于制造大功率晶体管、整流器、太阳能电池等。
硅在自然界分布极广,地壳中约含27.6%,主要以二氧化硅和硅酸盐的形式存在结晶型的硅是暗黑蓝色的,很脆,是典型的半导体。
化学性质非常稳定。
在常温下,除氟化氢以外,很难与其他物质发生反应。
硅的用途:①高纯的单晶硅是重要的半导体材料。
硅铁的用途和用法

硅铁的用途和用法硅铁是一种合金,由硅和铁组成,通常含硅量在70%-80%之间。
它具有一系列的用途和用法。
首先,硅铁被广泛用于钢铁冶炼业。
由于硅铁中含有高比例的硅,因此它能够提供高硅含量的熔体,可以用于合金钢、不锈钢等特殊钢的制备。
此外,硅铁还可以降低熔点和改善冶炼工艺,提高钢铁产品的质量和性能。
其次,硅铁也被用于铸造业。
硅铁中的硅具有很强的还原性和磨蚀性,可以帮助去除金属中的杂质和气泡,提高铸件的质量。
同时,硅铁还可以增加铸件的硬度和耐磨性,延长使用寿命。
因此,硅铁常被用于铸造汽车零部件、机械配件等。
另外,硅铁也广泛应用于铁合金冶炼业。
硅铁作为一种常用的铁合金原料,可用于制备硅铁合金、玻璃铁合金、铬铁合金等,这些铁合金在不同领域都有广泛的应用。
例如,硅铁合金被用作脱氧剂和合金添加剂,可以提高钢铁的品质和品种。
此外,硅铁还用于电子工业。
由于硅铁具有良好的导电性和磁性,所以它常被用作电子元件和传感器的关键材料。
硅铁还可以用于制造电动机、变压器和电磁铁等电器设备。
另外,硅铁也可以用于制备电子级硅材料,用于集成电路、太阳能电池等领域。
此外,硅铁还有一些其他的用途。
它可以用于制造沥青石墨石和沥青砂,用于建筑业和道路修复。
此外,硅铁还可用作电镀液的还原剂和添加剂,用于表面镀铜、镀镍等。
硅铁还可以用于制备防腐涂料、火花塞等。
总之,硅铁具有广泛的用途和用法,主要应用于钢铁冶炼业、铸造业、铁合金冶炼业、电子工业以及其他领域。
随着科技的发展和需求的增加,硅铁的用途还将不断扩大和深化。
硅铁的国家标准

中华人民共和国国家标准硅铁GB2272-87本标准适用于炼钢和铸造作脱氧剂或合金元素加入剂用的硅铁。
1技术要求1.1牌号和化学成分1.1.1硅铁按硅及其杂质含量.分为十六个牌弓,其化学成分应符合表1的规定表11.2物理状态1.2.1硅铁浇铸厚度:FeSi75系列各牌号硅铁锭不得超过100mm;FeSi65锭不得超过80mm。
硅的偏析不大于4%。
1.2.2硅铁供货粒度应按表2的规定。
表2 硅铁供货粒度注:FeSi45小于20mm×20mm的数量不得超过总重的15%。
1.2.3需方对供货粒度有特殊要求,可与供方协商解决2试验方法2.1取样化学分析试样的采取按GB4010-83(铁合金化学分析用试样的采取法)进行。
2.2制样化学分析用试样的采取法拉GB 4332—84铁合金化学分析用试样制备法》进行。
2.3化学分析方法硅铁的化学分析方法按GB 4333. l-4333.8—84《硅铁化学分析方法》进行。
2.4粒度试验采用方孔钢板筛或方孔筛进行筛。
3检验规则3.1质量检查和验收产品的质量检查相验收应符合GB3650一83《铁合金验收、包装、储运、标志和质量证书的一般规定》的要求。
3.2组批硅铁按同一牌号组批,但含Si量波动范围不应超过3%。
4包装、储运、标志和质量证明书4.1包装硅铁根据需方要求,可采用散袋、集装箱、袋装等形式发货。
采用袋装或集装箱包装时.包装外面应有明显标志。
4.2储运、标志和质量证明书产品的储运、标志和质量证明书应将合GB3650-83《铁合金验收、包装、储运、标志和质量证明书的一般规定》的要求。
附加说明;本标准由中华人民共和国冶金工业部提出。
本标准由上海铁合金厂负责起草。
本标准主要起草人陈震华、丁明。
本标准中FeSi75Al0.5-A、FeSi75-Al1.0-A、FeSi75Al1.5-A、FeSi75Al2.0-A、FeSi75Al2.0-B、FeSi75-A、FeSi75-B牌号标准水平等级标记为“Y”。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
二氧化硅
3.要除去SiO2中混有的少量杂质CaCO3,最适 宜的试剂是 A.水 B.盐酸 C.稀硫酸 D.氢氧化钠溶液
4.下列关于硅和二氧化硅的性质叙述中正确 A.常温下O2能把Si氧化成SiO2 B.SiO2是酸性氧化物,能与水反应生成硅酸 C.石英、水晶、海沙的主要成分都是SiO2 D.硅通常很稳定,自然界中存在单质硅
(3)装置改进后,将3中反应后溶液压入4中,在4中析出了
灰绿色沉淀。从实验操作过程分析没有产生白色沉淀
的原因: 装置4内的空气没有排尽
。
(1)在FeBr2溶液中通入少量Cl2,一定发生的离子
反应是 2Fe2+ + Cl2 = 2;Fe3+ + 2Cl-
还原性: Fe2+ > Br- ;
(2)在FeI2溶液中通入少量Cl2 ,一定发生的离子
4.有一块铁的“氧化物”样品,用140 mL 5.0 mol·L-1盐酸恰
好将之完全溶解,所得溶液还能吸收0.025 mol Cl2,恰好使其
中的Fe2+全部转变为Fe3+,则该样品可能的化学式为( )
A.Fe2O3 B.Fe3O4 C.Fe4O5 D.Fe5O7
D
下 列 各 图 示 中 能 较 长 时 间 看 到 Fe(OH)2 白 色 沉 淀 的 是 ________(填序号)。
D.SiO2
8.下列对实验现象的预测不正确的是 A.向Na2SiO3溶液中通入CO2,溶液变浑浊,继 续通CO2至过量,浑浊消失 B.向氢氧化铁胶体中滴加盐酸至过量,开始有沉 淀出现,后来沉淀又溶解 C.向Ca(ClO)2溶液中通入CO2,溶液变浑浊,再 加入品红溶液,红色褪去 D.向Ca(OH)2溶液中通入CO2,溶液变浑浊,继 续通CO2至过量,浑浊消失,再加入过量NaOH溶 液,又变浑浊
存在的二价铁,所以从实验结果只能判断样品溶解后的溶 液中存在三价铁而不能确定样品中铁元素的价态
练习3. 在铁与铜的混合物中,加入一定量
的稀硝酸,充分反应后剩余金属m1g,再向其 中加入一定量的稀硫酸,充分振荡后,剩余金
属m2g,则m1与m2之间的关系是:
A
(A) m1一定大于m2 (B) m1可能m2 (C) m1一定等于m2 (D) m1可能大于m2
B.氧化性
SiO2+2C 高温 Si + 2CO↑
C.与盐反应
高温
SiO2 + CaCO3
CaSiO3 + CO2 ↑
高温
SiO2 +Na2CO3
Na2SiO3 + CO2↑
D.与氢氟酸反应 (雕刻玻璃)
SiO2 + 4HF =SiF4 ↑+ 2H2O
硅的化学性质
常温下,化学性质不活泼,除氟气、氢氟酸 和强碱外,硅不跟其他物质(如氧气、氯气、 硫酸、硝酸等)起反应。在加热条件下,能跟 一些非金属反应。
想一想
1. 为什么在实验室中盛放NaOH 溶液的试剂瓶 用橡皮塞而不用玻璃塞?
2.实验室为什么不用玻璃瓶盛装氢氟酸? 3.某同学根据SiO2既可与碱反应,也能与氢氟酸反 应,推断SiO2为两性氧化物.是否正确?
二氧化硅的化学性质 A.酸性氧化物 SiO2 + CaO 高温 CaSiO3
SiO2 +2NaOH=Na2SiO3+H2O
知识应用1.
(2019·浙江4月学考)某同学设计如图装置(气密性已检
查)制备Fe(OH)2白色沉淀。
请(1回)仪答器:1的名称:分液漏斗.
,
装置5的作用:
.
液封,防止空气进入4
(2)实验开始时,关闭K2,打开K1,反应一段时间后,再打 开K2,关闭K1,发现3中溶液不能进入4中。请为装置作一 处改进,使溶液能进入4中:在2,3 之间增加控制开关
B.单质在加热时都能与氧气反应 C.氧化物都能溶于水生成相应的酸 D.在常温下,碳和硅的单质化学性质都不
活泼
7.将足量CO2气体通入水玻璃(Na2SiO3 溶液)中,然后加热蒸干,再在高温下充分
灼烧,最后得到的固体物质是( )
A.Na2SiO3
B.Na2CO3、Na2SiO3
C.Na2CO3、SiO2
Si+2NaOH + H2O = Na2SiO3 + 2H2↑ Si + 2F2 = SiF4 ↑ Si + 4HF = SiF4 ↑ + 2H2 ↑
Si + O2
SiO2
Si + 2H2 高温 SiH4(不稳定)
硅的工业制法
在工业上,用碳在高温下还原二氧化硅的方 法制得粗硅。
SiO2 +2C 高温 Si(粗硅)+2CO↑ 与氯反应:Si +2Cl2 = SiCl4(温度为400~500℃) 生成的SiCl4液体通过精馏,除去其中的硼、砷 等杂质。然后用氢气还原:
成功制备Fe(OH)2的关键
由于Fe(OH)2具有很强的还原性,易被氧化为 Fe(OH)3, 在实验室中制备Fe(OH)2,并使Fe(OH)2长时间保持白色 沉淀状态,成为物质制备实验探究的热点。 制备原理:Fe2++2OH-===Fe(OH)2↓ 成功关键:①溶液中不含Fe3+和O2等氧化性物质; ②制备过程中,保证生成的Fe(OH)2在密闭的隔绝空气 的体系中。
材料类 别
主要特性
示例
用途
高温结 构陶瓷
能承受高温, 强度高
氮化硅陶瓷
汽轮机叶片、轴 承、永久性模具
等
半导体 陶瓷
具有电学特性
氧化锡陶瓷
集成电路中的 半导体
光学材 料
具有光学特性
光导纤维
光缆通讯、医 疗、照明等
生物陶 瓷
具有生物功能
氧化铝陶瓷
人造骨骼、人造 关节、接骨螺钉
1.下列说法正确的是 ( )
练习1、往浅绿色的Fe(NO3)2溶液中逐滴加入稀盐酸时, 溶液的颜色变化是 ( )
A. 颜色变浅 B.逐渐变深绿 C.没有改变 D.变棕黄色
某种催化剂为铁的氧化物。化学兴趣小组在实验室对 该催化剂中铁元素的价态进行探究:将适量的稀硝酸 加入少许样品中,加热溶解;取少许溶液,滴加KSCN 溶液后出现红色。一位同学由此得出该催化剂中铁元 素价态为+3的结论。 (1)请指出该结论是否合理并说明理由 _____不_合__理__。__实_验__设__计不合理,因为硝酸会氧化催化剂中可能
反应是: 2I- + Cl2 = I2 + 2Cl- ;
还原性: I- > Fe2+ ;
5.下列说法正确的是( )
A.硅是良好的半导体材料,能与盐酸或氢 氧化钠溶液反应
B.二氧化硅不导电,能与盐酸或氢氧化钠 溶液反应
C.硅酸盐具有多孔性结构,可用作吸附剂 或催化剂载体
D.二氧化硅是酸性氧化物,能与氢氟酸反 应,也能与氢氧化钠溶液反应
6.关于碳和硅的叙述中,不正确的是:
A.其最高价氧化物都能与NaOH溶液反应
A.硅材料广泛应用于光纤通讯
B.工艺师利用盐酸刻蚀石英制作艺术品
A
C.水晶项链和餐桌上的瓷盘都是硅酸盐制品
D.粗硅制备单晶硅不涉及氧化还原反应
2.材料与化学密切相关,表中对应关系错误的是 ( )
材料
主要化学成分
A 刚玉、金刚石
三氧化通玻璃 硅酸盐
D
沙子、石英
SiCl4 +2H2 高温 Si + 4HCl
五.无机非金属材料
(1)传统无机非金属材料,如水泥、玻璃、陶瓷等硅酸盐材料。 ①常见硅酸盐材料比较
水泥
玻璃
陶瓷
生产原料 石灰石、黏土 纯碱、石灰石、石英 黏土
主要设备 水泥回转窑
玻璃熔窑
陶瓷窑
②玻璃生产中的两个重要反应:
(2)新型无机非金属材料,如高温结构陶瓷、光导纤维、生物 陶瓷、压电陶瓷等。
