供注射用辅料XXXX版药典与各国药典质量标准对比表
有关物质方法验证方案

分析方法预验证方案方案名称:XXXX有关物质测定方法预验证方案方案编号:版本号:01版起草人/日期:审核人/日期:审核人/日期:批准人/日期:目录1.概述 (1)2.分析方法 (1)2.1试剂 (1)2.2对照品 (1)2.3样品 (1)2.4仪器 (1)2.5色谱条件 (2)2.6溶液的配制 (2)2.7测定方法 (3)2.8计算 (3)3.方法验证 (3)3.1验证项目、验证方法及接受标准 (3)3.2系统适用性 (5)3.3专属性 (7)3.4精密度 (11)3.5线性 (12)3.6 定量限及检测限 (15)3.7准确度 (16)3.8溶液稳定性 (18)4.版本历史 (20)1.概述本品为xxxx注射液,规格为xxxx。
本品各国药典均未收载,本方法是参照欧洲药典(EP10.4)、美国药典(USP43)、中国药典2020年版收载的xxxx原料质量标准及英国药典(BP2020)收载的xxxx注射液质量标准及xxxx注射液进口注射标准(I物质A)项下的有关物质方法,采用中国药典2020年版四部通则0512高效液相色谱法,建立了本品的有关物质方法。
本预验证实验是为了确保该分析方法能够适用于当前本品有关物质的测定。
验证参数包括:系统适用性、专属性、重复性、精密度、线性、定量限(LOQ)、检测限(LOD)、准确度和溶液稳定性。
2.分析方法2.1试剂2.2对照品2.3样品2.4仪器2.5色谱条件色谱柱:C18,250×4.6mm,5μm或效能相当的色谱柱;检测波长:XXXnm;柱温:40℃;流速:1.0ml/min;进样体积:20μl;流动相A:0.2%磷酸氢二胺(pH7.5),流动相B:甲醇-异丙醇(87:13)。
梯度洗脱条件:时间(min)流动相A(%)流动相B(%)X X XX X XX X XX X XX X X2.6溶液的配制2.6.1 流动相流动相A:取磷酸氢二胺2g,加水1000ml溶解,用磷酸调pH值至7.5,过滤,取滤液,即得;流动相B:量取甲醇1000ml,超声,即得。
注射用XXXX CTD资料模板3.2.P.1~P.5

目录3.2.P.1 剂型及产品组成 (3)3.2.P.1.1剂型和产品组成 (3)3.2.P.1.2专用溶剂 (3)3.2.P.1.3包装 (3)3.2.P.2 产品开发 (3)3.2.P.2.1 处方组成 (4)3.2.P.2.1.1 原料药 (4)3.2.P.2.1.2 辅料 (7)3.2.P.2.2 制剂研究 (7)3.2.P.2.2.1 处方开发过程 (8)3.2.P.2.2.2 制剂相关特性 (14)3.2.P.2.3 生产工艺的开发 (16)3.2.P.2.3.1 小试工艺研究 (16)3.2.P.2.3.2 中试及验证生产工艺研究 (18)3.2.P.2.3.3 工艺变更情况汇总 (19)3.2.P.2.3.4代表性批次汇总 (19)3.2.P.2.4 包装材料/容器 (21)3.2.P.2.4.1 包材类型、来源及相关证明文件 (21)3.2.P.2.4.2 包材的选择依据 (21)3.2.P.2.4.3 包材选择的支持性研究 (22)3.2.P.2.5 相容性 (22)3.2.P.3 生产 (23)3.2.P.3.1 生产商 (23)3.2.P.3.2 批处方 (23)3.2.P.3.3 生产工艺和工艺控制 (23)3.2.P.3.3.1 工艺流程图 (23)3.2.P.3.3.2 工艺描述 (26)3.2.P.3.3.3 主要的生产设备 (26)3.2.P.3.3.4 拟定的大生产规模 (26)3.2.P.3.4关键步骤和中间体的控制 (26)3.2.P.3.4.1 关键步骤和工艺参数 (27)3.2.P.3.4.2 中间体的控制 (27)3.2.P.3.5 工艺验证和评价 (30)3.2.P.3.5.1 冻干粉针剂培养基模拟灌装验证 (30)3.2.P.3.5.2 除菌过滤系统验证 (30)3.2.P.3.5.3 内包材密封完整性验证 ........................................................ 错误!未定义书签。
各国药典比较ppt课件

英国药典
• 版本简介
英国 The Stationery Office出版社在 2001年五月出版发行的《英国药典 (2001)》(British Pharmacopoeia 2001) 的最新版本。收录有2760篇医药专论,其 中1305篇出自英国本土;其余1455篇套录 自欧洲药典(European Pharmacopiea) (第三版)。
内容基本介绍
• 英国药典是英国制药标准的重要来源。各
条目均以药品名称字母顺序排列,内容包 括药品性质、制法、血产品、免疫产品、 电磁药品制法及外科材料等部分。英国药 典书后附有全部内容关键词索引。不仅为 读者提供了药用和成药配方标准以及公式 配药标准,而且也向读者展示了许多明确 分类并可参照的欧洲药典专著。英国药典 出版周期不定,最新的版本为2004年的第 21版。
日本药典
• 版本简介
由日本药局方编辑委员会编纂,日本厚 生省颁布执行。分两部出版,第一部收载 原料药及其基础制剂,第二部主要收载生 药,家庭药制剂和制剂原料 。2005年11月 22日,日本厚生劳动省制定了日本药典第 15版,废除日本药典第14版。最新版本 JP15拟定生效日期为2006年4月1日。
各国药典比较
基本介绍 • 药典是通过建立国家技术标准来保证人 类和牲畜使用的药物的质量、剂量和药物纯 度和浓度标准的权威性出版物。它是在专业 的,通常是政府的权威人士的监督下进行编 辑,并且是所有药物的制造、分配和药物治 疗所必须遵照的标准 。 • 目前常用的药典标准有英国药典(BP)、 欧洲药典(EP)、美国药典(USP)、德国 药典(DAP)、日本药典(JP)、中国药典 (CP)。
该药典囊括了几千篇颇有价值医学专 题论文,其中有几百篇是医学新论。它不 仅为读者提供了药用和成药配方标准以及 公式配药标准,而且也向读者展示了所有 明确分类并可参照的欧洲药典专著。对于 制药厂和化学工业、政府管理者、医学研 究院及学习制药的学生都是一部必不可少 的工具书。
新旧药典原辅料对比

2、吸收系数
删除
3、有关物质:薄层色谱法
3鸟嘌呤与有关物质:色谱条件采用梯度洗脱;鸟嘌呤按外标法计算,不得过0.7%,其他各杂质峰面积之和不得大于对照品溶液峰面积(1.0%)
4、鸟嘌呤:供试品溶液的色谱图中鸟嘌呤色谱峰的峰面积不得大于鸟嘌呤对照品溶液峰面积(1.0%)
5、含量测定:色谱条件,流动相:以三乙胺磷酸溶液(取三乙胺5ml与磷酸7ml,加水至1000ml)-乙腈(82:18)
5、流动相:以三乙胺磷酸溶液(取三乙胺5ml与磷酸7ml,加水至1000ml)-乙腈(87:13)
30
氟康唑
无变化
31
胞磷胆碱钠
1、有关物质:各杂质峰面积的和不得大于对照溶液(1)的主峰面积。
3、
3、增加“铁盐”检查
16
吡拉西坦
1、有关物质:各杂质峰面积和,不得大于对照溶液主峰面积(1.0%)
1、有关物质:各杂质峰面积和,不得大于对照溶液主峰面积的0.5(0.5%)
17
利巴韦林
1、性状:本品为白色结晶性粉末;无臭,无味
1、性状:本品为白色或类白色结晶性粉末;无臭,无味
2、吸光度:吸收度不得大于0.02
1、更改为:薄层色谱鉴别
2、氯化物:限值≤0.1%
2、氯化物:限值≤0.01%
3、硫酸盐:限值≤0.1%
3、硫酸盐:限值≤0.01%
4、
4、增加“铁盐、有关物质(薄层法)”检查
7
甘氨酸
1、性状:本品为白色结晶性粉末;无臭;味甜
1、性状:本品为白色至类白色结晶性粉末;无臭;味甜
2、鉴别
2、鉴别:增加薄层色谱鉴别
中外医疗标准对照表

OCu宫内节育器
mod ISO 5832-1: 1997
外科植入物用不锈钢
医用诊断X线发生装置通用技术条件
针尖锋利度和强度试验方法
idt ISO 4135: 2001
麻醉呼吸设备 术语
牙科砂轮
牙科磨头
eqv IEC 60526: 1978
医用诊断X射线设备高压电缆插头插座连接
医用诊断X线机械装置通用技术条件
GB 9706.17-1999
GB 9706.18-2000
GB 9706.19-2000
GB 9706.20-2000
GB 9706.21-2003
GB 9706.22-2003
GB 9706.23-2005
GB 9706.24-2005 GB 9937-88 GB/T 9937.4-2005 GB 9938-88 GB 10035-94 GB 10149-88 GB 10151-88 GB 10152-1997 GB/T 10160-1995 GB 10162-88 GB 10793-2000 GB 11234-1995 GB 11235-1997 GB 11236-1995 GB 11239.1-2005
mod ISO 2000
10936.1:
手术显微镜
第1部分:
要求和试验方法
idt IEC 60601-219:1990
医用电气设备 第2部分:婴儿培养箱安全专用要求
neq ISO 8600: 1997
医用内窥镜及附件通用要求
B型超声诊断设备
参照ISO 7151-83 医用钳锁合力、脱开力测定方法
参照ISO 7151-83 医用钳夹持拉力测定方法
人工心肺机 热交换水箱
GB 12279-90
右旋糖酐40质量标准各国药典对照表
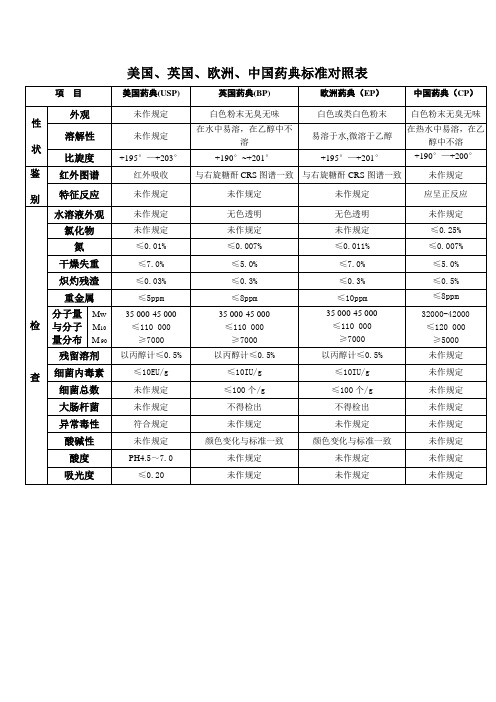
美国、英国、欧洲、中国药典标准对照表项目美国药典(USP) 英国药典(BP) 欧洲药典(EP)中国药典(CP)性状外观未作规定白色粉末无臭无味白色或类白色粉末白色粉末无臭无味溶解性未作规定在水中易溶,在乙醇中不溶易溶于水,微溶于乙醇在热水中易溶,在乙醇中不溶比旋度+195°—+203°+190°~+201°+195°—+201°+190°—+200°鉴别红外图谱红外吸收与右旋糖酐CRS图谱一致与右旋糖酐CRS图谱一致未作规定特征反应未作规定未作规定未作规定应呈正反应检查水溶液外观未作规定无色透明无色透明未作规定氯化物未作规定未作规定未作规定≤0.25%氮≤0.01%≤0.007%≤0.011%≤0.007%干燥失重≤7.0%≤5.0%≤7.0%≤5.0%炽灼残渣≤0.03%≤0.3%≤0.3%≤0.5%重金属≤5ppm≤8ppm≤10ppm≤8ppm分子量与分子量分布MwM10M 9035 000-45 000≤110 000≥700035 000-45 000≤110 000≥700035 000-45 000≤110 000≥700032000-42000≤120 000≥5000残留溶剂以丙醇计≤0.5%以丙醇计≤0.5%以丙醇计≤0.5%未作规定细菌内毒素≤10EU/g≤10IU/g≤10IU/g未作规定细菌总数未作规定≤100个/g≤100个/g未作规定大肠杆菌未作规定不得检出不得检出未作规定异常毒性符合规定未作规定未作规定未作规定酸碱性未作规定颜色变化与标准一致颜色变化与标准一致未作规定酸度PH4.5~7.0未作规定未作规定未作规定吸光度≤0.20未作规定未作规定未作规定。
中国药典与美英药典微生物限度比较

大豆酪蛋白消 化ห้องสมุดไป่ตู้养基 35~37℃24~48 h
增菌
大豆酪蛋白消化培养基 35~37℃18~48h
Cetrimide琼脂,培养18~72h 大豆酪蛋白消化培养基 41~43℃ 18~48h。薄膜过滤 大豆酪蛋白消化培养基18~48h, Cetrimide琼脂平板
分离
Cetrimide琼 脂 35~37℃72h 3种
BL增菌培养基 35~37℃18~24 h
BP I法 1 pH7.0氯化钠蛋白胨缓冲液 大豆酪胨肉汤 35~37℃18~48h Mac 肉汤 43~45℃18~24h Mac.琼脂平板 35~37℃18~72h +
USP IMViC法 10 乳糖液体培养基
MI法 1 09%氯化钠溶 液
乳糖液体培养基 35~37℃24~48h Mac 、 EMB 琼 脂 平板 35~37℃24~48h +
乳糖肉汤
1份80℃10min 另1份不加热 100ml 梭 菌 增 菌 培 养 基 35~37℃厌氧48h 含和不含庆大霉素哥 伦比亚琼脂平板 35~37℃48h
分离
过氧化氢酶 试 验
+
+
12.结果判断及复试 CP BP USP
进口药用辅料与国产药用辅料

