一次性使用无菌针灸针.doc
产品技术报告-一次性使用无菌注射器 带针

常州金龙医用塑料器械有限公司产品技术报告2.与已上市的产品比较序号项目内容春光已注册的一次性使用无菌注射器带针本公司申报的一次性使用无菌注射器带针01 标准医疗器械注册产品标准医疗器械注册产品标准02 材质主材:聚丙烯、活塞、不锈钢针管主材:聚丙烯、活塞、不锈钢针管辅材:ES-2单组分针头胶、油墨、二甲硅油辅材:ES-2单组分针头胶、油墨、二甲硅油03 结构组成芯杆、外套、活塞、注射针芯杆、外套、活塞、注射针04 工作原理 1.去护套,抽吸药液,排尽管内气体;2.进行皮下注射等。
1.去护套,抽吸药液,排尽管内气体;2.进行皮下注射等。
05 制造工艺流程注:1.本图为一次性使用无菌注射器带针工艺流程图;2.绿色□为十万级洁净区;3.□为一次性使用注射器配套用注射针生产工艺流程;4.外购协件为:PE包装、仿透析纸、PP、PE共挤医用包装膜、橡胶活塞;5.注塑、印刷、粗洗、组装为关键工序控制点;6.精洗、封口、灭菌为特殊过程7.原材料选择与组成见下表。
注:1.本图为一次性使用无菌注射器带针工艺流程图;2.绿色□为十万级洁净区;3.□为一次性使用注射器配套用注射针生产工艺流程;4.外购协件为:PE包装、仿透析纸、PP、PE共挤医用包装膜、橡胶活塞;5.注塑、印刷、粗洗、组装为关键工序控制点;6.精洗、封口、灭菌为特殊过程7.原材料选择与组成见下表。
3.产品命名一次性使用无菌注射器带针在国际、国内均属成熟产品,国际、国内标准化组织未制定一次性使用无菌注射器带针的相关标准;根据《中华人民共和国标准化法》规定,参照GB15810一次性使用无菌注射器修订稿、GB15811-2001一次性使用无菌注射针标准特制定《一次性使用无菌注射器带针医疗器械注册产品标准》,作为企业组织生产和经营活动的依据。
满足医疗器械行业及企业的检测及有效控制。
4.原材料控制4.1聚丙烯原材料名称聚丙烯供应商编号2011004化学结构式/分子式原材料代号GM1600E 符合标准YY/T0242-2007商品名聚丙烯树脂分子量分布不详供应商名称中国石化上海石油化工股份有限公司组成比例不详物理性能外观色粒0个/kg 弯曲模量:≥1.250Mpa 熔体质量流动速率±0.2n 悬臂梁缺口冲击强度(23℃) ≥2.0kj/m2密度≤0.91g/cm3雾度≤15拉伸屈服应力≥30Mpa化学性能生物性能重金属含量≤1.0镉含量<0.1细胞毒性、皮肤致敏、皮内反应、急性全身毒性、热原、溶血酸碱度≤1.0紫外吸光度≤0.084.2活塞原材料名称活塞供应商编号2011020 符合标准YY/T0243-2003 原材料代号不详化学结构式/分子式不详分子量分布不详商品名一次性使用无菌注射器用活塞原材料组成比例供应商名称常州京林医疗器械有限公司材料名称分子式比例% 材料名称分子式比例%物理性能外观1.不得有胶丝、胶屑、外来杂质、喷霜;天然橡胶(C5H8)n 55 氧化锌ZnO 3.02.外观色泽应均匀,表面不得有明显气泡、缺胶、切损、偏心;碳酸钙CaCO335抗氧剂2246C23H32O20.83.密封圈侧面顶部应有清晰的边缘基准线、基准线应完整、与注射器外套内表面接触应紧密;炭黑 C 4.0促进剂TMTMC6H12N2S30.54.修边部位的直径应不大于活塞密封圈直径;硫磺S 1.75.无泛黄现象。
一次性使用配药用无菌注射针产品技术要求changchuan

一次性使用配药用无菌注射针适用范围:本产品与一次性使用无菌注射器配套使用,适用于溶药、加药、配药或抽取药液时使用。
1.产品型号/规格及其划分说明1.1产品型号/规格一次性使用配药用无菌注射针(以下简称配药针):型号:CK规格:1.2、 1.61.2 划分说明CK:侧孔的拼音缩写依据注射针公称外径为划分(mm):1.2、1.61.3 产品组成1.3.1配药针由针座、护套和侧孔针组成,各部件名称术语如图1所示1、针座2、侧孔针针管3、侧孔4、护套图1 配药针的结构示意图1.3.2产品的标记配药针产品的标记以针管公称外径和针管标称长度表示。
1.1材料要求配药针材料:针管应采用符合表1、表2及表3中X5CrNi18-9奥氏体不锈钢的材料制成。
护套、针座材料:采用M1600E、K4912或物理机械性能、化学、生物性能均符合YY/T 0242-2007标准的医用聚丙烯专用高分子材料制造。
2.性能指标2.1 配药针外观2.1.1 配药针针管应清洁、无杂物,针管应平直。
2.1.2 配药针针座应无明显毛边、毛刺、塑流及气泡等注塑缺陷。
2.1.3 配药针针座的锥孔应无微粒和杂质。
2.1.4 配药针针尖应锋利、无毛刺、弯钩和平头等缺陷。
2.1.5 配药针针头锥体应正直、光滑、无弯曲、无明显褶皱。
2.1.6 配药针孔应畅通、侧孔外缘应光滑、无毛刺。
2.2 配药针尺寸配药针针管的外径、长度和锥体长度应符合表4的规定。
2.3 配药针针管2.3.1 刚性:针管应有良好的刚性,在附录A中规定的条件下试验,针管的最大挠度值应符合附录A中表7的规定。
注:必要时亦可对针管材料进行试验。
2.3.2 韧性:配药针应有良好的韧性,按附录B中表8规定的跨距及附录B中规定的周次,使针管在一个平面内按附录B中规定的摆角做双向反复弯曲不得折断。
注:此项指标亦可对针管材料进行试验。
2.3.3 耐腐蚀性:配药针应有良好的耐腐蚀性,应符合附录C中规定的要求。
注射器(针)技术报告

一次性使用无菌注射器(针)产品技术报告一次性使用无菌注射器(带针),是按照YZB/国××××—2006标准规定生产制造而成。
用于给患者注射用输送药液,该产品以无菌状态提供给用户,仅供一次性使用,可有效避免患者之间的交叉感染。
产品均采用符合医用级要求的材料及零部件,芯杆、外壳由医用级聚丙烯加工而成,橡胶活塞选用天然橡胶、配套用针采用医用级不锈钢针管等,产品经检验和试验均符合标准要求,一、产品用途、性能:主要用于预防和临床肌肉静脉注射用。
产品性能主要有:滑动性能、器身密合性、残留容量、可萃取金属含量、酸碱度、易氧化物、环氧乙烷残留量、急性全身毒性、溶血、无菌、无致热原等。
二、产品的基本结构形式:结构:由芯杆、外套、胶塞、配套用注射针组成。
形式:中头式,偏头式。
三、产品的基本规格:1ml, 2ml, 5ml,10ml,20ml,30ml,50ml。
四、产品的主要原辅材料:1.符合YY0242《医用输液、输血、注射用聚丙烯专用料》标准的PP料。
2.符合YYT0243《一次性使用无菌注射器用橡胶活塞》的活塞。
五、产品执行标准:执行YZB/国××××---2006《一次性使用无菌注射器针》六、适用范围、用途:本产品适用于供抽吸液体或注射液体用。
本产品只适用于皮下或肌肉注射和静脉抽血检验,由医务人员使用,禁止作其它用途和非医务人员使用。
七、物理指标:1、注射器有良好的滑动性能,其推、拉作用力符合下表的规定。
2.器身密合性将注射器吸入公称容量的水,用下表规定的轴向压力及侧向力,对芯杆作用30s,外套与活塞接触的部位无漏液现象。
在88kPa负压作用下保持60s±5s外套与活塞接触部位不产生漏气现象,且活塞与芯杆不脱离。
3.容量允差:小于二分之一公称容量和大于二分之一公称容量的最大允差符合上表中的有关规定。
4.残留容量:当芯杆完全推入到外套封底时,其残留在外套内的液体体积不超过上表的规定。
新一次性使用配药用无菌注射针技术要求

医疗器械产品技术要求编号:一次性使用配药用无菌注射针1.产品型号/规格及其划分说明1.1产品型号/规格一次性使用配药用无菌注射针(以下简称配药针):型号:CK规格:1.2、1.61.2划分说明CK:侧孔的拼音缩写依据注射针公称外径为划分(mm):1.2、1.61.3产品组成1.3.1配药针由针座、护套和侧孔针组成,各部件名称术语如图1所示1、针座2、侧孔针针管3、侧孔4、护套图1配药针的结构示意图1.3.2产品的标记配药针产品的标记以针管公称外径和针管标称长度表示。
标记示例:1.2X33针管标称长度(L): 33mm针管公称外径(D): 1.2mm1.1材料要求配药针材料:针管应采用符合表1、表2及表3中X5CrNi18-9奥氏体不锈钢的材料制成。
表1化学成分表2与其他国际标准不锈钢牌号对照护套、针座材料:采用M1600E、K4912或物理机械性能、化学、生物性能均符合YY/T 0242-2007标准的医用聚丙烯专用高分子材料制造。
2.性能指标2.1配药针外观2.1.1配药针针管应清洁、无杂物,针管应平直。
2.1.2配药针针座应无明显毛边、毛刺、塑流及气泡等注塑缺陷。
2.1.3配药针针座的锥孔应无微粒和杂质。
2.1.4配药针针尖应锋利、无毛刺、弯钩和平头等缺陷。
2.1.5配药针针头锥体应正直、光滑、无弯曲、无明显褶皱。
2.1.6配药针孔应畅通、侧孔外缘应光滑、无毛刺。
2.2配药针尺寸配药针针管的外径、长度和锥体长度应符合表4的规定。
表4配药针的结构尺寸单位:mm2.3配药针针管2.3.1刚性:针管应有良好的刚性,在附录A中规定的条件下试验,针管的最大挠度值应符合附录A中表7的规定。
注:必要时亦可对针管材料进行试验。
2.3.2韧性:配药针应有良好的韧性,按附录B中表8规定的跨距及附录B中规定的周次,使针管在一个平面内按附录B中规定的摆角做双向反复弯曲不得折断。
注:此项指标亦可对针管材料进行试验。
2.3.3耐腐蚀性:配药针应有良好的耐腐蚀性,应符合附录C中规定的要求。
一次性使用无菌针灸针产品技术要求keyuanda
一次性使用无菌针灸针适用范围:供中医针灸疗法使用。
1.1 产品名称一次性使用无菌针灸针(以下简称针灸针)。
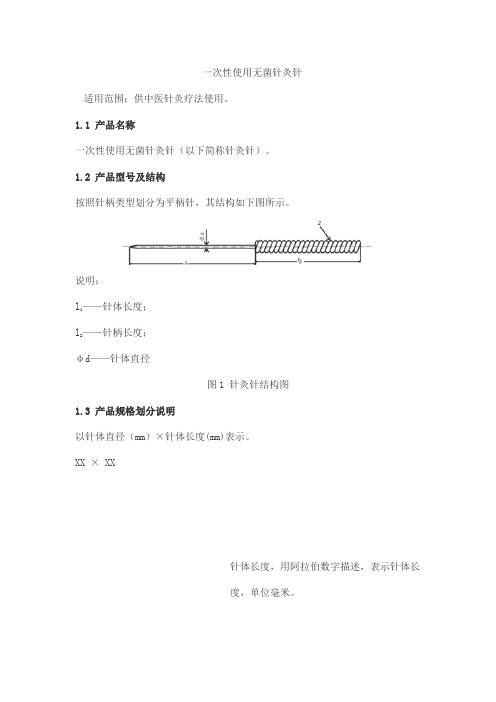
1.2 产品型号及结构按照针柄类型划分为平柄针,其结构如下图所示。
说明:——针体长度;l1——针柄长度;l2φd——针体直径图1 针灸针结构图1.3 产品规格划分说明以针体直径(mm)×针体长度(mm)表示。
XX × XX针体长度,用阿拉伯数字描述,表示针体长度,单位毫米。
针体直径,用阿拉伯数字描述,表示针体直径,单位毫米。
例:0.30×40,表示针体直径0.30毫米,针体长度40毫米的针灸针。
1.4 针灸针规格针灸针的规格如表1所示。
表1 单位:mm注:1.L括号中的尺寸为平柄针全长。
2.针体直径的圆度应不大于0.005mm。
3.特殊规格按合同要求定制,但其极限偏差应符合表1规定。
1.5 产品各规格之间的差异针灸针各规格间的差异主要体现在针体直径与针体长度上,详见表1。
2.1 材料针体材料应符合YY/T 0294.1-2005外科器械金属材料第1部分不锈钢标准中的奥氏体不锈钢“M、N、O、P”之一的化学成分;详见下表2。
针柄的材料可以是以下无毒材料:不锈钢、铜。
表22.2 外观2.2.1 针体表面应光滑。
2.2.2 针灸针的针柄部分不得有毛刺。
2.2.3 针灸针应挺直,不得有明显的弯曲。
2.2.4 针灸针的针柄部表面色泽应均匀。
2.2.5 针灸针的针柄采用缠绕丝,其螺旋圈应排列均匀,无明显离距。
2.3 物理性能2.3.1 尺寸针灸针的直径以及长度应符合表1的规定。
2.3.2 硬度针灸针针体的硬度应符合表3的规定。
表32.3.3 压顶力和针尖锋利度针灸针的针尖部位应圆正不偏、无毛刺、弯勾等缺陷;经规定的力与硬块接触顶压后,其穿刺力应不大于表4的规定。
表42.3.4 韧性针体应有良好的韧性,缠绕试验后不应有裂缝、折断和分层。
2.3.5 表面粗糙度针体表面应光滑,其外观质量和表面粗糙度参数Ra。
一次性使用无菌注射器国家标准编制说明

《一次性使用无菌注射器》国家标准编制说明一、任务来源本标准是根据国家标准化管理委员会下达的2006年第一批制修订国家标准项目计划通知(国标委计划[2006]48号)而修订的。
计划项目编号是20065424-Q-464。
本标准由全国医用注射器(针)标准化技术委员会归口管理,由上海康德莱企业发展集团股份有限公司、成都市新津事丰医疗器械有限公司、山东威高集团医用高分子制品股份有限公司、江西洪达医疗器械集团有限公司、上海市医疗器械检测所负责起草。
二、修定标准的目的及意义一次性使用无菌注射器是目前应用最广泛的无菌医疗器械之一。
其产品标准在国内应用已近三十年,最近一版距今已有十六年。
随着科学技术的发展和对临床安全不断提高,原国家标准已经不适应这种需求。
ISO国际标准化组织已于2017年修订了ISO 7886-1:2017《一次性使用无菌皮下注射器第1部分:手动注射器》的发行稿。
该标准对原ISO标准进行了较大修订。
它更多考虑的是在设计上充分保证产品的安全性要求。
为适应这种变化,相对应的国家标准有必要进行修订。
三、产品适用范围本标准规定了一次性使用无菌注射器(以下简称注射器)的分类与命名、要求、试验方法、包装、标识等。
本标准适用于供抽吸液体或抽吸液体后立即注射用的手动注射器。
本标准不适用于胰岛素注射器、玻璃注射器、永久带针注射器、带有动力驱动注射泵的注射器、自毁型固定剂量疫苗注射器、带防止再次使用特性的注射器、由制造厂预装药液的注射器以及与药液配套的注射器等。
本标准规定的不带针注射器应与符合GB 15811要求的一次性使用无菌注射针配套使用。
四、关于技术指标的说明本标准修改采用ISO 7886-1:2017《一次性使用无菌皮下注射器第1部分:手动注射器》本标准与GB15810-2001相比主要技术差异如下:1.修改了适用范围。
修定原因:与ISO 7886-1:2017标准保持一致。
一次性使用无菌注射器作为一个单器械,必须联合一次性使用无菌注射针组成组合器械应用于临床。
一次性使用无菌刃针产品技术要求特色东方

一次性使用无菌刃针适用范围:一次性使用无菌刃针作为中医器具,用于刃针疗法。
1. 产品型号/规格及其划分说明1.1一次性使用无菌刃针由针头及螺旋针柄组成。
1.1.1一次性使用无菌刃针针头部分应以GB/T 1220-2007中规定的30Cr13、针柄部分选用紫铜丝材料或其它PVC材料制成,所用材料应有生产厂家出具的材质证明。
1.2一次性使用无菌刃针型号/规格及划分说明。
1.2.1一次性使用无菌刃针型号由针体直径表示,一次性使用无菌刃针规格由针体直径X针体长度表示。
1.2.2一次性使用无菌刃针的型号/规格见表1。
表1 一次性使用无菌刃针规格型号1.3 一次性使用无菌刃针的样式如图1所示,其基本尺寸应符合表2的规定。
图1 一次性使用无菌刃针的样式图.性能指标2.1 外观一次性使用无菌刃针针头以目力观察,表面应光滑、无锈斑,无缺口、卷口、裂纹等缺陷及机械性损伤,螺旋针柄部分应排列均匀无明显距离。
2.2 尺寸一次性使用无菌刃针各部尺寸及允许偏差见表2。
表2一次性使用无菌刃针各部尺寸单位:mm2.3 材料一次性使用无菌刃针的针体应以GB/T1220-2007中规定的30Cr13制成,柄部以紫铜丝或PVC材料制成。
2.4硬度将本产品经过热处理后,硬度应在HV0.1 480 ~ HV0.1600。
2.5 锋利度一次性使用无菌刃针针头应锋利,不得有卷刃、崩刃等现象。
2.6 弹性一次性使用无菌刃针杆部应有弹性,经屈曲150后不得有变形,屈曲450不得产生断裂现象。
2.7表面粗糙度一次性使用无菌刃针表面应光滑,色泽均匀,表面粗糙度Ra应不大于0.8um。
2.8 腐蚀一次性使用无菌刃针应有良好的抗腐蚀性能。
2.9 牢固性一次性使用无菌刃针柄部缠绕丝应牢固,其螺旋圈应排列均匀,无明显距离。
2.10 无菌一次性使用无菌刃针用环氧乙烷灭菌,灭菌后,应无菌。
2.11 环氧乙烷残留量环氧乙烷残留量≤10μg/g。
一次性使用无菌注射器 带针技术报告

为确保产品质量符合标准要求,保证产品安全有效,公司对一次性使用无菌注射器带针产品生产过程设置了外套、芯杆、注射针座注塑成型、产品单包装封口四个关键工序,与环氧乙烷灭菌过程一个特殊过程。分别根据各关键工序与特殊过程的具体情况建立了若干个质量控制点,从设备工装配置、人员配置与培训、工艺参数确认、工艺纪律执行、生产环境控制到物资采购、采购产品检验、过程产品检验、产成品检验的全过程进行系统有效地控制。
1.工艺流程图(见附件)
此生产工艺经实际生产验证,设计合理,能保证产品各项性能要求。
2.工艺要求
(1)环境要求
注射器必须在10万级净化车间内生产、包装。
(2)注塑配件要求
注塑件完整、无毛刺飞边、无色斑、焦点,尺寸符合要求。
(3)装配粘接要求
各零部件无缺陷,外套与橡胶活塞既要滑动性能好又要密封性能好。配合针尖应粘接到位、牢固、粘接剂均匀、无堵塞。
注射针的检验液与同批对照液作对照,PH值之差不得超过1。
(3)易氧化物:注射器浸取液与等体积的同批空白对照液相比,0.002mol/L的高锰酸钾溶液消耗量之差应≤0.5mL。
(4)环氧乙烷残留量:环氧乙烷残留量应≤10μg/g。
3、生物性能:
(1)产品应无菌。
(2)产品应无致热原。
(3)产品应无溶血反应,溶血率∠5%。
(9)注射针针座与针管的连接应牢固应符合YZB/国XXXX-2006标准5.11.3、5.11.4条的规定。
(10)注射针针座与护套配合应良好,护套不得自然脱落,且两者分离力应不得大于15N。
(11)注射针针孔的畅通要求、针尖的锋利度要求应符合YZB/国XXXX-2006标准5.11.6、5.12条的规定。
4、原材料要求及选择
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一次性使用无菌针灸针
产品技术要求
2017-11-21发布2018-05-20 实施贵州安迪药械有限公司发布
一次性使用无菌针灸针
1.产品型号 / 规格及其划分说明
1.1产品分类
1.1.1针灸针的品种为一次性使用无菌针灸针,本要求以下简称灭菌针灸针。
1.1.2灭菌针灸针的针柄型式分为平柄针、环柄针、花柄针,如下图所示。
1.1.3灭菌针灸针型式分为带进针管和不带进针管两种。
第2页共5页
医疗器械产品技术要求编号:黔械注准 20182270011 1.2 型号、规格
1.2.1 灭 菌针灸针的规 格以 针体的直径 × 针体 长度 表示;针体直 径: d
0.16mm-0.45mm ;针体长度 :l 13mm-100mm 。
1.2.2 产品型号、规格划分说明
直径用 d 表示,针体长度用 l 表示
2. 性能指标
2.1 灭菌针灸针的基本尺寸
应符合表 1 规定。
表 1
单位: mm
产品 d
l
L
绕柄丝 基本 极限 基本 极限 基本 极限 规格
直径
尺寸
偏差
尺寸 偏差 尺寸 偏差
0.16 × 13 0.16
13 ±0.55 35 ±1.25 0.16 × 25
25 ±0.65 52(50) ±1.50
0.16 × 40
40 ±0.80 75(65)
0.30
0.18 × 13
13 ±0.55 35 ±1.25 0.18
0.18 × 25 ±0.008
25 ±0.65 52(50) ±1.50
0.18 × 40
40 ±0.80 75(65)
0.20 × 13
13 ±0.55 35 ±1.25 0.20 × 25 0.20
25 ±0.65
52(50) ±1.50
0.20 × 40
40
75(65)
±0.80
0.20 × 50 50 85(80) ±1.75
0.25 × 13 13 ±0.55 35 ±1.400.35 0.25 × 25 0.25
25 ±0.65 52(50) ±1.50
0.25 × 40
40 ±0.80
75(65)
0.25 × 50
50 85(80) ±1.75
0.25 × 75
75 ±0.95 110(105
0.30 × 13 13 ±0.55 35 ±1.25 0.30 × 25
25 ±0.65
52(50) ±1.50
0.30 × 40 0.30
40
75(65) 0.40
±0.80
0.30 × 50
50 85(80) ±1.75
0.30 × 75
±0.015
75 ±0.95 110(105
0.30 ×100
100 ±1.10 150(140 ±2.00
0.35 × 13 13 ±0.55 35 ±1.25 0.35 × 25
25 ±0.65 52(50) ±1.50
0.35 × 40
40 ±0.80
75(65)
0.35
0.40
0.35 × 50
50
85(80) ±1.75
0.35 × 75
75 ±0.95 110(105
0.35 ×100 100 ±1.10 150(140 ±2.00 0.40 × 13
13 ±0.55 35 ±1.25
0.40 × 25 0.40
25 ±0.65 52(50) ±1.50
0.45
0.40 × 40
40
±0.80
75(65)
第
3页共5页
医疗器械产品技术要求编号:黔械注准 20182270011
0.40 × 50 50
85(80)
±1.75
0.40 × 75 75 ±0.95 110(105
0.40 ×100 100 ±1.10 150(140 ±2.00 0.45 × 13 13 ±0.55 35 ±1.25 0.45 × 25 25 ±0.65 52(50)
±1.50
0.45 × 40 40
75(65)
±0.80
0.45 0.45
50 85(80)
× 50
±1.75
0.45 × 75 75 ±0.95 110(105
0.45 ×100
100
±1.10 150(140
±2.00
2.2 灭菌针灸针的针体硬度 应符合表 2 的规定
表 2
d ,mm
硬度 HV0.2kg
灭菌针灸针
0.16
, 0.18 , 0.20 ,0.25 ,0.30 ≥ 460 0.35
, 0.40 , 0.45 ≥
450
2.3 灭菌针灸针的针尖
灭菌针灸针的针尖部位应圆正不偏, 无毛刺、弯勾等缺
陷,经规定的力与硬块接触顶压后,其穿刺力应不大于表
3 的规定。
表 3
d,mm
顶压力, N
穿刺力, N
0.16,0.18,0.20,0.25
0.4 0.7 0.30,0.35
0.5 0.8 0.40,0.45
0.6
0.9
2.4 针体韧性 针体应有良好的韧性,缠绕试验后不应有裂缝、折断和分层。
2.5 表面质量 针体表面应光滑,其外观质量和表面粗糙度参数 Ra 值应符合表 4
的规定。
表 4
产品品种 灭菌针灸针
外观质量
不得有明显的伤痕、曲痕及丝纹等缺陷
Ra 值 ≤
0.63
2.6 针体与针柄的连接应牢固,在表 5 规定的力值下作拉拔试验,二者轴向移位
不得大于 3 mm 。
第 4页共5页
医疗器械产品技术要求编号:黔械注准20182270011
表 5
d,mm 拉力( N)
0.16 ,0.18 7
0.20 ,0.25 9
0.30 ,0.35 14
0.40 ,0.45 19
2.7 螺旋圈排列灭菌针灸针的针柄如采用缠绕丝,其螺旋圈应排列均匀,无明显离距。
2.8针柄灭菌针灸针的柄部不得有毛刺。
2.9平直灭菌针炙针应挺直,不得有明显的弯曲。
2.10色泽灭菌针灸针的柄部表面色泽应均匀。
柄部如采用镀银,镀层应呈银白色,不得有起层现象。
2.11耐腐蚀性灭菌针灸针应具有良好的抗腐蚀性能。
2.12无菌灭菌针灸针应无菌。
第5页共5页。
