中国农业大学_807环境化学与环境监测_《环境化学》课件_环境化学第三章
合集下载
环境化学-第三章-水环境化学-第二节-水中无机污染物的迁移转化知识交流

之,pE越大,电子浓度越低,体系接受电子的倾向就越强。
(2)氧化还原电位E和pE的关系
Ox +ne→Red
(1)
根据Nernst方程
E=E0-(2.303RT/nF)lg[Red]/[Ox] (2) 当反应达平衡时,定义
E0=(2.303RT/nF) lgK
(3)
从上述化学方程式(1),可写出
K= [Red]/{[Ox][e]n }
如果考虑到羟基配合作用,那么金属氧化物或氢氧化物的 溶解度(MeT)表征为:
MeT = [ Mez+ ] +∑[ Me(OH)nz-n ]
固体的氧化物和氢氧化物具有两性的特征,它们和质子或 羟基离子都发生反应,存在一个pH值,在该值下溶解度为最 小值。在碱性或酸性更强的pH值区域内,溶解度都会变得更 大。
因此,在 H2S 和硫化物均达到饱和的溶液中,溶液重金属离子 的饱和浓度为: [Me2+]=Ksp/[S2-]=Ksp [H+]2/Ksp´ =Ksp [H+]2/(0.1K1K2)
3、碳酸盐
——多相平衡,pH通过控制碳酸根浓度影响沉淀平衡
封闭体系: 只考虑固相和液相,把 H2CO3* 当作不挥发酸类处理。
吸附量随粒度增大而减少,并且当溶质浓度范围固定 时,吸附量随颗粒物浓度增大而减少。
温度变化、几种离子共存(竞争作用)等。
3、沉积物中重金属的释放——属于二次污染问题
诱发释放的主要因素有: (1)盐浓度升高:碱金属和碱土金属阳离子可将被吸附在固体颗
粒上的金属离子交换出来。
(2)氧化还原条件的变化:有机物增多,产生厌氧环境、铁锰氧 化物还原溶解,使结合在其中的金属释放出来。
2、它在中性表面甚至在与吸附离子带相同电荷符号的表面 也能进行吸附作用。
环境化学第3.2章水环境化学水中无机污染物的溶解和沉淀课件

纯水封闭体系中金属碳酸盐的溶解度
20
第三章/第二节/2.3 溶解和沉淀
2.3.4 碳酸盐 四、碳酸盐在开放体系的溶解度(二价金属)
[H2CO3*] = KHpCO2 [CO32-] = K1K2KHpCO2/[H+]2
pH>pK2(10.33) pK1<pH<pK2 (6.35~10.33) [Me2+] ≈ Ksp[H+]2/K1K2KHpCO2 pH<pK1(6.35)
第三章/第二节 水中无机污染物的迁移转化
2.3 溶解和沉淀
溶解/沉淀对迁移过程的影响
溶解/沉淀影响金属化合物溶解度,溶解度决定随水迁移能力 溶解度大,迁移能力大;溶解度小,迁移能力小
溶解/沉淀理论
溶解/沉淀受反应平衡和反应速率控制(化学热力学和动力学控制) 固-液平衡体系中,用溶度积来表征溶解度
第三章/第二节/2.3 溶解和沉淀
2.3.3 硫化物
二、金属硫化物的溶解度(以二价金属为例)
1. 金属硫化物的沉淀-溶解平衡
MeS (s) ⇌ Me2+ + S2-
[Me2+] = Ksp/[S2-]
2. H2S的电离平衡
H2S ⇌ H+ + HS- K1 = 8.9×10-8
HS- ⇌ H+ + S2-
= 2.532×10-3 mol/L
15
第三章/第二节/2.3 溶解和沉淀
2.3.4 碳酸盐
一、碳酸盐的沉淀-溶解平衡(以二价金属为例)
MeCO3 ⇌ Me2+ + CO32[Me2+] = Ksp/[CO32-] = Ksp/(CTα2)
H2CO3* ⇌ HCO3- + H+
20
第三章/第二节/2.3 溶解和沉淀
2.3.4 碳酸盐 四、碳酸盐在开放体系的溶解度(二价金属)
[H2CO3*] = KHpCO2 [CO32-] = K1K2KHpCO2/[H+]2
pH>pK2(10.33) pK1<pH<pK2 (6.35~10.33) [Me2+] ≈ Ksp[H+]2/K1K2KHpCO2 pH<pK1(6.35)
第三章/第二节 水中无机污染物的迁移转化
2.3 溶解和沉淀
溶解/沉淀对迁移过程的影响
溶解/沉淀影响金属化合物溶解度,溶解度决定随水迁移能力 溶解度大,迁移能力大;溶解度小,迁移能力小
溶解/沉淀理论
溶解/沉淀受反应平衡和反应速率控制(化学热力学和动力学控制) 固-液平衡体系中,用溶度积来表征溶解度
第三章/第二节/2.3 溶解和沉淀
2.3.3 硫化物
二、金属硫化物的溶解度(以二价金属为例)
1. 金属硫化物的沉淀-溶解平衡
MeS (s) ⇌ Me2+ + S2-
[Me2+] = Ksp/[S2-]
2. H2S的电离平衡
H2S ⇌ H+ + HS- K1 = 8.9×10-8
HS- ⇌ H+ + S2-
= 2.532×10-3 mol/L
15
第三章/第二节/2.3 溶解和沉淀
2.3.4 碳酸盐
一、碳酸盐的沉淀-溶解平衡(以二价金属为例)
MeCO3 ⇌ Me2+ + CO32[Me2+] = Ksp/[CO32-] = Ksp/(CTα2)
H2CO3* ⇌ HCO3- + H+
中国农业大学_807环境化学与环境监测_《环境化学》课件_环境化学第三章2

层状硅铝酸盐,代表性矿物有水云母、蒙脱石、高岭石等。
粘土矿物的粒径比原生矿物小得多,是一种凝胶。
第四节
水中胶体物质及其吸附作用
2.金属水合氧化物
铝、铁、锰、硅等金属的水合氧化物在天然水中以无机高
分子及溶胶的形态存在。
3.腐殖质和有机胶体 腐殖质是一种天然的带负电的有机胶体。藻类、细菌及病 毒是一类天然的生物有机胶体。排入废水中的表面活性剂, 与泄漏在水中的油滴、憎水有机物质形成的乳浊液也类似 于有机胶体。
第四节
水中胶体物质及其吸附作用
半径在 0.1~1 nm 的颗粒的许多性质与胶体相类似,一般也
将其归为胶体物质。下面分别叙述天然水中的胶体物质的 类别。 1. 矿物微粒和粘土矿物 天然水中常见矿物微粒一般为原生矿物,主要有石英、长 石、云母类矿物,这类矿物颗粒较粗,构成了水中颗粒物 的主要部分。粘土矿物为原生矿物经化学风化作用而成的
第四节
水中胶体物质及其吸附作用
一、
天然水中的胶体物质
水环境中的胶体物质主要有无机胶体,有机胶体和无
机 — 有机复合胶体。这些物质根据它们的半径的不同而呈
现为凝胶或溶胶的形式,有些胶体物质通过静电聚合作用
凝聚在一起,可形成颗粒物。 对分散系的划分大致为:溶解半径 < 1 nm溶质的溶液称 为真溶液;溶解粒子的半径 > 1 nm属粗分散系统。其中半 径在1~100 nm 的为胶体分散系统,对应大小的固体超细粉 料即为所谓的纳米材料。
Ka1 Ka2 +H NRCOOH === +H NRCOO- === H NRCOO3 3 2
低pH 中等pH 高4.胶体的双电层 胶体表面存在电荷,使溶液中固液界面区域内电荷分布被扰 乱而形成局部的不均等分布,由此构成胶体的双电层。根据 一系列的由于静电吸引作用和热运动两种效应,所以在溶液
环境化学 2008_第三章 化学污染物的转化行为
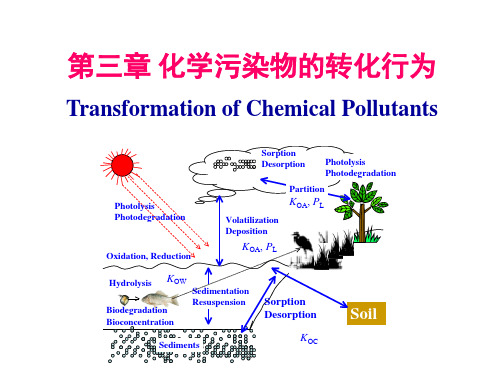
迁移:污染物在环境介质内部或环境介质之间的物理运动 (时间和空间)。不发生化学变化。 物理转化:相变、渗透、凝聚、吸附以及放射性元素蜕变等。 化学转化:光化学氧化、氧化还原和络合水解等作用。 生物化学转化:生物的吸收和代谢作用而发生的变化 。
二、空气中硫氧化物的转化和硫酸烟雾型污染
Transformation of Sulfur Oxides in Air and Pollution of Sulfuric Acid Aerosol 1. 硫的来源 人为来源: 含硫矿物燃料燃烧 煤 (0.5-6%)占60%
n MeT [Me ] [Me(OH)z n ] z 1 n
PbO (s) + 2H PbO (s) + H
+
+
Pb2++H2O Pb(OH)+ Pb(OH)2 Pb(OH)3- +H+
lgKs0=12.7 lgKs1=5.0 lgKs2=-4.4 lgKs3=-15.4
PbO (s) + H2O PbO (s) + 2H2O
四、配合平衡
重要的无机配位体有:OH-、Cl-、CO32-、HCO3-、F-、S2-等。 有机配位体:天然水体中有动植物组织的天然降解产物,如氨 基酸、糖、腐殖酸;生活废水中有洗涤剂、清洁剂、EDTA、 农药和大分子环状化合物等。这些有机物相当一部分具有配合 能力。 (1) 配合物在溶液中的稳定性
对眼睛和呼吸道有强刺激作用。 O3等氧化剂
臭氧浓度 出现时间 毒 性
严重时可导致死亡。
注:本表摘自王晓蓉,1993。
有强氧化破坏作用,严重时可导致死亡。
三、溶解-沉淀
1. 金属类污染物可能发生的迁移和转化过程
二、空气中硫氧化物的转化和硫酸烟雾型污染
Transformation of Sulfur Oxides in Air and Pollution of Sulfuric Acid Aerosol 1. 硫的来源 人为来源: 含硫矿物燃料燃烧 煤 (0.5-6%)占60%
n MeT [Me ] [Me(OH)z n ] z 1 n
PbO (s) + 2H PbO (s) + H
+
+
Pb2++H2O Pb(OH)+ Pb(OH)2 Pb(OH)3- +H+
lgKs0=12.7 lgKs1=5.0 lgKs2=-4.4 lgKs3=-15.4
PbO (s) + H2O PbO (s) + 2H2O
四、配合平衡
重要的无机配位体有:OH-、Cl-、CO32-、HCO3-、F-、S2-等。 有机配位体:天然水体中有动植物组织的天然降解产物,如氨 基酸、糖、腐殖酸;生活废水中有洗涤剂、清洁剂、EDTA、 农药和大分子环状化合物等。这些有机物相当一部分具有配合 能力。 (1) 配合物在溶液中的稳定性
对眼睛和呼吸道有强刺激作用。 O3等氧化剂
臭氧浓度 出现时间 毒 性
严重时可导致死亡。
注:本表摘自王晓蓉,1993。
有强氧化破坏作用,严重时可导致死亡。
三、溶解-沉淀
1. 金属类污染物可能发生的迁移和转化过程
环境化学 第三章空气与废气监测

1) 含硫化合物:SO2、H2S; SO3、硫酸、硫酸盐; 2) 含氮化合物:NO、NO2、NH3; 硝酸、硝酸盐; 3) 碳氧化合物:CO、CO2; 4) 卤素化合物:HF、HCl、Cl2; 5) 碳氢化合物: 6) 其它有机化合物:
粒子状态污染物
粒子状态污染物:即颗粒物,是分散在大
气中的微小固体和液体颗粒,粒径多在0.01100μm之间,是一个复杂的非均匀体系。
对动植物的危害
• 美国蒙塔那洲一铜冶炼厂排出大量SO2、 As2O3,污染周围牧草,草中含砷400PPm, 使在24Km内的羊群大量死亡。
• 臭氧使美国每年森林农作物经济损失超过30 亿美元
• 哥伦比亚的炼铜厂SO2污染,使该厂南部52 英里内30%的树木,南部33英里内60%的树 木死亡或者严重受损。
对材料的损坏
• SO2能腐蚀暴露于空气中的金属制品,使 皮革、纸张、纺织品变脆;
• H2S能使白色铅涂料变成黑色; • 光化学烟雾能使橡胶轮胎龟裂、电镀层加
速腐蚀; • 高浓度的NOx能使尼龙织品分解。
对大气的影响
改变大气的性质和气候的形式
• CO2吸收地面的辐射,颗粒物对阳光的散射 作用能改变地面温度,使温度上升或者下降 (温室效应)
1. 功能区布点法
多用于区域性的常规监测
(1) 先将监测区域划分成工业区、商业区、居 住区、工业和居住混合区、交通密集区、清洁 区等不同功能区
(2) 再根据具体污染情况,按功能区的地形、气 象、人口密度、建筑密度等,在每个功能区 设若干采样点
2. 网格布点法
•适用于有多个污染源,且污染源分布较均匀的地区 •将监测区域划分成若干均匀网状方格,采样点设在两 条直线的交点处或方格中心
家庭炉灶与取暖设备排气 室内空气污染源
粒子状态污染物
粒子状态污染物:即颗粒物,是分散在大
气中的微小固体和液体颗粒,粒径多在0.01100μm之间,是一个复杂的非均匀体系。
对动植物的危害
• 美国蒙塔那洲一铜冶炼厂排出大量SO2、 As2O3,污染周围牧草,草中含砷400PPm, 使在24Km内的羊群大量死亡。
• 臭氧使美国每年森林农作物经济损失超过30 亿美元
• 哥伦比亚的炼铜厂SO2污染,使该厂南部52 英里内30%的树木,南部33英里内60%的树 木死亡或者严重受损。
对材料的损坏
• SO2能腐蚀暴露于空气中的金属制品,使 皮革、纸张、纺织品变脆;
• H2S能使白色铅涂料变成黑色; • 光化学烟雾能使橡胶轮胎龟裂、电镀层加
速腐蚀; • 高浓度的NOx能使尼龙织品分解。
对大气的影响
改变大气的性质和气候的形式
• CO2吸收地面的辐射,颗粒物对阳光的散射 作用能改变地面温度,使温度上升或者下降 (温室效应)
1. 功能区布点法
多用于区域性的常规监测
(1) 先将监测区域划分成工业区、商业区、居 住区、工业和居住混合区、交通密集区、清洁 区等不同功能区
(2) 再根据具体污染情况,按功能区的地形、气 象、人口密度、建筑密度等,在每个功能区 设若干采样点
2. 网格布点法
•适用于有多个污染源,且污染源分布较均匀的地区 •将监测区域划分成若干均匀网状方格,采样点设在两 条直线的交点处或方格中心
家庭炉灶与取暖设备排气 室内空气污染源
中国农业大学_807环境化学与环境监测_《环境化学》课件_第二章 水环境化学

表面张力 溶解能力 介电常数 电离度 密 度 透明度 热传导 氢键 偶极矩 存在状态
2. 3 水质标准和水质指标
2.3 水质标准和水质指标
一、水质标准 水质标准是环境质量标准的重要组成部分。所谓环境质 量标准就是环境中的污染物具有法律效力的限量。包括 环境水质标准和污水排放标准两大类。前者又分为饮用 水质标准、渔业用水质标准,工业用水质标准等多种; 后者如工业“三废”排放标准等。理论上讲,排放标准 首要应当以保障环境水质标准为基本目标。 水质标准的确定是以保护人体健康和生态平衡为目的, 用客观的科学数据表示各污染物在适合于一种较高要求 的生态系统生存的水体中所允许的限量。同时还要考虑 具体的自然条件和国家的经济技术条件等因素。所以各 国的水质标准有明显的差异
凝固点 (摄氏度) 沸 点 (摄氏度) 偶极矩 (德 拜 ) 汽化热 (千焦/摩) 融化热 (千焦/摩) 生成热 (千焦/摩)
化合物
H2O H2O推测 H2S H2Se H2Te
0 (-95) -85.2 -65.7 -51
100 (-80) -60.3 -41.3 -2.2
1.84 (2.58) 1.10 0.40 <0.20
2.1 水在地球上的分布及水循环
一、天然水的分布 二、水循环
三、我国水资源状况
2.1
水在地球上的分布及水循环
全 球 水 量 分 布 比 例
2.1 水在地球上的分布及水循环
表2-1 地球上各种水的储量
序 号 类 别 水储量 (万亿m3)
1338000 23400 12870 10530 16.5 24064.1 300.0 176.4 85.4 91.0 11.47 2.12 1.12 12.9 1385984.61 35029.21
中国农业大学_807环境化学与环境监测_《环境化学》课件_第四章 大气环境和性质
中毒情况
数千人发病60人死亡,咳嗽、呼 吸短促、流泪等 4天内6000人患病,17人死亡, 咳嗽、喉痛、胸闷 5天内4000人死亡,已发生12次 死近万人,胸闷、咳嗽、喉痛 400人死亡,多数人患病,刺激 眼、鼻、喉,引起眼病,喉炎
原因
SO2转化为SO3进入 肺部 SO2同烟尘作用生成硫 酸盐,吸入肺部 粉尘中Fe2O3使SO2转为 硫酸,吸入肺部
食用含有甲基汞的鱼
使用含镉米和含镉水 有毒重金属颗粒及 SO2吸入肺部 食用含有多氯联苯的 米糠油
第一节 60年代后
大气污染化学概述
酸性降水在北美、北欧的出现,人们便开展了酸
雨形成机制的研究,并发现了酸雨的前体物(SOx和NOx)以 及几种氧化致酸的途径和作用。(发展了液相和多相化学)
70年代后 由于南极上空“臭氧洞”的发现以及温室效应对气
增加而降低。
第二节 天然大气环境特征及化学组成
2、电离状态------ 60km以上为电离层,离子密度大, 60~90km主要为NO光解离; 90~120km主要为O2光解
大气的总质量约为5.2×1015吨,仅占地球质量的106分之一。其中90%集中
在地球表面30km以内。
第二节 天然大气环境特征及化学组成 一、大气的范围及结构 根据大气在铅直方向上的温度、化学组成、物理特性,大气
圈可分为若干层次。
●按大气中化学组成的分布,大气圈可分为均质层(90km 以下)和非均质层(90km以上); ●按大气的电离状态分布,可将在大气分为电离层(60km 以上)和非电离层(60km以下)。
候变暖的作用,使得人们开始注意并研究 氯氟烃(CFCs)等痕量气体对平流层O3的耗损, 及CO2、CH4增多而造成的地球温室效应。 (平流层化学迅速发展)(目前臭氧洞已达2800万平方公里).
环境化学全部ppt课件
20世纪70年代:出版一系列专著,建立一系列 研究计划。《增长的极限》
25
20世纪80年代:生命元素的生物地球化 学循环、化学品安全评价、全球变化及全球 性环境问题研究。
26
2.环境化学的定义 环境化学:环境化学是一门研究有害化学物质在
环境介质中的存在、化学特性、行为和效应及其控 制的化学原理和方法的科学。
13
第一章 绪 论
1
环境化学
2
环境污染物
14
1. 环境问题(Environmental Problems)
1.1环境污染(Environmental pollution)
环境污染: 由于人为因素使环境的构成或状态发
生变化,环境素质下降,从而扰乱了生态系统和人 们的正常生活条件和生产条件,就叫做环境污染。
为是怎样的? 3.SO2及潜在有害物质在环境中经过迁移转化将会
产生哪些危害,其危害机制如何? 4.如何预防酸雨的产生或减缓酸雨产生的危害?
29
4. 环境化学的研究特点 ●从微观的原子、分子水平上,研究宏观的环境现
象与变化的化学机制及其防治途径; ● 其核心是研究化学污染物在环境中的化学转化和
效应。 ● 污染物种类众多,形态多变;浓度低;分布广泛,
第三阶段:90年代以来 巩固和发展“持续发展”的战略思想。 ——把环境保护与经济、社会协调发展。
23
二、环境化学
1. 环境化学的发展 环境化学的发展:
孕育阶段:二次大战-1970年; 形成阶段:70-80年代; 发展阶段:80年代。
24
二次大战-20世纪60年代:研究环境中农药 (有机氯)残留行为。《寂静的春天》-卡逊
27
3. 环境化学的研究内容
有害物质在环境中存在的浓度水平和形态;
25
20世纪80年代:生命元素的生物地球化 学循环、化学品安全评价、全球变化及全球 性环境问题研究。
26
2.环境化学的定义 环境化学:环境化学是一门研究有害化学物质在
环境介质中的存在、化学特性、行为和效应及其控 制的化学原理和方法的科学。
13
第一章 绪 论
1
环境化学
2
环境污染物
14
1. 环境问题(Environmental Problems)
1.1环境污染(Environmental pollution)
环境污染: 由于人为因素使环境的构成或状态发
生变化,环境素质下降,从而扰乱了生态系统和人 们的正常生活条件和生产条件,就叫做环境污染。
为是怎样的? 3.SO2及潜在有害物质在环境中经过迁移转化将会
产生哪些危害,其危害机制如何? 4.如何预防酸雨的产生或减缓酸雨产生的危害?
29
4. 环境化学的研究特点 ●从微观的原子、分子水平上,研究宏观的环境现
象与变化的化学机制及其防治途径; ● 其核心是研究化学污染物在环境中的化学转化和
效应。 ● 污染物种类众多,形态多变;浓度低;分布广泛,
第三阶段:90年代以来 巩固和发展“持续发展”的战略思想。 ——把环境保护与经济、社会协调发展。
23
二、环境化学
1. 环境化学的发展 环境化学的发展:
孕育阶段:二次大战-1970年; 形成阶段:70-80年代; 发展阶段:80年代。
24
二次大战-20世纪60年代:研究环境中农药 (有机氯)残留行为。《寂静的春天》-卡逊
27
3. 环境化学的研究内容
有害物质在环境中存在的浓度水平和形态;
环境化学 (第三章 水环境化学)第三节
根据上述方程,作者对虹鳟鱼又 得到下列相关方程: lg(BCF) = -0.802 lgSw - 0.497 n = 7 r = 0.977
27
生物浓缩因子 (BCF)
上述结果是对较高等生物而言, 对占水体生物量大部分的微生物也 可获得类似的相关方程。
28
二、挥发作用(略)
挥发作用是指有机物质从溶解态转向 气态的过程。挥发速率与有毒物的性 质和水体特征有关
分配作用(partition) 吸附作用(adsorption)
2
吸附作用(adsorption)
在非极性有机溶剂中,土壤矿物质对有机 化合物的表面吸附作用,或干土壤矿物 质对有机化合物的表面吸附作用。
前者靠范德华力,后者是化学键力,如氢 键、离子偶极键、配位键、π键等。
3
吸附作用(adsorption)
有机污染物的挥发速率( c / t )及
挥发速率常数( Kv )的关系:
C / t KvC
29
三、水解作用(简述)
有机毒物与水的反应是X-基团与OH-基 团交换的过程:
RX H 2O ROH HX
在水体环境条件下,可能发生水解的 官能团有烷基卤、酰胺、胺、氨基甲酸脂 羧酸脂、环氧化物、腈、磷酸脂、 磺酸脂、 硫酸脂等。
25
生物浓缩因子 (BCF)
lg(BCF) = 0.542 lgKow + 0.124 n=8 r=0.948
lg(BCF) = 0.980 lgKow - 0.063 n=5 r=0.991
将生物的类脂含量加以标化,两个 方程的差别将减少。
26
生物浓缩因子 (BCF)
同Koc的相关性一样,lg(BCF)也与 溶解度相关。
27
生物浓缩因子 (BCF)
上述结果是对较高等生物而言, 对占水体生物量大部分的微生物也 可获得类似的相关方程。
28
二、挥发作用(略)
挥发作用是指有机物质从溶解态转向 气态的过程。挥发速率与有毒物的性 质和水体特征有关
分配作用(partition) 吸附作用(adsorption)
2
吸附作用(adsorption)
在非极性有机溶剂中,土壤矿物质对有机 化合物的表面吸附作用,或干土壤矿物 质对有机化合物的表面吸附作用。
前者靠范德华力,后者是化学键力,如氢 键、离子偶极键、配位键、π键等。
3
吸附作用(adsorption)
有机污染物的挥发速率( c / t )及
挥发速率常数( Kv )的关系:
C / t KvC
29
三、水解作用(简述)
有机毒物与水的反应是X-基团与OH-基 团交换的过程:
RX H 2O ROH HX
在水体环境条件下,可能发生水解的 官能团有烷基卤、酰胺、胺、氨基甲酸脂 羧酸脂、环氧化物、腈、磷酸脂、 磺酸脂、 硫酸脂等。
25
生物浓缩因子 (BCF)
lg(BCF) = 0.542 lgKow + 0.124 n=8 r=0.948
lg(BCF) = 0.980 lgKow - 0.063 n=5 r=0.991
将生物的类脂含量加以标化,两个 方程的差别将减少。
26
生物浓缩因子 (BCF)
同Koc的相关性一样,lg(BCF)也与 溶解度相关。
环境化学-绪论 PPT课件
环境问题
• 人类生活和生产活动不断影响和改变环境条件,甚至引起环 境污染。
• 工业化过程中的处置失当,特别是对自然资源的不合理开发 利用,造成了全球性的环境污染和生态破坏。 空气、水和土地污染的环境退化现象 臭氧层破坏 气候变化 水资源的短缺和污染 有毒化学品和团体废弃物的危害 生物多样性的损伤
2. 造成环境污染的三因素 物理的
噪声、震动等 化学的
九大类 生物的
大米草、水葫芦、赤藻等
温室效应
酸雨
光化学烟雾
伦敦烟雾事件
臭氧空洞
海洋污染
赤潮
农药污染
3. 认识环境问题的三个阶段
环境问题并非只限于环境污染,人们对现代环境 问题的认识有个发展过程。 第一阶段:在20世纪60年代人们把环境问题只当成一 个污染问题,认为环境污染主要指的是城市和工农业 发展带来的对大气、水质、土壤、固体废弃物和噪声 的污染。对土地沙化、热带森林破坏和野生动物某些 品种的濒危灭绝等并未从战略上予以重视。我国当时 以污染控制为中心进行环境管理,曾对改善城市和人 民生活的环境质量起了重要作用。 存在问题:没有把环境问题与自然生态联系起来,低 估了环境污染的危害性和复杂性,没有把环境污染与 社会因素相联系,未能追根寻源。
每年有600万公顷具有生产力的旱地变成沙漠
有1100多万公顷的森林遭到破坏
在非洲,干旱将3500万人置于危难之中
在印度,博帕尔农药厂化学品泄漏造成两千人死亡
在墨西哥城,液化气罐爆炸使千人遇难
在前苏联,切尔诺贝利核反应堆爆炸使核尘埃遍布欧洲
在瑞士,农用化学品、溶剂和录污染了莱茵河,使数百万 尾鱼被毒死
样是热门课题。
(2)各圈层环境化学
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一节
水环境中的沉淀溶解反应
3、相互结合的离子半径差别愈小,其离子化合物愈牢固, 即难溶解。 溶解度小于0.01克/100克水的物质叫做“难溶物” 地表水和沉积物的孔隙水中主要阴离子Cl-、SO2-4、HCO-3
还原条件下有H2S衍生的HS-与S2-,碳酸盐、氢氧化物、硫 化物难溶。
第一节
水环境中的沉淀溶解反应
一、氧化物和氢氧化物
金属氢氧化物沉淀有多种形态,它们在水环境中的行为差
别很大。氧化物可看成是氢氧化物脱水而成。金属氢氧化 物的沉淀溶解平衡可以用化学反应的通式表述:
Me (OH)n(s) ==== Me n+ + nOH¯ Ksp = [Me n+][OH–]n [Me n+]= Ksp/[OH–]n = Ksp[H+]n / Knw
pc = ( pKsp – npKw ) + npH (3-1)
第一节
水环境中的沉淀溶解反应
1、pc 与pH成直线关系,即在一定的pH的范围内, pH 越高,金属离子的浓度越低;
2、金属离子的价数就是浓度随pH变化的斜率,其中
lg[Men+] 与pH的关系,斜率分别为 -1、-2、-3。 Ag+、Hg+ 的斜率为 1; Ca2+ 、 Mg2+ 、 Fe2+ 、 Mn2+ 、 Zn2+ 、 Pb2+ 、 Cu2+ 、 Hg2+ 、 Ni2+ 、 Cd2+ 、 Co2+ 的斜率为 2; Al3+、Fe3+、Cr3+ 的斜率为 3; 3、当pc = 0时(-lg[Men+] = 0 即 [Men+] = 1 mol/L), 直线在横轴上的pH值为截距 , 用下式计算:
上边所讨论的并不能充分反映出溶解度,应该考虑OH-与 金属离子可进行配合,金属离子氧化物和氢氧化物的溶解 度:
MeT=[Mez+]+∑[Me(OH)nz-n]
第一节
水环境中的沉淀溶解反应
铅的各种形态与水体pH的关系以及所对应的浓度
(1) H2O ==== H+ + OH¯ (2) PbO(s) + 2H+ ==== Pb2+ + H2O (3) PbO(s) + H+ ==== PbOH + lgKw = -14 lg*Ks0 = 12.7 lg*Ks1 = 5.0
(4) PbO(s) + H2O ==== Pb (OH)20 lg Ks2 = -4.4 (5) PbO(s) + 2H2O ==== Pb (OH)3¯+ H+ lg*Ks3 = -15.4 lg[Pb2+] = 12.7 – 2pH ①
lg[PbOH +] = 5.0 – pH
lg[Pb (OH)20] = – 4.4
(不同文献的平衡常数有差异)
第一节
水环境中的沉淀溶解反应
水对许多物质有很强的溶解能力,是由于它有很高的介电常数, 1、水是强极性分子,对极性大的离子键化合物的溶解能力比极
性小的共价键化合物的溶解能力大。金属离子与SO42-之间为离
子键,在水中的溶解度远大于共价键的金属硫化物。
AgF(离子晶格)的溶解度大于 AgCl(共价键) 2、对离子键化合物来说,溶解度随着离子半径的增大和电价 的减少而增加,Na3PO4、 Na2SO4 、 Na2CO3均易溶 ,而 Ca3(PO 4)2 、 CaSO4 、 CaCO3均难溶 。
水环境中的沉淀溶解反应
1、金属离子在水中的沉淀溶解过程往往是一些非均相反
应,这些反应进行得缓慢,在动态环境中不易达到平衡。
2、热力学理论中所阐述的物相关系不一定与实际沉淀反 应完全一致。(沉淀可以进一步转化) 3、在实际中往往出现化合物的溶解量大于其溶解度的情 况,即存在过饱和现象。 4、固体溶解所产生的离子可能在溶液中进一步反应。 5、用于计算的平衡常数因测定条一节
水环境中的沉淀溶解反应
图中阴影所包围的区域为PbO(s)稳定存在的区域,
阴影以外的区域为溶解的铅形态,
[Pb(Ⅱ)T]=[Pb2+]+[ PbOH +]+[ Pb (OH)20]+[ Pb (OH)3¯]
第三章
第一节
水环境化学
水环境中的沉淀溶解反应
金属离子在水环境中的迁移与否,迁移能力的大小多和这 些离子的化合物在水中的沉淀和溶解反应紧密相关。在金属离 子中,溶解度小者,其在水中的迁移能力小,溶解度大者的迁 移能力大。
第一节
水环境中的沉淀溶解反应
在固—液平衡体系中,一般用溶度积来表征溶解度大小。
第三章 水环境化学
Chapter3. Aquatic Environmental Chemistry
从化学过程和原理方面阐明天然水中的各种化学平衡 问题和无机离子,特别是重金属离子,有机化合物等 在天然水中分布、迁移、转化和归宿规律.
第三章
水环境化学
第一节 水环境中的沉淀溶解反应 第二节 水环境中的配合反应 第三节 水环境中的氧化与还原反应 第四节水中胶体物质及其吸附作用 第五节 水中有机污染物的迁移转化
尽管在化学理论研究上,溶度积的获得具有严格的条件, 将
其用于解释天然水中各种化合物的沉淀溶解性质时存在一定 偏差, 但在水环境中各种无机化合物的溶解度或沉淀反应仍 遵守溶度积原则。 在用溶度积讨论无机化合物的沉淀溶解反应平衡,以及
这一反应对金属离子迁移、转化的具体影响时----------?
第一节 要注意的是:
pH = 14 – 1/n pKsp
第一节
水环境中的沉淀溶解反应
第一节
水环境中的沉淀溶解反应
1、从图中可看出各金属离子生成氢氧化物沉淀的先后。 2、金属离子的浓度已知,可知道该金属离子开始沉淀时的 pH值。
3、同价金属离子均有相同的斜率,靠右边斜线代表的金属 氢氧化物的溶解度大于靠左边的金属氢氧化物的溶解度。
②
③
lg[Pb (OH)3¯] = – 15.4 + pH
④
第一节
水环境中的沉淀溶解反应
可见除[Pb (OH)20]与pH无关外,其余3种铅形态都与溶液
中H+离子浓度有关,Pb2+、PbOH +、Pb (OH)20和Pb(OH)3---对
数值作为pH值函数特征线的斜率分别为–2、–1、0和 +1, 将有关铅形态浓度的对数对 pH 作图,可得 Pb的溶解度与 pH的关系, 其中lg[Pb (OH)20]是一条与pH无关的水平线
