高一化学知识点总结铝及其化合物
高一上四大基本金属元素钠镁铝铁单质及其化合物化学和对应离子方程式总结
NO3- + 2+
Fe3+ + 3H2O
Fe(OH)3(胶体) + 3H+
Cl2 少量: 6FeBr2 + 3Cl2 == 2FeCl3 +4FeBr3 Cl2 过量:2FeBr2+ 3Cl2 == 2FeCl3 + 2Br2
2Fe2+ + Cl2 == 2Fe3+ + 2Cl2Fe2+ + 4Br- + 3Cl2 == 2Fe3+ + 2Br2 + 6Cl-
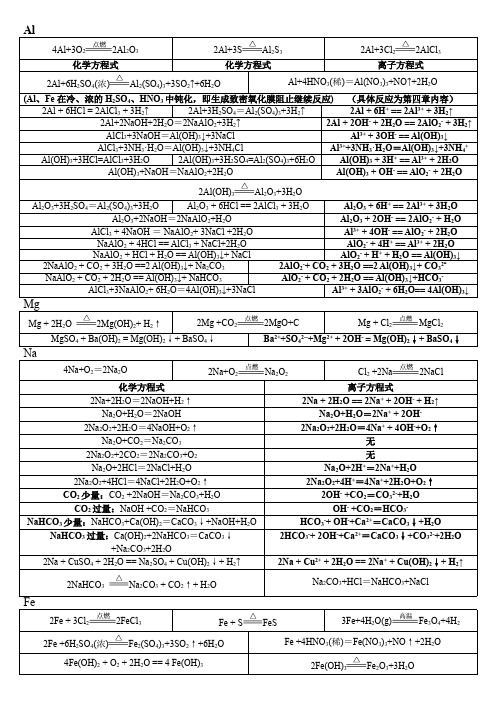
Al2O3+3H2SO4=Al2(SO4)3+3H2O Al2O3 + 6HCl == 2AlCl3 + 3H2O Al2O3 + 6H+ == 2Al3+ + 3H2O Al2O3+2NaOH=2NaAlO2+H2O Al2O3 + 2OH- == 2AlO2- + H2O AlCl3 + 4NaOH = NaAlO2+ 3NaCl +2H2O Al3+ + 4OH- == AlO2- + 2H2O NaAlO2 + 4HCl == AlCl3 + NaCl+2H2O AlO2- + 4H+ == Al3+ + 2H2O NaAlO2 + HCl + H2O == Al(OH)3↓+ NaCl AlO2- + H+ + H2O == Al(OH)3↓ 2NaAlO2 + CO2 + 3H2O ==2 Al(OH)3↓+ Na2CO3 2AlO2-+ CO2 + 3H2O ==2 Al(OH)3↓+ CO32NaAlO2 + CO2 + 2H2O == Al(OH)3↓+ NaHCO3 AlO2- + CO2 + 2H2O == Al(OH)3↓+HCO3AlCl3+3NaAlO2+ 6H2O=4Al(OH)3↓+3NaCl Al3+ + 3AlO2- + 6H2O== 4Al(OH)3↓
高一铝的重要化合物知识点

高一铝的重要化合物知识点铝是一种重要的金属元素,广泛应用于工业生产和日常生活中。
在高一化学学习中,了解铝及其重要化合物的性质、制备方法和应用是必要的。
下面将介绍铝的重要化合物知识点。
一、氢氧化铝(Al(OH)3)氢氧化铝是一种重要的铝化合物,它具有白色固体状,是一种弱碱性物质。
氢氧化铝是通过将铝金属与氢氧化钠或氢氧化铵反应得到的。
它可作为中和剂和絮凝剂在水处理、制造纸张和药品等工业中广泛应用。
二、硫酸铝(Al2(SO4)3)硫酸铝是一种无机酸盐,也是铝的重要化合物之一。
它是无色结晶体,可溶于水。
硫酸铝可以通过将铝与硫酸反应制得。
硫酸铝广泛用于制造调味品、颜料、纸张和防腐材料等。
三、铝酸盐(如铝石和伊利石)铝酸盐是铝和硅酸根离子组成的化合物,具有各种各样的结构和性质。
其中,铝石是一种常见的铝酸盐矿石,主要由三个氧化铝和两个硅酸盐组成。
伊利石则是一种含有铝的层状硅酸盐矿物,其结构稳定,常用于陶瓷工业和建筑材料中。
四、氯化铝(AlCl3)氯化铝是一种无机化合物,是由铝和氯原子组成的化合物。
它是无色结晶体,可溶于水和有机溶剂。
氯化铝是一种重要的催化剂,在有机合成和石油加工中有着广泛应用。
五、铝氧化物(Al2O3)铝氧化物是一种无机化合物,也被称为氧化铝。
它是铝的最常见的化合物,具有白色结晶体的外观。
铝氧化物具有较高的熔点和硬度,广泛用于制备陶瓷、磨料和电子器件等。
六、铝硅酸盐纤维铝硅酸盐纤维是一种由铝和硅酸盐组成的纤维材料。
它具有轻质、高强度和耐高温性能,常用于制造隔热材料、耐火材料和复合材料等。
综上所述,铝的重要化合物包括氢氧化铝、硫酸铝、铝酸盐、氯化铝、铝氧化物和铝硅酸盐纤维等。
这些化合物在工业和日常生活中发挥着重要的作用,对于高一化学学习是必要的知识点。
通过了解它们的性质、制备方法和应用,可以更好地理解铝及其化合物的特性和用途。
高一化学必修一铝知识点归纳总结

高一化学必修一铝知识点归纳总结化学是一门探索物质组成、性质以及变化规律的科学,而铝作为重要的金属元素之一,在化学中扮演着重要的角色。
本文将对高一化学必修一中关于铝的知识点进行归纳总结。
一、铝的基本性质1. 原子结构:铝的原子序数为13,原子结构为2, 8, 3。
2. 物理性质:铝是一种银白色的轻金属,在常温下具有良好的延展性和导电性。
3. 化学性质:铝与氧气反应生成三氧化二铝,与非金属元素如硫、碳等反应生成相应的硫化物和碳化物等。
二、铝的制备与加工1. 制备方法:铝的主要制备方法有金属铝的电解法、熔融法和气相还原法等。
2. 加工工艺:铝可通过挤压、拉伸、锻造等加工工艺进行成型,可制备成各种形状的铝材。
三、铝的化合物1. 氧化物:铝的氧化物为三氧化二铝(Al2O3),是一种无机化合物,常见的矿石为矾土。
2. 盐类:铝与酸反应可生成相应的铝盐类化合物,如硫酸铝(Al2(SO4)3)等。
3. 氢氧化物:铝的氢氧化物为氢氧化铝(Al(OH)3),常见的形式为白色胶状物。
四、铝的应用1. 金属铝:铝是一种重要的金属材料,广泛应用于航空航天、汽车制造、建筑等领域,具有轻质、强度高、耐腐蚀等优点。
2. 铝合金:铝合金是将铝与其他金属元素进行合金化制备而成,具有较高的强度和热性能,常用于制造飞机、火箭等。
3. 铝的化合物:铝的氧化物与硅、氧化镁等化合可制备陶瓷材料,氢氧化铝则常用于药物制剂和消化剂等领域。
综上所述,铝作为一种重要的金属元素,在化学中扮演着重要的角色。
它的基本性质、制备与加工方法、化合物以及应用领域等知识点对于高一化学学习至关重要。
我们应该深入学习铝的相关知识,加深对其性质和应用的理解,为今后的学习打下坚实的基础。
高一化学科目上学期笔记

高一化学科目上学期笔记(实用版)编制人:__审核人:__审批人:__编制单位:__编制时间:__年__月__日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的实用资料,如教案大全、书信范文、述职报告、合同范本、工作总结、演讲稿、心得体会、作文大全、工作计划、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor.I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!Moreover, our store provides various types of practical materials for everyone, such as lesson plans, letter templates, job reports, contract templates, work summaries, speeches, reflections, essay summaries, work plans, and other materials. If you want to learn about different data formats and writing methods, please stay tuned!高一化学科目上学期笔记本店铺为大家整理的,在我们平凡的学生生涯里,很多人都经常追着老师们要知识点吧,知识点就是学习的重点。
高一必修一化学铝知识点

高一必修一化学铝知识点铝是一种常见的金属元素,化学符号为Al,原子序数为13。
它是地壳中含量第三高的元素,仅次于氧和硅。
铝具有轻质、耐腐蚀、良好导电导热等特点,被广泛应用于各个领域。
下面将介绍一些高一化学必修一中与铝相关的知识点。
1. 铝的物理性质铝是一种银白色的金属,具有较低的密度和较好的延展性。
它的熔点为660.32摄氏度,沸点约为2450摄氏度。
铝在常温下较为稳定,能抵御大部分物质的腐蚀。
2. 铝的化学性质铝具有良好的物理和化学性质,可以通过与其他元素的反应制备出多种化合物。
例如,与氧反应可以生成氧化铝(Al2O3),与硫反应可以生成硫化铝(Al2S3)。
此外,铝还可以与氢反应生成氢化铝(AlH3)等化合物。
3. 铝的腐蚀性尽管铝自身具有一定的耐腐蚀性,但在一些特殊条件下,如浓硝酸和强碱的存在下,铝会发生腐蚀。
这是因为铝与空气中的氧气反应,形成氧化铝保护层保护自身,但浓硝酸和强碱会破坏这层保护层,导致铝的腐蚀。
4. 铝的应用领域由于铝具有轻质和良好的导电导热性,广泛应用于许多领域。
其中最常见的应用是在航空航天和汽车工业中,用于制造飞机、汽车车身和零部件。
此外,铝还被用于制造罐装饮料、建筑材料、电子产品和家居用品等。
5. 铝的提取与炼制铝的提取主要通过电解法进行。
首先,将含有氧化铝的矿石(如赤铁矿石)经过纯化和粉碎处理,得到氧化铝粉末。
然后,将氧化铝粉末与熔融的硫酸铝混合,这样就得到了电解池的电解液。
在电解池中,通过电流的作用下,将氧化铝还原成铝金属。
6. 铝的环境影响虽然铝在自然界中广泛存在,但铝的过量排放对环境和生物造成一定的影响。
过量的铝会对水资源造成污染,干扰水生生物的生长和繁殖。
此外,铝的工业生产和废弃物处理也会对土壤和大气环境造成一定程度的污染。
在学习高一必修一化学课程时,理解和掌握以上关于铝的知识点对于学生们深入了解金属元素和化学反应有着重要的意义。
通过学习铝的物理和化学特性,我们可以更好地理解其在工业生产和日常生活中的应用,同时也需要注意铝对环境和生态系统的影响,积极采取环保措施。
高一上学期化学期中知识点

高一上学期化学期中知识点1.高一上学期化学期中知识点篇一铝及其化合物的性质1.铝与盐酸的反应:2Al+6HCl=2AlCl3+3H2↑2.铝与强碱的反应:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑3.铝在空气中氧化:4Al+3O2==2Al2O34.氧化铝与酸反应:Al2O3+6HCl=2AlCl3+3H2O5.氧化铝与强碱反应:Al2O3+2NaOH+3H2O=2Na[Al(OH)4]6.氢氧化铝与强酸反应:Al(OH)3+3HCl=AlCl3+3H2O7.氢氧化铝与强碱反应:Al(OH)3+NaOH=Na[Al(OH)4]8.实验室制取氢氧化铝沉淀:Al3++3NH3?H2O=Al(OH)3↓+3NH4+2.高一上学期化学期中知识点篇二硫及其化合物的性质1.铁与硫蒸气反应:Fe+S△==FeS2.铜与硫蒸气反应:2Cu+S△==Cu2S3.硫与浓硫酸反应:S+2H2SO4(浓)△==3SO2↑+2H2O4.二氧化硫与硫化氢反应:SO2+2H2S=3S↓+2H2O5.铜与浓硫酸反应:Cu+2H2SO4△==CuSO4+SO2↑+2H2O6.二氧化硫的催化氧化:2SO2+O22SO37.二氧化硫与氯水的反应:SO2+Cl2+2H2O=H2SO4+2HCl8.二氧化硫与氢氧化钠反应:SO2+2NaOH=Na2SO3+H2O9.硫化氢在充足的氧气中燃烧:2H2S+3O2点燃===2SO2+2H2O10.硫化氢在不充足的氧气中燃烧:2H2S+O2点燃===2S+2H2O3.高一上学期化学期中知识点篇三钠及其化合物的性质:1.钠在空气中缓慢氧化:4Na+O2==2Na2O2.钠在空气中燃烧:2Na+O2点燃====Na2O23.钠与水反应:2Na+2H2O=2NaOH+H2↑现象:①钠浮在水面上;②熔化为银白色小球;③在水面上四处游动;④伴有嗞嗞响声;⑤滴有酚酞的水变红色.4.过氧化钠与水反应:2Na2O2+2H2O=4NaOH+O2↑5.过氧化钠与二氧化碳反应:2Na2O2+2CO2=2Na2CO3+O26.碳酸氢钠受热分2NaHCO3△==Na2CO3+H2O+CO2↑7.氢氧化钠与碳酸氢钠反应:NaOH+NaHCO3=Na2CO3+H2O8.在碳酸钠溶液中通入二氧化碳:Na2CO3+CO2+H2O=2NaHCO3。
人教版高中化学必修一《铝及其化合物》

点燃 铝及其化合物 知识点一. 铝单质的性质1.物理性质:银白色金属,硬度和密度小,具有良好的导电导热性和延展性。
在空气中具有很好的耐腐蚀性。
2.化学性质:(1)与非金属单质反应:A 、2Al+3Cl 2====2AlCl 3B 、铝在空气中缓慢氧化,在氧气中点燃剧烈燃烧。
4Al+3O 2 ========= 2Al 2O 3铝与空气中的氧气反应生成致密的氧化膜并牢固地覆盖在铝表面,阻止了内部的铝与空气接触。
(2)与盐溶液反应:2Al+3CuSO 4 =3Cu+Al 2(SO 4)3(3)与某些氧化物反应—铝热反应:2Al + Fe 2O 3 == 2Fe + Al 2O 3 铝热剂是Al 和 Fe 2O 3(4)与沸水微弱反应:2Al+6H 2O Δ 2Al (OH )3 + 3H 2↑(5)与酸反应::2Al+6HCl ====== 2AlCl 3+H2↑2Al+3H 2SO 4 ====== Al 2(SO 4)3+ 3H2↑注意:铝在冷的浓硫酸、浓硝酸中钝化。
某些金属在常温下遇强氧化性酸如浓硫酸、浓硝酸时在表面生成致密的氧化膜,从而阻止内部金属进一步发生反应,这种现象称为钝化。
(6)与碱反应: 2Al+2NaOH+2H 2O=2NaAlO 2+3H 2↑反应的实质:分两步进行:②Al(OH)3+NaOH ======== NaAlO 2+2H 2O知识点二. 铝的重要化合物1. 氧化铝(Al 2O 3)化合价降低,被还原,得6e —①2Al+6H 2O ====== 2Al(OH)3 + 3H 2↑化合价升高,被氧化,失6e —2Al+6H 2O+2NaOH = 2NaAlO 2+3H 2↑+4H 2O失2×3 e —得6×e —(1)物理性质:白色固体、熔点高(2054℃) 、不溶于水,不与水化合。
常作耐火材料。
刚玉的主要成分是Al 2O 3 ,其中把含少量铬元素的刚玉称为红宝石;含少量的铁和钛元素的刚玉称为蓝宝石。
高一化学必修一第三章知识点总结归纳

高一化学必修一第三章知识点总结归纳其实,不是化学太难,而是你的学习方法出现了严重的问题。
只要方法得当,你完全可以很快告别“差生”!今天小编在这给大家整理了高一化学必修一第三章,接下来随着小编一起来看看吧!高一化学必修一(一)金属的化学性质一金属的通性1.金属的存在(1)金属元素的存在绝大多数金属以化合态的形式存在于自然界中,如Al、Fe等,极少数化学性质不活泼的金属以游离态的形式存在于自然界中,如Au。
在地壳中的含量较多的为O、Si、Al、Fe、Ca。
2.金属单质的物理通性①状态:常温下,大部分为固体,唯一呈液态的是汞。
②色泽:除Cu、Au外,大多数金属为银白色,有金属光泽。
③三性:良好的导电性、导热性、延展性。
3.单质的化学性质(1)与非金属的反应常温下,镁在空气中跟氧气反应,生成一层致密的氧化物薄膜,能够阻止内部金属继续被氧化。
镁在空气中燃烧,产生耀眼的白光,生成白色固体,反应的化学方程式为:2Mg+O2点燃=====2MgO。
镁还可以和氮气点燃,反应方程式为:3Mg+N2点燃=====Mg3N2。
(2)与酸的反应Fe与稀H2SO4反应的离子方程式:Fe+2H+===Fe2++H2↑。
(3)与盐溶液的反应Cu与AgNO3溶液反应的离子方程式:Cu+2Ag+===Cu2++2Ag。
归纳总结金属的通性(1)金属化学性质特点(2)金属还原性的强弱取决于其失去电子的难易程度,而不是失去电子个数的多少。
【活学活用】1.判断下列说法是否正确,正确的划“√”,错误的划“×”(1)金属具有良好的导热、导电性()(2)金属单质在氧化还原反应中总是作还原剂()(3)钠原子在氧化还原反应中失去1个电子,而铝原子失去3个电子,所以铝比钠活泼()(4)金属在加热条件下均易与O2反应()答案(1)√(2)√(3)×(4)×解析(3)错误,金属的活泼性与原子失去电子个数无关,与失电子能力有关,钠比铝易失电子,钠比铝活泼;(4)错误,Au、Pt等金属不与O2反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高一化学知识点总结铝及其化合物这篇高一化学铝及其化合物知识点是特地为大家整理的,希望对大家有所帮助!
高一化学铝及其化合物知识点
Ⅰ、铝
①物理性质:银白色,较软的固体,导电、导热,延展性
②化学性质:Al3e-==Al3+
a、与非金属:4Al+3O2==2Al2O3,2Al+3S==Al2S3,
2Al+3Cl2==2AlCl3
b、与酸:2Al+6HCl==2AlCl3+3H2,
2Al+3H2SO4==Al2(SO4)3+3H2
常温常压下,铝遇浓硫酸或浓硝酸会发生钝化,所以可用铝制容器盛装浓硫酸或浓硝酸
c、与强碱:2Al+2NaOH+2H2O==2NaAlO2(偏铝酸钠)+3H2 (2Al+2OH-+2H2O==2AlO2-+3H2)
大多数金属不与碱反应,但铝却可以
d、铝热反应:2Al+Fe2O3===2Fe+Al2O3,铝具有较强的还原性,可以还原一些金属氧化物
Ⅱ、铝的化合物
①Al2O3(典型的两性氧化物)
a、与酸:Al2O3+6H+==2Al3++3H2O
b、与碱:
Al2O3+2OH-==2AlO2-+H2O
②Al(OH)3(典型的两性氢氧化物):白色不溶于水的胶状物质,具有吸附作用
a、实验室制备:AlCl3+3NH3H2O==Al(OH)3+3NH4Cl,
Al3++3NH3H2O==Al(OH)3+3NH4+
b、与酸、碱反应:与酸 Al(OH)3+3H+==Al3++3H2O 与碱Al(OH)3+OH-==AlO2-+2H2O
③KAl(SO4)2(硫酸铝钾)
KAl(SO4)212H2O,十二水和硫酸铝钾,俗名:明矾
KAl(SO4)2==K++Al3++2SO42-,Al3+会水解:Al3++3H2O Al(OH)3+3H+
因为Al(OH)3具有很强的吸附型,所以明矾可以做净水剂。
