气固相催化反应实验-预习
气固相催化反应过程

气固相催化反应过程
气固相反应本征动力学是研究不受扩散干扰条件下的固体催化剂与其相接触的气体之间的反应动力学。
一般而言,气固相催化反应过程经历一下七个步骤:
①反应组分从流体主体向固体催化剂外表面传递(外扩散过程)
②反应组分从催化剂外表面相催化剂内表面传递(内扩散过程)
③反应组分在催化剂表面的活性中心吸附(吸附过程)
④在催化剂表面上进行化学反应(表面反应过程)
⑤反应产物在催化剂表面上脱附(脱附过程)
⑥反应产物从催化剂内表面向催化剂外表面传递(内扩散过程)
⑦反应产物从催化剂外表面向流体主体传递(外扩散过程)
七个步骤中,第①和第⑦步是气相主题通过气膜与颗粒处表面进行物质传递,称为外扩散过程;第②和⑥步是颗粒内的传质,称为内扩散过程;第③和第④步是在颗粒表面上进行化学吸附和化学脱附的过程;第⑤步是在颗粒表面上进行的表面反应动力学过程。
以上气割步骤是前后串联的:
外扩散内扩散
表面过程
由此可见,气固相催化反应过程是一个步骤过程。
如果其中某一步骤的反应速率与其他各步的反应速率相比要慢得多,以致整个反应速率取决于这一步的反应速率,该步骤就称为反应速率控制步骤。
反应过程达到定态时,各步骤的反应速率应该相等,且过程的反应速率等于
控制步骤的反应速率。
这一点对于分析和解决实际问题非常重要。
气固相催化反应的动力学步骤

气固相催化反应的动力学步骤以气固相催化反应的动力学步骤为标题,本文将从理论和实践两方面介绍气固相催化反应的动力学步骤。
一、理论部分1.催化剂的吸附在气固相催化反应中,催化剂的吸附是反应的第一步。
催化剂表面存在各种吸附位,其中最常见的是吸附位和活性位。
吸附位是催化剂表面的一个缺陷,其表面结构与晶体结构不同,因此吸附能力较强。
活性位则是吸附位上的一些具有活性的物种,如氢原子、羟基、氧原子等。
催化剂表面的吸附位和活性位对反应物的吸附和反应至关重要。
2.反应物的吸附反应物吸附在催化剂表面的吸附位和活性位上,通过化学键形成催化剂-反应物复合物,这是反应的第二步。
3.反应反应物在复合物的作用下发生反应,形成产物。
反应速率取决于反应物的浓度、催化剂的活性、反应温度等因素。
4.产物的脱附产物脱附是反应的最后一步,当产物与催化剂之间的键断裂时,产物会从催化剂表面脱离。
二、实践部分以催化裂化反应为例,介绍气固相催化反应的动力学步骤。
1.催化剂的选择在催化裂化反应中,催化剂的选择非常重要。
催化剂应具有较高的活性和选择性,同时还应具有较高的稳定性和寿命。
2.反应条件的控制催化裂化反应需要适宜的反应温度、反应压力、反应时间等条件。
反应温度一般在450-550℃之间,反应压力一般为1-2MPa。
3.反应物的选择催化裂化反应的反应物为长链烷烃,反应物的选择对反应的效果有很大影响。
一般来说,碳数较多的长链烷烃反应活性较低,而碳数较少的烷烃反应活性较高。
4.反应机理的研究通过对反应物和产物的分析,可以确定反应的机理和动力学参数,如反应速率常数、反应级数等。
这对于优化反应条件、提高反应效率具有重要意义。
气固相催化反应的动力学步骤包括催化剂的吸附、反应物的吸附、反应和产物的脱附。
在实践中,催化剂的选择、反应条件的控制、反应物的选择和反应机理的研究是保证反应效率和催化剂寿命的关键。
气固相催化反应实验-预习

化工专业实验预习报告【1】实验名称气固相催化反应实验班级姓名学号成绩实验时间同组成员一、实验预习1.实验目的(1)掌握乙醇脱水实验的反应过程和反应机理、特点。
(2)学习气固管式催化反应器的构造、原理和使用方法。
(3)学习如何对实验体系进行物料衡算,确定收率和转化率。
(4)学习气体在线分析的方法和定性、定量分析,学习手动进样分析液体成分。
(5)学习微量泵的使用,学会使用湿式流量计测量气体流量。
2.实验原理1)乙醇脱水反应历程实验表明,乙醇脱水可生成乙烯和乙醚两种化合物,但在浓硫酸或三氧化二铝催化下,控制温度可使反应生成其中一种化合物为主,反应如下:可见,乙醇的脱水方式随反应温度而异,在较高温度时主要发生分子内脱水生成乙烯,在较低温度下则发生分子间脱水生成乙醚。
对于乙醇脱水反应,由于对机理及动力学的研究结论很难达成一致,主要存在两方面的争论:○1乙醇脱水机理是连串反应机理、平行反应机理还是平行-连串反应机理;○2反应机理是吸附于催化剂上的两个临近乙醇分子间进行的L-H模型,还是一个气相乙醇分子和一个催化剂上处于吸附态的乙醇分子之间进行的R-E模型。
乙醇脱水反应的催化剂主要由γ-Al2O3和酸性ZSM-5分子筛两大类。
Blaszkowski和Van Santen指出:氧化铝型催化剂的催化机理和分子筛不同,γ-Al2O3的催化活性与其表面脱氢过程中形成的Lewis酸-Lewis碱对有关,富电子的阴离子氧表现出碱的特性,缺电子的阳离子铝表现出酸的特性。
相反,酸性分子筛的催化活性与Bronst酸-Lewis碱对有关,Bronst酸发生氢转移,而它邻近的Lewis碱能接受质子。
在此基础上,Cory B.Phillips等以ZSM-5分子筛为催化剂,提出乙醇脱水反应属于平行反应,会生成乙氧基这一中间产物,并且他们认为生成乙醚的过程与甲醇脱水生成二甲醚的过程非常相似。
Junko N.Kondo 等利用原位红外检测也证实在反应过程中乙氧基这一中间产物的存在。
气固相催化反应本征及宏观动力学

阿尔法队 队长:徐晓杰
主要内容
1
气固相催化 过程及其特 征
2
固体催化剂 及其结构特 征参数
3
气固相催化 剂反应本征 动力学
4
气固相催化 本征动力学 实验测定
气固相催化反应过程步骤
催化剂多为多孔性介质,相对于丰富的内孔,外表面 的催化作用贡献量可忽略不计
• 1 外扩散:反应组分由物流主体→催化剂外表面 • 2 内扩散:反应组分由催化剂外表面→催化剂内表面 • 3 吸附:反应组分在催化剂活性中心上吸附 • 4 表面化学反应:在催化剂表面进行化学反应 • 5 脱附:反应产物在催化剂表面解吸 • 6 内扩散:反应产物由催化剂内表面→催化剂外表面 • 7 外扩散:反应产物由催化剂外表面→物流主体
催化反应过程的特征
Ø 1 催化剂改变反应历程和反应速率 Ø 2 催化剂的存在不改变反应过程的热 力学平衡特性(∆GO=-RTlnK) Ø 3 催化剂等速加快/减小可逆反应的正 逆反应速率 Ø 4 催化剂对反应过程的选择性至关重要 Ø 5 如果希望催化剂充分发挥作用,应当 尽可能增加反应物与催化剂的接触
固体催化剂的组成
固体催化剂由三部分组成:活性组分、助剂和载体; 三者不能截然分开。
• 1 活性组分
双重催化剂:异构 化、重整反应 半导体催化剂:金属氧 化物、硫化物等(氧化、 还原、脱氢、环化、脱 硫(少量用于加氢))
1 3
2 4
金属催化剂:Pd、 Ag、Fe、Cu等(加 氢、脱氢、裂解(少 量用于氧化)) 绝缘体催化剂:IIIA、 IVA、VA族金属或非 金属氧化物、卤化物 等
• 2助催化剂(促进剂)
• 电子型:碱金属或碱土金属氧化物(K2O、Na2O) • 结构型:用高熔点、难还原的氧化物可增加活性组分表 面积和热稳定性
气固相催化反应宏观反应速率的测定

2.1.3气-固催化反应过程与控制步骤(精)
2.1.3气-固催化反应过程与控制步骤
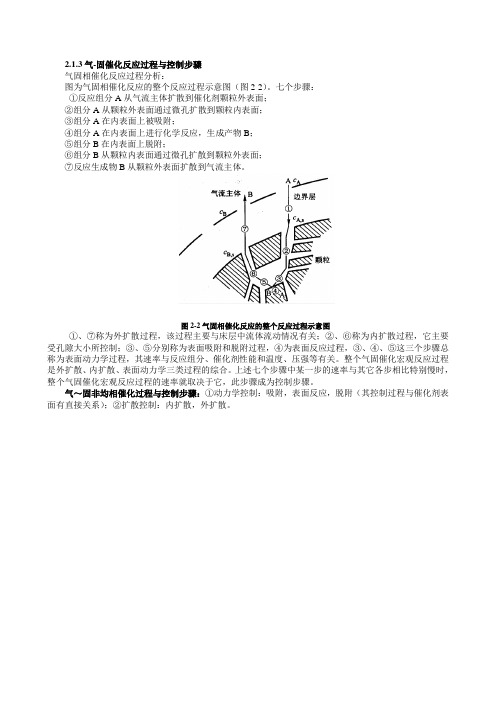
气固相催化反应过程分析:
图为气固相催化反应的整个反应过程示意图(图2-2)。
七个步骤:
①反应组分A从气流主体扩散到催化剂颗粒外表面;
②组分A从颗粒外表面通过微孔扩散到颗粒内表面;
③组分A在内表面上被吸附;
④组分A在内表面上进行化学反应,生成产物B;
⑤组分B在内表面上脱附;
⑥组分B从颗粒内表面通过微孔扩散到颗粒外表面;
⑦反应生成物B从颗粒外表面扩散到气流主体。
图2-2气固相催化反应的整个反应过程示意图
①、⑦称为外扩散过程,该过程主要与床层中流体流动情况有关;②、⑥称为内扩散过程,它主要受孔隙大小所控制;③、⑤分别称为表面吸附和脱附过程,④为表面反应过程,③、④、⑤这三个步骤总称为表面动力学过程,其速率与反应组分、催化剂性能和温度、压强等有关。
整个气固催化宏观反应过程是外扩散、内扩散、表面动力学三类过程的综合。
上述七个步骤中某一步的速率与其它各步相比特别慢时,整个气固催化宏观反应过程的速率就取决于它,此步骤成为控制步骤。
气~固非均相催化过程与控制步骤:①动力学控制:吸附,表面反应,脱附(其控制过程与催化剂表面有直接关系);②扩散控制:内扩散,外扩散。
化学反应工程-15-第四章-气固相催化反应

0.5
1.5 PH 2
PNH
3
P PN 3 2 P H2 PNH k 2 1.53 PH
2
2 NH 3
0.5
KA kd K2 P
0.5
P 3 PH 2
2 NH 3
0.5
该式子一直到现在仍广泛应用。
4.4本征动力学方程的实验测定法
故
PR k PA K r 1 K1PA
4、两种活性中心 对反应: A B R S ,设表面反应控制
' r r3 k3 A B k3 R S
S K5 PSV 2 A K1 PAV 1 , B K 2 PBV 2 , , R K 4 PRV 1
r r3 k3 A B
应用Langmuir均匀吸附理论,可以求出 A 和 B 的值! 对(1):因达到平衡
k1 PAV k1 A
A K A PAV
同理对(2)
k1 设K A k 1 1
B K B PBV
2
2
h g h
2 K PNH 3 k a PN A 3 2 K2 P P H2
g g h
2 K PNH 3 kd A 2 3 KP PH 2
由实验获得模型参数g=h=0.5,上式:
KA r ka K2 P k1 PN
2、内扩散影响的检验:
方法:改变催化剂的粒度(直径 d P),在恒定的 w / FA0下测量转化率 x A 以xA ~ d P 作图:
若 d P 在b点左边,x A 不变。表明内扩散无影响。
第五章气固相催化反应本征动力学

rd kd exp(h ) kd kd 0 f ( ) exp( Ed0 RT ) h RT
表观吸附速率为 r ra rd ka pA exp(g ) kd exp(h )
平衡时:ka kd
pA
exp[( g h) ]
令
K
A
ka kd
f hg
则
1 f
ln(K A pA )
焦姆金等温吸附方程
令
ka ka0 exp( Ea0 RT ) f ( )
活性 选择性 寿命
催化剂的性能
影响
物理性质: 比表面积; 孔容积; 孔容积分布。
1、比表面积:单位质量的催化剂具有的表面积Sg,m2/g; 影响催化剂的吸附量和活性。
!!!测定表面积的方法是:氮吸附法。
2、孔容积:每克催化剂内部微孔的容积Vg。cm3/g !!!测定孔容积较准确的方法是:氦-汞法。
非活化的,低活化能;活化的, 高活化能。>40kJ/mol
<8kJ/mol
>40kJ/mol
多分子层
单分子层
高度可逆
常不可逆
用于测定表面积、微孔尺寸
用于测定活化中心的面积及阐 明反应动力学规律
2、化学吸附速率的一般表达式
1)吸附方程:
A+σ→A σ
吸附率: A
被A组分覆盖的活性中心数 总的活性中心数
3)提高催化剂的机械强度。
4、催化剂活化:目的是除去吸附和沉积Байду номын сангаас外来杂质。
方法是:1)适度加热驱除易除去的外来杂质; 2)小心燃烧除去顽固杂质; 3)用氢气、硫化氢、一氧化碳或氯化烃作为活化剂
活化催化剂。
5、催化剂的开工和停工
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化工专业实验预习报告
实验名称气固相催化反应实验 班级姓名学号成绩 实验时间同组成员
一、实验预习
(1) 掌握乙醇脱水实验的反应过稈和反应机理、特点。
(2)
学习气固管式催化反应器的构造、原理和使用方法。
(3) 学习如何对实验体系进行物料衡算,确定收率和转化率。
(4) 学习气体在线分析的方法和定性、定最分析,学习手动进样分析液体成分。
(5) 学习微量泵的使用,学会使用湿式流最计测量气体流量。
2 •实验原理 1)乙醇脱水反应历程
实验表明,乙醇脱水町生成乙烯和乙讎两种化合物,但在浓硫酸或三氧化二铝催化卜,控制温度 可使反应生成其中一种化合物为主,反应如下:
町见.乙醇的脱水方式随反应温度而异,在较高温度时主要发生分子内脱水生成乙烯,在较低温 [卜•则发生分子间脱水生成乙醛。
对于乙醇脱水反"由于对机理及动力学的研究结论很难达成一致.
主要存在两方面的争论:①乙醇脱水机理是连串反应机理.平行反应机理还是平行•连串反应机理:② 反应机理是吸附于催化剂上的两个临近乙醇分子间进行的L ・H 模型.还是一个气相乙醇分子和一个催 化剂上处于吸附态的乙醇分子之间进行的R-E 模型。
乙醇脱水反应的催化剂主要由fAbO3和酸性 ZSM-5分子筛两人类。
Blaszkowski 和Van Santen 指出:氧化铝型催化剂的催化机理和分子筛不同,
Y-AhO 3的催化活性与其表面脱氢过程中形成的Lewis 酸-Lewis 碱对有关.富电子的阴离子氧表现出碱 的特性,缺电子的阳离子铝表现出酸的特性。
相反,酸性分子筛的催化活性与Bronst fi§-Lewis 碱对冇
关,Bronst 酸发生氢转移.而它邻近的Lewis 碱能接受质子。
在此基础匕Cory B Phillips 等以ZSM ・5 分子筛为催化剂,提出乙醇脱水反应属于平行反应,会生成乙氧基这一中间产物,并且他们认为生成 乙謎的过程与甲醇脱水生成二甲醛的过程卄常相似。
JunkoNKondo 等利用原位红外检测也证实在反 应过程中乙氧基这一中间产物的存在。
Chang 等提出只要催化剂上存在足够藝的酸性位,乙醇可以直 接反应生成乙烯。
R LeVan Mao 等在ZSM-5分子筛基础上提出在523-598 K 范闱内乙醇直接生成乙
烯,448M98K 范I 制内乙醇生成乙凝,而494523K 范惘内生成乙烯和乙瞇.反应是在Bronst 酸中心 上进行的。
河北工业人学及上海石油化工研究院等对乙醇脱水反应进行了研究,同样认为乙醇脱水反 应符合平行反应机理。
实验以改性分子筛为催化剂,在消除内外扩散的前提卜•,对乙醇脱水反应的机 理进行了研究。
结
CH 3CH 2OH
浓H2S04」70・C ------------------ ► 或
A120y350~40(rC
CH 2 = CH 2 + H 2O
2CH 3CH 70H
細 2SO4WC
P XA1203,260*C
合文献,对本体系条件卜提出如卜•反应机理:乙醇脱水生成乙烯和乙醛的反应属于平行反应,反应机理模
型是吸附于催化剂上的2个邻近乙醇分子之间进行的L-H模型,具体反应历程如下:
CH3CH2OH + HX T HXCH3CH2OH (1)
HXCH3CH2OH t CH3CH2OH; + X~ (2)
CH3CH2OH; + HX-> CH,CH2 + HXH2O (3)
CHjCH2 + X- t CH3CH2X (4)
CH3CH2X + HXCH3CH2OH T HXCH3CH2OCH2CHjH + X-(5)
CH3CH2XTC2H4 + HX (6)
HXCH3CH2OCH2CHjH->HXCH3CH2OCH2CH3H+(7)
HXCH3CH2OCH2CHjH T HXCH3CH2OCH2CH3 + H+(8)
HXCH3CH2OCH2CH3 t HX + CH3CH2OCH2CH3 (9)
HXH2OTHX+ H20(10)
H+ + XJHX (11)
反应(3)、(7)或(8)、(12)分别为乙醇吸附、表面反应、水脱附的反应,均有可能成为反应的控制步骤,其余步骤为快速平衡的过程。
2)乙醇脱水反应所采用的催化剂
冃前己报道的乙醇脱水催化剂有:白土、活性氧化铝、氧化硅、磷酸、硫酸、氧化社、氧化镉、氧化错、磷酸钙、杂多酸盐、分子筛、铝酸锌、A12O3 /S I O2. AI2O3/CHO3、Al2O32MgO /SiO?等,在工业上有应用报道的乙醇脱水催化剂主要有活性氧化铝、活性白土、A13O3/S I O2. Al2O32MgO /Si6等。
本实验采用的催化剂(ZSM・5分子筛)。
ZSM — 5沸石分子筛的晶体,貝有丰富的微孔通道和孔穴,在ZSM — 5分子筛中进行的催化反应面临以下三种不同的条件和结果(即选择性):
(1)由于犬多数活性中心都己被限制在孔结构之内,所以,只有那些半径与分子筛孔径相当(较大或略大)的反应物分子,才有可能进入孔内,并在其中的活性中心上发生反应。
而无法进入孔内的反应物,只有在为数很少的外表面的活性中心上反应。
(2)只有那些进入孔后而又能再从孔中扩散出来的分子,才可能作为产品出现。
当然,这种分子也只占一部分,而其余的产物分子,或者体积较人,或裂解成堵塞孔道、或使催化剂失活的小分子,则也不能从孔中排除作为产物出现。
(3)某些孔内反应,因为需要形成体积校大的过度状态(或中间态)分子,由于它们受到分子筛孔道孔穴尺寸的约束和限制,使得这些过度态的中间产物,难以在孔中形成;反之,分子较小的过度态产物,则町以形成。
由于ZSM・5分子筛具有巨大的内表面,因此分子筛的活性中心不仅存在于分子筛表面上,而且内表面业存在催化活性中心起到催化作用。
在实验中,由于反应生成的产物乙瞇和未反应的乙醇留在了液体冷凝器中,而其他几个产物都是挥发气体,进入尾气湿式流量计计量总体积后排岀。
对于不I可的反应温度,通过计算不冋的转化率和反应速率,叫以得到不I可反应温度卜的反应速率常数,并得到温度的关联式。
3 •实验仪器和药品
仪器:乙醇脱水气固反应器、气相色谱及计算机数据釆集和处理系统、精密微最液体泵。
药品:乙醇脱水催化剂、化学纯乙醇、分析纯乙瞇、蒸谓水。
4 •实验步骤
< 1)装填催化剂
(2)流量计准备
(3)安装反应器
(以上三步实验时己做好)
(4)打开电源总开关,按照实验要求,调整好色谱条件:载气;氢气(氢气发生器);柱箱温度:150°C:进样器温度:150°C;检测器温度:150°C;色谱柱:乙醇脱水专用(内径4mm,长3m)。
(5)将反应器加热温度设定为260°C,预热器温度设定为200°C (町以根据反应器温度的分配情况调节〉。
温度设定无误后,打开加热开关,在开始加热时可用自擬定设置.
(6)在温度达到设定值后,继续稳定10〜20分钟,然后开始加入乙醇。
乙醇的加料速度为05〜1 5mL/mino
(7)反应进行20分钟后,正式开始实验。
先换掉反应器卜的吸收瓶,并换上清洗干净的新瓶,检杳升降台的高度,应该调节升降台,使冰水混合物尽可能多的浸没分离器。
记录湿式流最计读数,应每隔一定时间记录反应温度,压力等实验条件。
(8)反应开始每隔10〜20分钟取一次数据,每个温度至少取两个数据,粗产品从分离器中放入量筒内。
(9)取少最样品,用气相色谱分析其组成,并计算出各组分的百分含最。
(10)改变反应温度,每次提高20〜30°C,觅复上述实验步骤,则得到不同反应温度下的原料转化率、产物乙烯,乙瞇收率,并根据动力学模型,可以得到反应速率常数。
二、实验记录
260° C:
280° C:。
