高中化学方程式 水解反应素材
初高中化学段的水解反应知识点

初高中化学段的水解反应知识点一、无机物的水解1.单质的水解:Cl-Cl+H-OH == HCl + HClO2.氧化物的水解:Na2O + H-OH == 2NaOH3.盐类的水解:化学反应原理:盐的离子(一般是弱酸的阴离子或弱碱的阳离子)跟水电离出来的H+或OH-结合形成弱电解质,从而促进水的电离。
如:NH4++H2O=NH3·H2O+H+4.非盐型离子化合物的水解这类水解主要是指活泼金属的氢化物、氮化物、磷化物、碳化物等的水解。
如:CaH2+2H2O=Ca(OH)2+2H2↑Mg3N2+6H2O=3Mg(OH)2+2NH3↑CaC2+2H2O→Ca(OH)2+C2H2↑不难写出BN、MgC2、Al4C3等.如:Al4C3+12H2O→4Al(OH)↓+3CH4↑35.非金属卤化物的水解(1)卤素互化物:IBr+H2O=HIO+HBr(2)氮族元素卤化物的水解,如:NCl3+H2O(少)=HClO + NH3 (初级产物),或NCl3+2H2O (多)=2HClO+ NH3·H2O。
而在一定条件下,HClO是强氧化剂,能再将NH3氧化成N2和HCl.(一般不考虑)注意:NH3能在加热条件下被HNO3,浓H2SO4,HClO氧化,在水中NH3,NH4+均不易被氧化。
此外还有:PCl3+3H-OH= H3PO3+3HClAsX3+3H2O=H3AsO3+3HXBCl3+3H2O=H3BO3↓+3HCl↑等.二、有机物的水解1.卤代烃的水解;2.醇钠、酚钠的水解;3.羧酸衍生物的水解;4.糖类的水解;5.多肽、蛋白质的水解。
口诀:离换离、基换基,异电相吸去分析,初级产物优先写,二级反应后考虑。
最新高中化学——常见水解反应总结教学内容
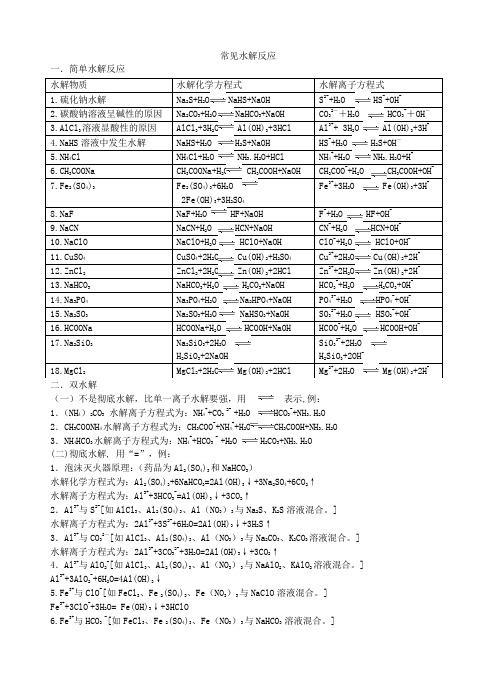
常见水解反应一.简单水解反应 二.双水解(一)不是彻底水解,比单一离子水解要强,用 表示,例:1.(NH 4)2CO 3 水解离子方程式为:NH 4++CO 3 2- +H 2O HCO 3-+NH 3.H 2O 2.CH 3COONH 4水解离子方程式为:CH 3COO -+NH 4++H 2O CH 3COOH+NH 3.H 2O3.NH 4HCO 3水解离子方程式为:NH 4++HCO 3 - +H 2O H 2CO 3+NH 3.H 2O(二)彻底水解, 用“=”,例: 1.泡沫灭火器原理:(药品为Al 2(SO 4)3和NaHCO 3)水解化学方程式为:Al 2(SO 4)3+6NaHCO 3=2Al(OH)3↓+3Na 2SO 4+6CO 2↑水解离子方程式为:Al 3++3HCO 3-=Al(OH)3↓+3CO 2↑2.Al 3+与S 2-[如AlCl 3、Al 2(SO 4)3、Al (NO 3)3与Na 2S 、K 2S 溶液混合。
]水解离子方程式为:2Al 3++3S 2-+6H 2O=2Al(OH)3↓+3H 2S ↑3.Al 3+与CO 32-[如AlCl 3、Al 2(SO 4)3、Al (NO 3)3与Na 2CO 3、K 2CO 3溶液混合。
]水解离子方程式为:2Al 3++3CO 32-+3H 2O=2Al(OH)3↓+3CO 2↑4.Al 3+与AlO 2-[如AlCl 3、Al 2(SO 4)3、Al (NO 3)3与NaAlO 2、KAlO 2溶液混合。
] Al 3++3AlO 2-+6H 2O=4Al(OH)3↓ 5.Fe 3+与ClO -[如FeCl 3、Fe 2(SO 4)3、Fe (NO 3)3与NaClO 溶液混合。
] Fe 3++3ClO -+3H 2O= Fe(OH)3↓+3HClO 6.Fe 3+与HCO 3 -[如FeCl 3、Fe 2(SO 4)3、Fe (NO 3)3与NaHCO 3 溶液混合。
高考化学水解反应方程式大全

2019年高考化学水解反应方程式大全化学方程式是化学的语言,是化学灵魂内容,是化学的一个重点也是一个难点,小编为大家准备了2019年高考化学水解反应方程式大全,希望对大家有所帮助!水解反应1、单水解---可逆水解NH4Cl+H2O NH3·H2O+HCl NH4++H2O H++NH3·H2O FeCl3+3H2O Fe(OH)3+3HCl Fe3++3H2O Fe(OH)3+3H+ AlCl3+3H2O Al(OH)3+3HCl Al3++3H2O Al(OH)3+3H+ CuSO4+2H2O Cu(OH)2+H2SO4 (金属活动顺序表中Mg2+以后的阳离子均水解)NaHCO3+H2O H2CO3+NaOH (NaHSO4不水解,NaHSO3电离大于水解)Na2CO3+H2O NaHCO3+NaOH CO32-+H2O HCO3-+OH–NaHCO3+H2O H2CO3+NaOH(第一步远远大于第二步,二步不能叠加)Na2SO3+H2O NaHSO3+NaOH SO32-+H2O HSO3-+OH–NaHSO3+H2O H2SO3+NaOH(第一步远远大于第二步,二步不能叠加)HSO3-+H2O H2SO3+OH-Na2S+H2O NaHS+NaOH S2-+H2O HS-+OH–NaHS+H2O H2S+NaOH(第一步远远大于第二步,二步不能叠加)HS-+H2O H2S+OH-Na3PO4+H2O Na2HPO4+NaOH PO43-+H2O HPO42-+OH–Na2HPO4+H2O NaH2PO4+NaOH HPO42-+H2OH2PO4-+OH–NaH2PO4+H2O H3PO4+NaOH H2PO4-+H2O H3PO4+OH–CH3COONa+H2O CH3COOH+NaOH CH3COO-+H2OCH3COOH+OH–C6H5ONa+H2O C6H5OH+NaOH C6H5O-+H2OC6H5OH+OH–2、双水解CH3COONH4+H2O CH3COOH+NH3·H2ONH4F+H2O HF+NH3·H2OAl2S3+6H2O==Al(OH)3↓+H2S↑ (隔绝空气,密封保存)Mg3N2+6H2O==Mg(OH)2↓+NH3↑(隔绝空气,密封保存) Na3P+3H2O==3NaOH+PH3↑(隔绝空气,密封保存)Zn3P2+6H2O==Zn(OH)2↓+PH3↑(Zn3P2一种老鼠药,PH3剧毒神经毒剂)CaC2+2H2O==Ca(OH)3↓+C2H2↑(隔绝空气,密封保存)C2H5ONa+H2O==C2H5OH+NaOH以上就是查字典化学网为大家提供的2019年高考化学水解反应方程式大全,更多精彩尽在查字典化学网,敬请关注!。
高中盐类水解方程式50个

高中盐类水解方程式50个1、氧化性:(在水溶液中)2FeCl3+Fe==3FeCl2 2Fe3++Fe=3Fe2+2FeCl3+Cu===2FeCl2+CuCl2 (用于雕刻铜线路版)2Fe3++Cu=2Fe2++Cu2+2FeCl3+Zn(少量)===2FeCl2+ZnCl2 2Fe3++Zn=2Fe2++Zn2+FeCl3+Ag===FeCl2+AgCl↓2Fe3++Cl-+2Ag=2Fe2++2AgCl↓Fe2(SO4)3+2Ag===FeSO4+Ag2SO4↓(较难反应) Fe(NO3)3+Ag不反应2FeCl3+H2S===2FeCl2+2HCl+S↓2Fe3++H2S=2Fe2++2H++S↓2FeCl3+2KI===2FeCl2+2KCl+I2 2Fe3++2I-=2Fe2++I2FeCl2+Mg===Fe+MgCl2 Fe2++Mg=Fe+Mg2+NaNO2+NH4Cl==NaCl+N2↑+2H2O (实验室制氮气) NH4++NO2-=N2↑+2H2O2、还原性:2FeCl2+3Cl2===2FeCl3 (在水溶液中不需加热)2Fe2++3Cl2=2Fe3++6Cl-3Na2S+8HNO3(稀)===6NaNO3+2NO↑+3S+4H2O3S2-+8H++2NO3-=2NO↑+3S+4H2O3Na2SO3+2HNO3(稀)===3Na2SO4+2NO↑+H2O3SO32-+2H++2NO3-=3SO42-+2NO↑+H2O2Na2SO3+O2===2Na2SO4 (Na2SO3在空气中易变质)Na2SO3+S Na2S2O3Na2S+Cl2==2NaCl+S↓(在水溶液中) S2-+Cl2=2Cl-+S↓3、与碱性物质的作用:Ca(OH)2+CuSO4==Cu(OH)2↓+CaSO4↓(波尔多液)MgCl2+2NH3H2O===Mg(OH)2↓+2NH4ClMg2++2NH3H2O=Mg(OH)2↓+2NH4+AlCl3+3NH3H2O===Al(OH)3↓+3NH4ClAl3++3NH3H2O=Al(OH)2↓+3NH4+FeCl3+3NH3H2O===Fe(OH)3↓+3NH4ClFe3++3NH3H2O=Fe(OH)3↓+3NH4+CuSO4+2NH3H2O(不足)==Cu(OH)2↓+(NH4)2SO4Cu2++2NH3H2O=Cu(OH)2↓+2NH4+Cu(OH)2+4NH3H2O=Cu(NH3)4(OH)2+4H2OCu(OH)2+4NH3H2O=[Cu(NH3)4]2++2OH-+4H2O 铜氨溶液CuSO4+4NH3H2O(足)==Cu(NH3)4SO4+4H2O 总方程式Cu2++4NH3H2O=[Cu(NH3)4]2++4H2O 铜氨溶液AgNO3+NH3H2O==AgOH↓+NH4NO3 2AgOH=Ag2O(灰黑色)+H2O Ag2O+4NH3H2O=2[Ag(NH3)2]++2OH-+3H2O 银氨溶液AgNO3+2NH3H2O==Ag(NH3)2NO3+2H2OAg++2NH3H2O=[Ag(NH3)2]++2H2O 总方程式ZnSO4+2NH3H2O(不足)==Zn(OH)2↓+(NH4)2SO4Zn(OH)2+4NH3H2O=Zn(NH3)4(OH)2+4H2OZnSO4+4NH3H2O(足)==Zn(NH3)4SO4+4H2OZn2++4NH3H2O=[Zn(NH3)4]2++4H2O 总方程式4、与酸性物质的作用:强酸制弱酸,或不挥发性酸制挥发性酸Na3PO4+2HCl===Na2HPO4+2NaCl PO43-+2H+=H2PO4-Na2HPO4+HCl===NaH2PO4+NaCl HPO42-+H+=H2PO4-NaH2PO4+HCl===H3PO4+NaCl H2PO4-+H+=H3PO4Na2CO3+HCl===NaHCO3+NaCl CO32-+H+=HCO3-NaHCO3+HCl===NaCl+H2O+CO2↑HCO3-+H+=CO2↑+H2O3Na2CO3+2AlCl3+3H2O==2Al(OH)3↓+3CO2↑+6NaCl (物质之间的.双水解反应)3CO32-+2Al3++3H2O=2Al(OH)3↓+3CO2↑3Na2CO3+2FeCl3+3H2O===2Fe(OH)3↓+3CO2+6NaCl (物质之间的双水解反应)3CO32-+2Fe3++3H2O=2Fe(OH)3↓+3CO2↑3NaHCO3+AlCl3===Al(OH)3↓+3CO2↑(物质之间的双水解反应)3HCO3-+Al3+=2Al(OH)3↓+3CO2↑3NaHCO3+FeCl3===Fe(OH)3↓+3CO2↑(物质之间的双水解反应)3HCO3-+Fe3+=2Fe(OH)3↓+3CO2↑3Na2S+Al2(SO4)3+6H2O===2Al(OH)3↓+3H2S↑(物质之间的双水解反应)3NaAlO2+AlCl3+6H2O==4Al(OH)3↓+3NaCl (物质之间的双水解反应)3AlO2-+Al3++6H2O=4Al(OH)3↓3NaAlO2+FeCl3+6H2O==3Al(OH)3↓+Fe(OH)3↓+3NaCl3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓NaAlO2+NH4Cl+2H2O==Al(OH)3↓+NH3H2O+NaClAlO2-+NH4++2H2O=Al(OH)3↓+NH3H2ONa2CO3+H2O+CO2===2NaHCO3CO32-+H2O+CO2=2HCO3-Na2CO3+H2O+2SO2==2NaHSO3+CO2↑(1:2)CO32-+H2O+2SO2=2HSO3-+CO2↑2Na2CO3(足)+H2O+SO2==Na2SO3+2NaHCO3 (CO2中的SO2不能用Na2CO3洗气)2CO32-+H2O+SO2=SO32-+2HCO3- (2:1)Na2CO3+SO2==Na2SO3+CO2 (1:1)CO32-+SO2=SO32-+CO2NaHCO3+SO2===NaHSO3+CO2 (CO2中的SO2可能用NaHCO3洗气)2HCO3-+SO2=2HSO3-+CO22NaHCO3+SO2==Na2SO3+2CO2+H2O2HCO3-+SO2=SO32-+2CO2+H2ONa2SiO3+2HCl===H2SiO3↓+NaCl 或Na2SiO3+2HCl+H2O===H4SiO4↓+2NaClSiO32-+2H+=H2SiO3↓或SiO32-+2H++H2O=H4SiO4↓Na2SiO3+CO2+2H2O===H2SiO3↓+Na2CO3SiO32-+CO2+2H2O=H4SiO4↓+CO32-5、盐与盐复分解反应Na2SO4+BaCl2==BaSO4↓+2NaCl(沉淀不溶于盐酸、硝酸)SO32-+Ba2+=BaSO4↓Na2SO3+BaCl2==BaSO3↓+2NaCl (沉淀溶于盐酸,在硝酸中生成新的沉淀,沉淀不消失)SO32-+Ba2+=BaSO3↓Na2CO3+BaCl2==BaCO3↓+2NaCl(沉淀溶于盐酸、沉淀消失)CO32-+Ba2+=BaCO3↓Na2CO3+CaCl2==CaCO3↓+2NaCl (NaHCO3不反应)CO32-+Ca2+=CaCO3↓AgNO3+NaCl==AgCl↓+NaNO3 Ag++Cl-=AgCl↓AgNO3+NaBr==AgBr↓+NaNO3 Ag++Br-=AgBr↓AgNO3+KI==AgCl↓+KNO3 Ag++I-=AgI↓3AgNO3+Na3PO4==Ag3PO4↓+3NaNO3 3Ag++PO43-=Ag3PO4↓CuSO4+Na2S==CuS↓+Na2SO4 Cu2++S2-=CuS↓FeCl3+3KSCN==Fe(SCN)3+3KClFe3++3SCN-=Fe(SCN)3 (血红色,用于Fe3+的特性检验) 6、不稳定性:Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2OS2O32-+2H+=S↓+SO2↑+H2ONH4Cl NH3↑+HCl↑NH4I NH3↑+HI↑2HI H2+I2NH4I NH3↑+H2↑+I2↑NH4HCO3 NH3↑+H2O+CO2↑2KNO3 2KNO2+O2↑2Cu(NO3)3 2CuO+4NO2↑+O2↑2AgNO3 2Ag+2NO2↑+O2↑(保存在棕色瓶中)5NH4NO3 4N2↑+2HNO3+9H2O10NH4NO3 8N2↑+4NO2↑+O2↑+20H2O↑(硝酸铵爆炸反应) 2KMnO4 K2MnO4+MnO2+O2↑2KClO3 2KCl+3O2↑2NaHCO3 Na2CO3+H2O+CO2↑Ca(HCO3)2 CaCO3+H2O+CO2↑CaCO3 CaO+CO2↑MgCO3 MgO+CO2↑。
高考化学复习:水解反应的方程式

高考化学复习:水解反应的方程式1、单水解---可逆水解NH4Cl+H2O NH3H2O+HCl NH4++H2O H++NH3H2OFeCl3+3H2O Fe(OH)3+3HCl Fe3++3H2O Fe(OH)3+3H+AlCl3+3H2O Al(OH)3+3HCl Al3++3H2O Al(OH)3+3H+CuSO4+2H2O Cu(OH)2+H2SO4 (金属活动顺序表中Mg2+以后的阳离子均水解)NaHCO3+H2O H2CO3+NaOH (NaHSO4不水解,NaHSO3电离大于水解)Na2CO3+H2O NaHCO3+NaOH CO32-+H2O HCO3-+OHNaHCO3+H2O H2CO3+NaOH(第一步远远大于第二步,二步不能叠加)Na2SO3+H2O NaHSO3+NaOH SO32-+H2O HSO3-+OHNaHSO3+H2O H2SO3+NaOH(第一步远远大于第二步,二步不能叠加)HSO3-+H2O H2SO3+OH-Na2S+H2O NaHS+NaOH S2-+H2O HS-+OHNaHS+H2O H2S+NaOH(第一步远远大于第二步,二步不能叠加) HS-+H2O H2S+OH-Na3PO4+H2O Na2HPO4+NaOH PO43-+H2O HPO42-+OHNa2HPO4+H2O NaH2PO4+NaOH HPO42-+H2O H2PO4-+OHNaH2PO4+H2O H3PO4+NaOH H2PO4-+H2O H3PO4+OHCH3COONa+H2O CH3COOH+NaOH CH3COO-+H2O CH3COOH+OHC6H5ONa+H2O C6H5OH+NaOH C6H5O-+H2O C6H5OH+OH2、双水解CH3COONH4+H2O CH3COOH+NH3H2ONH4F+H2O HF+NH3H2OAl2S3+6H2O==Al(OH)3+H2S (隔绝空气,密封保存)Mg3N2+6H2O==Mg(OH)2+NH3(隔绝空气,密封保存)Na3P+3H2O==3NaOH+PH3(隔绝空气,密封保存)Zn3P2+6H2O==Zn(OH)2+PH3(Zn3P2一种老鼠药,PH3剧毒神经毒剂)CaC2+2H2O==Ca(OH)3+C2H2(隔绝空气,密封保存)C2H5ONa+H2O==C2H5OH+NaOH高考如何复习一直都是考生们关注的话题,下面是的编辑为大家准备的高考化学复习:水解反应的方程式。
水解反应的化学方程式

水解反应的化学方程式水解反应的化学方程式可是化学里超有趣的一部分呢!水解反应就是化合物与水发生的复分解反应。
咱先来说说盐类的水解吧。
比如说氯化铵,它的水解方程式是NH₄Cl + H₂O ⇌NH₃·H₂O+ HCl。
你看啊,氯化铵这个盐,铵根离子它可不安分呢,它会和水电离出来的氢氧根离子结合,变成一水合氨,这样就剩下了氢离子,溶液就显酸性啦。
还有碳酸钠,它的水解方程式是Na₂CO₃+ H₂O ⇌NaHCO₃+ NaOH。
碳酸根离子可调皮了,它要从水里抢一个氢离子过来,变成碳酸氢根离子,然后就有多余的氢氧根离子了,溶液就呈碱性咯。
酯类的水解也很有意思。
像乙酸乙酯的水解,在酸性条件下,它的反应方程式是CH₃COOC₂H₅+ H₂O ⇌CH₃COOH + C₂H₅OH。
你可以想象成乙酸乙酯这个小团体,在水这个大环境里,被酸催化着,然后就分解成了乙酸和乙醇这两个小伙伴。
要是在碱性条件下呢,反应方程式就变成了CH₃COOC₂H₅+ NaOH → CH₃COONa + C₂H₅OH。
这里啊,氢氧化钠这个强碱可厉害了,它不但促使酯水解,还把生成的乙酸变成了乙酸钠呢。
卤代烃的水解也值得唠唠。
像溴乙烷的水解,方程式是CH₃CH₂Br + H₂O → CH₃CH₂OH + HBr。
溴乙烷这个家伙,在水的作用下,把溴原子换成了羟基,就变成乙醇啦。
水解反应在生活里也有很多例子呢。
比如说肥皂的制作,就涉及到油脂的水解。
油脂在碱性条件下水解,生成甘油和高级脂肪酸盐,这个高级脂肪酸盐就是肥皂的主要成分啦。
还有淀粉的水解,淀粉在淀粉酶等的作用下,逐步水解成葡萄糖。
这个过程对我们人体可重要了,因为葡萄糖是我们能量的重要来源呢。
在化学学习中,水解反应的方程式是很重要的一部分,理解了这些方程式,就能更好地理解很多化学现象和化学过程啦。
你要是把这些方程式都搞清楚了,就像掌握了化学世界里的一把小钥匙,可以打开很多知识的小盒子哦。
高中化学常见水解反应方程式汇总

高中化学常见水解反应方程式汇总水与另一化合物反应,该化合物分解为两部分,水中氢原子加到其中的一部分,而羟基加到另一部分,因而得到两种或两种以上新的化合物的反应过程。
那么高中化学水解反应的化学方程式又有哪些呢?下面是高中化学常见水解反应方程式汇总,供参考。
高中化学常见水解反应方程式汇总点击查看:高中化学方程式汇总高中化学水解反应方程式如下Al2S3+6H2O==Al(OH)3↓+H2S↑(隔绝空气,密封保存)Mg3N2+6H2O==Mg(OH)2↓+NH3↑(隔绝空气,密封保存)Na3P+3H2O==3NaOH+PH3↑(隔绝空气,密封保存)Zn3P2+6H2O==Zn(OH)2↓+PH3↑(Zn3P2一种老鼠药,PH3剧毒神经毒剂)CaC2+2H2O==Ca(OH)3↓+C2H2↑(隔绝空气,密封保存)NaHCO3+H2O H2CO3+NaOH(NaHSO4不水解,NaHSO3电离大于水解) Na2HPO4+H2O NaH2PO4+NaOH HPO42-+H2O H2PO4-+OH–NaH2PO4+H2O H3PO4+NaOH H2PO4-+H2O H3PO4+OH–CH3COONa+H2O CH3COOH+NaOH CH3COO-+H2O CH3COOH+OH–C6H5ONa+H2O C6H5OH+NaOH C6H5O-+H2O C6H5OH+OH–C17H35COO-CH+3H2O====CH-OH+3C17H35COOHC17H35COO-CH+3NaOH====CH2OH+3C17H35COONaCH3COOC2H5+NaoH=CH3COONa+c2H5oH(条件加热水)可逆CaC2+2H2O→Ca(OH)2+C2H2↑C2H4+H20→CH3CH2OH(条件为催化剂)C2H2+H2O→C2H4O(条件为催化剂,加热加压)CH2=CH2+H20→CH3CH2OH(条件为催化剂)c2H5Br+NaoH→C2H5OH+NABr(条件是加热水)以上是小编整理的高中化学常见水解反应方程式汇总,更多更详细的高中化学方程式请关注。
高中化学水解反应方程式

水解反应中有机部分是水与另一化合物反应。
以下是水解反应方程式。
1、单水解---可逆水解1.NH4Cl+H2O NH3•H2O+HCl NH4++H2O H++NH3•H2O2.FeCl3+3H2O Fe(OH)3+3HCl Fe3++3H2O Fe(OH)3+3H+3.AlCl3+3H2O Al(OH)3+3HCl Al3++3H2O Al(OH)3+3H+4.CuSO4+2H2O Cu(OH)2+H2SO4 (金属活动顺序表中Mg2+以后的阳离子均水解)5.NaHCO3+H2O H2CO3+NaOH (NaHSO4不水解,NaHSO3电离大于水解)6.Na2CO3+H2O NaHCO3+NaOH CO32-+H2O HCO3-+OH–7.NaHCO3+H2O H2CO3+NaOH(第一步远远大于第二步,二步不能叠加)8.Na2SO3+H2O NaHSO3+NaOH SO32-+H2O HSO3-+OH–9.NaHSO3+H2O H2SO3+NaOH(第一步远远大于第二步,二步不能叠加)10.HSO3-+H2O H2SO3+OH-11.Na2S+H2O NaHS+NaOH S2-+H2O HS-+OH–12.NaHS+H2O H2S+NaOH(第一步远远大于第二步,二步不能叠加)13.HS-+H2O H2S+OH-14.Na3PO4+H2O Na2HPO4+NaOH PO43-+H2O HPO42-+OH–15.Na2HPO4+H2O NaH2PO4+NaOH HPO42-+H2O H2PO4-+OH–16.NaH2PO4+H2O H3PO4+NaOH H2PO4-+H2O H3PO4+OH–17.CH3COONa+H2O CH3COOH+NaOH CH3COO-+H2O CH3COOH+OH–18.C6H5ONa+H2O C6H5OH+NaOH C6H5O-+H2O C6H5OH+OH–2、双水解19.CH3COONH4+H2O CH3COOH+NH3•H2O20.NH4F+H2O HF+NH3•H2O21.Al2S3+6H2O==Al(OH)3↓+H2S↑(隔绝空气,密封保存)22.Mg3N2+6H2O==Mg(OH)2↓+NH3↑(隔绝空气,密封保存)23.Na3P+3H2O==3NaOH+PH3↑(隔绝空气,密封保存)24.Zn3P2+6H2O==Zn(OH)2↓+PH3↑(Zn3P2一种老鼠药,PH3剧毒神经毒剂)25.CaC2+2H2O==Ca(OH)3↓+C2H2↑(隔绝空气,密封保存)26.C2H5ONa+H2O==C2H5OH+NaOH。
