高中化学常见的水解反应
高中阶段能水解的有机物

高中阶段能水解的有机物一、引言有机物是由碳和氢构成的化合物,广泛存在于自然界中。
在高中化学学习中,我们了解到有机物可以被水解,即通过水的作用分解成更简单的有机物或无机物。
本文将介绍高中阶段能水解的一些常见有机物及其水解反应。
二、脂肪类1. 甘油三酯甘油三酯是一种常见的脂肪类有机物,它由一个甘油分子与三个脂肪酸分子结合而成。
当甘油三酯与水反应时,水分子与甘油三酯中的酯键发生水解反应,生成甘油和三个脂肪酸分子。
2. 磷脂类磷脂类是一类含磷的脂类有机物,常见的有磷脂酰胆碱、磷脂酰乙醇胺等。
磷脂类与水反应时,磷脂酯键发生水解反应,生成磷酸、醇或胆碱等物质。
三、糖类1. 单糖葡萄糖、果糖等单糖是高中化学中常见的有机物。
它们可以通过水的作用分解成更小的分子。
例如,葡萄糖与水反应时,葡萄糖分子中的糖苷键发生水解反应,生成葡萄糖醛酮和葡萄糖。
2. 多糖淀粉、纤维素等多糖也可以被水分解。
当淀粉与水反应时,淀粉分子中的糖苷键发生水解反应,生成葡萄糖单体。
四、蛋白质蛋白质是生物体中重要的有机物之一,由氨基酸分子通过肽键连接而成。
蛋白质可以被水分解为氨基酸。
水解反应发生在肽键上,使蛋白质分子断裂,生成氨基酸。
五、酶酶是生物体内催化反应的生物催化剂,也是一种特殊的蛋白质。
酶可以催化有机物的水解反应,使其分解成更小的有机物或无机物。
例如,淀粉酶可以催化淀粉的水解反应,将淀粉分解成葡萄糖单体。
六、植物中的有机物水解植物体内存在着大量的有机物,这些有机物在植物的生长和代谢过程中起着重要的作用。
在植物的生长过程中,一些有机物可以被水解,以提供植物所需的养分。
例如,植物体内的葡萄糖可以通过水解反应分解成葡萄糖醛酮和葡萄糖,以供植物进行能量代谢。
七、总结高中阶段能水解的有机物包括脂肪类、糖类、蛋白质等。
它们在与水反应时,发生水解反应,分解成更简单的有机物或无机物。
了解这些有机物的水解反应对我们理解生物体代谢过程和化学反应机理具有重要意义。
初高中化学段的水解反应知识点

初高中化学段的水解反应知识点一、无机物的水解1.单质的水解:Cl-Cl+H-OH == HCl + HClO2.氧化物的水解:Na2O + H-OH == 2NaOH3.盐类的水解:化学反应原理:盐的离子(一般是弱酸的阴离子或弱碱的阳离子)跟水电离出来的H+或OH-结合形成弱电解质,从而促进水的电离。
如:NH4++H2O=NH3·H2O+H+4.非盐型离子化合物的水解这类水解主要是指活泼金属的氢化物、氮化物、磷化物、碳化物等的水解。
如:CaH2+2H2O=Ca(OH)2+2H2↑Mg3N2+6H2O=3Mg(OH)2+2NH3↑CaC2+2H2O→Ca(OH)2+C2H2↑不难写出BN、MgC2、Al4C3等.如:Al4C3+12H2O→4Al(OH)↓+3CH4↑35.非金属卤化物的水解(1)卤素互化物:IBr+H2O=HIO+HBr(2)氮族元素卤化物的水解,如:NCl3+H2O(少)=HClO + NH3 (初级产物),或NCl3+2H2O (多)=2HClO+ NH3·H2O。
而在一定条件下,HClO是强氧化剂,能再将NH3氧化成N2和HCl.(一般不考虑)注意:NH3能在加热条件下被HNO3,浓H2SO4,HClO氧化,在水中NH3,NH4+均不易被氧化。
此外还有:PCl3+3H-OH= H3PO3+3HClAsX3+3H2O=H3AsO3+3HXBCl3+3H2O=H3BO3↓+3HCl↑等.二、有机物的水解1.卤代烃的水解;2.醇钠、酚钠的水解;3.羧酸衍生物的水解;4.糖类的水解;5.多肽、蛋白质的水解。
口诀:离换离、基换基,异电相吸去分析,初级产物优先写,二级反应后考虑。
高考化学水解知识点大全

高考化学水解知识点大全高考化学水解知识点1.概述:水解是高中化学较常见、也是较重要的一类化学反应,说到底就是和水发生的复分解或取代反应。
均为吸热反应,升高温度,水解程度增大。
溶液越稀,水解程度越大。
2.实质:被水解是物质,在水分子作用下断键后,其阳性基团结合水分子中的阴性基团OH,阴性基团结合水分子中的阳性基团H,可表示为:3.分类:⑴卤代烃(卤素原子)的水解:氢氧化钠水溶液(NaOH作催化剂)生成醇。
⑵酯的水解:酯化反应的逆反应,生成醇和酸;酸做催化剂可逆,碱作催化剂不可逆,(油脂碱性条件下的水解为皂化反应)。
⑶蛋白质的水解:生成氨基酸,酸或碱均可作催化剂,且均不可逆。
⑷多糖的水解:蔗糖水解得一分子葡萄糖一分子果糖,麦芽糖水解得两分子葡萄糖,淀粉、纤维素水解的最终产物都是葡萄糖。
纤维素水解用浓硫酸作催化剂,其他三个水解用稀硫酸作催化剂。
⑸一些特殊金属化合物水解:①碳化物:CaC2+2H2O=Ca(OH)2+C2H2↑,Al4C3+12H2O=4Al(OH)3+3CH4↑,②氮化物:Mg3N2+6H2O=3Mg(OH)2+2NH3↑,③硫化物:Al2S3+6H2O= 2Al(OH)3+3H2S↑,④非金属卤化物:PCl5+4H2O=5HCl+H3PO4,ICl+H2O=HCl+HIO,⑤氢化物:NaH+H2O=NaOH+H2↑⑹盐类的水解:中和反应的逆反应,生成酸和碱。
除少数强烈双水解外,通常都十分微弱。
处理该部分问题需要牢记:有弱才水解,无弱不水解;谁弱谁水解,越弱越水解;谁强呈谁性,同强呈中性。
4.延伸⑴醇解,⑵氨解,⑶酯交换等盐类的水解第一片:概述1.概念:在水溶液中,盐电离出来的离子结合水电离的H+或OH_生成弱电解质的过程。
2.条件:⑴盐应是可溶性的,⑵能电离出弱酸根离子或弱碱的阳离子3.实质:生成弱电解质,破坏了水的电离平衡,促进了水的电离。
4.规律:有弱才水解,无弱不水解;谁弱谁水解,都弱都水解;越弱越水解,越稀越水解,越热越水解。
高中化学能发生水解的官能团

水解是一种化学反应,涉及到某些官能团在水的存在下发生分解。
以下是高中化学中常见能发生水解的一些官能团:
1. 酯水解:酯在水中可以水解成相应的醇和酸。
- 例如:RCOOR' + H2O→RCOOH + R'OH
2. 醚水解:醚分子在水中可以发生醚水解反应。
- 例如:ROR' + H2O→ROH + R'OH
3. 酰胺水解:酰胺在水中可以水解成相应的酸和胺。
- 例如:RCONH2 + H2O→RCOOH + NH3
4. 酰氯水解:酰氯在水中可以水解成相应的酸和盐酸。
- 例如:RCOCl + H2O→RCOOH + HCl
5. 亚胺水解:亚胺在水中可以水解成相应的醛和胺。
- 例如:R2NCHOH + H2O→RCHO + R2NH2
这些反应是有机化学中常见的水解反应,其中含有酯、醚、酰胺、酰氯和亚胺等官能团的有机物在水中分解成不同的产物。
在高中化学学科中,这些反应通常属于有机化学的范畴。
高中生物水解和彻底水解总结

高中生物水解和彻底水解总结一、水解的概念水解是指通过加入水分子,将化合物分解成更简单的物质的化学反应过程。
在生物学中,水解是一种常见的分解反应,能够将复杂的有机物分解为简单的有机物、离子或原子。
二、水解的种类1. 酸性水解:酸性水解是指在酸性条件下进行的水解反应。
酸性条件下,酸能够提供H+离子,使水解反应发生。
例如,蛋白质在胃酸的作用下发生酸性水解,被分解成氨基酸。
2. 碱性水解:碱性水解是指在碱性条件下进行的水解反应。
碱性条件下,碱能够提供OH-离子,使水解反应发生。
例如,油脂在碱性溶液中发生碱性水解,生成甘油和脂肪酸。
3. 酶促水解:酶促水解是指在酶的催化下进行的水解反应。
酶是生物体内催化反应的生物催化剂,能够降低反应的活化能,加速水解反应的进行。
例如,淀粉在口腔和胰液中的淀粉酶的作用下发生酶促水解,生成葡萄糖。
三、水解的意义水解在生物学中具有重要的意义:1. 营养吸收:通过水解,生物体能够将复杂的有机物分解成可溶性的小分子物质,便于吸收和利用。
例如,食物中的蛋白质在胃酸和胃蛋白酶的作用下发生水解,生成氨基酸,被小肠吸收利用。
2. 废物排出:水解也参与了废物的分解和排出。
例如,肝脏通过水解将无法利用的氨基酸转化成尿素,经过肾脏排出体外。
3. 能量供应:一些有机物的水解反应能够释放出能量,在细胞代谢中起到能量供应的作用。
例如,葡萄糖的水解反应能够释放出能量,提供给细胞进行生命活动。
水解是一种常见的生物化学反应,通过加入水分子将复杂的有机物分解成更简单的物质。
根据不同的条件和催化剂,水解可以分为酸性水解、碱性水解和酶促水解。
水解在生物学中具有重要的意义,包括营养吸收、废物排出和能量供应等方面。
了解水解的原理和意义对于我们理解生物体的代谢过程具有重要的意义。
最新高中化学常见的水解反应培训讲学
1.(NH4)2CO3
水解离子方程式为:NH4++CO32-+H2O
HCO3-+NH3.H2O
2.CH3COONH4水解离子方程式为:CH3COO-+NH4++H2O
CH3COOH+NH3.H2O
3.NH4HCO3水解离子方程式为:NH4++HCO3-+H2O
H2CO3+NH3.H2O
(二)彻底水解, 用“=”,例:
Al3++3AlO2-+6H2O=4Al(OH)3↓
5.Fe3+与ClO-[如FeCl3、Fe2(SO4)3、Fe(NO3)3与NaClO溶液混合。]
Fe3++3ClO-+3H2O= Fe(OH)3↓+3HClO
6.Fe3+与HCO3-[如FeCl3、Fe2(SO4)3、Fe(NO3)3与NaHCO3溶液混合。]
HCOO-+H2O
HCOOH+OH-
17.Na2SiO3
Na2SiO3+2H2O
H2SiO3+2NaOH
SiO32-+2H2O
H2SiO3+2OH-
18.MgCl2
MgCl2+2H2O
Mg(OH)2+2HCl
Mg2++2H2O
Mg(OH)2+2H+
二.双水解
(一)不是彻底水解,比单一离子水解要强,用
CH3COO-+H2O
CH3COOH+OH-
7.Fe2(SO4)3
Fe2(SO4)3+6H2O
最新高中化学——常见水解反应总结教学内容
常见水解反应一.简单水解反应 二.双水解(一)不是彻底水解,比单一离子水解要强,用 表示,例:1.(NH 4)2CO 3 水解离子方程式为:NH 4++CO 3 2- +H 2O HCO 3-+NH 3.H 2O 2.CH 3COONH 4水解离子方程式为:CH 3COO -+NH 4++H 2O CH 3COOH+NH 3.H 2O3.NH 4HCO 3水解离子方程式为:NH 4++HCO 3 - +H 2O H 2CO 3+NH 3.H 2O(二)彻底水解, 用“=”,例: 1.泡沫灭火器原理:(药品为Al 2(SO 4)3和NaHCO 3)水解化学方程式为:Al 2(SO 4)3+6NaHCO 3=2Al(OH)3↓+3Na 2SO 4+6CO 2↑水解离子方程式为:Al 3++3HCO 3-=Al(OH)3↓+3CO 2↑2.Al 3+与S 2-[如AlCl 3、Al 2(SO 4)3、Al (NO 3)3与Na 2S 、K 2S 溶液混合。
]水解离子方程式为:2Al 3++3S 2-+6H 2O=2Al(OH)3↓+3H 2S ↑3.Al 3+与CO 32-[如AlCl 3、Al 2(SO 4)3、Al (NO 3)3与Na 2CO 3、K 2CO 3溶液混合。
]水解离子方程式为:2Al 3++3CO 32-+3H 2O=2Al(OH)3↓+3CO 2↑4.Al 3+与AlO 2-[如AlCl 3、Al 2(SO 4)3、Al (NO 3)3与NaAlO 2、KAlO 2溶液混合。
] Al 3++3AlO 2-+6H 2O=4Al(OH)3↓ 5.Fe 3+与ClO -[如FeCl 3、Fe 2(SO 4)3、Fe (NO 3)3与NaClO 溶液混合。
] Fe 3++3ClO -+3H 2O= Fe(OH)3↓+3HClO 6.Fe 3+与HCO 3 -[如FeCl 3、Fe 2(SO 4)3、Fe (NO 3)3与NaHCO 3 溶液混合。
高三化学电离与水解知识点
高三化学电离与水解知识点电离与水解是高中化学中重要的知识点,涉及到溶液的离子化程度、酸碱中和反应等概念。
本文将围绕电离与水解的定义、化学平衡中的应用以及相关实例进行详细阐述。
一、电离与水解的定义电离是指化学物质在溶液中或熔融状态下,通过释放离子而转变为离子的过程。
以强酸HCl为例,当它溶解在水中时,会释放出H+离子和Cl-离子:HCl(气体)→ H+(溶液)+ Cl-(溶液)水解是指化学物质在水溶液中与水发生反应,产生离子和水的过程。
以强碱NaOH为例,当它溶解在水中时,会发生水解反应:NaOH(固体)+ H2O(液体)→ Na+(溶液)+ OH-(溶液)二、化学平衡中的电离与水解在酸碱中和反应中,离子的电离与水解是化学平衡过程中重要的组成部分。
根据勒夏特列原理,对于弱电解质溶液,它的电离与水解可以相互制约,形成动态平衡。
以弱酸HAc(醋酸)的电离与水解为例,该过程可以表达为如下平衡反应:HAc(溶液)⇄ H+(溶液)+ Ac-(溶液)在水中,HAc分子发生电离,部分转化为离子H+和Ac-,同时也会出现Ac-与水分子的水解反应:Ac-(溶液)+ H2O(溶液)⇄ HAc(溶液)+ OH-(溶液)这两个反应相互制约,不断进行,直到达到化学平衡。
三、电离与水解的相关实例1. 酸碱指示剂的应用酸碱指示剂是根据溶液的酸碱性质发生颜色变化的物质。
这种颜色变化与指示剂分子的电离与水解有关。
如甲基橙指示剂,在酸性溶液中会接受H+离子而发生电离,呈现红色;在碱性溶液中,指示剂分子与OH-离子发生水解,呈现黄色。
通过观察指示剂的颜色变化,可以判断溶液的酸碱性质。
2. 酸碱中和反应酸碱中和反应是指酸溶液与碱溶液按化学计量比发生完全反应的过程。
在这个过程中,酸与碱溶液中的离子发生重新组合,形成中和盐和水。
例如,盐酸和氢氧化钠反应生成氯化钠和水的化学方程式为:HCl(溶液)+ NaOH(溶液)→ NaCl(溶液)+ H2O(溶液)该反应中,HCl中的H+离子与NaOH中的OH-离子结合,生成中和盐NaCl和水。
高中化学:水解反应方程式
高中化学:水解反应方程式AlCl3+3H2O Al(OH)3+3HCl Al3++3H2O Al(OH)3+3H+CuSO4+2H2O Cu(OH)2+H2SO4(金属活动顺序表中Mg2+以后的阳离子均水解)NaHCO3+H2O H2CO3+NaOH(NaHSO4不水解,NaHSO3电离大于水解)Na2CO3+H2O NaHCO3+NaOH CO32-+H2O HCO3-+OH–NaHCO3+H2O H2CO3+NaOH(第一步远远大于第二步,二步不能叠加)Na2SO3+H2O NaHSO3+NaOH SO32-+H2O HSO3-+OH–NaHSO3+H2O H2SO3+NaOH(第一步远远大于第二步,二步不能叠加)Na2S+H2O NaHS+NaOH S2-+H2O HS-+OH–NaHS+H2O H2S+NaOH(第一步远远大于第二步,二步不能叠加)HS-+H2O H2S+OH-Na3PO4+H2O Na2HPO4+NaOH PO43-+H2O HPO42-+OH–NaH2PO4+H2O H3PO4+NaOH H2PO4-+H2O H3PO4+OH–CH3COONa+H2O CH3COOH+NaOH CH3COO-+H2O CH3COOH+OH–C6H5ONa+H2O C6H5OH+NaOH C6H5O-+H2O C6H5OH+OH–NH4F+H2O HF+NH3H2OAl2S3+6H2O==Al(OH)3↓+H2S↑(隔绝空气,密封保存)Mg3N2+6H2O==Mg(OH)2↓+NH3↑(隔绝空气,密封保存)Na3P+3H2O==3NaOH+PH3↑(隔绝空气,密封保存)Zn3P2+6H2O==Zn(OH)2↓+PH3↑(Zn3P2一种老鼠药,PH3剧毒神经毒剂)C2H5ONa+H2O==C2H5OH+NaOH总结:高中化学:水解反应方程式就为大家介绍到这儿了,希望小编的整理可以帮助到大家,祝大家学习进步。
高中有机化学发生水解反应
典型类型:高中有机化学发生水解反应1、卤化物的水解;通常用氢氧化钠水溶液作水解剂,反应通式如下:R—X+H2O-─→R—OH+HXAr—X+2H2O─→Ar—OH+HX+H2O 式中R、Ar、X分别表示烷基、芳基、卤素。
2、脂链上的卤素一般比较活泼,可在较温和的条件下水解,如从氯苄制苯甲醇;芳环上的卤素被邻位或对位硝基活化时,水解较易进行,如从对硝基氯苯制对硝基酚钠。
3、酯的水解;油脂在酸或碱催化条件下可以水解.①酸性条件下的水解;在酸性条件下水解为甘油(丙三醇)高级脂酸.C17H35COO-CH2CH2-OHC17H35COO-CH+3H2O====CH-OH+3C 17H35COOHC17H35COO-CH2CH2-OH②碱性条件下的水解;在碱性条件下水解为甘油高级脂肪酸盐.C17H35COO-CH2CH2OHC17H35COO-CH+3NaOH====CH2OH+3C 17H35COONaC17H35COO-CH2CH2OH两种水解都会产生甘油.4、油脂在碱性条件下的水解反应称为皂化反应.工业上就是利用油脂的皂化反应制取肥皂.低碳烯烃与浓硫酸作用所得烷基硫酸酯,经加酸水解可得低碳醇。
5、淀粉/纤维素水解(C6H10O5)n(淀粉/纤维素)+nH2O→nC6H12O6(葡萄糖)GAGGAGAGGAFFFFAFAF6、蔗糖水解C12H22O11(蔗糖)+H2O→C6H12O6(果糖)+C6H12O6(葡萄糖)7、麦芽糖水解C12H22O11(麦芽糖)+H2O→2C6H12O6(葡萄糖)8、芳磺酸盐的水解通常不易进行,须先经碱熔,即以熔融的氢氧化钠在高温下与芳磺酸钠作用生成酚钠,后者可通过加酸水解生成酚。
如萘-2-磺酸钠在300~340℃常压碱熔后水解而得2-萘酚。
某些芳磺酸盐还需用氢氧化钠和氢氧化钾的混合碱作为碱熔的反应剂。
芳磺酸盐较活泼时可用氢氧化钠水溶液在较低温度下进行碱熔。
9、胺的水解脂胺和芳胺一般不易水解。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
HClO+NaOH
ClO-+H2O
HClO+OH-
11.CuSO4
CuSO4+2H2O
Cu(OH)2+H2SO4
Cu2++2H2O
Cu(OH)2+2H+
12.ZnCl2
ZnCl2+2H2O
Zn(OH)2+2HCl
Zn2++2H2O
Zn(OH)2+2H+
13.NaHCO3
NaHCO3+H2O
Al3++3AlO2-+6H2O=4Al(OH)3↓
5.Fe3+与ClO-[如FeCl3、Fe2(SO4)3、Fe(NO3)3与NaClO溶液混合。]
Fe3++3ClO-+3H2O= Fe(OH)3↓+3HClO
6.Fe3+与HCO3-[如FeCl3、Fe2(SO4)3、Fe(NO3)3与NaHCO3溶液混合。]
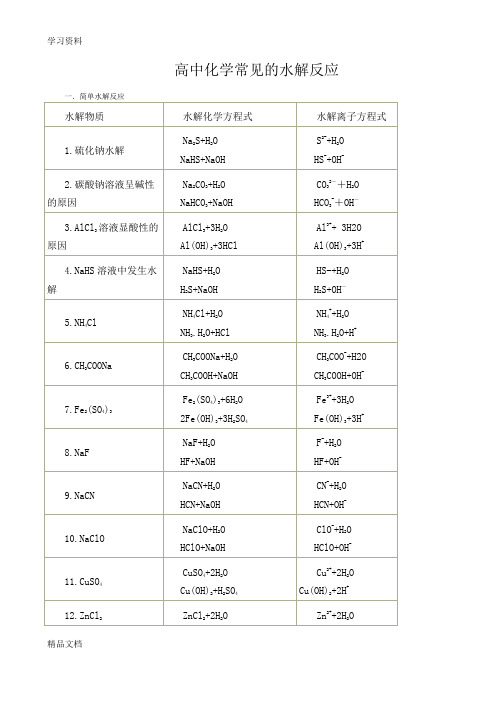
高中化学常见的水解反应
一.简单水解反应
水解物质
水解化学方程式
水解离子方程式
1.硫化钠水解
Na2S+H2O
NaHS+NaOH
S2-+H2O
HS-+OH-
2.碳酸钠溶液呈碱性的原因
Na2CO3+H2O
NaHCO3+NaOH
CO32-+H2O
HCO3-+OH-
3.AlCl3溶液显酸性的原因
AlCl3+3H2O
H2CO3+NaOH
HCO3-+H2O
H2CO3+OH-
14.Na3PO4
Na3PO4+H2O
Na2HPO4+NaOH
PO43-+H2O
HPO4-+OH-
15.Na2SO3
Na2SO3+H2O
NaHSO3+NaOH
SO32-+H2O
HSO3-+OH-
16.HCOONa
HCOONa+H2O
HCOOH+NaOH
HCOO-+H2O
HCOOH+OH-
17.Na2SiO3
Na2SiO3+2H2O
H2SiO3+2NaOH
SiO32-+2H2O
H2SiO3+2OH-
18.MgCl2
MgCl2+2H2O
Mg(OH)2+2HCl
Mg2++2H2O
Mg(OH)2+2H+
二.双水解
(一)不是彻底水解,比单一离子水解要强,用
Fe3++3HCO3-=Fe(OH)3↓+3CO2↑
CH3COO-+H2O
CH3COOH+OH-
7.Fe2(SO4)3
Fe2(SO4)3+6H2O
2Fe(OH)3+3H2SO4
Fe3++3H2O
Fe(OH)3+3H+
8.NaF
NaF+H2O
HF+NaOH
F-+H2O
HF+OH-
9.NaCN
NaCN+H2O
HCN+NaOH
CN-+H2O
HCN+OH-
10.NaClO
Al(OH)3+3HCl
Al3++ 3H2O
Al(OH)3+3H+
4.NaHS溶液中发生水解
NaHS+H2O
H2S+NaOH
HS-+H2O
H2S+OH-
5.NH4Leabharlann lNH4Cl+H2O
NH3.H2O+HCl
NH4++H2O
NH3.H2O+H+
6.CH3COONa
CH3COONa+H2O
CH3COOH+NaOH
1.泡沫灭火器原理:(药品为Al2(SO4)3和NaHCO3)
水解化学方程式为:Al2(SO4)3+6NaHCO3=2Al(OH)3↓+3Na2SO4+6CO2↑
水解离子方程式为:Al3++3HCO3-=Al(OH)3↓+3CO2↑
2.Al3+与S2-[如AlCl3、Al2(SO4)3、Al(NO3)3与Na2S、K2S溶液混合。]
水解离子方程式为:2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑
3.Al3+与CO32-[如AlCl3、Al2(SO4)3、Al(NO3)3与Na2CO3、K2CO3溶液混合。]
水解离子方程式为:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑
4.Al3+与AlO2-[如AlCl3、Al2(SO4)3、Al(NO3)3与NaAlO2、KAlO2溶液混合。]
表示,例:
1.(NH4)2CO3
水解离子方程式为:NH4++CO32-+H2O
HCO3-+NH3.H2O
2.CH3COONH4水解离子方程式为:CH3COO-+NH4++H2O
CH3COOH+NH3.H2O
3.NH4HCO3水解离子方程式为:NH4++HCO3-+H2O
H2CO3+NH3.H2O
(二)彻底水解, 用“=”,例:
