溶解度曲线知识点及习题
(word完整版)2015年初三化学溶解度曲线知识点及习题,推荐文档
溶解度曲线知识点一、正确理解溶解度曲线的涵义溶解度曲线就是在直角坐标系中,用来描绘物质的溶解度随温度变化而变化的曲线。
依据溶解度曲线可进行溶液的配制,混淆物的分别与提纯,以及进行物质结晶或溶解的计算。
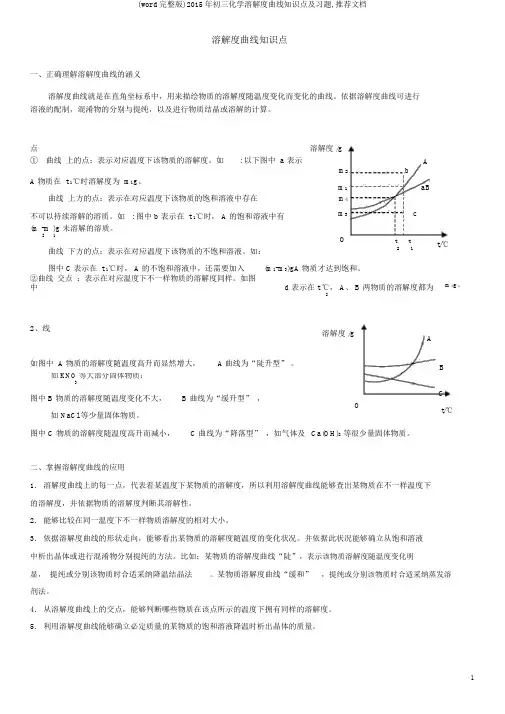
点溶解度 /g① 曲线上的点:表示对应温度下该物质的溶解度。
如: 以下图中 a 表示b Am2A 物质在 t 1℃时溶解度为 m1g。
m1 aB 曲线上方的点:表示在对应温度下该物质的饱和溶液中存在m4不可以持续溶解的溶质。
如 : 图中 b 表示在 t 1℃时, A 的饱和溶液中有m3 c (m -m )g 未溶解的溶质。
2 1 O t t曲线下方的点:表示在对应温度下该物质的不饱和溶液。
如: 2 1 图中 C表示在 t 1℃时, A 的不饱和溶液中,还需要加入(m1-m3)gA 物质才达到饱和。
②曲线交点:表示在对应温度下不一样物质的溶解度同样。
如图中 d 表示在 t ℃, A、 B 两物质的溶解度都为2 t/℃m4g。
2、线溶解度 /gA如图中 A 物质的溶解度随温度高升而显然增大,A曲线为“陡升型”。
B 如 KNO等大部分固体物质:3图中 B 物质的溶解度随温度变化不大, B 曲线为“缓升型” ,C O如 NaCl 等少量固体物质。
t/℃图中 C 物质的溶解度随温度高升而减小, C 曲线为“降落型” ,如气体及Ca(OH)2等很少量固体物质。
二、掌握溶解度曲线的应用1.溶解度曲线上的每一点,代表着某温度下某物质的溶解度,所以利用溶解度曲线能够查出某物质在不一样温度下的溶解度,并依据物质的溶解度判断其溶解性。
2.能够比较在同一温度下不一样物质溶解度的相对大小。
3.依据溶解度曲线的形状走向,能够看出某物质的溶解度随温度的变化状况。
并依据此状况能够确立从饱和溶液中析出晶体或进行混淆物分别提纯的方法。
比如:某物质的溶解度曲线“陡”,表示该物质溶解度随温度变化明显,提纯或分别该物质时合适采纳降温结晶法。
溶解度、质量分数、溶解度曲线相关计算有含答案

化学的相关计算:溶解度和质量百分数------讲义课前热身:1. 饱和溶液:在 下,在 里, 继续溶解某种溶质的溶液,称为这种溶质的饱和溶液。
2.不饱和溶液:在 下,在 里, 继续溶解某种溶质的溶液,称为这种溶质的不饱和溶液。
3.溶解度的定义:在 下,某物质在 溶剂中达到饱和时所溶解的该物质的 。
代表符号:S知识点一:关于溶解度的计算:公式:溶液的质量= +即:=溶液M +=溶剂的质量溶质的质量 ;=溶液的质量溶质的质量 例题一:把50克20℃时的硝酸钾饱和溶液蒸干,得到12克硝酸钾。
求20℃时硝酸钾的溶解度。
例题二:已知15℃时碘化钾的溶解度为140g ,计算在该温度下250g 水中最多能溶解多少克碘化钾?练习一:某温度下,a 克溶质溶解在2a 克水中恰好饱和,此溶质在该温度下的溶解度是( )A. 100克B. a 克C. 2a 克D. 50克练习二:t ℃将12克某物质溶于30克水中,恰好配制成该温度下的饱和溶液,则t ℃时该物质的溶解度?例题三:一定温度下,将200g 硝酸钠溶液蒸发掉10g 水后,析出晶体6g ,再蒸发掉5g 后,又析出晶体4g ,则该温度下,硝酸钠的溶解度是( )A. 40gB. 80gC. 60gD. 20g提示:一定要是饱和溶液才能运用溶解度的公式练习三:现有500g20℃的A 物质溶液,若保持温度不变,蒸发掉20g 水后,有5gA 析出,若再蒸发掉20g 水后,又有7gA 析出,则在20℃时A 物质的溶解度?练习四: 20℃时,100 g A 物质的溶液,温度不变,蒸发掉10 g 水后有2 g A析出,又蒸发掉10 g水有4 g A析出,则:20℃时A物质的溶解度为()A. 20gB. 40 gC. 30 gD. 无法计算例题四: 20℃时,将一定质量的NH4NO3完全溶解于100g水中,将所得溶液分成两等份,其中一份蒸发18g水,可使溶液饱和,另一份加入36g NH4NO3也达饱和,求⑴20℃时NH4NO3的溶解度。
溶解度曲线练习题.doc

溶解度曲线练习题溶解度曲线的应用例1:右图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。
据图答复:〔1〕P点的含义是。
〔2〕t2℃时30g a物质参加到50g水中不断搅拌,形成的溶液是〔饱和或不饱和〕溶液,溶液质量是g。
〔3〕t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是__________〔填写物质序号〕。
〔4〕在t2℃时,将等质量的a、b、c三种物质的饱和溶液同时降温至t1℃时,析出晶体最多的是,所得溶液中溶质质量分数〔浓度〕由大到小的顺序是。
〔5〕把t1℃a、b、c三种物质的饱和溶液升温到t2℃时,所得a、b、c三种物质的溶液中溶质质量分数〔浓度〕大小关系。
〔6〕假设把混在a中的少量b除去,应采用___________方法;假设要使b从饱和溶液中结晶出去,最好采用___________。
假设要使C从饱和溶液中结晶出去,最好采用___________。
稳固练习1、图2是硝酸钾和氯化钠的溶液度曲线,以下表达中不正确的选项是〔〕A. t1℃时,120gKNO3饱和溶液中含有20gKNO320B. t2℃时,KNO3和NaCl的饱和溶液中溶质的质量分数一样C. KNO3的溶解度大于NaCl的溶解度D. 当KNO3中含有少量的NaCl时,可以用结晶方法提纯KNO32、右图为A物质的溶解度曲线。
M、N两点分别表示A物质的两种溶液。
以下做法不能实现M、N间的相互转化的是〔〕A.从N→M:先向N中参加适量固体A再降温B.从N→M:先将N降温再参加适量固体A甲 乙溶解度 g 0 t 1 t 2 温度/℃3050 20 40 10 C .从M→N :先将M 降温,过滤后再将其升温D .从M→N :先将M 升温再将其蒸发掉局部水3、图1是a 、b 两种物质的溶解度曲线。
室温时,将盛有a 、b 饱和溶液的试管分别放入烧杯内的水中,均无晶体析出。
当向烧杯内的水中参加硝酸铵固体或浓硫酸后,图2试管内所示现象正确的选项是〔 〕(A) (B) (C) (D)图24、t ℃时,某物质的溶液220g ,蒸发去15g 水后,析出晶体6g ,又蒸发去10g 水,析出6g 晶体,再蒸去10g 水又析出晶体的质量为〔 〕A .4gB .6gC .10gD .15g5.20℃时,甲、乙两烧杯内依次放入A 物质的饱和溶液100g 、200g ,假设各蒸发5g 水,再恢复到20℃后,两杯中析出晶体质量为〔 〕A .甲>乙B .甲<乙C .甲=乙D .无法判断6、如图3是A 、B 、C 三种物质的溶解度曲线,以下说法中不正确的选项是〔 〕〔A 〕A 的饱和溶液从t 2℃降温到t 1℃时变为不饱和溶液〔B 〕C 的溶解度随温度的升高而减小 〔C 〕在t 1℃时,A 的溶解度等于C 的溶解度〔D 〕当A 中含有少量B 时,可以用降温结晶的方法提纯A7. 25℃时向一定量不饱和KNO3溶液中逐渐参加KNO3固体,那么以下图像中能正确表示此过程溶质质量变化规律的是〔 〕1.甲、乙两物质的溶解度曲线如右图所示。
(完整版)课题2溶解度知识点、习题及答案

(完整版)课题2溶解度知识点、习题及答案知识点1 饱和溶液、不饱和溶液1、饱和溶液、不饱和溶液2、浓、稀溶液与饱和不饱和溶液之间的关系在⼀定量的溶液⾥含溶质的量相对较多的是浓溶液,含溶质的量相对较少的是稀溶液。
①饱和溶液不⼀定是浓溶液②不饱和溶液不⼀定是稀溶液,如饱和的⽯灰⽔溶液就是稀溶液③在⼀定温度时,同⼀种溶质的饱和溶液要⽐它的不饱和溶液浓知识点2 固体物质的溶解度知识解读:⼀、对溶解度含义的理解:(1)20℃时NaCl 的溶液度为36g 含义:在20℃时,在100克⽔中最多能溶解36克NaCl 或在20℃时,NaCl 在100克⽔中达到饱和状态时所溶解的质量为36克。
(2)通过溶解度可得该温度下该物质的饱和溶液中,溶质、溶剂和溶液的质量⽐。
假设某温度下,某溶质的溶解度为Sg ,则溶质、溶剂和溶液之间的质量⽐为S :100 :(S+100)。
S =剂质m m ×100g⼆、影响固体溶解度的因素:(1)内部因素:溶质、溶剂的性质。
如20℃时,KNO 3的溶解度为31.6g ,⾷盐的溶解度为36g ,造成溶解度不同的原因是两种溶质的性质不同。
20℃时 KNO 3在⽔中、汽油中的溶解度相差很⼤,是由于溶剂的原因。
(2)外部因素:温度。
与溶剂量的多少没有关系,因为定义中已经规定了溶剂为100g ,所以固体物质的溶解度只随温度的变化⽽变化。
三、固体物质溶解度的表⽰⽅法(1)列表法(2)曲线法:⽤横坐标表⽰温度,纵坐标表⽰溶解度,画出物质的溶解度随温度变化的曲线,这种曲线叫做溶解度曲线。
(3)溶解度曲线的意义点:①溶解度曲线上的每⼀个点表⽰该溶质在某温度下的溶解度,②两条曲线交叉点表⽰两种溶质在同⼀温度下具有相同的溶解度,此时的溶液必然是饱和溶液,其饱和溶液中溶质质量分数也相同。
线:曲线表⽰物质的溶解度随温度的改变⽽变化的情况。
曲线变化幅度⼤,说明溶解度受温度影响⼤;曲线变化⽐较平坦,说明溶解度随温度变化⼩。
溶解度曲线训练专题

<<固体溶解度曲线>>训练专题【固体溶解度曲线知识点】固体溶解度曲线:就是用纵坐标表示溶解度(用字母S表示,单位为克/g),横坐标表示温度(用字母t表示,单位为℃),根据物质在不同温度时的溶解度不同,画出的物质溶解度随温度变化线。
溶解度曲线的作用可从点、线、面几个方面来理解.具体如下:1.点:溶解度曲线上的每个点(即饱和点)表示的是某温度下某种物质的溶解度,即曲线上的任意一点都对应有相应的温度和溶解度.溶解度曲线上的点有三个作用:(1)根据已知的温度可以查出有关物质的溶解度;(2)根据物质的溶解度也可以查出它所对应的温度;(3)可以判断或比较相同温度下,不同物质溶解度的大小(或饱和溶液中溶质的质量分数的大小)。
交点(两条溶解度曲线的交点)表示该点所示的温度下,两物质的溶解度是相同的,并且此时两种物质饱和溶液的溶质质量分数也相同的.2.线:溶解度曲线表示某物质在不同温度下的溶解度或溶解度随温度的变化情况,曲线的坡度越大,说明溶解度受温度影响越大;反之说明受温度影响较小。
溶解度曲线也有三个应用:(1)根据溶解度曲线,可以看出物质的溶解度随着温度的变化而变化的情况。
一般规律是:大部分固体随温度升高溶解度增大,如硝酸钾;只有少数固体溶解度受温度影响不大,如氯化钠;极少数物质溶解度随温度升高反而减小,如熟石灰.(2)根据溶解度曲线,判断或比较某一物质在不同温度下的溶解度大小。
(3)根据溶解度曲线,选择分离、提纯某些可溶性混合物的方法(即选用“蒸发结晶”还是“降温结晶”);并且还可以判断或比较析出晶体的质量大小(即饱和溶液质量相同时曲线越陡,析出的晶体就越多)。
3.面:曲线下部上的任何点,依其数据配制的溶液为对应温度时的不饱和溶液;曲线上部上的点,依其数据配制的溶液为对应温度时的饱和溶液,并且溶质有剩余。
如果要使不饱和溶液(曲线下部的一点)变成对应温度下的饱和溶液,方法有两种:一是向该溶液中添加适量的溶质使之到达曲线上;二是恒温蒸发掉过量的溶剂。
2016年初三化学溶解度曲线知识点及习题
2016年初三化学复习材料溶解度曲线知识点一、正确理解溶解度曲线的涵义溶解度曲线就是在直角坐标系中,用来描述物质的溶解度随温度变化而变化的曲线。
根据溶解度曲线可进行溶液的配制,混合物的分离与提纯,以及进行物质结晶或溶解的计算。
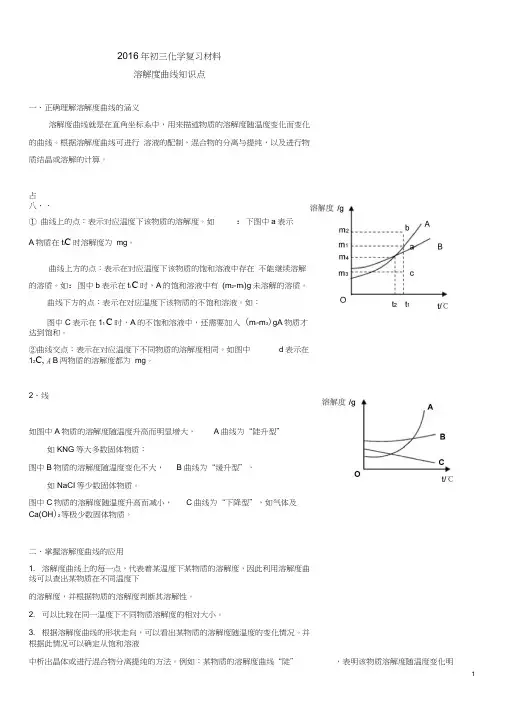
占八、、① 曲线上的点:表示对应温度下该物质的溶解度。
如:下图中a表示A物质在t i C时溶解度为mg。
曲线上方的点:表示在对应温度下该物质的饱和溶液中存在不能继续溶解的溶质。
如:图中b表示在t i C时,A的饱和溶液中有(m2-m i)g未溶解的溶质。
曲线下方的点:表示在对应温度下该物质的不饱和溶液。
如:图中C表示在11 C时,A的不饱和溶液中,还需要加入(m i-m3)gA物质才达到饱和。
②曲线交点:表示在对应温度下不同物质的溶解度相同。
如图中d表示在12C, A B两物质的溶解度都为mg。
2、线如图中A物质的溶解度随温度升高而明显增大,A曲线为“陡升型”如KNG等大多数固体物质:图中B物质的溶解度随温度变化不大,B曲线为“缓升型”,如NaCI等少数固体物质。
图中C物质的溶解度随温度升高而减小,C曲线为“下降型”,如气体及Ca(OH)2等极少数固体物质。
二、掌握溶解度曲线的应用1. 溶解度曲线上的每一点,代表着某温度下某物质的溶解度,因此利用溶解度曲线可以查出某物质在不同温度下的溶解度,并根据物质的溶解度判断其溶解性。
2. 可以比较在同一温度下不同物质溶解度的相对大小。
3. 根据溶解度曲线的形状走向,可以看出某物质的溶解度随温度的变化情况。
并根据此情况可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法。
例如:某物质的溶解度曲线“陡”,表明该物质溶解度随温度变化明显,提纯或分离该物质时适合采用降温结晶法。
某物质溶解度曲线“平缓”,提纯或分离该物质时适合采用蒸发溶剂法。
4. 从溶解度曲线上的交点,可以判断哪些物质在该点所示的温度下具有相同的溶解度。
5. 利用溶解度曲线可以确定一定质量的某物质的饱和溶液降温时析出晶体的质量。
初中化学溶解度曲线知识汇总
一、有关溶解度曲线的题1、溶解度曲线知识(1)、比较不同温度时溶解度的大小。
在t 1℃时,三种物质的溶解度的大小顺序是 。
(2)、图中M 点表示的意义是 。
(3)、温度因素对溶解度的影响A 。
B 。
C 。
(4)、不饱和溶液变饱和溶液的方法A , , 。
B , 。
C , , 。
(5)、饱和溶液变不饱和溶液的方法A , 。
B , 。
C , 。
(6)、A 物质中含有少量B 物质提纯的方法是 。
B 物质中含有少量A 物质提纯的方法是 。
(7)、溶解度曲线上的点表示 ,溶解度曲线以上的点表示 ,溶解度曲线以下的点表示 。
2、规律知识总结(1)溶解度曲线题解答要点:①温度②物质③溶解度 (2)两溶液中溶质质量分数和溶质质量的大小比较 ①同种溶质A 同温→饱和比不饱和的 大B 同温、等量溶液→饱和比不饱和含的 多。
②不同溶质A 同温、饱和→溶解度大的物质 大B 同温、饱和、等量溶液→溶解度大的物质含的 多。
(3)溶解度曲线X 穿越溶解度曲线Y 的条件:①低温t 1℃,S x <S y (比小的小)②高温t 3℃,S x >S y (比大的大) (4)曲线中溶质质量分数大小比较(平移法)①t 3℃甲、乙、丙三种物质饱和溶液降温到t 1℃时,三种物质溶质质量分数的大小顺序是 。
②t 3℃等质量的甲、乙、丙三种物质饱和溶液降温到t 1℃时,三种溶液所含溶质质量的大小顺序是 。
二、河北中考试题1、(2006河北中考)如图是a 、b 、c 三种固体物质的溶解度曲线,下列说法不正确的是( )A.t 2℃时a 的溶解度等于b 的溶解度B. t 1℃时a 、c 饱和溶液的溶质质量分数相同C.c 的饱和溶液由t 1℃升温至t 2℃时,变成不饱和溶液D.当a 中含有少量b 时,可以采用降温的方法提纯a2、(2007河北中考)图1是a 、b 两种物质的溶解度曲线。
室温时,将盛有a 、b 饱和溶液的试管分别放入烧杯内的水中,均无晶体析出。
初中化学溶解度曲线练习精品
溶解度曲线及溶质质量分数计算专项训练 姓名:溶解度曲线知识归纳 一、点的意义1.溶解度曲线上的点表示物质在该点所示温度下的溶解度,溶液所处的状态是饱和溶液。
2.溶解度曲线下面的面积上的点,表示溶液所处的状态是不饱和状态,依其数据配制的溶液为对应温度时的不饱和溶液。
3.两条溶解度曲线的交点,表示在该点所示的温度下,两种物质的溶解度相等。
二、变化规律1.大多数固体物质的溶解度随湿度升高而增大,曲线为"陡升型,如硝酸钾。
2.少数固体物质的溶解度受湿度的影响很小,曲线为"缓升型,如氯化钠。
3.极少数固体物质的溶解度随湿度的升高而减小,曲线为"下降型,如氢氧化钙。
4.气体物质的溶解度均随湿度的升高而减小(纵坐标表示体积),曲线也为"下降型,如氧气。
三、应用1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性。
2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小。
3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法。
4.确定溶液的状态(饱和与不饱和)。
(一)确定某温度下物质的溶解度,比较溶解度的大小关系 1、右图表示M 、N 两种固体物质的溶解度曲线。
下列说法正确的是( )A.20℃时,M 的溶解度大于N 的溶解度B.M 、N 都不是易溶物质C.P 点表示t ℃时M 、N 的溶解度相等D.阴影处M 、N 均为饱和溶液2、右图是KNO 3和NaCl 的溶解度曲线。
下列说法中正确的是( )A. NaCl 的溶解度不受温度的影响B. KNO 3的溶解度大于NaCl 的溶解度C.t 1℃时,100g KNO 3的饱和溶液中含有20克 KNO 3D. t 2℃时,NaCl 的饱和溶液与KNO 3的饱和溶液中溶质的质量分数相等 3、右图是甲、乙两种固体物质的溶解度曲线。
下列说法正确的是( ) A.甲物质的溶解度为60gB.t ℃时,甲、乙两物质的溶解度相等C.升高温度可使不饱和的甲溶液变为饱和D.乙物质的溶解度随温度的升高而增大4、右图是A 、B 、C 三种物质的溶解度曲线。
溶解度曲线专题练习
溶解度曲线专题练习【知识点的认识】所谓固体溶解度曲线如图所示:就是用纵坐标表示溶解度(用字母S表示,单位为克/g),横坐标表示温度(用字母t表示,单位为℃),根据物质在不同温度时的溶解度不同,画出的物质溶解度随温度变化的曲线。
固体溶解度曲线的作用可从点、线、面和交点四方面来理解。
具体如下:1.点,溶解度曲线上的每个点(即饱和点)表示的是某温度下某种物质的溶解度。
即曲线上的任意一点都对应有相应的温度和溶解度。
温度在横坐标上可以找到,溶解度在纵坐标上可以找到。
溶解度曲线上的点有三个方面的作用: (1)根据已知的温度可以查出有关物质的溶解度;(2)根据物质的溶解度也可以查出它所对应的温度;(3)可以判断或比较相同温度下,不同物质溶解度的大小(或饱和溶液中溶质的质量分数的大小)。
2.线,溶解度曲线表示某物质在不同温度下的溶解度或溶解度随温度的变化情况。
曲线的坡度越大,说明溶解度受温度影响越大;反之,说明受温度影响较小。
溶解度曲线也有三个方面的应用: (1)根据溶解度曲线,可以看出物质的溶解度随着温度的变化而变化的情况。
一般规律是:大部分固体随温度升高溶解度增大,如硝酸钾;只有少数固体溶解度受温度影响不大,如食盐(氯化钠);极少数物质溶解度随温度升高反而减小,如熟石灰。
(2)根据溶解度曲线,判断或比较某一物质在不同温度下的溶解度大小。
(3)根据溶解度曲线,选择分离、提纯某些可溶性混合物的方法(即选用蒸发结晶还是降温结晶);并且,还可以判断或比较析出晶体的质量大小(即曲线越陡,析出的晶体就越多)。
3.面,对于曲线下部面积上的任何点,依其数据配制的溶液为对应温度时的不饱和溶液;曲线上部面积上的点,依其数据配制的溶液为对应温度时的饱和溶液,且溶质有剩余。
如果要使不饱和溶液(曲线下部的一点)变成对应温度下的饱和溶液,方法有两种:第一种方法是向该溶液中添加适量的溶质使之到达曲线上;第二种方法是蒸发掉过量的溶剂。
4.交点,两条溶解度曲线的交点表示该点所示的温度下,两物质的溶解度是相同的;并且,此时两种物质饱和溶液的溶质质量分数也相同的。
溶解度曲线图试题题型总结
溶解度曲线图试题题型总结standalone; self-contained; independent; self-governed;autocephalous; indie; absolute; unattached; substantive正确的说法:1、t2℃时,甲、乙两饱和溶液溶质质量分数相等,2、甲、乙饱和溶液变为不饱和溶液,可升温。
而丙的饱和溶液变为不饱和溶液,可降温。
3、t2℃时,甲、乙两种物质各50g分别加入到100g水中,充分溶解得到溶液质量都是140g。
4、t2℃时,质量相同的甲、乙饱和溶液分别升温至t3℃,为达到饱和状态需要加入甲的质量大于乙。
5、当甲中混有少量乙时可用降温结晶的方法提纯。
6、若要将N点的甲溶液转变为M点的甲溶液,可在恒温条件下采用蒸发溶剂法。
7、分别将t3℃时,甲、乙、丙的饱和溶液降温至t1℃,则所得三种溶液中溶质质量分数大小关系:乙>甲>丙。
不正确的说法:1、t3℃时,甲、乙两饱和溶液的溶质质量相等。
2、将乙的溶液由t3℃降低到t2℃,乙溶液中一定有固体析出。
3、t3℃时,将甲、乙的饱和溶液降温到t2℃时,析出晶体的质量一定大于乙。
4、将甲、乙、丙的饱和溶液从t3℃降温到t2℃溶液中均有固体析出。
5、t3℃时,甲、乙、丙三种物质的饱和溶液中溶质质量由大到小的顺序是:甲>乙>丙。
6、t3℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数。
7、t3℃时,将47g甲完全溶于100g水中,得到甲的饱和溶液。
8、t2℃时,甲、乙饱和溶液的溶质质量分数都为40%。
9、t2℃时,甲、乙的饱和溶液分别降温至t0℃,甲溶液饱和,乙溶液不饱和。
10、t3℃时,甲、乙、丙三种物质的饱和溶液,分别蒸发相等质量的水后恢复到t3℃,析出溶质质量:丙>乙>甲。
11、将t2℃时,甲、乙、丙三种物质的饱和溶液降温至t1℃时,所得溶液溶质质量分数关系是:乙>甲=丙。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
溶解度/gt/℃21m m m m 溶解度曲线知识点一、正确理解溶解度曲线的涵义溶解度曲线就是在直角坐标系中,用来描述物质的溶解度随温度变化而变化的曲线。
根据溶解度曲线可进行溶液的配制,混合物的分离与提纯,以及进行物质结晶或溶解的计算。
点① 曲线上的点:表示对应温度下该物质的溶解度。
如:下图中a 表示 A 物质在t 1℃时溶解度为m 1g 。
曲线上方的点:表示在对应温度下该物质的饱和溶液中存在 不能继续溶解的溶质。
如:图中b 表示在t 1℃时,A 的饱和溶液中有 (m 2-m 1)g 未溶解的溶质。
曲线下方的点:表示在对应温度下该物质的不饱和溶液。
如:图中C 表示在t 1℃时,A 的不饱和溶液中,还需要加入(m 1-m 3)gA 物质才达到饱和。
②曲线交点:表示在对应温度下不同物质的溶解度相同。
如图中d 表示在t 2℃,A 、B 两物质的溶解度都为m 4g 。
2、线如图中A 物质的溶解度随温度升高而明显增大,A 曲线为“陡升型”。
如KNO 3等大多数固体物质:图中B 物质的溶解度随温度变化不大,B 曲线为“缓升型”,如NaCl 等少数固体物质。
图中C 物质的溶解度随温度升高而减小,C 曲线为“下降型”,如气体及Ca(OH)2等极少数固体物质。
二、掌握溶解度曲线的应用1. 溶解度曲线上的每一点,代表着某温度下某物质的溶解度,因此利用溶解度曲线可以查出某物质在不同温度下的溶解度,并根据物质的溶解度判断其溶解性。
2. 可以比较在同一温度下不同物质溶解度的相对大小。
3. 根据溶解度曲线的形状走向,可以看出某物质的溶解度随温度的变化情况。
并根据此情况可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法。
例如:某物质的溶解度曲线“陡”,表明该物质溶解度随温度变化明显,提纯或分离该物质时适合采用降温结晶法。
某物质溶解度曲线“平缓”,提纯或分离该物质时适合采用蒸发溶剂法。
4. 从溶解度曲线上的交点,可以判断哪些物质在该点所示的温度下具有相同的溶解度。
5. 利用溶解度曲线可以确定一定质量的某物质的饱和溶液降温时析出晶体的质量。
溶解度曲线专题练习溶解度/g度1. 甲、乙两物质的溶解度曲线如图所示,下列说法正确的是A.甲和乙的饱和溶液,从t1℃升温到t2℃,仍是饱和溶液B.t1℃时,甲和乙的溶解度相等C.t1℃时,甲和乙各30g分别加入80g水中,均能恰好完全溶解D.t2℃时,在100g水中放入60g甲,形成不饱和溶液2.右图是a、b两种固体物质的溶解度曲线。
从图中可获得的信息是A. 固体物质的溶解度均随温度升高而增大B.t℃,相同质量的a、b溶解时放出热量相同C.升高温度,可使a或b的饱和溶液变为不饱和溶液D.将相同质量的a、b分别加入100g水中,所得溶液质量分数相同3.右图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是A.甲的溶解度大于乙的溶解度B.乙的不饱和溶液降温可变成饱和溶液C.20o C时,甲、乙两种物质的溶解度相等D.50o C时,甲的饱和溶液中溶质的质量分数为40%4. 右图是a、b两种固体物质(不含结晶水)的溶解度曲线。
下列说法正确的是A.b的溶解度大于a的溶解度B.t1℃时,将a、b两种物质的饱和溶液分别恒温蒸发等质量的水,析出晶体的质量一定相等C.将t2℃时的b的不饱和溶液降温至t1℃,一定能得到b的饱和溶液D.t2℃时,a溶液的溶质质量分数一定小于b溶液的溶质质量分数5.右图是a、b两种固体物质的溶解度曲线,下列说法中正确的是A.a的溶解度大于b的溶解度B.在20℃时,a、b的溶液中溶质的质量分数相同C.a、b的溶解度都随温度升高而增大D.a、b都属于易溶物质6.t2℃时往盛有100g水的烧杯中先后加入a g M和a g N(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌。
将混合物的温度降低到t1℃,下列说法正确的是A.t2℃时,得到M的饱和溶液B.t2℃时,得到N的不饱和溶液C.温度降低到t 1℃时,M 、N 的溶质质量分数相等,得到M 、N 的不饱和溶液D.温度降低到t 1℃时,M 、N 的溶解度相等,得到M 、N 的饱和溶液7.右图是a 、b 、c 三种固体物质的溶解度曲线,下列叙述正确的是 A .将a 、b 、c 三种物质t 1℃时的饱和溶液升温至t 2℃, 所得溶液的溶质质量分数大小关系是a>b>cB .t 2℃时30g 物质a 加入到50g 水中不断搅拌,形成80g 溶液C .t 1℃时a 、b 、c 三种物质的饱和溶液中含有溶质质量按由小到大的顺序排列是b>a=cD. 若a 中混有少量c ,可以采用冷却热饱和溶液的方法提纯a8.两种不含结晶水的固体物质a 、b 的溶解度曲线如右图,下列说法正确的是 A .b 的溶解度小于a 的溶解度B .分别将t 2℃时a 、b 两种物质的溶液降温至t 1℃,肯定都有晶体析出C .要从含有少量a 的b 溶液中得到较多的b 晶体,通常可采用降温结 晶的方法D .在t 2℃时,用a 、b 两种固体和水分别配制等质量的两种物质的饱和 溶液,需要量取相同体积的水9.右图所示曲线a 、b 、c 分别代表A 、B 、C 三种物质的溶解度曲线。
下列说法正确的是A .t 1 ℃时,三种物质溶解度大小的顺序是B >C >A B .t 2℃时,A 和B 两种物质的饱和溶液中溶质质量相同C .t 3℃时,在100g 水里分别加入三种物质各mg ,只有b 能形成饱和溶液D .从混有少量C 的A 物质中提取较纯净的A ,最适宜用蒸发溶剂的方法10.右图是a 、b 、c 三种固体的溶解度曲线,下列说法正确的是 A .b 的溶解度一定小于a 的溶解度B .当a 中含有少量b 时,可以用降温结晶的方法提纯aC .通过降低温度可将c 的不饱和溶液变为饱和溶液D .a 的饱和溶液从t 2℃降温至t 1℃时变为不饱和溶液11.有关a 、b 两种物质的溶解度曲线如图所示,下列叙述不正确的是 A .a 物质的溶解度随着温度的升高而增大B .在t 2℃时,a 、b 两种物质的溶液中溶质的质量分数一定相等C .将a 、b 两种物质的饱和溶液从t 3℃降温至t 1℃,a 有晶体析出,b 无晶体析出D .t 3℃时,a 物质的溶解度大于b 物质的溶解度12.a 、b 、c 三种物质的溶解度曲线如右图所示。
现有t 1℃时的a 、b 、c 三种物质的饱和溶液,将其都升温至t 2℃时,下列说法中,正确的是 A .b 溶液为饱和溶液温度/℃12溶解度g甲乙溶解度 g0 t 1 t 2 温度/℃30 50 20 4010B .a 溶液中有晶体析出C .c 溶液为不饱和溶液D .b 溶液中的溶质质量分数最大13.右图所示为甲、乙两物质(均不含结晶水)的溶解度曲线。
50℃时,取甲、乙两种物质各50g ,分别加人100g 水中,使之充分溶解。
下列有关说法不正确的是………( )A .上述混合物在20℃时,甲和乙形成溶液的质量相等B .在0℃时,溶液中溶质的质量分数甲小于乙C .温度高于50℃时,甲和乙形成的溶液都变为不饱和溶液D .50℃时,将甲、乙两种物质的混合物分别降温至20℃,溶液中未溶解晶体的质量相等14、右图是a 、b 两种固体物质的溶解度曲线图,下列说法中不正确的是A .任何温度下,a 的溶解度大于b 的溶解度B .a 的溶解度受温度变化的影响比b 的大C .t 1 ℃至t 2 ℃之间b 曲线以下区域为a 、b 两物质的不饱和溶液D .对于a 与b 混合溶液,可利用冷却结晶的方法来分离15.甲、乙两物质的溶解度曲线如右图所示。
下列叙述中,正确的是 A .t 1℃时,甲和乙的溶解度均为30B .t 2℃时,甲和乙的饱和溶液中溶质质量分数相等C .t 2℃时,在100 g 水中放入60 g 甲,其溶质的质量分数为37.5%D .t 2℃时, 分别在100 g 水中各溶解20 g 甲、乙,同时降低温度,甲先达到饱和16.根据右图A 、B 、C 三种物质的溶解度曲线,判断下列说法是否正确 A. 温度从t 2℃降到t 1℃时三种物质析出晶体由多到少的顺序为 A>B>C B.t 2℃时A 溶液溶质的质量分数最大,C 溶液溶质的质量分数最小 C.A 物质中混有C 物质,可以用蒸发溶剂的方法提纯A D.t 1℃时,A 、B 、C 三种物质的饱和溶液溶质的质量分数相等17、几种物质的溶解度曲线如右图。
则下列说法正确的是 A .氯化铵的溶解度最大B .随着温度升高,硫酸钠的溶解度不断增大C .40℃时硫酸钠饱和溶液溶质的质量分数为50%D .把40℃时等质量的三种物质的饱和溶液降温到20℃, 硫酸钠析出晶体最多18.右图表示A 、B 两种物质的溶解度(s)随温度(t)的变化情况,下列说法正确的是A .A 的溶解度大于B 的溶解度温度/ C溶解度/gB .升高温度可使A 的不饱和溶液变为饱和C .t 3℃时,在100g 水中溶解60gA 能形成饱和溶液D .t 2℃时,A 和B 的饱和溶液的溶质质量分数相等19、右图中M 、N 分别表示二种固体物质(不含结晶水)的溶解度曲线,试根据图中曲线判断下列说法正确的是A .图中A 点表示M 、N 二种物质在t 1℃时均达到饱和B .M 、N 二种饱和溶液,当温度从t 1降至t 2时,一定析出相同质量的晶体C .同处A 点的相同质量的M 、N 二种溶液,当温度从t 1降至t 2后,剩余溶液 的质量分数相等D .0℃时,M 、N 具有相同的溶解度20、右图是a 、b 、c 三种固体物质的溶解度曲线。
由图示判断下列说法中正确的是 A .b 物质的溶解度大于c 物质的溶解度 B .a 物质的溶解度大于c 物质的溶解度C .a 物质的饱和溶液从t 2℃降温至t 1℃时变为不饱和溶液D .c 物质的不饱和溶液从t 2℃降温至t 1℃时变为饱和溶液21.右图是A 、B 两种固体物质的溶解度曲线。
下列说法中错误的是A .A 物质的溶解度受温度变化的影响较大,B 物质的溶解度受温度变化的影响较小 B .t ℃时,等质量的A 、B 饱和溶液中含有相同质量的溶质C .当温度大于t ℃时,A 溶液一定比B 溶液浓D .B 中含有少量A 时,用溶解、蒸发、结晶的方法除去B 中的A22.右图是A 、B 、C 三种物质的溶解度曲线,据图回答:(1) t 1℃时A 、B 、C 三种物质的溶解度由大到小的顺序是 (填写序号,下同)。
(2) t 1℃时30gA 物质加入到50g 水中不断搅拌,形成的溶液质 量是 g 。
(3) 将t 1℃时A 、B 、C 三种物质饱和溶液的温度升高到t 2℃时, 三种溶液的溶质质量分数由大小关系是(3)右图是a 、b 两种物质的溶解度曲线。
