第四章纳米微粒的化学特性详解演示文稿
合集下载
纳米微粒的基础理论课件

的方法。
沉淀法是通过化学反应使溶液中的离子形成沉淀,再 经过洗涤、干燥得到纳米微粒的方法。
化学法是通过化学反应制备纳米微粒的方法, 主要包括化学气相沉积法、溶胶-凝胶法、沉淀 法等。
溶胶-凝胶法是利用溶胶中的胶体粒子相互聚结 形成凝胶,再通过干燥和热处理得到纳米微粒的 方法。
生物法
1
生物法是利用生物体系中的酶、微生物等生物分 子进行催化或合成纳米微粒的方法,主要包括生 物合成法和生物提取法。
根据应用需求选择合适的制备方法, 如根据所需纳米微粒的尺寸、形貌、 化学成分等特性选择合适的制备方法 。
03
纳米微粒的性质与应用
纳米微粒的物理性质
小尺寸效应
由于纳米微粒的尺寸在纳米级别,其电子能级发 生分裂,导致新的光学、电学和磁学等性质。
表面效应
纳米微粒的巨大表面积与体积比使其表面原子活 性增加,影响其化学反应活性。
量子效应
在纳米尺度上,电子的运动受到限制,表现出显 著的量子效应,影响材料的导电性和磁性。
纳米微粒的化学性质
01
02
03
高反应活性
纳米微粒具有高表面能, 使其在化学反应中表现出 高反应活性。
催化性能
纳米微粒可作为高效的催 化剂,应用于许多化学反 应中。
稳定性与相容性
通过表面修饰,纳米微粒 可以改善其在不同介质中 的稳定性和相容性。
研究和评估。
跨学科合作
纳米微粒的研究和应用涉及多 个学科领域,需要加强跨学科 的合作和交流,促进创新发展 。
技术瓶颈
目前纳米微粒的制备、表征和 应用技术还存在一些瓶颈,需 要加强技术研发和创新。
法规和伦理问题
随着纳米微粒的广泛应用,相 关的法规和伦理问题也逐渐凸 显,需要建立相应的规范和标
沉淀法是通过化学反应使溶液中的离子形成沉淀,再 经过洗涤、干燥得到纳米微粒的方法。
化学法是通过化学反应制备纳米微粒的方法, 主要包括化学气相沉积法、溶胶-凝胶法、沉淀 法等。
溶胶-凝胶法是利用溶胶中的胶体粒子相互聚结 形成凝胶,再通过干燥和热处理得到纳米微粒的 方法。
生物法
1
生物法是利用生物体系中的酶、微生物等生物分 子进行催化或合成纳米微粒的方法,主要包括生 物合成法和生物提取法。
根据应用需求选择合适的制备方法, 如根据所需纳米微粒的尺寸、形貌、 化学成分等特性选择合适的制备方法 。
03
纳米微粒的性质与应用
纳米微粒的物理性质
小尺寸效应
由于纳米微粒的尺寸在纳米级别,其电子能级发 生分裂,导致新的光学、电学和磁学等性质。
表面效应
纳米微粒的巨大表面积与体积比使其表面原子活 性增加,影响其化学反应活性。
量子效应
在纳米尺度上,电子的运动受到限制,表现出显 著的量子效应,影响材料的导电性和磁性。
纳米微粒的化学性质
01
02
03
高反应活性
纳米微粒具有高表面能, 使其在化学反应中表现出 高反应活性。
催化性能
纳米微粒可作为高效的催 化剂,应用于许多化学反 应中。
稳定性与相容性
通过表面修饰,纳米微粒 可以改善其在不同介质中 的稳定性和相容性。
研究和评估。
跨学科合作
纳米微粒的研究和应用涉及多 个学科领域,需要加强跨学科 的合作和交流,促进创新发展 。
技术瓶颈
目前纳米微粒的制备、表征和 应用技术还存在一些瓶颈,需 要加强技术研发和创新。
法规和伦理问题
随着纳米微粒的广泛应用,相 关的法规和伦理问题也逐渐凸 显,需要建立相应的规范和标
纳米粒子的特性ppt课件
(i)纳米金属和合金与常规材料金属与合金电
导(电阻)行为是否相同?
(ii)纳米材料电导(电阻)与温度的关系有什
么差别?
(iii)电子在纳米结构体系中的运动和散射有什
么新的特点?
精选ppt
27
纳米金属与合金的电阻
Gleiter等对纳米金属Cu,Pd,Fe块体的电 阻与温度关系,电阻温度系数与颗粒尺寸的关 系进行了系统的研究表明:随颗粒尺寸减小, 电阻温度系数下降,与常规粗晶基本相似.其 差别在于纳米材料的电阻高于常规材料,电阻 温度系数强烈依赖于晶粒尺寸.当颗粒小于某 一临界尺寸(电子平均自由程)时,电阻温度 系数可能由正变负。
第四节 纳米粒子的特性.
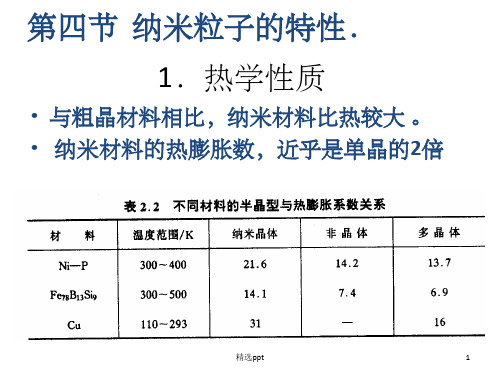
1.热学性质
• 与粗晶材料相比,纳米材料比热较大 。 • 纳米材料的热膨胀数,近乎是单晶的2倍
精选ppt
1
• 纳米微粒的熔点、开始烧结温度和晶化温 度均比常规粉体低得多。
• 例如,平均粒径为40nm的纳米铜粒子的熔 点由l 053℃降到750℃,降低了300℃左右;
• 块状的金的熔点l 064℃,当颗粒尺度减到 10nm时,则降低为1037℃,降低了27℃, 2nm时变为327℃;
•
1988年法国科学家Fert小组在[Fe/Cr]周期性多层
膜中,观察 到当施加外磁场时,其电阻下降,变化
率高达50%。因此称之为巨磁电阻效应
(giant magnetoresistance, GMR)。
❖ 1995年,人们以绝缘层Al2O3代替导体Cr,观察 到很大的隧道磁电阻(TMR)现象。 基于GMR和TMR的发现,一个新的学科分支— —磁电子学的概念被提出了。 从那时起,科技人员 一直坚持不懈地努力,将上述创新性发现转化为信息 技术(IT)产业化。
3.纳米微粒的基本理论与特性2011

限定了磁带、磁盘进行信息存储的时间极 限 确立了现在微电子器件进一步微型化的极 限 例如,在制造半导体集成电路时,当电路 的尺寸接近电子波长时,电子就通过隧道 效应而溢出器件,使器件无法正常工作, 经典电路的极限尺寸大概在0.25微米。目前 研制的量子共振隧穿晶体管就是利用量子 效应制成的新一代器件。(摩尔定律:集 成电路上晶体管的数量每隔18个月增加一 倍。)
纳米晶体结构:当超微粒子的尺寸与光波波 长、德布罗依波波长以及超导态的相干波长 或透射深度等物理特征尺寸相当时,晶体周 期性的条件被迫坏,点阵结构的周期性消失, 不再是原来意义的晶体。以金属为例,不但 能带变为离散能级,引起导电性能下降等物 理性质的变化,而且表面原子数显著增加, 表面原子是化学键不饱和原子,这类原子多 了会使粒子的化学活性(如催化性能)和表面能 显著增加。表面原子密度也显著减小,缺陷 显著增加。缺陷是指实际晶体结构中和理想 点阵结构发生偏差的区域。缺陷的存在使纳 米材料结构中的平移周期遭到很大破坏,严 重偏离了理想晶体的结构。
一般来说,过渡族金属氧化物和半导体微 粒都可能产生介电限域效应。纳米微粒的 介电限域效应对光吸收、光化学、光学非 线性等会有重要的影响。因此,在分析材 料光学现象的时候,既要考虑量子尺寸效 应又要考虑介电限域效应。
界面相关效应
由于纳米结构材料中有大量的界面,与单晶材料相比, 纳米结构材料具有反常高的扩散率,它对蠕变、超塑 性等力学性能有显著影响;可以在较低的温度对材料 进行有效的掺杂,并可使不混溶金属形成新的合金相; 出现超强度、超硬度、超塑性等
如果量子点的尺寸为1nm左右,我们可以在 室温下观察到上述效应.当量子点尺寸在 十几纳米范围,观察上述效应必须在液氮 温度下.原因很容易理解,体系的尺寸越 小,电容C越小,e2/C越大,这就允许我们 在较高温度下进行观察.由于库仑堵塞效 应的存在,电流随电压的上升不再是直线 介电限域效应
纳米粒子PowerPoint 幻灯片 (2)

液晶显示材料
纳米材料的应用——储氢材料
• 氢能是人类未来最理想的能源, 其热值高,资源丰富,无毒无污 染,并可再生。氢-氧燃料电池 可做汽车发动机的动力,达到零 排放。纳米材料可以作为储氢材 料,反复循环使用。研究表明许 多合金可作为储氢材料,如 LaNi5,FeTi的纳米颗粒可作为储 氢材料,若包覆V,Pd后,其储 氢性能将更大提高。
纳米复合膜陶瓷过滤机图
纳米材料的应用——光学材料
液晶显示材料
• 从光学角度来说,石墨烯是一种 “透明”的导体,可以用来替代现在 的液晶显示材料。目前的液晶显示器 利用的是以铟为基础的金属氧化物薄 膜,而铟这种金属十分稀有,预计在 未来十年内就可能出现供应短缺。另 外,与目前电脑、手机等电子产品的 重要原材料硅相比,石墨烯也具有诸 多优势,因此它将来有望取代硅,在 电子产品生产中得到广泛应用。
•
1959年,美国著名理论物理学R.Feynma曾说过: “我深信,当人们能操纵细微物体排列时,将可获得 极其丰富的新的物质的质”。如今,这一梦想终于能 在纳米材料得以实现。人们对纳米粒子的物理化学性 质的研究逐步深入,到了20世纪90年代,人工制备 的纳米材料已达百种以上。1990年7月在美国巴尔的 摩召开的第一届NST会议,标志着这一全新的技术— —纳米科技正式诞生。
氧化锌纳米粒子
纳米材料制备方法分类 纳米材料的类别
纳米粉体
化学法
沉淀法(共沉淀、均相 沉淀) 化学气相凝聚 (CVC ),水热法 相转移 法 溶胶-凝胶法 溶胶--凝胶法 电沉淀பைடு நூலகம் 还原法 非晶晶化法 原位聚合法 抽层法 乳液法 超微乳法 悬浮法 高分子包覆法 乳液法
物理法
综合法
惰性气体沉淀法 蒸发法 激光 辐射化学合成法 溅射法 真空蒸镀法 球磨法 爆炸法 喷雾法 溶剂挥发法 惰性气体蒸发法 高速粒子沉 淀法 激光溅射法 超声沉淀法
纳米微粒的基本性质

一、 电子能级的不连续性
Kubo理论
1 .简介: Kubo 理论是关于金属粒子电子性质 的理论。 提出:该理论最初 (1962 年 ) 由 Kubo 及其合 作者提出,后经他们发展。 发展:1986年,Halperin对这一理论又进行 了比较全面的归纳,并对金属超微颗粒的量子 尺寸效应进行了深入的分析。
波数K只能取分立值→动量空间中,电子的状态 只能取一系列分立的点→ N个电子将按能量 的大小依次从K小的状态向K大的状态逐一填 充(如此分布的状态,其整体能量最低,称为 体系的基态。) → N个电子填完后最大动量 是PF,其对应的最大波数为KF; 费米动量: N个电子填完后最大动量PF; 费米能EF:根据PF可以求出电子的最大能量 对二维体系和三维体系作类似的处理也可以得 到类似的结果。
设一维体系的长度为L,其中有N个可以自由运 动的电子,当电子运动时,设其动量为P,波 数K与P之间的关系:用K=P/h表示 电子波函数:也可以转化为用波数表达的形式。 当电子在长度为L的直链中运动时:其波函数要 满足周期性的边界条件,即要求在链的两端波 函数要相等。根据这一条件得到波数K只能取 分立值。 K空间:固体物理中常用K作为坐标轴来表示电 子的运动状态,以K为坐标轴的空间称为K空 间,也可称为动量空间,对于一维空间,动量 空间也是一维的。
3、意义 宏观量子隧道效应的研究对基础研究及实用都有着 重要意义。 它限定了磁带、磁盘进行信息贮存的时间极限。量 子尺寸效应、隧道效应将会是未来微电子器件的基 础,或者它确立了现存微电子器件进一步微型化的 极限。当微电子器件进一步细微化时,必须要考虑 上述的量子效应。 总结: 上述的小尺寸效应、表面界面效应、量子尺寸效应 及宏观量子隧道效应是纳米微粒与纳米固体的基本 特性。它使纳米微粒和纳米固体呈现许多奇异的物 理、化学性质,出现一些“反常现象”。
纳米粒子的分散性及分散稳定性课件

生物法
利用微生物或植物提取物 等生物资源制备纳米材料 ,具有环保、低成本等优 点。
纳米粒子的应用领域
能源领域
用于太阳能电池、燃料 电池、锂电池等,提高 能源利用效率和性能。
医学领域
用于药物输送、肿瘤诊 断与治疗、生物成像等 ,改善医疗效果和降低
副作用。
环境领域
用于水处理、空气净化 、土壤修复等,提高环
在塑料工业中的应用
总结词
改善塑料性能
详细描述
在塑料工业中,纳米粒子的分散性和分散稳定性对于改善塑料的性能至关重要。纳米粒子可以增强塑料的力学性 能,如强度、韧性和耐磨性,同时还可以提高塑料的阻隔性能和热稳定性。这使得塑料在汽车、航空航天、电子 和医疗器械等领域的应用更加广泛。
在医药领域的应用
总结词
实验原理
分散性是指纳米粒子在溶液中均匀分散的能力,而分散稳定性则是指纳米粒子 在长时间放置或受到外界干扰时保持分散状态的能力。实验原理涉及流体力学 、表面化学和胶体科学等领域的知识。
实验材料与实验步骤
实验材料:需要准备纳米粒子、分散 剂、溶剂、搅拌器、离心机等。
实验步骤
1. 将纳米粒子与适量的分散剂混合, 加入溶剂中,搅拌均匀。
纳米粒子分散稳定性的定义与评价标准
定义
纳米粒子分散稳定性是指纳米粒子在 分散介质中保持均匀分散的能力,即 在长时间内不发生聚集、沉淀或浮选 等现象。
评价标准
通常通过测量分散体系在不同时间点 的粒度分布、电位差、沉降速度、分 散指数等参数来评估纳米粒子的分散 稳定性。
影响纳米粒子分散稳定性的因素
粒子表面性质
特性
纳米粒子具有高比表面积、小尺 寸效应、量子效应和表面效应等 特点,使其在催化、能源、医学 等领域具有广泛的应用前景。
纳米材料的结构和性质ppt课件

可编辑课件
16
可编辑课件
此外,纳米磁 性微粒还具备 许多其他的磁 特性.纳米金 属Fe(8nm)饱和 磁化强度比常 规α-Fe低40%, 纳米Fe的比饱 和磁化强度随 粒径的减小而 下降(见图);
17
2.3光学性能
纳米粒子的一个最重要的标志是尺寸与物理的 特征量相差不多,例如,当纳米粒子的粒径与 超导相干波长、玻尔半径以及电子的德布罗意 波长相当时,小颗粒的量子尺寸效应十分显 著.与此同时,大的比表面使处于表面态的原 子,电子与处于小颗粒内部的原子、电子的行 为有很大的差别,这种表面效应和量子尺寸效 应对纳米微粒的光学特性有很大的影响.甚至 使纳米微粒具有同样材质的宏观大块物体不具 备的新的光学特性.主要表现为如下几方面:
可编辑课件
36
例如可以将酯类氧化变成醇,醇再氧化 变成醛,醛再氧化变成酸,酸进一步氧 化变成CO2和水.半导体的光催化活性主 要取决导带与价带的氧化-还原电位,价 带的氧化—还原电位越正,导带的氧 化—还原电位越负,则光生电子和空穴 的氧化及还原能力就越强,从而使光催 化降解有机物的效率大大提高.
硅作载体的镍纳米微粒作催化剂时,当粒径小
于5nm时,不仅表面活性好,使催化效应明显,
而且对丙醛的氢化反应中反应选择性急剧上升,
即使丙醛到正丙醇氢化反应优先进行,而使脱
碳引起的副反应受到抑制.
可编辑课件
33
由于纳米微粒具有大的比表面积,高的 表面活性,及表面活性能与气氛性气体 相互作用强等原因,纳米微粒对周围环 境十分敏感.如光、温、气氛、湿度等, 因此可用作各种传感器,如温度、气体、 光、湿度等传感器。
可编辑课件
25
这是因为光吸收带的位置是由影响峰位的蓝移 因素和红移因素共同作用的结果,如果前者的 影响大于后者,吸收带蓝移,反之,红移.随 着粒径的减小,量子尺寸效应会导致吸收带的 蓝移,但是粒径减小的同时,颗粒内部的内应 力会增加,这种压应力的增加会导致能带结构 的变化,电子波函数重叠加大,结果带隙、能 级间距变窄,这就导致电子由低能级向高能级 及半导体电子由价带到导带跃迁引起的光吸收 带和吸收带发生红移.纳米NiO中出现的光吸 收带的红移是由于粒径减小时红移因素大于蓝 移因素所致.
纳米颗粒(课堂PPT)

11
二、 纳米粒的载体材料
生物降解材料:有天然与合成高分子材料两类。
天然大分子物质如蛋白质、明胶、桃胶、甲壳 素等,由于许多药物易与蛋白质亲和,所以载 药容易。 主要缺点是制备工艺复杂,有时用于人体具有 抗原反应。
12
二、 纳米粒的载体材料
生物降解材料:有天然与合成高分子材料两类。
合成高分子材料主要有氰基丙烯酸酯、聚乳酸、 聚乳酸-聚乙二醇嵌段共聚物、聚羟基乙酸等。 这类载体材料制备工艺简单,由于所得纳米粒 为多孔性的,故载药量高,同时,毒性较非生 物降解材料低得多。
23
聚甲基烯酸甲酯(PMMA)为高分子生物材料, 在20世纪30年代开始就已用作假牙、晶状体、骨 水泥等人体植入材料。
PMMA纳米球悬浮液 注射入人体组织的PMMA2纳4 米球
2、天然高分子凝聚法
白蛋白 微球
天然高分子材料可由化学交联、 加热变性
或盐析脱水法凝聚成纳米囊或纳米球。
单凝聚法
制备明胶
19
条件
2 %的单体制得纳米粒的粒径最小,较 低或较高浓度制得的粒径都较大; 搅拌速率增大可导致粒径变大 600 r/ min 及3000 r/ min 分别得 126nm 及161 nm 的平均粒径,粒径增 大的同时粒径分布也变宽;
20
条件
温度高过20 ℃,粒径变大且粒径分布变宽; 无乳化剂制得的纳米球在贮放时易粘连; 碱性药物可起引发剂的作用,且药物也结合 进入聚合物链中,通常在聚合后再加入药物。
(1)聚氰基丙烯酸烷基酯纳米球(囊)
聚合引发剂:水中OH-离子。 通常制得的聚合物平均分子量较低,纳米球软 且易粘连,需应用稳定剂,如右旋糖酐。 影响粒径的重要因素:溶液的pH值和单体的 浓度。 本法制得的纳米囊或纳米球中药物的收率在 15%~90%范围内,亲脂性药物收率较高。
二、 纳米粒的载体材料
生物降解材料:有天然与合成高分子材料两类。
天然大分子物质如蛋白质、明胶、桃胶、甲壳 素等,由于许多药物易与蛋白质亲和,所以载 药容易。 主要缺点是制备工艺复杂,有时用于人体具有 抗原反应。
12
二、 纳米粒的载体材料
生物降解材料:有天然与合成高分子材料两类。
合成高分子材料主要有氰基丙烯酸酯、聚乳酸、 聚乳酸-聚乙二醇嵌段共聚物、聚羟基乙酸等。 这类载体材料制备工艺简单,由于所得纳米粒 为多孔性的,故载药量高,同时,毒性较非生 物降解材料低得多。
23
聚甲基烯酸甲酯(PMMA)为高分子生物材料, 在20世纪30年代开始就已用作假牙、晶状体、骨 水泥等人体植入材料。
PMMA纳米球悬浮液 注射入人体组织的PMMA2纳4 米球
2、天然高分子凝聚法
白蛋白 微球
天然高分子材料可由化学交联、 加热变性
或盐析脱水法凝聚成纳米囊或纳米球。
单凝聚法
制备明胶
19
条件
2 %的单体制得纳米粒的粒径最小,较 低或较高浓度制得的粒径都较大; 搅拌速率增大可导致粒径变大 600 r/ min 及3000 r/ min 分别得 126nm 及161 nm 的平均粒径,粒径增 大的同时粒径分布也变宽;
20
条件
温度高过20 ℃,粒径变大且粒径分布变宽; 无乳化剂制得的纳米球在贮放时易粘连; 碱性药物可起引发剂的作用,且药物也结合 进入聚合物链中,通常在聚合后再加入药物。
(1)聚氰基丙烯酸烷基酯纳米球(囊)
聚合引发剂:水中OH-离子。 通常制得的聚合物平均分子量较低,纳米球软 且易粘连,需应用稳定剂,如右旋糖酐。 影响粒径的重要因素:溶液的pH值和单体的 浓度。 本法制得的纳米囊或纳米球中药物的收率在 15%~90%范围内,亲脂性药物收率较高。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第四章纳米微粒的化学特性详解演示文稿
优选第四章纳米微粒的化学特性
§4.1吸附
吸附的概念
吸附是相接触的不同相之间产生的结合现象
吸附的分类
物理吸附 吸附剂与吸附相之间是以范德瓦
耳斯力之类较弱的物理力结合
化学吸附 吸附剂与吸附相之间是以化学键强
结合
§4.1吸附
纳米微粒吸附性特点
1、纳米微粒由于有大的比表面和表面原子配 位不足,与相同材质的大块材料相比较,有较强 的吸附性。
§4.2纳米微粒的分散和团聚
4.2.1分散
1分散机理:
A现象 尺寸较大的粒子容易沉淀下来,当粒径在 纳米级(1—100nm),由于布朗运动等因素阻止它 们沉淀而形成一种悬浮液,纳米微粒称为胶体。 由于小微粒之间库仑力或范德瓦耳斯力团聚现象 仍可能发生。
B方法 通常用超声波将分散剂(水或有机试剂)中 的团聚体打碎。
图4.1 在低pH下吸附于氧化硅表面的醇、酰胺、醚分子。
§4.1吸附
4.1.1非电解质的吸附
三、影响吸附的因素
受粒子表面性质的影响
由上述例子可知
受吸附相的性质影响
说明 :即使吸附相是相同的,但由于溶剂种类不 同吸附量也不一样。例如,以直链脂肪酸为吸附 相,以苯及正己烷溶液为溶剂,结果以正己烷为 溶剂时直链脂肪酸在氧化硅微粒表面上的吸附量 比以苯为溶剂时多,这是因为在苯的情况下形成 的氢键很少。从水溶液中吸附非电解质时,受pH 值影响很大,pH值高时,氧化硅表面带负电,水 的存在使得氢键难以形成,吸附能力下降。
二、吸附的典型例子
例如:氧化硅粒子对醇、酰胺、醚的吸 附过程中氧化硅微粒与有机试剂中间的接触 为硅烷醇层,硅烷醇在吸附中起着重要作用。
§4.1吸附
4.1.1非电解质的吸附
作用机制:上述有机试剂中的O或N与硅烷醇的羟基 (OH基)中的H形成O—H或N—H氢键,从而完成SiO2微 粒对有机试剂的吸附,如图4.1所示。
例子 如,纳米氧化物SiO2,Al2O3和TiO2等在 水中的pH高低不同(带正电或负电),因此可选 Na+,NH4+或Cl-,NO3-异电离子作反絮凝剂,使 微粒表面形成双电层,从而达到分散的目的。
§4.2纳米微粒的分散和团聚
4.2.1分散
B、加表(界)面活性剂包裹微粒 为了防止分散的纳米粒 子团聚也可加入表面活性剂,使其吸附在粒子表面, 形成微胞状态,由于活性剂的存在而产生了粒子间的 排斥力,使得粒子间不能接触,从而防止团聚体的产 生。对于磁性纳米微粒,由于颗粒之间磁吸引力,很 容易团聚,加入界面活性剂(如油酸)使其包裹在磁 性粒子表面,造成粒子间排斥作用,避免了团聚体的 生成。
§4.1吸附
4.1.2电解质吸附
一、吸附的机理:电解质在溶液中以离子形 式存在,其吸附能力大小由库仑力来决定。 纳米微粒在电解质溶液中的吸附现象大多数 属于物理吸附。 1缘由:由于纳米粒子的大的比表面常常产生键的
不饱和性,致使纳米粒子表面失去电中性而带电 (例如纳米氧化物,氮化物粒子),而电解质溶液中 往往把带有相反电荷的离子吸引到表面上以平衡其 表面上的电荷,这种吸附主要是通过库仑交互作用 而实现的。
pH值处于中间值,则纳米氧化物表 面形成M—OH键,粒子呈电中性。
§4.2纳米微粒的分散和团聚
4.2.1分散
一、面临的问题
在纳米微粒制备过程中,纳米微粒表 面的活性使它们很容易团聚在一起从而形 成带有若干弱连接界面的尺寸较大的团聚 体,这给纳米微粒的收集带来很大的困难。
二、解决的方案
用物理方法或化学方法制备的纳米粒 子经常采用分散在溶液中进行收集。
§4.1吸附
4.1.2电解质吸附
2实例列举:例如,纳米尺寸的黏土小颗粒在碱
或碱土类金属的电解液中的吸附(这是一种物理 吸附过程,它是有层次的)。吸附层的电学性质 也有很大的差别.
二、吸附层的电学性质
1靠近纳米微粒表面的一层属于强物理吸 附,称为紧密层,它的作用是平衡了超微 粒子表面的电性。 2离超微粒子稍远的离子形成较弱吸附层, 称为 分散层。
§4.1吸附
4.1.2电解质Байду номын сангаас附
三、纳米氧化物随pH值可带不同的电荷
纳米氧化物的粒子,如石英、氧化铝 和二氧化钛等根据它们在水溶液中的pH值 不同可带正电、负电或呈电中性。
图4.2 pH值对氧化物带电 状况的影响
pH比较小时,粒子表面形成M—O H2(M代表金属离子,如Si,Al,Ti 等),导致粒子表面带正电。 pH高时,粒子表面形成M—O键, 使粒子表面带负电。
2、纳米粒子的吸附性与被吸附物质的性质、 溶剂的性质以及溶液的性质有关。
3、电解质和非电解质溶液以及溶液的pH值等 都对纳米微粒的吸附产生强烈的影响。
4、不同种类的纳米微粒吸附性质有很大差别。
§4.1吸附
4.1.1非电解质的吸附
一、概念
非电解质是指电中性的分子,它们可通 过氢键、范德瓦耳斯力、偶极子的弱静电引 力吸附在粒子表面。其中主要是以氢键形成 而吸附在其它相上。
C原理 其原理是由于超声频振荡破坏了团聚体中 小微粒之间的库仑力或范德瓦耳斯力,从而使小 颗粒分散于分散剂中。
§4.2纳米微粒的分散和团聚
4.2.1分散
2防止小颗粒团聚采用的方法:
A、加入反絮凝剂形成双电层 反絮凝剂的选择可 依纳米微粒的性质、带电类型等来定。即:选择 适当的电解质作分散剂,使纳米粒子表面吸引异 电离子形成双电层,通过双电层之间库仑排斥作 用使粒子之间发生团聚的引力大大降低,实现纳 米微粒分散的目的。
§4.1吸附
4.1.2电解质吸附
上述两层构成双电层。 双电层中电位分布可用 一表示式来表明,例如把Cu离子—黏土粒子之间 吸附当作强电解质吸附来计算,以粒子表面为原 点,在溶液中任意距离x的电位可用下式表示:
Z为原子价,NA为阿伏伽德罗常数, C为强电解质的摩尔浓 度 ,k 表示双电层的扩展程度.1/ k称为双电层的厚度.由式 看出, 1/ k反比于Z和C1/2,这表明高价离子、高电解质浓度下, 双电层很薄。
例子 如, PaPell在制备Fe3O4的磁性液体时就采用 油酸防止团聚,达到分散的目的。
方法将约30μm的Fe3O4粒子放人油酸和n庚烷中进行 长时间的球磨,得到约10nm的Fe3O4微粒稳定地分散在 n庚烷中的磁流体,每个Fe3O4微粒均包裹了一层油酸。
优选第四章纳米微粒的化学特性
§4.1吸附
吸附的概念
吸附是相接触的不同相之间产生的结合现象
吸附的分类
物理吸附 吸附剂与吸附相之间是以范德瓦
耳斯力之类较弱的物理力结合
化学吸附 吸附剂与吸附相之间是以化学键强
结合
§4.1吸附
纳米微粒吸附性特点
1、纳米微粒由于有大的比表面和表面原子配 位不足,与相同材质的大块材料相比较,有较强 的吸附性。
§4.2纳米微粒的分散和团聚
4.2.1分散
1分散机理:
A现象 尺寸较大的粒子容易沉淀下来,当粒径在 纳米级(1—100nm),由于布朗运动等因素阻止它 们沉淀而形成一种悬浮液,纳米微粒称为胶体。 由于小微粒之间库仑力或范德瓦耳斯力团聚现象 仍可能发生。
B方法 通常用超声波将分散剂(水或有机试剂)中 的团聚体打碎。
图4.1 在低pH下吸附于氧化硅表面的醇、酰胺、醚分子。
§4.1吸附
4.1.1非电解质的吸附
三、影响吸附的因素
受粒子表面性质的影响
由上述例子可知
受吸附相的性质影响
说明 :即使吸附相是相同的,但由于溶剂种类不 同吸附量也不一样。例如,以直链脂肪酸为吸附 相,以苯及正己烷溶液为溶剂,结果以正己烷为 溶剂时直链脂肪酸在氧化硅微粒表面上的吸附量 比以苯为溶剂时多,这是因为在苯的情况下形成 的氢键很少。从水溶液中吸附非电解质时,受pH 值影响很大,pH值高时,氧化硅表面带负电,水 的存在使得氢键难以形成,吸附能力下降。
二、吸附的典型例子
例如:氧化硅粒子对醇、酰胺、醚的吸 附过程中氧化硅微粒与有机试剂中间的接触 为硅烷醇层,硅烷醇在吸附中起着重要作用。
§4.1吸附
4.1.1非电解质的吸附
作用机制:上述有机试剂中的O或N与硅烷醇的羟基 (OH基)中的H形成O—H或N—H氢键,从而完成SiO2微 粒对有机试剂的吸附,如图4.1所示。
例子 如,纳米氧化物SiO2,Al2O3和TiO2等在 水中的pH高低不同(带正电或负电),因此可选 Na+,NH4+或Cl-,NO3-异电离子作反絮凝剂,使 微粒表面形成双电层,从而达到分散的目的。
§4.2纳米微粒的分散和团聚
4.2.1分散
B、加表(界)面活性剂包裹微粒 为了防止分散的纳米粒 子团聚也可加入表面活性剂,使其吸附在粒子表面, 形成微胞状态,由于活性剂的存在而产生了粒子间的 排斥力,使得粒子间不能接触,从而防止团聚体的产 生。对于磁性纳米微粒,由于颗粒之间磁吸引力,很 容易团聚,加入界面活性剂(如油酸)使其包裹在磁 性粒子表面,造成粒子间排斥作用,避免了团聚体的 生成。
§4.1吸附
4.1.2电解质吸附
一、吸附的机理:电解质在溶液中以离子形 式存在,其吸附能力大小由库仑力来决定。 纳米微粒在电解质溶液中的吸附现象大多数 属于物理吸附。 1缘由:由于纳米粒子的大的比表面常常产生键的
不饱和性,致使纳米粒子表面失去电中性而带电 (例如纳米氧化物,氮化物粒子),而电解质溶液中 往往把带有相反电荷的离子吸引到表面上以平衡其 表面上的电荷,这种吸附主要是通过库仑交互作用 而实现的。
pH值处于中间值,则纳米氧化物表 面形成M—OH键,粒子呈电中性。
§4.2纳米微粒的分散和团聚
4.2.1分散
一、面临的问题
在纳米微粒制备过程中,纳米微粒表 面的活性使它们很容易团聚在一起从而形 成带有若干弱连接界面的尺寸较大的团聚 体,这给纳米微粒的收集带来很大的困难。
二、解决的方案
用物理方法或化学方法制备的纳米粒 子经常采用分散在溶液中进行收集。
§4.1吸附
4.1.2电解质吸附
2实例列举:例如,纳米尺寸的黏土小颗粒在碱
或碱土类金属的电解液中的吸附(这是一种物理 吸附过程,它是有层次的)。吸附层的电学性质 也有很大的差别.
二、吸附层的电学性质
1靠近纳米微粒表面的一层属于强物理吸 附,称为紧密层,它的作用是平衡了超微 粒子表面的电性。 2离超微粒子稍远的离子形成较弱吸附层, 称为 分散层。
§4.1吸附
4.1.2电解质Байду номын сангаас附
三、纳米氧化物随pH值可带不同的电荷
纳米氧化物的粒子,如石英、氧化铝 和二氧化钛等根据它们在水溶液中的pH值 不同可带正电、负电或呈电中性。
图4.2 pH值对氧化物带电 状况的影响
pH比较小时,粒子表面形成M—O H2(M代表金属离子,如Si,Al,Ti 等),导致粒子表面带正电。 pH高时,粒子表面形成M—O键, 使粒子表面带负电。
2、纳米粒子的吸附性与被吸附物质的性质、 溶剂的性质以及溶液的性质有关。
3、电解质和非电解质溶液以及溶液的pH值等 都对纳米微粒的吸附产生强烈的影响。
4、不同种类的纳米微粒吸附性质有很大差别。
§4.1吸附
4.1.1非电解质的吸附
一、概念
非电解质是指电中性的分子,它们可通 过氢键、范德瓦耳斯力、偶极子的弱静电引 力吸附在粒子表面。其中主要是以氢键形成 而吸附在其它相上。
C原理 其原理是由于超声频振荡破坏了团聚体中 小微粒之间的库仑力或范德瓦耳斯力,从而使小 颗粒分散于分散剂中。
§4.2纳米微粒的分散和团聚
4.2.1分散
2防止小颗粒团聚采用的方法:
A、加入反絮凝剂形成双电层 反絮凝剂的选择可 依纳米微粒的性质、带电类型等来定。即:选择 适当的电解质作分散剂,使纳米粒子表面吸引异 电离子形成双电层,通过双电层之间库仑排斥作 用使粒子之间发生团聚的引力大大降低,实现纳 米微粒分散的目的。
§4.1吸附
4.1.2电解质吸附
上述两层构成双电层。 双电层中电位分布可用 一表示式来表明,例如把Cu离子—黏土粒子之间 吸附当作强电解质吸附来计算,以粒子表面为原 点,在溶液中任意距离x的电位可用下式表示:
Z为原子价,NA为阿伏伽德罗常数, C为强电解质的摩尔浓 度 ,k 表示双电层的扩展程度.1/ k称为双电层的厚度.由式 看出, 1/ k反比于Z和C1/2,这表明高价离子、高电解质浓度下, 双电层很薄。
例子 如, PaPell在制备Fe3O4的磁性液体时就采用 油酸防止团聚,达到分散的目的。
方法将约30μm的Fe3O4粒子放人油酸和n庚烷中进行 长时间的球磨,得到约10nm的Fe3O4微粒稳定地分散在 n庚烷中的磁流体,每个Fe3O4微粒均包裹了一层油酸。
