铁粉与水蒸气反应图示
铁与水蒸气反应演示器
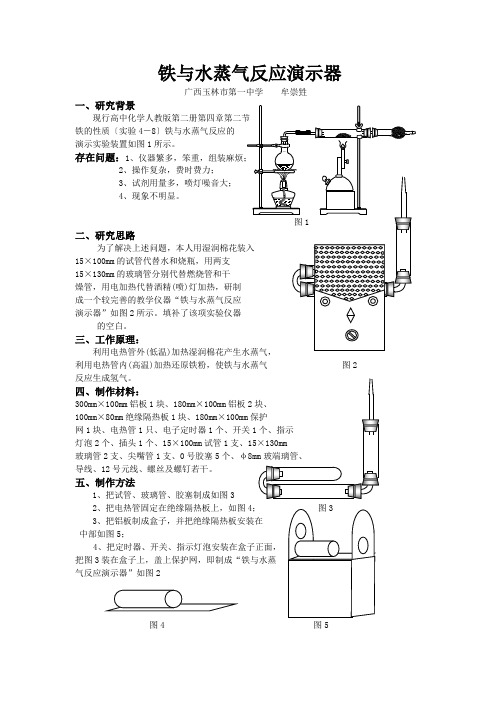
铁与水蒸气反应演示器广西玉林市第一中学牟崇甡一、研究背景铁的性质…实验4-8‟铁与水蒸气反应的演示实验装置如图1所示。
存在问题:12、操作复杂,费时费力;3、试剂用量多,喷灯噪音大;4、现象不明显。
二、研究思路15×100mm的试管代替水和烧瓶,用两支15×130mm的玻璃管分别代替燃烧管和干燥管,用电加热代替酒精(喷)灯加热,研制成一个较完善的教学仪器“铁与水蒸气反应演示器”如图2所示。
填补了该项实验仪器的空白。
三、工作原理:利用电热管外(低温)利用电热管内(高温)加热还原铁粉,使铁与水蒸气图2 反应生成氢气。
四、制作材料:300mm×100mm铝板1块、180mm×100mm铝板2100mm×80mm绝缘隔热板1块、180mm×100mm网1块、电热管1只、电子定时器1个、开关1灯泡2个、插头1个、15×100mm试管1支、15玻璃管2支、尖嘴管1支、0号胶塞5个、φ导线、12号元线、螺丝及螺钉若干。
五、制作方法1、把试管、玻璃管、胶塞制成如图32、把电热管固定在绝缘隔热板上,如图4;3、把铝板制成盒子,并把绝缘隔热板安装在中部如图5;4、把定时器、开关、指示灯泡安装在盒子正面,把图3装在盒子上,盖上保护网,即制成“铁与水蒸气反应演示器”如图2图4 图5六、使用方法1、在15×150mm试管中放入一小团湿润棉花(挤干无滴水为宜);2、在15×130mm玻璃管一端塞上一小团石棉绒,装入10克还原铁粉,再塞上石棉绒;(铁粉部位一定要留有空隙,让水蒸气通过,并能防止铁粉受热胀大玻璃管,拔不出来);3、用帶胶塞的U型导管将装有棉花的试管和装有还原铁粉的玻璃管连接起来;4、另一支15×130mm玻璃管一端塞上一小团石棉绒,装入10克干燥剂,再塞上石棉绒;5、把装有还原铁粉的玻璃管插入电热管中,装有湿润棉花的试管同时插到电热管上方,另一端用带胶塞的直角玻璃导管与装有干燥剂的玻璃管连接(垂直向上),再塞上带胶塞的尖嘴玻管;6、插上电源,设定时间3~4min,打开开关,加热指示灯亮,到时间加热指示灯灭,停止加热,同时,点燃指示灯亮,提示可点燃氢气,并能继续燃烧1~2min,现象十分明显,成功率100%。
铁粉与水蒸气的反应

科学探讨:铁粉与水蒸气的反响一.教材:人教版通俗高中课程尺度试验教科书化学(必修1)50页至51页二.课时安插:15分钟三.教授教养对象:高一学生四.教授教养设计思绪:本课题内容选自人教版高中化学必修1 第三章金属及其化合物第一节金属的化学性质第二课时金属与酸和水的反响,铁粉与水蒸气的反响是以科学探讨的情势呈现的,是学生在进修钠与水的反响后,进一步研讨金属与水的反响.高中化学新课标提出:“经由过程以化学试验为主的多种探讨运动使学生体验科学研讨的进程,激发进修化学的兴致,强化科学探讨的意识,促进进修方法的改变,造就学生的创新精力和实践才能”.科学探讨的目标是让学生在获得常识的同时,体验科学探讨的进程,懂得科学探讨的办法,达成情绪.立场.价值不雅目标.该试验难度大,是以不合适学生同步试验,经由过程重复摸索试验办法,教师演示试验能确保成功,以冲破教授教养难点.思维才能是一切才能的焦点,是以,教授教养重点放在学生设计计划上,经由过程计划设计.筛选.完美的进程激活学生思维,激发创新意识,造就合作与交换的才能.初中化学中学生学过二氧化碳制取的研讨,对试验室肯定制取气体装配斟酌的身分有必定懂得;接触过一氧化碳还原氧化铜的试验装配;知道氢气的磨练办法.这些基本使学生自立设计试验计划成为可能.新课由工件淬火视频引入,提出问题,激发进修兴致;学生依据已有常识猜测与假设并设计计划,演示试验验证假说,得出结论.因为学生不具备化学办法磨练四氧化三铁的常识,教授教养处理采取介绍x射线衍射仪测定反响后固体产品的办法,将先辈技巧装备的应用引入教授教养介绍给学生,目标是坦荡视野,也使探讨进程更为周密.五.教授教养目标:(一)常识与技巧目标1.控制铁与水蒸气反响的道理;2.能设计出简略的铁与水蒸气反响的试验装配;3.造就学生发明问题.剖析.解决问题的才能.(二)进程与办法目标1.经由过程探讨铁粉与水蒸气的反响,熟悉设计试验的一般办法,体验科学探讨的进程.2.练习学生科学思维办法,成长其思维的逻辑性.周密性.深入性.辽阔性.(三)情绪立场与价值不雅目标在科学探讨进程中,激发学生进修兴致,造就积极思虑.勇于摸索的科学品德,成长合作精力.六.教授教养重点.难点:重点:学生设计铁粉与水蒸气反响的试验装配难点:铁粉与水蒸气反响试验七.教授教养办法:试验探讨.多媒体帮助教授教养八.课型:新讲课九.教授教养器具:仪器:铁架台.大试管.铁夹.有孔橡胶塞.造就皿.坩埚钳.带防风罩的酒精灯.导管.橡胶管.玻璃棒.药匙.纸槽.课件和多媒体装备;药品:洗涤剂液.蒸馏水.脱脂棉.还原铁粉.火柴.课前预备:《教室学案》十.教授教养流程:【引入课题】【视频播放】请看“工件淬火”视频,不雅察工件概况有什么变更?【讲授】工件淬火是将钢铁成品加热到必定温度,保温后快速冷却以进步钢的强度和硬度,强化钢的机能的热处理工艺.工件是钢铁成品,水是碳钢经常应用的淬火介质.【生】铁与冷水无显著的反响现象,有黑色物资生成.【师】铁与冷水无显著的反响现象,热水呢?也无显著的反响现象.输送自来水和热水的铁管就是最好的例证.【板书】1.铁与冷水.热水——无显著的反响现象【师】工件概况生成黑色物资,是产生了化学反响吗?铁与水蒸气在高温前提下是否产生了反响呢?【教室探讨】【师】工件概况的那层黑色物资是什么?铁与水蒸气在高温前提下是否反响了呢?依据所学常识猜测.【投影】科学探讨:铁粉与水蒸气的反响提出问题:铁能不克不及在加热前提下与水蒸气产生反响呢?可能有哪些产物?【生】从氧化还道理论剖析,假如Fe与水蒸气的反响,Fe化合价将由0价升高,生成铁的化合物,那么哪种元素的化合价能下降呢?H元素.黑色物资是一种铁的化合物,我们知道铁的罕有化合物有FeO,Fe2O3,Fe3O4,Fe(OH)2 ,Fe(OH)3,到底是哪一种呢?生成物除了铁的化合物,还有什么其他物资呢?【生】从钠与水反响类推猜测:是铁的氢氧化物和氢气.……【猜测与假设】铁与水蒸气能在高温前提下产生反响,生成H2和铁的化合物.【师】实践是验证真谛的独一尺度.请同窗们设计试验验证猜测.思虑:铁粉与水蒸气反响的试验装配应当包含哪几个部分?各部分斟酌的身分有哪些?浏览教材50页科学探讨第二段.【生】水蒸气的产生装配.水蒸气与铁粉的反响装配.磨练产朝气体3部分【板书】2.铁粉在高温下与水蒸气反响:【投影】设计试验:装配的3个部分水蒸气的产生装配铁粉与水蒸气的反响装配(反响物状况.反响产生的前提)气体收集及磨练(气体性质)【设计试验】请联合所学的试验常识,评论辩论后在学案一中画出设计的装配简图.【生】小组评论辩论并画出试验装配简图.【表达与交换】报告请示交换并互相评价.【投影】归纳试验装配简图.【先生讲授】总结设计的试验装配图,点拨症结:装配的连接与简化.【投影】铁粉与水蒸气反响的试验装配图【演示试验】铁粉在高温下与水蒸气反响:脱脂棉用水浸湿后挤干,塞入试管底部,脱脂棉厚度1~2cm,铁粉1g,铁粉中间至棉花外沿距离为2cm.加热至试管壁上有渺小的水滴时,将导气管伸入盛有洗涤剂液的造就皿中吹泡,当有大量气泡时,停滞吹气泡.用点燃的火柴接近气泡,有爆鸣声.【拓展思维】【师】不雅察试验现象并填入学案二,请同窗对演示试验提问并说明.【生】不雅察试验现象,完成学案二,小组交换结论.【生】为什么要挤干棉花上的水?为什么要控制棉花与铁粉的距离?固体产品若何磨练?【生】应用加热试管中还原铁粉时的余热使潮湿的脱脂棉产生水蒸气,因为气体与铁粉概况接触,产朝气体量不久不多,所以用吹番笕泡的方法收集气体.【师】经x 射线衍射仪测定反响后固体物资,发明除铁粉外,有四氧化三铁生成.X 射线衍射图谱【师】请写出化学反响方程式:【投影】试验现象及结论 【板书】【师】该反响是工件概况在淬火进程中陪同的化学反响之一.【归纳总结】【师】你对演示试验装配还有什么问题或建议?有哪些收成?【生】为什么要用造就皿代替书上蒸发皿?还可以用什么装配?氢气还可以如何磨练?……【生】总结【安插功课】3Fe + Fe 3O 4 + 4△ 3Fe + Fe 3O 4 +4△1.比较钠与水反响和铁粉与水蒸气反响异同并剖析原因.2.化学兴致小组运动:查阅材料肯定磨练四氧化三铁的办法. 板书设计:科学探讨:铁粉与水蒸气的反响1.铁与冷水.热水——无显著的反响现象2.铁粉在高温下与水蒸气反响:H2O(g)产生Fe 粉 + H2O(g)反响装配气体磨练3Fe + Fe3O4+4△。
铁与水蒸气反应

2、钠与硫酸铜
3、钠与氯化铁反应
4、铁与水蒸气反应
科学探究
方案一:
铁不能与冷水、 热水反应。能否与 水蒸气反应?
设计实验验证铁 是否与水蒸气反应?
①水蒸气的产生装置→ ②水蒸气与铁粉的反应装置 ③气体产物检验(收集)装置
方案二:
方案三: [科学探究]按图组装实验装置进行实验
推测实验现象 1、加热时试管内铁粉红热 2、点燃肥皂泡可听到爆鸣声 3、反应后,试管内的固体仍呈黑色
3Fe+4H2O(g)
Fe3O4+4H2
金属与水的反应
小结
与冷水反应 生成碱和氢 气
与沸水反应 生成碱和氢 气
高温下与水蒸气 反应生成氧化物 和氢气
巩固练习:
A
上图为铁与水蒸气反应的实验装置,请回答下列问题: 1、仪器A的名称是:圆__底__烧___瓶___
2、写出该反应的化学方程式:3F__e_+___4_H__2_O__(g__)__
Al与NaOH反应的实质
铝先与水反应: 2Al+6H2O === 2Al(OH)3+3H2(很微弱)
生成Al(OH)3再与强碱反应 Al(OH)3+NaOH===NaAlO2+2H2O
铝与强碱反应的实质是铝和其中的水反应放出氢气。
练习:向一金属铝的易拉罐内充满CO2,然后向罐内注 入足量NaOH溶液,立即用胶布严封罐口,过一段时间 后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓 起,解释上述变化的实验现象:
三.铝与氢氧化钠溶液的反应
化学方程式: 2Al+2NaOH+2H2O ==== 2NaAlO2+3H2
离子方程式: 2Al+2OH-+2H2O ==== 2AlO-2+3H2
铁粉在高温下与水蒸气反应的化学方程式

铁粉在高温下与水蒸气反应的化学方程式1. 引言大家好,今天咱们聊聊一个有点儿“炫酷”的化学反应——铁粉和水蒸气的化学反应。
这不是科幻电影里的情节,而是咱们真实生活中的一部分。
好了,话不多说,咱们开始吧!2. 铁粉和水蒸气的反应2.1 什么是铁粉和水蒸气的反应铁粉和水蒸气反应,听上去有点儿像化学实验室里的高大上操作,但实际上,这个反应其实很有趣。
简单来说,就是把铁粉和水蒸气放在一块儿,然后加热。
你会看到铁粉会被水蒸气搞定,生成一些新的东西。
这个反应的化学方程式是这样的:3Fe +4H2O → Fe3O4 + 4H2。
2.2 反应的过程咱们来一步步看看这个反应的过程。
首先,铁粉在高温下和水蒸气接触,这时候铁粉就开始变得“热情”起来了。
它们的“热情”可不是一般的高哦,因为这时候铁粉变成了铁的氧化物——就是 Fe3O4。
而水蒸气呢,经过反应,就会变成氢气和铁氧化物。
你可以想象一下,就像一对老朋友在聚会上聊得特别开心,最后聊成了一对好搭档。
3. 化学反应的具体细节3.1 反应的实际意义好啦,既然我们知道了这个反应的化学方程式,那我们为什么要了解这个呢?这个反应其实有它的实际意义。
首先,它展示了铁在高温下的反应能力,这对于工业生产特别重要。
比如,制造钢铁的时候,就会用到这种反应。
它帮助我们了解如何在高温下处理铁粉,并将其转化为更有用的物质。
3.2 反应的结果反应的结果是生成了铁的氧化物 Fe3O4 和氢气。
氢气是一种非常有用的气体,尤其是在化学工业中,它可以作为燃料,或者用来制造其他化学品。
而 Fe3O4 则是一种黑色的固体,它在磁性材料中有很重要的作用。
你看,这个反应虽然看似简单,但它的结果可是对我们有很大帮助的。
4. 实验中的注意事项4.1 安全措施在实验室里做这个反应的时候,有几个注意事项必须得记住。
首先,高温操作的时候一定要小心,别让自己变成“小火炉”。
其次,铁粉在加热过程中可能会引起火灾,所以一定要在通风良好的地方进行实验,确保安全。
证明还原铁粉与水蒸气反应的方法

证明还原铁粉与水蒸气反应的方法
1还原铁粉与水蒸气反应的原理
铁粉与水蒸气的反应是由一种叫做弗雷反应的化学反应引起的。
该反应的方程式如下所示:4Fe3O4(s)+8H2O(g)→4Fe(s)+O2(g)+8H2O(l)。
弗雷反应是一种氧化还原反应,其中水蒸气氧离子(H2O+)以氧化剂的角色反应,而铁粉以红色磁铁矿铁氧化物的角色反应,即3价铁被还原为2价碳(Fe),产生了氧气作为副产物。
2验证还原铁粉与水蒸气反应的方法
1.将足够数量的铁粉和分离放置在烧瓶中,并将盖子封上,确保没有外来气体进入瓶中。
2.建立烧瓶和水浴,并将瓶子在水浴中加热到临界温度。
3.在临界温度的情况下,观察反应液中水蒸气的变化,水蒸气随着温度的升高而增多。
4.在烧瓶口加入一些碱性指示剂,如蓝色紫罗兰(PH范围3-5)。
碱性指示剂的溶液应受到水蒸气的影响,蓝色逐渐变成紫色,表明气体室有氧气。
5.将水浴中的烧瓶拔出,观察里面的物质发生变化,可以发现铁粉已经变成了小小的磁铁,被还原成了Fe。
这证明还原铁粉与水蒸气反应确实发生了,发生了氧化还原反应。
3结论
通过还原铁粉与水蒸气反应可以清楚地证明水蒸气可以作为氧化剂反应,而被氧化物是3价元素铁。
通过实验,我们可以看到氧气是反应产物,用碱性指示剂可以观察氧气,而铁粉已经变成了磁铁,表明铁粉已经被还原成了2价碳(Fe),证明反应成功发生。
铁粉与水蒸气的反应

铁粉与水蒸气的反应引言:铁粉与水蒸气的反应是一种常见的化学反应,也是我们日常生活中经常接触到的现象之一。
这种反应不仅有着实际应用价值,还具有一定的科学研究意义。
本文将从不同角度探讨铁粉与水蒸气的反应,包括反应机理、实验现象、应用领域等方面。
一、反应机理铁粉与水蒸气的反应主要是氧化还原反应,具体反应机理如下:铁粉中的铁原子经过加热,变为铁离子,释放出电子;然后,水蒸气中的氧分子接受这些电子,还原为氢离子,并与铁离子结合形成氢氧化铁;氢氧化铁与水反应生成氢氧化亚铁和氢氧根离子。
二、实验现象进行实验时,我们可以将铁粉放入加热的试管中,然后通过加热使铁粉与水蒸气接触。
在实验过程中,我们可以观察到以下现象:1. 铁粉表面开始出现白色烟雾,烟雾逐渐变浓;2. 试管周围可见水珠凝结;3. 试管内部出现红棕色沉淀。
三、反应方程式根据反应机理和实验现象,可以得到以下反应方程式:Fe + H2O -> Fe(OH)2Fe(OH)2 + H2O -> Fe(OH)3四、应用领域铁粉与水蒸气的反应在生活和工业中具有一定的应用价值,主要体现在以下几个方面:1. 脱氧剂:铁粉通过与水蒸气反应可以吸附其中的氧分子,起到脱氧的作用。
因此,在一些高温高压的工艺中,可以使用铁粉作为脱氧剂,保证工艺的顺利进行。
2. 氢气制备:在铁粉与水蒸气反应的过程中,产生了大量的氢气。
这种氢气可以用于氢能源的制备,具有环保和可再生的特点。
3. 清洁剂:铁粉与水蒸气的反应生成的氢氧化亚铁是一种优良的清洁剂。
它可以去除金属表面的氧化物和污垢,还原金属的亮度。
4. 催化剂:铁粉与水蒸气的反应还可以产生一定的热量。
因此,在一些需要催化剂的反应中,可以使用铁粉作为热源,提高反应速率。
结语:铁粉与水蒸气的反应是一种重要的化学反应,具有广泛的应用价值。
通过深入研究和理解这种反应的机理和实验现象,我们可以更好地应用它,为生活和工业带来更多的便利和效益。
铁粉与水蒸气的反应操作现象

铁粉与水蒸气在一定条件下可以发生化学反应,这个反应被称为氢气化反应或水蒸气还原反应。
该反应在工业上具有重要意义,例如在钢铁生产中,铁粉可以通过与水蒸气的反应来生产氢气,也可以作为还原剂来还原金属氧化物。
铁粉与水蒸气的反应通常需要在高温下进行,反应的化学方程式如下:\[ \text{Fe} + \text{H}_2\text{O} \rightarrow \text{FeO} + \text{H}_2 \]\[ \text{FeO} + \text{H}_2\text{O} \rightarrow \text{Fe(OH)}_2 \]\[ \text{Fe(OH)}_2 + \text{H}_2\text{O} \rightarrow \text{Fe(OH)}_3 \]\[ \text{Fe(OH)}_3 + \text{3H}_2 \rightarrow \text{Fe} + \text{3H}_2\text{O} \]在实际操作中,铁粉与水蒸气的反应现象如下:1. 温度升高:由于反应是放热反应,反应过程中温度会显著升高。
2. 氢气生成:反应中会产生氢气,可以通过收集管道收集。
3. 颜色变化:铁粉在与水蒸气反应后会生成红褐色的氢氧化铁(Fe(OH)3),从而铁粉的颜色会由银灰色变为红褐色。
4. 固体产物:反应后会在铁粉表面形成氢氧化铁固体,这可能会减少铁粉的表面积,影响反应速率。
5. 设备腐蚀:在高温下,铁粉与水蒸气的反应可能会导致设备(如反应器)的腐蚀,因此需要使用耐腐蚀的材料。
6. 反应控制:为了安全和效率,需要对反应的温度、压力、反应时间等参数进行严格控制。
需要注意的是,铁粉与水蒸气的反应在工业应用中通常需要精确的工程控制,以确保安全和效率。
此外,铁粉也可以与其他物质(如碳)混合,以提高氢气的产量和纯度。
实验改进22:铁与水蒸气反应实验

实验改进22 :铁与水蒸气反应实验新教材第二册中铁与水蒸气反应的演示实验,按教材的叙述来做时,成功率非常低,近日在中国基础教育网的《化学生物论坛》上,也看到这个实验做不成功的讨论。
据笔者了解,不少学校的同行干脆不做这个实验。
尽管已有同行对此实验有过研究,笔者认为仍不成熟,其装置和操作反而更复杂,成功率仍然不太高。
笔者仔细思考教材上该实验的装置和操作,认为:一是由于用烧瓶产生水蒸气时,蒸气流速太快,从而导致喷灯处加热的温度不易达到反应所需温度;二是由于气流过程中,很难用肉眼观察出反应是否开始就收集气体,这样会不易收集到氢气,导致点燃时无爆鸣声。
鉴于以上两点,笔者对此实验进行了如下几种改进,效果较好,这里介绍如下,供同行参考。
改进1取建筑用红砖砸成黄豆大小左右的颗粒用水浸湿,再捞出与干燥的还原铁粉混合,半在硬质试管中直接用喷灯加热,省去水蒸气生成装置,将反应和产生水蒸气的装置合二为一,同时也不用试管收集气,改为在球形干燥管出口处直接连接一注射用针头。
装置如图1所示。
实验时先来回移动酒精喷灯使试管受热均匀,以免炸裂,再从上到下加热。
待灯焰稳定后,直接将针头片伸到酒精灯上点燃,可观察到氢气在针头处产生明显的淡蓝色火焰,由此可证明发生了反应。
若在试管中装3cm长的铁粉与砖粒的混合物,可观察到氢气持续燃烧10min左右。
该改进使装置和操作都大为简便,且现象明显。
改进2取普通粉笔两支,用水浸湿,趁湿在其外面裹一层还原铁粉,装入硬质试管中,其余与改进1相同,加热时也可观察到氢气燃烧的现象。
同样,还可用煤渣代替砖粒、粉笔。
总之,吸水性好、在高温下不与铁粉和水蒸气反应的物质均可作为替代物。
以上改进由于省去了产生水蒸气的烧瓶,替代原料价廉且随处易得使实验不但操作简单、现象明显、成功率大大提高,而且还降低了实验成本。
不仅城市学校适合,农村学校和不发达地区更适用。
这样改进还使整个实验所需时间大大缩短,当酒精喷灯烧好后,通常只需3min左右就可完成。
