一分类分为酰卤酸酐酯酰胺等酰卤是羧酸
有机化学——10羧酸衍生物和脂类

=
R C OH + N2 + H2O
3.霍夫曼降解反应
=
O R C NH2 + Br2
NaOH
R NH2 + NaBr + Na2CO3 + H2O
反应使碳链减少一个碳原子
=
O
O
五、碳酸衍生物
(一)脲(尿素)——碳酸的二元酰胺
1. 弱碱性 不能使石蕊试纸变色, 只能与强酸成盐
= = =
O R C NHOH +
=
R'COOH
O
R C O R'
=
+ H NH OH
O R C NHOH +
= =
R'OH
O
R C NH2 + H NH OH
O R C NHOH + NH3 异羟肟酸
3R C NHOH + FeCl3
=
异羟肟酸铁 (红~紫色)
可用做羧酸及其衍生物的定性检验
=
O
O (R C NHO)3Fe + 3HCl
(四)酯缩合反应
具有α-H的酯在碱的作用下与另一分子酯发生 反应称酯缩合反应或克莱森(Claisen)缩合反应
CH3 O O O O ① C2H5ONa C OC2H5 + H CH2 C O C2H5 CH3 C CH2 C OC2H5 + C2H5OH ②H
=
=
=
(五)还原反应
卤、酸酐和酯还原成伯醇
乙酰乙酸乙酯 β 丁酮酸乙酯
羧酸衍生物比羧酸容易还原。氢化铝锂可将酰
=
O R C O R C
羧酸衍生物的命名和结构

羧酸衍生物的命名和结构羧酸衍生物通式:R C L O根据L 的不同,分为酰卤、酸酐、酯和酰胺,表示如下:R C XO R C O C R(R')OOR C O R(R')OR C NH(R)2O酰卤 酸酐 酯 酰胺一、命名1、酰基:酰基=羧酸-羟基,因此⨯酸形成的酰基就称为⨯酰2、酰卤:称为⨯⨯酰卤(氯,溴,碘)3、酸酐:两分子羧酸、二元酸脱水得酐,故称为⨯(酸)⨯(酸)酐或者⨯⨯二酸酐4、酯:(1)一元酸酯→⨯酸⨯(醇)酯(2)多元酸酯→⨯酸氢⨯酯、⨯酸二⨯酯、……(3)内酯→根据C 个数称为⨯内酯,羟基 、取代基要注位 5、酰胺:(1)称为⨯⨯酰胺(2)N 上有取代→取代基前标注N-(3)内酰胺→根据C 个数称为⨯内酰胺,氨基、取代基要注位 (4)N 上连2个酰基→⨯⨯酰亚胺例如:1、C 6H 5CO2、HOOCCO3、C 6H 5SO 24、C 6H 5COCl5、CH 3C O C O OCH 2CH 3 6、OOO7、CH 2COOH COOC 2H 58、CH 2COOC 2H 5COOC 2H 5 9、CH 2COOCH 3COOC 2H 5 10、OOCH 3O S OCH 311、O OO 12、HCOOCH 2CH 2CH 3 13、CH 3C O OCH 2C 6H 514、C 6H C O OCH 2C 6H 5 15、CH 3COCH 2COOC 2H 516、HOOCCOCH 2COOC 2H 5 17、OO18、OOEt19、CH 3ONH 220、CONH 221、C ONH22、CH 3CH=CHCONH 2323、H 2NSO 2NH 224、HCONH25、CH 3CONH26、CH 2=CHCONH 2 27、CON(CH 3)228、H 2C C H 2O C ONH29、CH 3CHCH 2CONHCH 3330、ONH31、ONH32、O NH33、ONH34、HCON(CH 3)2解:1、苯甲酰基 2、草酰基 3、苯磺酰基 4、苯甲酰氯5、乙丙酐6、邻苯二甲酸酐(苯酐)7、丙二酸氢乙酯8、丙二酸二乙酯9、丙二酸甲乙酯 10、硫酸二甲酯 11、丁烯二酸酐 12、甲酸丙酯 13、乙酸苄酯 14、苯甲酸苄酯 15、乙酰乙酸乙酯16、草酰乙酸乙酯 17、γ-丁内酯 18、β-乙基-γ-丁内酯19、乙酰胺 20、苯甲酰胺 21、苯甲酰苯胺(N-苯基苯甲酰胺) 22、3-甲基-2-丁稀酰胺 23、对氨基苯磺酰胺 24、N-环己基甲酰胺 25、乙酰苯胺 26、丙稀酰胺 27、N,N-二甲基苯甲酰胺 28、丁二酰亚胺 29、N,3-二甲基丁酰胺 30、γ-丁内酰胺 31、δ-戊内酰胺 32、ε-己内酰胺33、γ-甲基-γ-丁内酰胺(γ-戊内酰胺) 34、N,N-二甲基甲酰胺(DMF)二、羧酸衍生物的结构特点R C L O酰基RCO 与L 基团存在共轭,但酰卤的共轭较其他弱,因卤原子的轨道匹配性差。
有机化学--羧酸及其衍生物

POCl3
HCl↑
O R C OH
SOCl2
O R C Cl
SO2↑
低、高沸点 ↑ HCl 的酰氯制备 都适合
② 酸酐的生成
羧酸在脱水剂如五氧化二磷的存在下,加热。两分子羧 酸失去一分子水而形成酸酐。
R-C OH R-C OH O R-C O R-C + H2O
P2O5
△
(产率较低)
O
分子量较大的羧酸在乙酐(作脱水剂)存在下,失水生 成酸酐。反应平衡中发生了酸和酸酐的交换。 O O CH3-C 2R-C-OH + O CH3-C O
任何使酸根负离子稳定的因素都将增加其酸性,羧酸根负离 子愈稳定,愈容易生成,酸性就愈强。
(1)电子效应的影响
诱导效应:X—COOH
-I使酸性增强, +I使酸性减弱
X= F Cl Br I CHO 3.53 NO2 1.68
+N(CH ) 3 3
pKa 2.66 2.86 2.90 3.18
1.83
O CH3CH2 C
丙酰基
O C
苯甲酰基
CH3 CH3 CH3CH-CHCH2COOH CH3CH-CHCH21 COOH 4 3 2 CH2CH3 CH
5 6 3
CH3-C =CH-COOH CH3 3-甲基-2-丁烯酸
γ β α
4
3
2
1
3,4-二甲基戊酸 CH2-COOH CH2-COOH 丁二酸
羧酸铵盐 腈的水解为其逆反应:
酰胺
腈
O C OH + HNH-
O C NHN-苯基苯甲酰胺
+ H2 O
扑热息痛
3、羧基的还原 (LiAlH4)
羧酸及羧酸衍生物(酰卤、酸酐、酯、酰胺),含氮有机物的红外光谱谱图
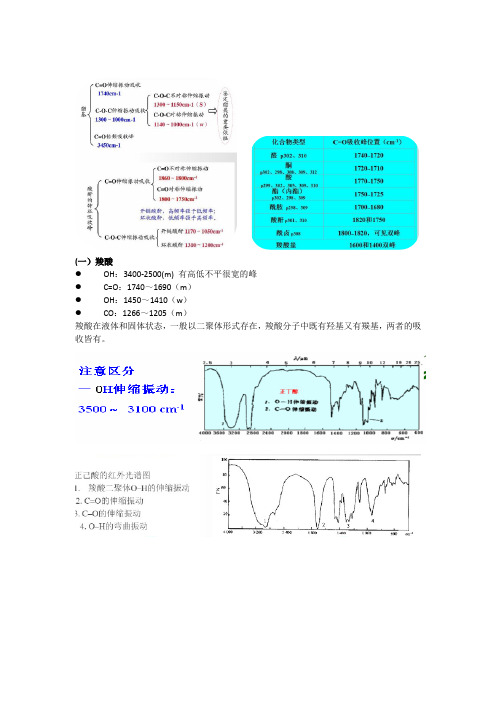
(一)羧酸●OH:3400-2500(m) 有高低不平很宽的峰●C=O:1740~1690(m)●OH:1450~1410(w)●CO:1266~1205(m)羧酸在液体和固体状态,一般以二聚体形式存在,羧酸分子中既有羟基又有羰基,两者的吸收皆有。
10-十一烯酸的谱图红外光谱(KBr压片法)苯甲酸的红外光谱图(二)酰卤●卤素原子直接与羰基相连,强诱导效应使羰基极性降低,键能增加,吸收移向高频●脂肪族位于1800cm -1附近●芳香族在1770附近,常为双峰●C-X❖str:脂肪族1000—910cm-1 峰形宽大,芳香族❖1250—1110cm-1,通常分裂为数个峰(三)酰胺●N-H str:3540-3125●C=O str:1690-1620(M效应和I效应的净作用决定)●N-H def+C-N str:❖1650-1580:主要是仲酰胺NH和C=H反式存在的吸收❖1450-1310:内酰胺是以顺式存在●N-H def 倍频:3020●Ar-C:1335-1250,s而强●N-H str 770-625,宽而散●(四)酸酐●酸酐的C=0基的吸收有两个峰,出现在较高波数处( 1820cm 1 及1750cm-1)。
●两个吸收峰的出现是由于两个羰基振动的偶合所致。
●线性酸酐的两峰强度接近相等,高波数峰仅比较低波数峰稍强。
但环状酸酐的低波数峰却比较高波数峰稍强。
●●(五)酯 (RCOOR ’)(1)酯有两个特征吸收,即υC=O 和υC -O -C 。
(2)酯羰基的伸缩振动υC=O :● R -CO -OR ’ (RR ’为烷基) 1750~1735cm -1(S) ● Ph -CO -OR 、C=C -CO -OR 1730~1717cm -1(S) ● R -CO -O -C=C 、R -CO -OPh 1800~1770cm -1(S) (1) υC -O -C在1330~1050cm -1有两个吸收带,即υcoc as和υcoc s。
羧酸是一类含有羧基(一COOH)官能团的化合物

CH 3CH CH COOHRH羧酸是一类含有羧基(一COOH )官能团的化合物,一元饱和脂肪羧酸的通式为C n H 2n O 2 。
羧基中的羟基被其它原子或基团取代的产物称为羧酸衍生物(如酰卤、酸酐、酯、酰胺等),羧酸烃基上的氢原子被其他原子或基团取代的产物称为取代酸(如卤代酸、羟基酸、羰基酸、氨基酸等)。
羧酸是许多有机化合物氧化的最终产物,常以盐和酯的形式广泛存在于自然界,许多羧酸在生物体的代谢过程中起着重要作用。
羧酸对于人们的日常生活非常重要,也是重要的化工原料和有机合成中间体。
(一) 羧酸13.1羧酸的结构、分类和命名13.1.1羧酸的结构在羧酸分子中,羧基碳原子是sp 2杂化的,其未参与杂化的p 轨道与一个氧原子的p 轨道形成C=O 中的π键,而羧基中羟基氧原子上的未共用电子对与羧基中的C=O 形成p -π共轭体系,从而使羟基氧原子上的电子向C=O 转移,结果使C=O 和C —O 的键长趋于平均化。
X 光衍射测定结果表明:甲酸分子中C=O 的键长(0.123 nm )比醛、酮分子中C=O 的键长(0.120nm )略长,而C —O 的键长(0.136nm )比醇分子中C —O 的键长(0.143nm )稍短。
羧基上的p -π共轭示意图13.1.2 羧酸的分类和命名 1.羧酸的分类根据分子中烃基的结构,可把羧酸分为脂肪羧酸(饱和脂肪羧酸和不饱和脂肪羧酸)、脂环羧酸(饱和脂环羧酸和不饱和脂环羧酸)、芳香羧酸等;根据分子中羧基的数目,又可把羧酸分为一元羧酸、二元羧酸、多元羧酸等。
例如:脂肪羧酸一元羧酸脂环羧酸芳香羧酸CH 3COOHCH 2CH 2COOHCOOHCOOHCH 3CH CH COOHCOOHHOOC HOOC CH 2COOHCH 2COOHCH 2HOOC COOHHOOC 二元羧酸多元羧酸2.羧酸的命名羧酸的命名方法有俗名和系统命名两种。
俗名是根据羧酸的最初来源的命名。
(二) 羧酸衍生物

Nu-:进攻的亲核试剂,即H2O、ROH、NH3、RNH2或R2NH等。
L-:离去基团,即X、-OOCR 、-OR、-NH2、-NHR或-NR2
总的反应速度和两步反应的速度都有关系,但第一步更为重要。酰基中羰基碳原子是sp2杂化,三个σ键是平面形分布。羰基碳上如果连有吸电子基团,将增加羰基碳的正电性,有利于亲核试剂的进攻;反之,如果连有供电子基团,将不利于亲核试剂的进攻。亲核加成生成的中间体,其碳原子为sp3杂化,即四面体结构。如果原来羰基碳原子上连接的基团过于庞大,在四面体结构中就显得过于拥挤而不利于反应进行。上述电子效应和空间效应都将对第一步的反应速度有所影响。第二步反应易否进行,取决于离去基团L-的碱性,碱性越弱,越易离去。羧酸衍生物各离去基团离去的难易次序为:
在有机合成中酯的还原是使羧酸间接转变为伯醇的重要方法,因为羧酸的还原比酯困难。
14.8.3 α-氢化反应
羧酸衍生物分子中的α-氢由于受羰基影响(σ-π超共轭和吸电诱导效应),比较活泼,与醛酮相似,在一些碱性试剂催化下可以发生缩合反应。在有机合成中酯缩合反应应用较多。
由于酯的α-H酸性小于醛酮,也小于酰氯(但大于酰胺),所以酯缩合用的碱是醇钠或其他碱性催化剂(如氨基钠)而不是氢氧化钠的水溶液。酯在强碱作用下发生分子间的缩合反应,称为(Claisen)酯缩合反应,在制备β-二羰基化合物时很有用。
一般克莱森酯缩合反应是在两个相同的酯之间进行。虽然我们可以进行混合酯的交叉缩合反应,即采用两种不同的酯,但产物太复杂,没有实用价值,除非一个酯有α-氢,一个酯没有α-氢,才有制备意义。例如草酸乙酯、苯甲酸酯、甲酸酯等都是不含α-氢的酯,可用于交叉酯缩合反应。这时产物比较纯。
己二酸酯和庚二酸酯在醇钠作用下主要是发生分子内的酯缩合反应,称为狄克曼(Dieckmann) 缩合反应,生成环状的β-酮酸酯。
羧酸及其衍生物

羧酸及其衍生物羧酸及其衍生物Ⅰ 目的要求羧酸是含有羧基(―COOH)的含氧有机化合物,我们平常所说的有机酸就是指的这类化合物。
所谓羧酸衍生物,包括的化合物种类很多,诸如羧酸盐类、酰卤类、酯类(包括内酯、交酯、聚酯等)、酸酐类、酰胺类(包括酰亚胺、内酰胺)等都是羧酸衍生物,有人甚至把腈类也包括在羧酸衍生物的范围之内。
其实,比较常见的而又比较重要的是酰卤、酸酐、酯和酰胺这四类化合物。
羧酸盐与一般无机酸盐在键价类型上没大区别,不作专门介绍。
至于腈类,将放在含氮化合物中加以介绍。
这四类化合物都是羧酸分子中,因酰基转移而产生的衍生物,所以又叫羧酸的酰基衍生物。
羧酸及其衍生物RCOL(L:-OH、-X、-OOCR′、-OR′、-NH2)在许多重要天然产物的构成以及在生物代谢过程中均占有重要地位。
本章将以饱和一元脂肪酸为重点,讨论羧酸及其衍生物的结构和性质。
鉴于乙酰乙酸乙酯和丙二酸二乙酯在有机合成上的重要地位,本章作概括介绍。
希望学生在此基础上,探讨设计合成路线的一般方法。
本章学习的具体要求1、掌握羧酸的结构与性质之间的关系。
2、掌握羧酸衍生物的主要化学性质。
3、了解羧酸衍生物的亲核取代反应机理。
4、掌握羧酸与羧酸衍生物之间相互转变条件。
5、了解卤代酸、羟基酸的特性。
6、掌握乙酰乙酸乙酯和丙二酸二乙酯的制法、性质和在有机合成上的应用。
这也是本章的重点之一。
Ⅱ 学习提要(一)羧酸一、概述羧酸往往有俗名,希望学生有所了解,尽可能记忆一些,脂肪酸的系统命名原则和醛相β α同。
γCH3-CH-CH2-COOH2 14 3 OH 芳香酸命名是把芳环视作取代基。
76羧酸的沸点比分子量相近的其它有机物高,这是由于羧酸能以氢键缔合。
同时,即使在气态时,羧酸也是双分子缔合的,所以羧酸的沸点比分子量相近的醇还要高。
二、羧酸结构和化学性质亲核取代O 还原R-C-C-O-H α-H反应H 脱羧酸性1、酸性?E O O O +?R-C H + R-C R-C E EO-H O OO O NaOH/Na2CO3/ NaHCO3H2O + R-C E R-C EH+ O-Na O-H应用:①鉴别:与酚不同,与非酸性物质不同。
羧酸衍生物-有机化学

/
HCl
水解反应的活性次序是: 酰卤 > 酸酐 > 酯 > 酰胺 [提示]
羧酸衍生物易水解,在使用和保存含有该类结构 的药物时应注意防止水解失效。某些易水解的药物, 如含有酰胺结构的氨苄西林钠注射剂,都是在临用 时再加水配成注射液。许多酯类和酰胺类药物在一 定的pH范围内较稳定,配成水溶液时,必须控制溶 液的pH。羧酸衍生物类药物的注射剂消毒灭菌时, 应注意控制温度和时间。
酮式
O H
烯醇式
O
CH3 C CH C OC2H5
★ 凡是具有 H-C-C=O 基本结构的化合物都可能 发生酮式-烯醇式互变异构现象。 ★互变异构现象在其它化合物中也常见。 例如:
H O C N OH C N
S H C N
SH C N
第十章
羧酸衍生物
(carboxylic acid derivatives) 指羧酸分子中的羟基被其他原子或基 团取代后所生成的化合物。 包括 酰卤(acylhalide) 酸酐(anhydride) 酯(ester) 酰胺(amide)等,
ቤተ መጻሕፍቲ ባይዱ
它们的结构通式如下:
O R C O O R C OH R C O R C O R C NH2
CH3 C Cl + H2O
O
O
CH3 C OH + HCl↑
加热
CH3 CH3
C O C O + H2O 2 CH3COOH
加热 酸碱 加热 回流
O R C OR + H2O
O R C NH2 + H2O
NaOH
/
O
NaOH
R C ONa + ROH
O R C O R C ONa + NH3↑ OH + NH4Cl
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
O
O–
慢
快
OH– + R C OR' 快 R – c OR' 慢
O
OH
R C OH+R'OH
如: HOOCCH2CH2COOCH3+H2O18 H+
HOOCCH2CH2COO18H+CH3OH
2、酯的酸性水解:
酯的酸性水解绝大多数都是酰氧键断裂的 双分子历程,只有少量特定结构的酯,才发生单分 子的酰氧键或烷氧键断裂的历程。如:
干性油:干结成膜快; 半干性油:干结成膜慢; 不干性油:不能干结成膜。
结膜过程是一个复杂的氧化聚合过程。 3、加成: 1>、氢化:不饱和油通过催化加氢可转变为饱 和的脂。这种脂称为氢化油或硬化油。 2>、加碘:不饱和油中的烯键可以和I2 加成。
碘值:100g油脂所能吸收的碘的克数 称为碘值(又称碘价)。
CNCH2COONa
C2H5OH H2SO4
CH2(COOC2H5)2
应用:与卤代烃或α,ω-二元卤代烃作用。
在有机合成中丙二酸二乙酯与卤代烃或α,ω-二 元卤代烃作用相当于乙酰乙酸乙酯与卤代烃或α, ω-二元卤代烃作用后进行酸式分解。
§13.6酰胺
羧酸铵加热失水可得酰胺;酰卤、酸酐 以及酯的氨解也可得到酰胺;控制腈的水解 也能得到酰胺。 一、物理性质: 沸点比相应的羧酸高,但—NH2上的H被R取 代后沸点下降。
R'N=C=O+ROH
(异氰酸酯)
R'N=C=O+2HCl
O
R' — NH C OR
2>、重要的氨基甲酸酯有:西维因,灭菌灵等, 见P66 。
§13.9有机合成路线 一、有机合成的基本要求
产率高、副反应少、反应速度快、原料易得、步 骤少、安全。
二、有机合成的任务
1、 建立产物分子可需的骨架 2、 官能团的转化
1>、阴离子型洗涤剂:典型的代表是十二烷
基苯磺酸钠R — —SO3Na,普通洗衣粉的
主要成分就是它。
2>、阳离子型洗涤剂:典型的代表是溴化十 二烷基二甲基苄基铵,即“新洁尔灭”。常用 来洗伤口,给伤口消毒。
3>、非离子型洗涤剂:这类洗涤剂在水中不 离解,是中性化合物。如:
C8H17— —(OCH2CH2—)nOH
3、酯:有无机酸酯和有机酸酯。
O
R C OR '
4、酰胺:是羧酸分子中的羟基被氨基(—NH2) 或烃氨基(—NHR,—NR2)取代后的生成物。
二、命名:
O
R C 的名称是将RCOOH中的“酸”字改 为“酰”字。 1、酰卤和胺:酰基名称+卤素名称或胺。如: 乙酰氯、丁酰溴、丙烯酰胺、N—乙基乙酰胺等。
2、乙酸戊酯:是香蕉水的主要成分。
§13.4油脂和合成洗涤剂
一、油脂 油脂普遍存在与动物的脂肪组织和植物
的种子中。习惯上把室温下呈固态或半固态 的叫脂肪;呈液态的叫油。 油脂是高级脂肪 酸甘油酯的总称。常用
CH2OCOR CHOCOR'来表示,如果R、R'、R''相同则称为
CH2OCOR ''
单纯甘油酯;不同则称为混合甘油酯。 1、水解:
EtONa
CH3COOC2H5
CH3COCH2COOC2H5+C2H5OH
2>、Dieckmann狄克曼反应:
二羧酸酯在钠或醇钠的作用下发生分子 内缩合,生成β—酮酸酯,后者经水解可以得脂 环酮。 狄克曼反应是分子内的酯缩合反应,是 合成五元、六元环的一个方法。
如:
CH2CH2COOC2H5
CH2 – CH–COOC2H5
CO2+HCl
COCl2+NH3 COCl2+C2H5OH
CO(NH2)2+HCl
O
C2H5O C OC2H5
二、碳酸的酰胺: 1、尿素: 1>、制备:
工业上用CO2和过量NH3在加热、加压 下合成尿素:
O
加压
CO2 + NH3 加热
NH2 C NH2
2>、水解:
酶
CO(NH2)2+H2O
CO2+2NH3
第十三章 羧酸衍生物
羧酸衍生物也叫酰基化合物,是指羧酸分子中 羧基上的羟基被其它原子或基团取代后生成的 化合物。
§13.1羧酸衍生物
一、分类:
分为酰卤、酸酐、酯、酰胺等。
1、酰卤:是羧酸分子中的羟基被卤原子取 代后的生成物。RCOX
O
O
2、酸酐: R C O C R,R,R' 相同叫单酐, 不同叫混酐。有些二元酸脱水可形成环酐。
RCOCl+R'MgX
RCOR'
R'MgX
R'2RCOH
§13.3羧酸酯
羧酸与醇作用脱水生成酯的反应叫酯化 反应。当醇与酰基化试剂(酰氯、酸酐)作 用,也可生成酯。酯也广泛存在于植物的花、 果等自然界中。
一、物理性质:
沸点与含同数碳的醛酮相当。溶解度小,一 般有香味。
二、化学性质:
1、酯的水解、醇解、氨解:
RCOOC(CH3)3+H+ 快
快
RCOOH+ (CH3)3
慢
快 RCOOH+(CH3)3C+
快
(CH3)3C+ + H2O 慢 (CH3)3C–O – H
快
快 (CH3)3CO H+H +
二、酰基衍生物的水解、氨解、醇解
酰氯、酸酐、酰胺的水解、氨解、醇解历
程与酯的碱性水解历程是相似的,都是加成-
如:CH2=CH2→CH3CH2CH2CH=C-COOCH2CH2CH2CH3 CH3 OH
再如:由CH2=CH2→CH3CHCH2CH3
2>、小碎片分子是否允许使用?若不允许使用, 则继续开裂,直到基本原料或给定原料。
CHO
如:由CH2=CH2→CH3CH2CH2CH=C-CH2CH3。 时,CH3CH2CH2CHO不允许使用
O
O
Cl C Cl
O
NH2 C
NH2
O
NH2 C OR
RO C OR
Cl C OR
一、碳酰氯(光气):
1、制备:
O
日光作用
CO+Cl2
Cl C Cl
Or:活性炭,200℃
或 CCl4 +H2O
500℃
O
Cl C Cl +HCl
2、物理性质: 常温下是有毒气体,溶于苯及甲苯。
3、化学性质:
COCl2+H2O
3、还原:羧酸衍生物都能被LiAlH4还原。酯 的还原比羧酸容易。
4、酯缩合反应:
1>、Claisen克莱森缩合:
羧酸酯与活性亚甲基化合物,如酯类、 酮类或腈等缩合,脱去一分子醇,相应得到β— 酮酯、β—二酮、β—酮腈。
—COOR+ CH R' EtONa
O
C C —R ' +ROH
同类的酯也能进行此反应,如:
O
(憎水) R C ONa (亲水)
2>、肥皂的去污原理:
在水面时,亲水部分插入水中,憎水部分 翘出水面。在水中时,形成胶束,R靠色散力
聚集在一起。R易溶在(进入)油污中,使 油污与它的附着物逐渐松开,在受机械震动 下,脱离附着物。
2、合成洗涤剂:
按合成洗涤剂的分子结构特点,把它分 为离子型和非离子型两' 类,离子型又分为阴 离子型和阳离子型两种。
5、霍夫曼降级反应:(也称Hofmann重排)
在碱性溶液中,用氯或溴与氮原子上没有取
代的酰胺作用可以得到第一胺。
O
NaOX
OH–
RCONH2
RCONHX
RCN
R—N=C=O H2O RNH2+CO2
§13.7酰基衍生物的水解、氨解、醇解历程
一、酯的水解历程:
1、酯的碱性水解:
酯的碱性水解一般是BAC2(碱催化,酰氧 键断裂,双分子历程):
酯的水解是酯化反应的逆反应,需用酸或 碱作催化剂,用碱催化时的水解也叫皂化反应。 而酯的醇解也叫酯交换反应。由于氨本身是碱, 所以氨解不需用催化剂。肼和羟氨也能与酯作 用分别形成酰肼和羟肟酸,羟肟酸能与FeCl3作 用形成红色络合物,这是定性鉴定酯的一种很 好的方法。酰卤、酸酐也呈正性结果。
2、与格氏试剂的作用:由于酮与格氏试剂作 用的活性更大,所以产物一般为第三醇。
5、建立较复杂的骨架时常用的试剂和反应
二、化学性质:
1、酰胺的酸碱性:由于羰基的吸电子使氨基 的碱性很弱,遇强酸(如硝酸)才能形成盐; 如果有两个羰基连在氨基上,则氨基还具有弱 酸性,能与强碱形成盐(如邻苯二甲酰亚胺与 氢氧化钠)。
2、水解:用酸或碱催化都能水解形成羧酸。
3、脱水:
Δ RCONH2+P2O5
RCN+2HPO3
4、还原:能被LiAlH4还原为胺,如: C6H5CON(CH3) LiAlH4 C6H5CH2N(CH3)
憎水
亲水
n在10左右,是家用液态洗涤剂的主要成分。这 类洗涤剂除用作洗涤剂外,还可用于矿石浮选的 起泡剂。
三、磷脂和生物膜
在动植物体内含有与油脂类似的化合物, 含磷酸的类脂称为磷脂,其中最重要的是 脑磷脂和卵磷脂,存在于植物的种子、蛋 黄、动物的脑等器官中。生物细胞膜是由 蛋白质和脂类(主要是磷脂)构成的。
O
NH2 C NH C NH2+NH3
双缩尿与碱和CuSO4作用成紫色,这个颜色 反应叫双缩尿反应。
2、氨基甲酸酯:
1 >、制法:
O
方法1: COCl2+ROH
Cl C Cl +HCl
