第七章_有机化合物结构的光谱分析习题
(完整版)有机波谱习题及答案

11. 波谱分析法通常获得其他分析方法不能获得的那些信息? (B) A. 组成信息; B. 原子或分子结构信息; C. 化合物存在形态; D. 化合物极性大小
12. 激光拉曼光谱属于(D) A. 吸收光谱; B. 发射光谱; C. 原子光谱; D. 分子光谱
13. 有机波谱分析方法和仪器分析法的主要不足是(B) A. 样品用量大; B. 相对误差大; C. 选择性差; D. 重现性低
24. 对各种氨基酸的分析,最有效的方法是(D) A. 紫外吸收光谱; B. 红外光谱; C. 气相色谱; D. 高效液相色谱
25. 电感耦合等离子体发射光谱(ICP)有如下特点, 其中错误的是(C) A. 动态范围宽,标准曲线的线性范围可达105~106; B.基体效应比较低,较易建立分析方法; C. 只能进行单元素测定; D. 精密度好
要比化学分析法高得多。(×)
10. 一般讲,分子光谱远比原子光谱复杂,原子光 谱通常为线状光谱,而分子光谱为带状光谱。(√)
11. 吸收定律偏离线性完全是由仪器因素引起 的。(×)
12. 电子能级间隔越小跃迁时吸收光子的频率 越大。(× )
13. 分子光谱是由电子的发射而产生的。(×)
14. 分子荧光也叫二次光,都属于吸收光谱的 范围。(×)
A. GC-MS; B. LC-MS; C. ICP-MS; D. GC-IR 19. 下列那种简写代表核磁共振波谱?(B)
A. UV; B. NMR; C. IR; D. MS 20. 下列有机波谱分析法中,哪种谱图的横轴不表示光或电磁
波的能量?(D) A. 紫外-可见光谱; B. 红外吸收光谱; C. 核磁共振波谱; D. 质谱
3.可见光区、紫外光区、红外光区、无线电波区四个电磁波 区域中,能量最大和最小的区域分别是(A) A. 紫外光区和无线电波区; B. 紫外光区和红外光区; C. 红外光区和无线电波区; D. 可见光区和红外光区
第七章 有机波谱分析
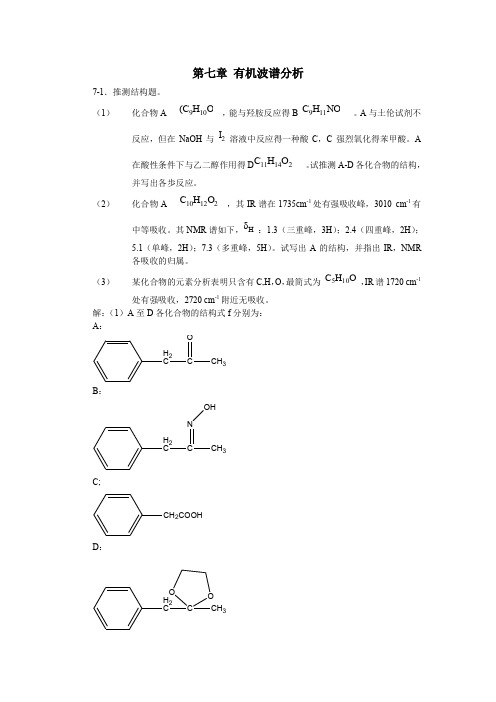
第七章 有机波谱分析7-1.推测结构题。
(1)化合物A (C 9H 10O ,能与羟胺反应得B C 9H 11NO 。
A 与土伦试剂不反应,但在NaOH 与 I 2 溶液中反应得一种酸C ,C 强烈氧化得苯甲酸。
A 在酸性条件下与乙二醇作用得D C 11H 14O 2 。
试推测A-D 各化合物的结构,并写出各歩反应。
(2)化合物A C 10H 12O 2 ,其IR 谱在1735cm -1处有强吸收峰,3010 cm -1有中等吸收。
其NMR 谱如下,δH :1.3(三重峰,3H );2.4(四重峰,2H );5.1(单峰,2H );7.3(多重峰,5H )。
试写出A 的结构,并指出IR ,NMR 各吸收的归属。
(3)某化合物的元素分析表明只含有C,H ,O ,最简式为 C 5H 10O ,IR 谱1720 cm -1处有强吸收,2720 cm -1附近无吸收。
解:(1)A 至D 各化合物的结构式f 分别为: A :H 2CCH 3OB :H 2CCNCH 3OHC;CH 2COOHD :H 2CCCH 3O O各步反应如下:H 2CCCH 3OH 2CCCH 3NOHNH 2OHH 2CCCH 3O H 2CCCH3O O 22+CH 3IH 2CCH 3O H 2CCCH3O O 22+CH 3ICH 2COOHCOOH[O](2)A 的结构式为:H 2COCOH 2CCH 3A 的IR ,NMR 各吸收归属为:H 2COCOH 2CCH 3dcbaIR :1735 cm -1(强)酯的 v Ar-H ;3010 cm -1(中强) v c=O 。
NMR :δH :1.3(三重峰,3H )a ;2.4(四重峰,2H )b ;5.1(单峰,2H )c ;7.3(多重峰,5H )d 。
(3)IR 的谱1720 cm -1处有强吸收,2720 cm -1附近处无吸收,表明有酮羰基 RCOR '。
有机物波普分析习题及解析

第一章质谱习题1、有机质谱图的表示方法有哪些是否谱图中质量数最大的峰就是分子离子峰,为什么2、以单聚焦质谱仪为例,说明质谱仪的组成,各主要部件的作用及原理。
3、有机质谱的分析原理及其能提供的信息是什么4、有机化合物在离子源中有可能形成哪些类型的离子从这些离子的质谱峰中可以得到一些什么信息5、同位素峰的特点是什么如何在谱图中识别同位素峰6、谱图解析的一般原则是什么7.初步推断某一酯类(M=116)的结构可能为A或B或C,质谱图上m/z 87、m/z 59、m/z 57、m/z29处均有离子峰,试问该化合物的结构为何(A)(B)(C)8.下列化合物哪些能发生McLafferty重排9.下列化合物哪些能发生RDA重排10.某化合物的紫外光谱:262nm(15);红外光谱:3330~2500cm-1间有强宽吸收,1715 cm-1处有强宽吸收;核磁共振氢谱:δ处为单质子单峰,δ处为四质子宽单峰,δ处为三质子单峰,质谱如图所示。
参照同位素峰强比及元素分析结果,分子式为C5H8O3,试推测其结构式。
部分习题参考答案1、表示方法有质谱图和质谱表格。
质量分析器出来的离子流经过计算机处理,给出质谱图和质谱数据,纵坐标为离子流的相对强度(相对丰度),通常最强的峰称为基峰,其强度定为100%,其余的峰以基峰为基础确定其相对强度;横坐标为质荷比,一条直线代表一个峰。
也可以质谱表格的形式给出质谱数据。
最大的质荷比很可能是分子离子峰。
但是分子离子如果不稳定,在质谱上就不出现分子离子峰。
根据氮规则和分子离子峰与邻近峰的质量差是否合理来判断。
2、质谱仪的组成:进样系统,离子源,质量分析器,检测器,数据处理系统和真空系统。
进样系统:在不破坏真空度的情况下,使样品进入离子源。
气体可通过储气器进入离子源;易挥发的液体,在进样系统内汽化后进入离子源;难挥发的液体或固体样品,通过探针直接插入离子源。
真空系统:质谱仪需要在高真空下工作:离子源(10-3~10-5Pa );质量分析器(10 -6 Pa )。
分析化学第七章吸光光度分析法

图8-1吸收曲线
分析化学第七章吸光光度分析法
8
吸收曲线的讨论:
(1)同一种物质对不同波长光的吸光度不同。 吸光度最大处对应的波长称为最大吸收波长 λmax
(2)不同浓度的同一种物质,其吸收曲线形 状相似λmax不变。而对于不同物质,它们的 吸收曲线形状和λmax则不同。
(3)吸收曲线可以提供物质的结构信息,并 作为物质定性分析的依据之一。
红外吸收光谱:分子振动光谱,吸收光波长 范围2.51000m ,
主要用于有机化合物结构鉴定。 紫外吸收光谱:电子跃迁光谱,吸收光波长 范围200400 nm(近紫外区) ,可用于结 构鉴定和定量分析。
分析化学第七章吸光光度分析法
2
可见吸收光谱:电子跃迁光谱,吸收光波长范 围400750 nm ,主要用于有色物质的定量 分析。
nm (真空紫外区)
分析化学第七章吸光光度分析法
4Байду номын сангаас
一、物质的颜色
物质的颜色是由于物质对不同波长的光 具有选择性吸收而产生的。
物质颜色
黄绿 黄 橙 红 紫红 紫 蓝 绿蓝 蓝绿
吸收光
颜色
波长/nm
紫
400~450
蓝
450~480
绿蓝
480~490
蓝绿
490~500
绿
500~560
黄绿
560~580
黄
10
三、光吸收的基本定律
1.朗伯—比耳定律 • 布格(Bouguer)和朗伯(Lambert)先后于
1729年和1760年阐明了光的吸收程度和吸收
层厚度的关系。A∝b
• 1852年比耳(Beer)又提出了光的吸收程度和
吸收物浓度之间也具有类似的关系。A∝ c
波谱解析第7章(综合解析)

可由元素分析氧含量推测氧原子个数。与波谱数据对照。 (d)确定氮原子数
可由元素分析氮含量推测氮原子个数。与波谱数据对照。
若MS中有分子离子峰且m/z为奇数时,分子中应含奇 数个氮。分子量和从a~c项计算的分子量之间差为14的整 数倍或者只用上述a~c各项而在图谱中还有不能说明的问 题时,可能有氮原子。应由IR研究相应的官能团,并检查 是否尚有不能用b解释的地方(b即指HH-HC之差值),进一 步检查备图谱中相应吸收峰,以确定氮原子数。 (e)确定卤素原子数 从MS中M、M+2、M+4很容易确定是否含有Cl和Br原 子及它们的个数。 由于碘和氟元素中只含一种同位素,因此它们没有同 位素峰。 如果注意到质谱峰与上述各项所确定的不一致时,在 大多数情况下,能确定是有卤素原子存在。
7.2 波谱解析的一般程序(从送样到定结构) 1.测试样品的纯度: 作结构分析,样品应是高纯度的。应事先做纯度检验。 另外,考察样品中杂质的混入途经也是很重要的。 有些实验,可用于混合物的定性分析,如GC/MS HPLC/MS,GC/IR 2.做必要的图谱及元素分析。先选择性做几个重要、方 便的,再根据情况做其他谱。 3.分子量或分子式的确定: (1)经典的分子量测定方法 可用沸点升高、凝固点降低法、蒸汽密度法、渗透压 法。有些样品可用紫外光谱根据Beer定律测定分子量。 误差大。 大分子可用排阻色谱测定。
(2)质谱法 高分辨质谱在测定精确分子量的同时,还能推出分子 式,这是有机质谱最大的贡献。 低分辨质谱由测得的同位素丰度比也可推出分子中元素 的组成,进而得到可能的分子式。 (3)结合核磁共振氢谱、碳谱推测简单烃类等分子的分 子式。 (4)综合光谱材料与元素分析确定分子式 (a)确定碳原子数: 从13C-NMR宽带去偶谱的吸收峰数,得出碳原子的类 型数。在分子无对称因素的条件下,一条谱线即为一个 碳。
有机化学 12 第七章 波谱分析 (三) 核磁共振

H 实 = H 0 H 0σ = H 0 (1 σ )
在真实分子中,发生核磁共振的条件是:
ν RF
γ = H 0 (1 σ ) 2π
这里σ是屏蔽常数. 不同化学环境的质子,因其周围电子云密度不同,裸 露程度不同,其σ值也不同,从而发生核磁共振的H0 不 同.这就是化学位移的来源. 所以,化学位移也可定义为由于屏蔽程度不同 由于屏蔽程度不同而引起 由于屏蔽程度不同 的NMR吸收峰位置的变化.
OCH3
的NMR?
与氧原子相 连的甲基氢
δ3.9(单峰 单峰) 单峰 -OCH3 δ6.7~7.3 苯环氢
苯氢
所以,该图是2,3,4-三氯苯甲醚的NMR.
例3:下图与A,B,C哪个化合物的结构符合?
ClCH2C(OCH2CH3)2 Cl A Cl2CHCH(OCH2CH3)2 B CH3CH2OCH-CHOCH2CH3 Cl Cl C
例1:CH3CH2CH2NO2的NMR谱.
例2:CH3CH2OH的NMR谱.
通常,只有相邻碳 1H才相互偶合. 相邻碳上 相邻碳
1,1,2-三溴乙烷
(4) 积分曲线与质子的数目
积分曲线的高度与其相对应的一组吸收峰的峰面积成正 比,而峰面积与一组磁等价质子的数目成正比. 以乙醇 乙醇的NMR为例. 乙醇
(三) 核磁共振
(1) 1H-NMR的基本原理 (2) 1H-NMR的化学位移 (3) 1H-NMR的自旋偶合与自旋裂分 (4) 积分曲线与质子的数目 (5) 1H-NMR的谱图解析 (6) 13C-NMR谱简介(自学)
(三) 核磁共振
(Nuclear Magnetic Resonance Spectroscopy)
C Ha C Hb Ha C C Ha Hb C C Hb
有机化学第七章光谱

一些常见化学键的力常数如下表所示:
键型 O H N H
-1
C H C O C C C O C C 4.8 17.7 15.6 12.1 9.6 5.4 4.5
k /N.cm
7.7 6.4
折合质量μ :两振动原子只要有一个的质量↓, μ ↓,(v)↑
C H 2800-3000cm
3.其他:
N-H弯曲振动在1600-1650cm-1 四个或四个以上CH2 相连,其CH2 的面内摇摆 振动在 720cm-1
7.1.4 红外谱图解析
红外谱图解析的基本步骤是:
1.观察特征频率区:判断官能团,以确定所属化 合物的类型。
2.观察指纹区:进一步确定基团的结合方式。 3.对照标准谱图验证。
E:光量子能量,J h: Planck常数, 6.626×10-34 J.S
分子吸收光谱 分子吸收电磁幅射,就获得能量,从而引起分子 某些能级的变化,如增加原子间键的振动,或激发 电子到较高的能级,或引起原子核的自旋跃迁等。 但它们是量子化的,因此只有光子的能量恰等于两 个能级之间的能量差时(即ΔE)才能被吸收。所以 对于某一分子来说,只能吸收某一特定频率的辐射, 从而引起分子转动或振动能级的变化,或使电子激 发到较高的能级。光谱便是记录分子对不同波长 (频率)的电磁波吸收或透过情况的图谱。
叔醇:1150~1120cm-1
4. 醛与酮
二者的异同点:
1. 在1700cm-1处均有一个强而尖的吸收峰,为 C= O(羰基)的特征吸收峰。 C=O(羰基)吸收峰的位置与其邻近基团有关, 若羰基与双键共轭,吸收峰将向低波数区位移。
2.醛基在2715cm-1处有一个强度中等的尖峰,这是 鉴别分子中是否存在— CHO的特征基团。
红外光谱分析法习题(含答案)

红外光谱分析法试题一、简答题1.产生红外吸收的条件是什么?是否所有的分子振动都会产生红外吸收光谱?为什么?2.以亚甲基为例说明分子的基本振动模式.3.何谓基团频率?它有什么重要用途?4.红外光谱定性分析的基本依据是什么?简要叙述红外定性分析的过程.5.影响基团频率的因素有哪些?6.何谓指纹区?它有什么特点和用途?二、选择题1.在红外光谱分析中,用 KBr制作为试样池,这是因为 ( )A KBr晶体在 4000~ 400cm -1 范围内不会散射红外光B KBr在 4000~ 400 cm -1 范围内有良好的红外光吸收特性C KBr在 4000~ 400 cm -1 范围内无红外光吸收D 在 4000~ 400 cm -1 范围内,KBr 对红外无反射2.一种能作为色散型红外光谱仪色散元件的材料为 ( )A 玻璃B 石英C 卤化物晶体D 有机玻璃3.并不是所有的分子振动形式其相应的红外谱带都能被观察到,这是因为 ( )A 分子既有振动运动,又有转动运动,太复杂B 分子中有些振动能量是简并的C 因为分子中有 C、H、O以外的原子存在D 分子某些振动能量相互抵消了4.下列四种化合物中,羰基化合物频率出现最低者为 ( )A IB IIC IIID IV5.在下列不同溶剂中,测定羧酸的红外光谱时,C=O伸缩振动频率出现最高者为( )A 气体B 正构烷烃C 乙醚D 乙醇6.水分子有几个红外谱带,波数最高的谱带对应于何种振动 ? ( )A 2个,不对称伸缩B 4个,弯曲C 3个,不对称伸缩D 2个,对称伸缩7.苯分子的振动自由度为 ( )A 18B 12C 30D 318.在以下三种分子式中 C=C双键的红外吸收哪一种最强?(1) CH3-CH = CH2 (2) CH3- CH = CH-CH3(顺式) (3) CH3-CH = CH-CH3(反式) ( )A(1)最强 B (2)最强 C (3)最强 D 强度相同9.在含羰基的分子中,增加羰基的极性会使分子中该键的红外吸收带 ( )A 向高波数方向移动B 向低波数方向移动C 不移动D 稍有振动10.以下四种气体不吸收红外光的是 ( )A H2OB CO 2C HClD N211.某化合物的相对分子质量Mr=72,红外光谱指出,该化合物含羰基,则该化合物可能的分子式为 ( )A C4H8OB C3H4O 2C C3H6NOD (1) 或(2)12.红外吸收光谱的产生是由于 ( )A 分子外层电子、振动、转动能级的跃迁B 原子外层电子、振动、转动能级的跃迁C 分子振动-转动能级的跃迁D 分子外层电子的能级跃迁13. Cl2分子在红外光谱图上基频吸收峰的数目为 ( )A 0B 1C 2D 314.红外光谱法试样可以是 ( )A 水溶液B 含游离水C 含结晶水D 不含水15.能与气相色谱仪联用的红外光谱仪为 ( )A 色散型红外分光光度计B 双光束红外分光光度计C 傅里叶变换红外分光光度计D 快扫描红外分光光度计16.试比较同一周期内下列情况的伸缩振动(不考虑费米共振与生成氢键)产生的红外吸收峰,频率最小的是( )A C-HB N-HC O-HD F-H17.已知下列单键伸缩振动中 C-C C-N C-O键力常数k/(N•cm-1) 4.5 5.8 5.0吸收峰波长λ/μm 6 6.46 6.85问C-C, C-N, C-O键振动能级之差⊿E顺序为 ( )A C-C > C-N > C-OB C-N > C-O > C-CC C-C > C-O > C-ND C-O > C-N > C-C18.一个含氧化合物的红外光谱图在3600~ 3200cm -1有吸收峰,下列化合物最可能的是 ( )A CH3-CHOB CH3-CO-CH3C CH3-CHOH-CH3D CH3-O-CH2-CH319.用红外吸收光谱法测定有机物结构时,试样应该是 ( )A 单质B 纯物质C 混合物D 任何试样20.下列关于分子振动的红外活性的叙述中正确的是 ( )A 凡极性分子的各种振动都是红外活性的,非极性分子的各种振动都不是红外活性的B 极性键的伸缩和变形振动都是红外活性的C 分子的偶极矩在振动时周期地变化,即为红外活性振动D 分子的偶极矩的大小在振动时周期地变化,必为红外活性振动,反之则不是三、填空题1.在分子的红外光谱实验中,并非每一种振动都能产生一种红外吸收带,常常是实际吸收带比预期的要少得多。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第七章 有机化合物结构的光谱分析习题
1.指出哪些化合物可在近紫外区产生吸收带.
(1)
(2) CH 3CH 2OCH(CH 3)2
(3) CH 3CH 2
C CH
(6)
(5) CH 2=C=O
(4) CH 2=CHCH=CHCH 3
2. 如何用IR 或1HNMR 谱鉴别下列各组化合物?
(2)OH O
与(3)
(4)
O
与
CH 3CH 2CHCH 3OH
与
O
(1)CH 3CH 2CH 2CHO 与 CH 3CH 2COCH 3
3. 具有下列各分子式的化合物在1HNMR 谱中均只出现1个信号,其可能的结构式是什么?
(1)C 5H 10; (2)C 3H 6Br 2; (3)C 2H 6O ; (4)C 3H 6O ; (5)C 4H 6; (6)C 8H 18。
4. 如何用1HNMR 谱区分下列各组化合物? (1) 环丁烷和甲基环丙烷
(2) C(CH 3)4和CH 3CH 2CH 2CH 2CH 3 (3) ClCH 2CH 2Br 和BrCH 2CH 2Br
(4)
CH 3CH 2OCH 2CH 3CH 3
2
O CH
和
5. 某化合物的分子式为C 4H 8O ,它的红外光谱在1715cm -1有强吸收峰;它的核磁共振谱有一个单峰(3H),有一个四重峰(2H),有一个三重峰(3H)。
试写出该化合物的结构式。
6. 某化合物的实验式为C 3H 6O ,1HNMR :δ=1.2(6H)单峰,δ=2.2(3H)单峰,δ=2.6(2H)单峰,δ=4.0(1H)单峰;IR 在1700cm -1及3400cm -1处有吸收带;推测该化合物的结构。
7. 某化合物的分子式为C 4H 6O ,其光谱性质为:UV 谱:在230nm 附近有吸收峰,ε>5000;IR 谱:在1720 cm -1、2720 cm -1处有强吸收。
1HNMR 谱:δ=2.03,双峰,3H ;δ=6.13,多重峰,1H ;δ=6.87,多重峰,1H ;δ=9.48,双峰,1H 。
试推测该化合物的结构式。
