有机高分子材料的结构
【知识解析】高分子的结构与性质
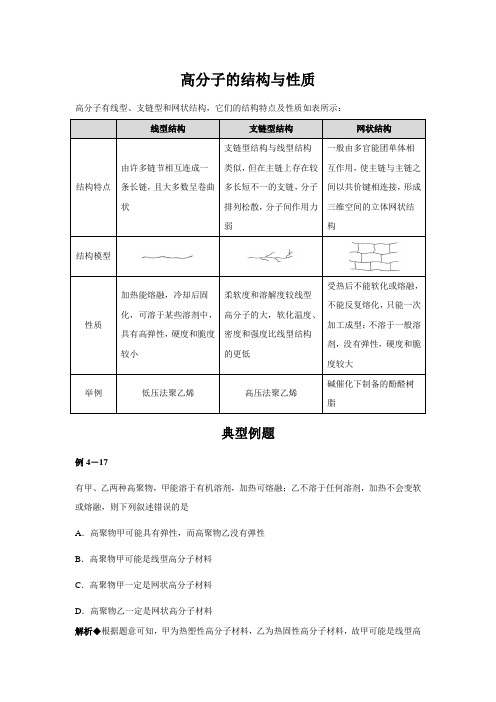
高分子的结构与性质
高分子有线型、支链型和网状结构,它们的结构特点及性质如表所示:
线型结构支链型结构网状结构
结构特点由许多链节相互连成一
条长链,且大多数呈卷曲
状
支链型结构与线型结构
类似,但在主链上存在较
多长短不一的支链,分子
排列松散,分子间作用力
弱
一般由多官能团单体相
互作用,使主链与主链之
间以共价键相连接,形成
三维空间的立体网状结
构
结构模型
性质加热能熔融,冷却后固
化,可溶于某些溶剂中,
具有高弹性,硬度和脆度
较小
柔软度和溶解度较线型
高分子的大,软化温度、
密度和强度比线型结构
的更低
受热后不能软化或熔融,
不能反复熔化,只能一次
加工成型;不溶于一般溶
剂,没有弹性,硬度和脆
度较大
举例低压法聚乙烯高压法聚乙烯
碱催化下制备的酚醛树
脂
典型例题
例4-17
有甲、乙两种高聚物,甲能溶于有机溶剂,加热可熔融;乙不溶于任何溶剂,加热不会变软或熔融,则下列叙述错误的是
A.高聚物甲可能具有弹性,而高聚物乙没有弹性
B.高聚物甲可能是线型高分子材料
C.高聚物甲一定是网状高分子材料
D.高聚物乙一定是网状高分子材料
解析◆根据题意可知,甲为热塑性高分子材料,乙为热固性高分子材料,故甲可能是线型高
分子材料也可能是支链型高分子材料,乙一定是网状高分子材料,C项符合题意。
答案◆C。
7有机高分子材料

①硬质聚氯乙烯(UPVC)管
②聚乙烯(PE)管 ③聚丙烯(PP)管和无规共聚聚丙烯( PPR )管 ④聚丁烯(PB)管
塑料管与镀锌铁管优缺点比较
请观察使用两年后的塑料管和镀锌铁管的照片,对其优缺 点予以比较。
塑料管
镀锌铁管
3)塑料贴面装饰板 面层为三聚氰胺甲醛树脂渍过的印有各种色彩、
n
表观密度较小,有耐低温(-70℃)和耐化学腐蚀,电绝缘性, 耐磨性、耐水性均较好。 缺点:机械强度不高;易燃,熔融滴落,常加阻燃剂。 聚乙烯塑料主要用于化工耐腐蚀管道,用于配制多种涂料, 也可作防水、防潮材料。
聚丙烯(PP)
刚性大, 密度小0.90g/cm3~0.91g/cm3。
耐热性好, 使用温度为100℃~110℃。优良的电绝缘性能和耐 蚀性能,在常温下能耐酸、碱,导线外皮 制作零部件,如法兰、齿轮、风扇叶轮、把手及壳体等,还 可制作化工管道、容器。
线性非晶态聚合物的物 理形态与温度的关系
粘流态:链节可以自由地旋转,整个分子链也能自由移动,从而 成为能流动的粘液,比液态低分子化合物的粘度要大得多,又称 为塑性态。例如胶粘剂或涂料。
玻璃化温度 由高弹态向玻璃态转变的温度,用Tg 表示。
粘流化温度 由高弹态向粘流态转变的温度,用Tf 表示。
塑料与纤维: 要求Tg 高, Tf 低(较耐热,加工成型温度不高) 橡胶:要求Tg 低, Tf 高(耐寒又耐热) 一些非晶态高聚物的Tg和Tf值: 聚氯乙烯 Tg =81 ℃ 聚苯乙烯 Tg =100 ℃ 聚丁二烯(顺丁橡胶) Tg =-108 ℃ 天然橡胶 Tg =-73 ℃ Tf =175℃ Tf =135℃ Tf =122℃
一些聚合物的名称、商品名称、符号及单体
高分子材料的结构及其性能PPT(36张)

B、高弹性 随着温度的升高,当T>Tg 时,分子的动能增加,使链段的自由旋转成为可能,此时,试
样的形变明显增加,在这一区域中,试样变成柔软的弹性体,称为高弹态。 高弹态时,弹性模量显著降低,外力去除后,变形量可以回复,有明显的时间依赖性。由
如图16-7,在间同立构高聚物中, 原子或原子团会交替分布在主链两侧; 在全同立构高聚物中,原子或原子团 则全部排列在主链同一侧;而在无规立构高聚物中,主链两侧原子分布是随机的。
这种化学成分相同,但由于不对称取代基沿分子主链分布不同的现象,就叫做 高分子的立体异构现象。
2、大分子链的构象及柔性 高聚物结构单元是通过共价键重复连接形成线型大分子,共价键的特点是键能
2、单体 高分子化合物是由低分子化合物通过聚合反应获得。
组成高分子化合物的低分子 化合物称作单体。所以我们经 常说,高分子化合物是由单体 合成的,单体是高分子化合物 的合成原料。如图16-2,聚乙 烯是由乙烯(CH2=CH2)单 体聚合而成的。 高分子化合物的相对分子质 量很大,主要呈长链形,因此 常称作大分子链或者分子链。 大分子链极长,可达几百纳米以上,而截面一般小于1nm。
物,简称高聚物材料,是以高分子化合物为主要组分的有机 材料,可分为天然高分子材料和人工合成高分子材料两大类。 天然高分子材料包括如蚕丝、羊毛、纤维素、油脂、天然橡 胶、淀粉和蛋白质等。 人工合成高分子材料包括如塑料、合成橡胶、胶粘剂和涂料 等。工程上使用的主要是人工合成的高分子材料。
一、高聚物的基本概念 1、高聚物和低聚物 高分子化合物是指相对分子质量很大的化合物,其相对分子质量在5000
有机高分孑材料定义

有机高分孑材料定义有机高分子材料是指由碳、氢、氧、氮等元素构成的高分子化合物,具有较高的分子量和一定的结晶性或无定形性。
这类材料具有良好的可塑性、耐热性、耐腐蚀性和机械强度,广泛应用于各个领域。
一、有机高分子材料的分类有机高分子材料根据其结构和用途可以分为以下几类:1.聚合物:由单体通过聚合反应而形成的大分子化合物,如聚乙烯、聚丙烯等。
2.共聚物:由两种或两种以上单体通过共聚反应而形成的大分子化合物,如苯乙烯-丁二烯共聚物。
3.交联聚合物:在聚合过程中引入交联剂使得链之间相互交联而形成三维网络结构的高分子化合物,如环氧树脂等。
4.复合材料:将不同种类或不同形态的材料组装在一起形成新材料,如玻璃纤维增强塑料。
5.功能性高分子:在普通高分子基础上引入某些特殊结构或功能单元而形成的高分子化合物,如聚酰亚胺。
二、有机高分子材料的性质有机高分子材料具有以下几种基本性质:1.可塑性:有机高分子材料易于加工成各种形状,如薄膜、管道、板材等。
2.耐热性:有机高分子材料的熔点较高,耐热温度可达数百摄氏度。
3.耐腐蚀性:大多数有机高分子材料具有良好的耐酸碱、耐溶剂等化学稳定性。
4.机械强度:由于其长链结构和三维网络结构,有机高分子材料具有较好的强度和硬度。
5.导电性:一些功能性高分子具有良好的导电性能。
三、有机高分子材料的应用由于其优良的物理化学性质和广泛适用范围,有机高分子材料在各个领域都得到了广泛应用:1.包装领域:聚乙烯、聚丙烯等塑料袋和容器广泛应用于食品、化妆品、药品等包装行业。
2.建筑领域:聚氯乙烯、聚苯乙烯等塑料材料广泛应用于隔音、保温、防水等方面。
3.汽车工业:聚酰亚胺等高性能塑料材料广泛应用于汽车零部件制造。
4.电子领域:聚酰胺、聚碳酸酯等高性能塑料材料广泛应用于电子器件制造。
5.医疗领域:聚乳酸等生物降解塑料材料广泛应用于医疗器械和医用耗材制造。
四、有机高分子材料的发展趋势有机高分子材料的发展趋势主要体现在以下几个方面:1.功能性高分子的开发和应用,如导电高分子、光学高分子等。
第1章 有机高分子材料的结构

一个高分子可穿越若干结晶区和非结晶区。
在80年代初期,一些科技工作者在观察从稀释的液体中结晶出单晶时发现,单晶体呈薄片状,10-20纳米一片,10微米大小的片状,通常这些片形成一个多片层的结构。
从理论分析可知,单晶体内的每个片层是由于分子链形成折叠弯曲的规则排列,从而形成薄片晶体,这就是所谓的折叠链状模型。
许多大块的高分子物质从液态结晶时,形成所谓的球晶。
在球晶中,经电镜分析可知,球晶是由若干放射状的片组成的,每个片层都是由分子折链形成的。
折链晶片是由一层非晶区隔开的,非晶区内的分子起连接片层的作用。
在完全结晶时,这些片层相互衔接,形成整个晶体。
1.11总结绝大多数高聚物分子是以碳链为主链的链状结构,它可以在某个氢原子处缺位而代之以其余元素原子或原子基团。
高聚物也可认为是由称为基元的小的原子重复单位构成。
我们给出了一些简单的高聚物的基元。
高聚物分子量可达百万单位,然而由于分子量有一个分布,因此,常用数均或重均分子量表示。
分子聚合度也可以用数均或重均基元数加以表示。
高分子化合物的结构可分为不同的几个层次的描述,即分子基元的化学组成、分子的尺寸、形状和结构。
分子的基元的化学组成可以用化学分析和其它的方式推断;分子的尺寸由分子量表示出来;分子的形状可用分子链是否弯曲、折叠、螺旋环绕和缠结来加以表示;分子结构可用构成分子的结构单元的构造方式来加以决定;其中包含分子链的四种聚集状态:直链聚合、多分支链聚合、交链式聚合和三维网状聚合等,从分子构型方面考虑可有五种不同的异构形式:等规异构、间规异构、随机异构、顺式异构和反式异构等五种异构形式,其中前三种可称为立体异构,后两种可称为几何异构。
这种分类关系可以用如下分类图表示,应该指出的是,有些分类关系决不是完全排它的,有时候还必须兼用两种以上的分类方式。
如一个直链状高分子也可能同时是等规异构的。
当高聚物分子规则堆积时就形成晶体,结晶往往是不完全的,结晶度可用密度测量标定。
高一有机高分子材料知识点

高一有机高分子材料知识点有机高分子材料是高一化学课程中的重要内容之一。
本文将从定义、分类、性质和应用等方面介绍有机高分子材料的知识点。
一、定义有机高分子材料是由碳、氢和其他元素(如氮、氧、硫等)组成的大分子化合物。
其分子量通常很大,可以达到数万甚至几百万。
二、分类有机高分子材料可以按照形状、结构和合成方法等不同的角度进行分类。
1. 形状分类有机高分子材料根据形状可以分为线性高分子、支化高分子和网络高分子。
线性高分子是由线性排列的单体重复单元组成;支化高分子在线性结构的基础上引入支链,增加了分子间的交联点;网络高分子是由三维交联结构构成,具有更高的机械强度。
2. 结构分类有机高分子材料可以根据其结构特点分为聚合物、共聚物和聚合物共混物等。
聚合物是由同种单体组成的,例如聚乙烯、聚丙烯等;共聚物由两种或多种不同的单体共同聚合而成,例如丙烯酸-丙烯腈共聚物;聚合物共混物是由两种或多种不同聚合物混合而成,例如聚苯乙烯与聚苯乙烯均聚物的共混物。
3. 合成方法分类有机高分子材料的合成方法多种多样,常见的有聚合反应、缩聚反应和交联反应等。
聚合反应是指通过将单体分子进行化学反应,使其相互连接形成高分子链。
缩聚反应是将两个或以上的小分子通过化学反应互相连接。
交联反应是指通过化学反应或物理交联手段,使高分子链之间产生交联,增加材料的稳定性和机械强度。
三、性质有机高分子材料的性质取决于其分子结构和合成方法等因素。
1. 物理性质有机高分子材料通常是非晶态或有序部分结晶态的。
其物理性质包括密度、硬度、弹性、熔点、玻璃化转变温度等。
不同的有机高分子材料具有不同的物理性质,如聚乙烯具有良好的韧性和柔软性,而聚苯乙烯则具有较高的硬度和脆性。
2. 化学性质有机高分子材料的化学性质表现为与其他物质的反应。
例如,聚氯乙烯在高温下可与溴发生取代反应,聚丙烯可以与氧气发生氧化反应,聚酯可以与醇类发生酯交换反应等。
四、应用有机高分子材料在生活和工业中有广泛的应用。
高分子材料和小分子材料结构差异

高分子材料和小分子材料结构差异
高分子材料和小分子材料是化学领域中的两类材料,它们的结构有很大的差异。
高分子材料是指分子量大于1000的有
机物质,也称为高聚物。
它们在分子结构上具有高度的分子重复和复杂性,并且以高分子链形式存在。
它们的特点是具有可塑性、可柔性、可结合性、可溶解性、可粘连性、可热塑性等特征。
而小分子材料是指分子量比高分子材料小的化合物,它们是由单体分子组成,分子量比较小,比如由氢、氧、碳和氮组成的有机物质和无机物质等。
它们一般没有可塑性,但是具有较好的抗热性、抗腐蚀性、耐磨性、耐老化性等特点。
从结构上来看,高分子材料是由高分子链组成的,它们的分子量较大,而小分子材料是由单体分子组成的,分子量较小。
从性能上来看,高分子材料具有可塑性、可柔性、可结合性、可溶解性、可粘连性、可热塑性等特点,而小分子材料具有较好的抗热性、抗腐蚀性、耐磨性、耐老化性等特点。
高分子材料和小分子材料都有其独特的结构和性能,这些特性决定了它们在应用中的不同。
高分子材料主要用于塑料、橡胶、涂料、纤维、地板面层等,小分子材料主要用于精细化学品、农药、润滑油、汽油、柴油、添加剂等。
总之,高分子材料和小分子材料之间存在着显著的结构和性能差异,他们各自都有其独特的应用领域,为不同的应用提供了不同的材料选择。
第五章 有机高分子材料(共100张PPT)

数学模型,故测定的统计平均值互不相等,常见的相对分子质量
有数均相对分子质量、重均相对分子质量、黏均相对分子质量
等。
第二节 高分子的合成、结构与性能
1. 高分子的合成原理及方法
2. 高分子的结构和性能
一、 高分子的合成原理及方法
1. 高分子的合成原理
高功能化
对高分子功能的研究正在深度和广度上获得进展,从离子交
换开展到电子交换,又开展到各种高分子别离膜和高分子吸附
剂。从电绝缘体扩展到半导体、导体,甚至超导体。由电性能扩
展到光、磁、声、热、力等性能。从化学、物理性能扩展到了生
物性能。
复合化
高分子材料是结构复合材料的最主要的基体之一,以玻璃纤
➢ 60年代,是聚烯烃、合成橡胶、工程塑料、溶液聚合、配位聚合、 离子聚合的开展时期,形成了高分子全面繁荣的局面。
➢ 70年代,开展了液晶高分子。
➢ 70年代以后,主要提高产量、改进性能、开展功能等方面。
四、高分子材料的战略地位和开展趋势
1.高分子材料在国民经济和科学技术中的战略地位
材料是工业生产开展的根底,新材料的出现往往会给新技术带来划时代的 突破。高分子材料是材料领域中的后起之秀,它的出现带来了材料领 域的重大变革,从而形成了金属材料、无机材料、高分子材料和复合 材料多角共存的格局。
生。
智能化
智能材料使材料本身带有生物所具有的高级功能,例如具有 预知预告性、自我诊断、自我修复、自我增殖、认识识别能力、 刺激反响性、环境应答性等种种特性,对环境条件的变化能作出
符合要求的应答。
五、高分子材料的根本概念
1. 高分子的链结构
2. 高分子的聚合度及其计算
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第1章 有机高分子材料的结构1.1引言天然有机高分子化合物,如木材、橡胶、棉花、毛皮和蚕丝等都已经被人类广泛应用;生命运动中天然有机高分子化合物也不乏其广泛的应用,如蛋白质、酶、淀粉、纤维素等都是动植物体内生物和生理学过程中不可缺少的基本有机物。
在科学发展到二十世纪初期,知识和技术的积累已经可以使人类来逐步确定这些高分子化合物的结构,并通过低分子有机物来合成它们。
许多我们常用的塑料、橡胶和纤维材料都是合成高分子材料。
事实上从第二次世界大战结束后,材料领域中高分子材料的发展可以说是日新月异,一个个高分子材料的新发明和新发现冲击着材料领域,给人以世界变得太快的感觉。
塑料、橡胶和纤维都可以廉价合成,有许多性能还比天然生产的产品有更优越的性能;在许多应用上,它们已经逐步在取代木材和金属材料,并且有更好的性能价格比。
与其他材料一样,高分子合成材料的性能和它们的结构有密切的关系,在本章中我们着重研究它们的分子和晶体结构,而把结构和性能的关系和制备工艺放到以后的章节中加以阐述。
1.2碳氢化合物分子由于许多高分子化合物都是有机物,我们要简单回顾一下它们的分子结构。
首先,许多有机化合物都是碳氢化合物,即它们主要由氢和碳元素组成。
碳原子有四个电子,可供形成共价键,然而,氢原子只有一个电子,每个氢原子贡献一个电子与碳原子的一个电子形成一个共价键,就像甲烷(CH 4)分子中那样。
碳原子间也可共用两对电子,形成双键,两个碳原子还分别和两个氢原子形成单键,如乙烯(C 2H 4)分子中就是这样。
在少数情况下,碳原子还可以形成三键。
如乙炔(C 2H 2)中就是这样。
甲烷、乙烯和乙炔的结构分子式分别如下:图 1.1 烷烃的结构举例双键和三键称为不饱和键,也就是说碳原子没有充分地和其它原子结合。
双键可看成是两个单键,碳原子位置稍加调整就可以允许两个其余碳原子以外的其它原子和它成键。
饱和碳氢化合物中,所有原子都是单键结合,因此如果没有移去一个原子,就不能加入另一个原子。
饱和碳氢化合如表1.1所示。
表1.1 饱和烷烃化学式和结构式举例C H H HH C HH C HH CH C H名称化学成分结构式举例甲烷(Methane)乙烷(Ethane)丙烷(Propane)丁烷(Butane)戊烷(Pentane)己烷(Hexane)CH4 C2H6 C3H8 C4H10 C5H12 C6H14相互结合的共价键很强,但分子间的相互作用为范德瓦尔斯力(Van de Waals bond),键很弱,因此,这些碳氢化合物的熔点和沸点都不高;但熔点和沸点随分子量的上升呈上升趋势。
有些碳氢化合物有相同的分子式,但分子结构不同,这就构成了所谓的同分异构现象,如丁烷的两种同分异构体如图1.2所示。
正丁烷异丁烷图1.2 丁烷同素异构体碳氢化合物的一些物理性能和其同分异构的结构状态有关,如正丁烷与异丁烷的沸点分别是-0.5与-12.3℃。
还有许多的有机合物,他们中的许多种都可在有机高分子化合物中。
表1.2列出了几种常用的碳氢化合物,其中R和R’表示的是一些官能团,即在化学反应中保持整体性的原子集合体,如CH3,C2H5和C6H5(甲基、乙基和苯基)等。
表1.2 有机化合物举例种类特征单元代表物质结构式名称醇(alcohols) R—OH 甲醇醚(ethers) R-O-R’二甲基乙醚酸(acids)OHR—COH OHH C CH O乙酸醛(aldehydes)RC=OHHC=OH甲醛CHHHC HHHCHHH CHHC HHHCHHCHHHCHHCHHCHH HOHHCHHHOHCHHC HHCHHHCHHC HHHCH HHH芳香烃(Aromatichydrocarbon)ROH苯酚1.3高分子化合物分子高分子化合物顾名思义,其分子和前面所讲的碳氢化合物相比是巨大无比的,因此也常常被称为“宏观分子”。
在这些分子中,原子经常以共价键方式结合,对大多数高分子化合物来说,分子呈柔性链状,主链通常由碳原子组成,链上碳原子分别以一个单键和旁边的两个碳原子成键,如图1.3所示。
图1.3 高分子化合物的分子链其余剩下的两个电子可以和相邻原子或原子基团形成共价结合,形成边界原子或支链。
很显然,在主链或支链上形成双键是可能的。
这些大分子都可以认为是由若干小的基元(mer )在链上不断重复而组成,一个单一基元称为单体(monomer )。
高分子(polymer )其含义就是大量的基元组成的分子;然而,单体指的是由一个基元组成的分子。
1.4高分子化学重新考察一下乙烯这个碳氢化合物,它在室温和常压下是气体,并有如下结构式:图1.4 乙烯分子结构如果它在特定的温度和压力下加以催化合成,那么,就变成为聚乙烯[Polyethylene (PE )]高分子化合物,它在常压下是固态物质。
在这个过程中,形成了很多的乙烯单体单元,双键变成为单键,打开的两个单键现在比较活跃,可以和邻近碳原子形成键接,或者是形成其余可能的共价键。
这个反应可写成以下的结构式:图1.5 乙烯分子的活化式中黑点表示的是活化的电子。
由此,这些活化的单体相互靠近,然后形成一系列的链结,最后生成长链,可用图1.6(a)表示。
但是,图中的直链表达并不是一种完全准确的描述,碳原子间的键接角并不是图中所示的180︒而是109︒。
更精确的示意图如图1.6(b)所示,其实碳链是一条之字型弯曲的长链,C —C 键长为0.154纳米。
通常,在我们的讲课中这个细节被忽略,而简单地用直链加以描述。
如果聚乙烯中所有的氢原子都被氟原子所替代,那么,所生成的就是聚四氟乙烯塑料[polytetrafluoroethylene(PTFE)], 它的结构式和基元由图1.7(a)表示;聚四氟乙烯塑料属于一C H H C HH C HH CHHC HH CHH C H HC H HC H HC H HC H HC H HCHHC H H个被称为碳氟化合物的高分子化合物系,它的商业名称为特氟隆(telflon),它具有非常好的耐酸碱腐蚀性能。
(a)(b)图1.6 聚乙烯[Polyethylene(PE)]分子及其链结构聚乙烯单元中,如有一个氢原子被氯原子规则替代就形成了聚氯乙烯[polyvinyl chloride(PVC)]高分子塑料,它的结构式和基元如图1.7(b)所示。
聚氯乙烯基元中,氯基被换成甲基就形成了聚丙烯[polypropylene(PP)]塑料,它的结构式和基元如图1.7(c)所示。
所述的高分子都是由同一个基元重复排列而成,这样的高分子化合物称为均聚高分子化合物。
很显然,高分子化合物也可以是由不同基元按一定规律成链的方式形成的化合物,这种更为普遍的化合物称为共聚物。
(a)聚四氟乙烯塑料[polytetrafluoroethylene(PTFE)]或TEFLON(b)聚氯乙烯[polyvinyl chloride(PVC)](c)聚丙烯[polypropylene(PP)]塑料图1.7不同高分子的分子及其链结构我们讨论到此,可以发现,我们研究的基元总是只有两个激活的键,这些基元称为双向功能基元,即它可以通过和其它基元和基团形成链状分子结构;当然,也存在有三个激活键的基团,如下表中的酚醛基元就是一个代表,这些基元称为三向功能基元,即它可以和其余基元和基团形成空间三维的分子结构,这将在稍后讨论。
为了方便查阅,表1.3中列出了一些常见的高分子化合物和基元。
表1.3 常见的高分子化合物和基元序号中文名英文名简称结构基元1 2 3 4 5 6聚乙烯聚氯乙烯聚四氟乙烯聚丙烯聚苯乙烯聚甲基丙烯酸甲酯polyethylenepolyvinyl chloridepolytetrafluo-roethylenepolypropylenepolystyrenepolymethyl methacrylatePEPVCPTFEPPPSPMMAF FCHHCHHCHClCHH CHHCHHCHHCHHCHHCHHCHHCHH基元C C C C C C C基元F F F FF F F FF F F FF F F FCCHHHClCHHHClCHHHClCHHHCl基元C C C CCHHHCH3CHHHCHHHCHHHCH3CH3CH3基元CCCC7 8(有机玻璃) 酚醛塑料 尼龙66Phenol-formaldehyde polyhexamethyleneadipamidebakelite nylon661.5分子量在高分子物质中,分子链很长,因此有很大的分子量,但是在高分子物质的合成过程中,可存在一个分子链长短不一的一系列从大到小的分子群,也就是说可以有不同长短的链状分子分布,或从分子量上说就是有一定的分子量分布。
通常需确定一个平均分子量,可以通过测量粘度和渗透压的方法加以测定。
一般可用两种平均分子量的概念来描述平均分子量。
第一种定义称为数均分子量,设M 为总重量,M 1,M 2,...,M i ,...分别是分子中值链长为n 1,n 2,...n i ...范围内的分子的平均(中值)分子量,数均分子量W n 定义为:niiM X M =∑(1)其中X i 是中值链长为n i 的分子数量百分比。
同理可定义重均分子量为:Wi i MW M =∑ (2)其中W i 是中值重量为M i 的分子的重量百分比。
另外还可以用平均链长来表是分子的聚合度,定义为平均分子量和基元质量的比值:mM ii=n (3)其中i =n 或w ,它标志着以基元长度标定的平均链长度,其中m 是基元质量。
显见,不同定义的平均分子量是不会完全相同的,因此分子聚合度的量值也随定义而略有不同。
例题:假定聚氯乙烯的分子量分布由图1.8(a)、(b)和相应的数表1.4(a)、(b)给出。
试求其:(a) 数均分子量和重均分子量;(b) 数均聚合度。
(a )分子量和数量百分比 (b )分子量和重量百分比图1.8 某聚氯乙烯材料分子量分布图解:a) 数均分子量和重均分子量见表1.4。
表1.4分子量g/mole 中值M i (g/mole)x i x i M i 5000—1000075000.0537510000—15000 15000—20000 20000—25000 25000—30000 30000—35000 35000—40000 12500 17500 22500 27500 32500 37500 0.16 0.22 0.27 0.20 0.08 0.02 2000 3850 6075 5500 2600 750 分子量g/mole 中值M i (g/mole)W i W i M i 5000—10000 10000—15000 15000—20000 20000—25000 25000—30000 30000—35000 35000—40000 7500 12500 17500 22500 27500 32500 375000.02 0.10 0.18 0.29 0.26 0.13 0.02150 **** **** 6525 7150 4225 750b)m g m o l e=⨯+⨯+=21201310135456250....(/) 许多高分子物质的性质都随分子量增加而有所改变,比如,分子量在100克/摩尔以下时,在标准条件下,有机物常处于气态,在1000克/摩尔以下,有机物常呈蜡状。
