双光子吸收截面
双光子荧光概述.

一个虚能态 , 通过两个光子的
能量进行叠加而使处于基态的 电子达到激发态。
Has not been difficult, then does not have attains
Has not been difficult, then does not have attains
荧光物质在吸收了与其能级结 构匹配的能量后,电子由基态
S0 被激发至激发态 S1 ,经过辐
射跃迁后电子又回到基态 S0 , 这一过程中发射出荧光。与单 光子荧光不同,双光子吸收过 程中,基态与激发态之间存在
目录
1.研究背景
2.基本原理
3.特点及优点
4.应
用
Has not been difficult, then does not have attains
1 双光子荧光背景介绍
双光子吸收是指在强光激发下,介质分子同时吸收两 个光子,从基态跃迁到两倍光子能量的激发态的过程。 早在1931年, Gppert Mayer 就在理论上预言了双光
双光子荧光产生原理:荧光分子吸收第一个光子后,跃迁 到虚能级上,该能级仅能存在几飞秒,便自动返回基态, 第二个光子必须在这几飞秒内与虚能级上的分子作用,从 基态跃迁到激发态,能量较大的激发态分子,通过内转换
使自己回到最低电子激发态的最低振动能级。处于此能级
的分子不是通过内转换的方式来消耗能量,回到基态,而 是通过发射出相应的光量子来释放能量,回到基态的各个 不同的振动能级时,就发射荧光。
子吸收的存在。
直到上世纪60年代初激光器出现后,才由Kaiser等首 先从实验上证实了双光子吸收过程。然而,由于一般材料 的双光子吸收截面很小,双光子吸收的实际应用受到限制, 使双光子吸收研究一直停留在基础研究水平。
双光子吸收——精选推荐
4.3 双光子吸收用红宝石激光照射掺铕的氟化钙晶体时,探测其荧光光谱时发现了红宝石激光的倍频光谱。
但是1、该材料不存在与单个红宝石激光光子对应的任何激发态,因此不能用连续吸收两个红宝石激光光子来解释;2、该材料为立方晶体,具有反演对称性,因此不存在(2)χ,不会出现二次谐波的频率。
唯一的解释是同时吸收了两个光子。
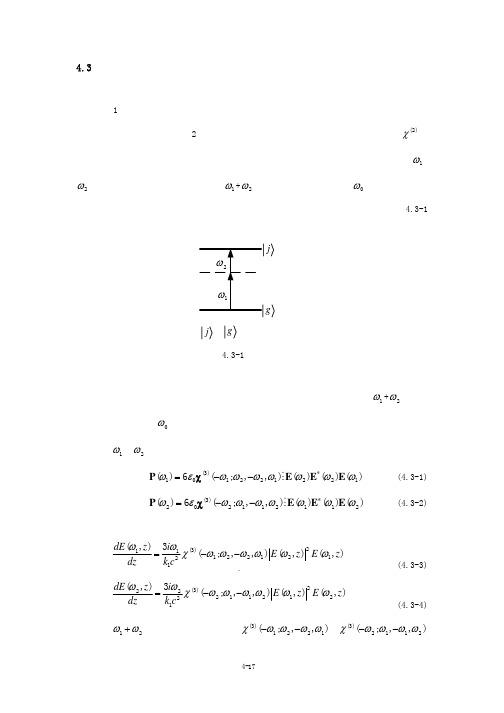
更一般地,当频率分别为1ω、2ω的两束光通过非线性媒质时,如果1ω+2ω接近媒质的某个跃迁频率0ω,媒质就会从每一束光波中同时各吸收一个光子,而引起两束波的同时衰减,这就是双光子吸收,如图4.3-1所示。
j g 宇称相同图4.3-1 双光子共振设媒质中只传输两束光,而且没有二阶非线性效应,或者不满足产生和频、差频和二次谐波相对应的相位匹配条件,同时不满足产生三次谐波的相位匹配条件,而1ω+2ω对应与媒质的某个跃迁频率0ω。
这时只需考虑辐射场之间的耦合作用所产生的结果,所以必须考虑频率为1ω和2ω的三阶非线性极化强度:(3)*101221221()6(;,,)()()()χ=−−P E E E M ωεωωωωωωω (4.3-1)(3)*202112112()6(;,,)()()()χ=−−P E E E M ωεωωωωωωω (4.3-2)耦合方程:2(3)1112212121(,)3(;,,)(,)(,)dE z i E z E z dz k c ωωχωωωωωω=−− (4.3-3) 2(3)2221121221(,)3(;,,)(,)(,)dE z i E z E z dz k c ωωχωωωωωω=−− (4.3-4) 由于12+ωω接近媒质共振频率,因此(3)1221(;,,)−−χωωωω,(3)2112(;,,)−−χωωωω.中的实部与虚部都应当是有限值,在方程中都必须考虑。
非线性极化率的实部具有完全对易对称性,即:Re{(3)2112(;,,)−−χωωωω}=Re[(3)1221(;,,)−−χωωωω]=χ (4.3-5) 非线性极化率的虚部,可以从式(1.3-23)得到:4(3)212211************Im (;,,)Im {[()()(0)]}23()()()()−=+−+++×−−+Ne B A F F F m F F F F χωωωωωωωωεωωωωωω 2201()=−−F i ωωωΓω由于1ω+2ω≈0ω,因此1ω,2ω,12−ωω都远离共振频率0ω,这样(0)F 、12()−F ωω、2()F ω、1()F ω等都是实数,这样:42(3)221221121230(3)2112Im (;,,)()()Im ()3Im (;,,)Ne A F F F m χωωωωωωωωεχωωωω−−=+=−− 因此,令:Im[(3)2112(;,,)−−χωωωω]=Im[(3)1221(;,,)−−χωωωω]=TA χ (4.3-6)由此可见,不仅极化率张量(3)2112(;,,)ωωωω−−χ和(3)1221(;,,)ωωωω−−χ的虚部相同,而且还与与跃迁频率接近0ω的上下两能级之间的集居数密度差有相同的符号。
双光子吸收法-概念解析以及定义

双光子吸收法-概述说明以及解释1.引言1.1 概述双光子吸收法是一种用于研究和探索材料和分子结构的前沿技术。
随着科学技术的不断发展,双光子吸收法已成为物理化学领域中一个重要的研究手段。
通过该方法,我们可以更深入地了解物质内部的复杂结构和性质,从而为材料科学、化学生物学等领域的研究提供有力支持。
双光子吸收法的原理相对复杂,但简单来说,它是利用两个光子同时作用于分子或材料时的吸收现象。
与传统的单光子吸收法不同,双光子吸收法能够提供更高的分辨率和更准确的结果。
其基本原理是两个光子在同时作用于目标物质上时,能量的总和正好等于目标分子的激发能级的能量。
因此,通过测量吸收光的强度和频率,我们可以得到目标物质的结构和性质信息。
双光子吸收法在许多领域中具有广泛的应用。
例如,在材料科学中,它可以用来研究纳米材料的光学和电子性质,以及材料的非线性光学行为。
在化学生物学领域,双光子吸收法可以用于研究生物分子的结构和功能,以及分子与细胞相互作用的过程。
此外,它还被广泛应用于光子学、光催化、光电子学等领域。
然而,双光子吸收法也存在一些局限性。
首先,由于双光子吸收过程的低概率性,它通常需要较高的光强和长的激光脉冲宽度,这限制了其在实际应用中的灵活性和可行性。
其次,鉴于双光子吸收法的复杂性和技术要求,研究人员需要具备较高的实验技能和仪器设备,这也限制了其在广泛领域的推广和应用。
总之,双光子吸收法作为一种先进的研究手段,为我们研究材料和分子结构提供了新的途径和突破口。
通过深入了解其原理和应用领域,我们能够更好地发挥它在科学研究和技术创新中的作用,并为未来的研究方向提供更广阔的空间。
1.2 文章结构本文将按照如下结构来展开对双光子吸收法的介绍和分析:第一部分是引言部分,其中包括对双光子吸收法的概述,即双光子吸收法的基本原理、应用领域以及它在科学研究和工程实践中的重要性。
同时,引言部分也会明确文章的结构和目的。
第二部分是正文部分,将重点介绍双光子吸收法的原理。
双光子吸收技术

双光子吸收技术双光子吸收技术(Two-photon absorption, TPA)是一种基于非线性光学效应的先进技术,具有广泛应用前景。
本文将介绍双光子吸收技术的原理和应用领域,并探讨其在科学研究和工程应用中的发展前景。
一、双光子吸收技术的原理双光子吸收技术是指当两个光子几乎同时与目标物质相互作用时,它们的能量叠加在一起,达到目标物质电子激发的能量阈值,从而引发非线性光学过程。
相比于单光子吸收技术,双光子吸收技术具有以下几点优势:1. 较高的空间分辨率:由于双光子吸收过程具有非常小的横向光强分布,使得在高分辨显微镜成像中能够获得更清晰、更精确的图像。
2. 较低的光损伤风险:双光子吸收技术采用红外光源,较短的波长可以减少光敏感材料的光损伤风险,提高材料的使用寿命。
3. 较大的穿透深度:红外光在生物组织中的穿透深度较大,可以实现对生物样本内部结构的观察和研究。
二、双光子吸收技术的应用领域双光子吸收技术在众多领域中具有重要的应用价值。
以下是其中几个典型的应用领域:1. 生物医学研究:双光子显微镜可以实现对生命体内动态过程的实时观察,例如细胞内亚细胞器的运动、荧光标记的蛋白质等。
这为生物医学研究提供了有力的工具。
2. 材料科学:双光子聚合技术可以实现微纳结构的精确制备,从而在材料科学领域发挥重要作用。
例如,通过控制双光子吸收过程可以实现高性能的光子晶体、光学波导和传感器等。
3. 光子学器件:双光子吸收技术可以用于制备各种光子学器件,包括非线性光学晶体、光学调制器和光电探测器等。
这些器件在光通信、光存储和光计算等领域有着广泛的应用。
三、双光子吸收技术的未来发展双光子吸收技术在科学研究和工程应用中具有巨大的潜力。
随着技术的不断发展,我们可以期待以下几个方面的进一步突破:1. 新型光源的研发:目前,红外激光仍然是双光子吸收技术的主要光源,但其成本较高,体积较大。
研究人员正在积极寻求更便携、更高效的光源,以推动技术的广泛应用。
有机杂环分子的双光子吸收特性

近年来, 双光子吸收截面大的材料在三维光信 息存储 、 双光子荧光显微和成像 、 光学微加工 、 频率 上 转 换激 射 、 限幅 以及 光生 物 学 等方 面 显示 出 的 光 良好应用前景【】 l, - 使得从理论 和实验上寻找 、 3 合成
i o tn a a fc a g g o lcrn d a n ru .T i id o lc l a etrTP (wo p oo mp r ttn t to h i fee t r wig g o p h skn fmoe ue h d a b t A t ・h tn a h h n n o e
具 有 大 的 双光 子 吸 收截 面 的材 料 以及 了解 分 子 结 构 与性 能 的关 系成 为 材料 学 、 电子 学 等领 域 研究 光
的热 点.
素有 关 . 按供 吸电子 的性质划 分, 官能 团分 为给体( ) D 和受体 ( 两类 . 称分 子是 指分 子 两端 的官 能 团 同 A】 对
( ol e f hs s n l t nc, hn ogN r a nvri, i n 2 0 1 , . hn ) C l g P yi d e r i S a d n om l iesy J a 5 0 4 P R C ia e o ca E co s U t n
Abs r c : ta t T e n n ie ro t a r p riso r eb n o h a o y . e v t e e y s nhe ie r ac lt d h o l a pi l o e t ft e e z t iz l 1d r a i sn wl y t s d we e c lu a e n c p e h i v z
双光子显微镜

双光子显微镜/view/1428311.htm?fr=ala0_1双光子荧光显微镜是结合了激光扫描共聚焦显微镜和双光子激发技术的一种新技术。
双光子激发的基本原理是:在高光子密度的情况下,荧光分子可以同时吸收 2 个长波长的光子,在经过一个很短的所谓激发态寿命的时间后,发射出一个波长较短的光子;其效果和使用一个波长为长波长一半的光子去激发荧光分子是相同的。
双光子激发需要很高的光子密度,为了不损伤细胞,双光子显微镜使用高能量锁模脉冲激光器。
这种激光器发出的激光具有很高的峰值能量和很低的平均能量,其脉冲宽度只有100 飞秒,而其周期可以达到80 至100 兆赫。
在使用高数值孔径的物镜将脉冲激光的光子聚焦时,物镜的焦点处的光子密度是最高的,双光子激发只发生在物镜的焦点上,所以双光子显微镜不需要共聚焦针孔,提高了荧光检测效率。
双光子荧光显微镜有很多优点:1)长波长的光比短波长的光受散射影响较小容易穿透标本;2)焦平面外的荧光分子不被激发使较多的激发光可以到达焦平面,使激发光可以穿透更深的标本;3)长波长的近红外光比短波长的光对细胞毒性小;4)使用双光子显微镜观察标本的时候,只有在焦平面上才有光漂白和光毒性。
所以,双光子显微镜比单光子显微镜更适合用来观察厚标本、更适合用来观察活细胞、或用来进行定点光漂白实验。
激光共聚焦显微镜在进行生物样品研究工作中还存在很多局限和问题:一是标记染料的光漂白现象。
因为共焦孔径光阑必须足够小以获得高分辨率的图像,而孔径小又会挡掉很大部分从样品发出的荧光,包括从焦平面发出的荧光,相应的,激发光必须足够强以获得足够的信噪比;而高强度的激光会使荧光染料在连续扫描过程中迅速褪色,荧光信号会随着扫描进程度进行变得越来越弱。
光毒作用是另外一个问题,在激光照射下,许多荧光染料分子会产生诸如单态氧或自由基等细胞毒素,所以实验中要限制扫描时间和激发光的光功率密度以保持样品的活性。
在针对活性样品的研究中,尤其是活性样品生长、发育过程的各个阶段,光漂白和光毒现象使这些研究受到很大的限制。
高聚物双光子吸收材料研究进展

随之 引起 的物理 和化学 变化 都发 生在 该体 积 内 , 而 在 其 他 位 置 的光 强 不 足 以发 生 双 光 子 吸 收 。 双光 子的 吸收能力 由吸收 截面值 表示 。
维普资讯
现 代 塑 料 加 工 应 用
200 7年 第 19 卷 第 3 期
M 0DERN I ASTI P CS PROCESS NG ND I A APP CAT1 II 0NS
高 聚 物双 光 子 吸收 材 料 研 究 进展 *
s p i n pr pe t a e e e or to o r y w s r viw d.
Ke r s t — h t n a s r to c nu a e ywo d :wo p o o b o p in;o j g td;p l me ;a s r t n s c in oy r b o p i e t o o
种 现象 。双光 子 吸 收是 一 种 重 要 的光 学 非 线 性
效应 。在 双光 子吸 收过程 中 , 子 能 同时 吸 收 2 分
个光 子 , 基 态 S 从 O到 达 第 二 激 发态 S , 由第 2再
二激 发态 S 2无辐 射 跃迁 到 第 一激 发态 S 1后 发 出荧 光 ( loe cn ) F u rse e 。双 光 子 吸 收几 率 与 入射 光光 强 的平方 成 正 比 , 在密 聚 焦 的条 件 下 , 收 吸
Ab t a t : sr c The p l me s wih t — ho o bs p i n pr pe t o d be us d a im — o y r t wo p t n a or to o r y c ul e s fl be c us he rhi n e iy a d t na iy The a plc to fp y e swih t — ho o b a eoft i gh i t nst n e ct . p ia ins o ol m r t wo p t n a — s p i n we e i r uc d or to r ntod e .The r s a c d v l pme t of t ol me s wih t — ot b ee r h e eo n he p y r t wo ph on a —
一种新型双光子吸收材料的合成、光学性质及生物成像

一种新型双光子吸收材料的合成、光学性质及生物成像李宁宁;宁鹏;冯燕;孟祥明【摘要】A novel naphthalimide derivative, N-(morpholinoethyl)-4-(4-ethynyl-phenol)-1, 8-naphthalimide (A) was synthesized by Sonogashira couple reaction by using 4-bromo-1, 8-naphthalicanhydride as the raw material. Its molecular structure was characterized by 1H NMR, 13C NMR and HR-MS (ESI). By analyzing the fluorescence emission spectra of compound A in six different polar organic solvents andmethanol/tetrahydrofuran mixed solvents, along with the two-photon induced fluorescence spectra of A in tetrahydrofuran, the results showed that it has a significant response to the polarity with a solvatochromic effect. With the increase in solvent's polarity, the fluorescence emission peak of A is red-shifted and the fluorescence intensity is decreased. The two-photon absorption action cross section of A at 820 nm is 90 GM. In addition, A could be successfully localized to lysosomes, and the co-localization coefficient with lysosome commercial dye Lyso Tracker Red is as high as 0.902 6. Therefore, compound A as a novel two-photon absorption material could be used as a two-photon lysosomal tracking agent for cell imaging.%以4-溴-1, 8-萘二甲酸酐为起始原料通过Sonogashira 偶联反应合成了一种新型萘酰亚胺衍生物 (N-吗啉乙基)-4-(4-羟基苯乙炔基)-1, 8-萘酰亚胺 (A), 其结构通过1H NMR、13C NMR、HR-MS (ESI) 表征, 并对化合物A在6种不同极性有机溶剂和甲醇/四氢呋喃混合溶剂中的荧光发射光谱, 以及A 在四氢呋喃中的双光子诱导荧光光谱进行了分析.结果表明:A具有溶质变色效应, 随溶剂极性的增大, A的荧光发射峰发生红移, 且荧光强度下降.并且A在波长820 nm处的有效双光子吸收截面为90 GM.此外, A可成功定位于溶酶体, 与溶酶体商品化染料Lyso Tracker Red的共定位系数高达0.902 6.因此, 化合物A作为一个新型的双光子吸收材料, 可作为双光子溶酶体示踪剂用于细胞成像.【期刊名称】《安徽大学学报(自然科学版)》【年(卷),期】2019(043)002【总页数】7页(P82-88)【关键词】萘酰亚胺;溶致变色;极性;双光子吸收;生物成像【作者】李宁宁;宁鹏;冯燕;孟祥明【作者单位】安徽大学化学化工学院, 安徽合肥 230601;安徽大学化学化工学院, 安徽合肥 230601;安徽大学化学化工学院, 安徽合肥 230601;安徽大学化学化工学院, 安徽合肥 230601【正文语种】中文【中图分类】O625.31.31,8-萘酰亚胺及其衍生物作为一种性能良好的有机材料, 被广泛应用于聚合物工业着色剂、荧光增白剂、激光染料、二极管、液晶添加剂、荧光细胞标记物以及潜在抗癌药物方面的研究[1-4]. 由于其具有荧光量子产率高、光学性稳定、对溶液pH 不敏感[5-8]、良好的双光子吸收性能[9]等优点, 而被广泛用于双光子吸收材料的设计[10]. 尤为重要的是, 1, 8-萘酰亚胺及其衍生物在结构上易于修饰, 在其分子中的4号位碳上可以引入不同的功能性基团, 从而得到具有不同功能的材料. 因此对1,8-萘酰亚胺及其衍生物的设计合成及性质研究成了一大热点[11].笔者以萘酰亚胺为生色团, 通过在萘酰亚胺的酰亚胺氮原子上引入具有亚细胞器溶酶体定位功能的烷基吗啉基团[12], 4号位上接入4-羟基苯乙炔, 其中4-羟基苯乙炔作为给体(D), 酰亚氨基作为受体(A)和生色团, 构建了一个典型的D-π-A结构的ICT[13-15]体系, 设计出了化合物A分子, 以期得到具有良好的光学性质和生物学应用潜能的新型双光子吸收材料. 化合物A的合成路线见图1所示.图1 目标化合物A的合成路线1 实验部分1.1 仪器与试剂Bruker Avance- 400核磁共振仪, 美国布鲁克公司; LTQ Orbitrap XL高分辨质谱仪, 赛默飞世尔科技(中国)有限公司; Tech-comp UV 1000紫外可见分光光度计, 上海天美科技有限公司; FL- 2500型荧光发射光谱仪, 日本岛津公司; Mira Optima 900F④钛宝石飞秒可调谐激光器(脉冲140 fs, 频率80 MHz), Coherent 公司; LSM 710激光共聚焦显微镜, 德国卡尔·蔡司公司.4-溴-1,8-萘二甲酸酐、N-(2-氨基乙基)吗啉、无水乙醇、N-甲基吡咯烷酮、三乙胺、碘化亚铜、三苯基膦二氯化钯、4-羟基苯乙炔, 分析纯, 上海麦克林试剂公司; 四氢呋喃、二氯乙烷、苯甲腈、正己醇、二甲亚砜、甲醇, 色谱纯, 北京安耐吉试剂公司.1.2 合成1.2.1 化合物1的合成称取4-溴-1, 8-萘二甲酸酐2.5 g(9.01 mmol)于100 mL的圆底烧瓶中, 加入无水乙醇50 mL溶解,随后加入N-(2-氨基乙基)吗啉1.3 g(10.01 mmol), 在80 ℃下回流反应5 h, 待反应结束后, 冷却至室温, 旋干无水乙醇, 用二氯甲烷萃取, 制样, 用柱色谱进行纯化, 洗脱液体系为石油醚与乙酸乙酯的体积比为2∶1, 最终得到白色固体(化合物1)3.4 g (8.62 mmol), 产率为94%. 1H NMR (400 MHz,CDCl3): δ 8.63 (dd, J = 7.3, 1.1 Hz, 1H ), 8.55 (dd, J = 8.5, 1.1 Hz, 1H), 8.39 (d, J = 7.9 Hz, 1H), 8.03 (d, J = 7.9 Hz, 1H), 7.84 (dd, J = 8.5, 7.3 Hz, 1H), 4.33 (t, J = 6.9 Hz, 2H), 3.68 (t, J =5.2Hz, 4H), 2.71 ( t, J = 6.9 Hz, 2H), 2.60 (br s, 4H). 13C NMR (100 MHz, CDCl3): δ 163.59, 163.57, 133.28, 132.02, 131.21, 131.10, 130.61, 130.30, 129.00, 128.08, 123.02, 122.15, 67.02, 56.07, 53.81, 37.30. 1.2.2 化合物A的合成在控制无水无氧的条件下, 往150 mL的斯莱克瓶中加入1.94 g的化合物1 (5.00 mmol)、4-羟基苯乙炔0.71 g (6.00 mmol)、三苯基膦二氯化钯0.05 g (0.07 mmol)、碘化亚铜0.25 g (1.3 mmol)、三乙胺1.83 g (18.1 mmol) 和N-甲基吡咯烷酮30 mL, 随后升温至80 ℃, 磁力搅拌反应15 h. 待反应结束后,抽滤,用二氯甲烷萃取, 旋干制样用柱色谱分离(v(石油醚)∶v(乙酸乙酯)=2∶1), 得到黄色固体(化合物A)1.2 g, 产率为 55%. 1H NMR (600 MHz, DMSO-d6) δ 10.17 (s, 1H), 8.74 (d, J = 8.3 Hz, 1H), 8.54 (d, J = 7.1 Hz, 1H), 8.43 (d, J = 7.6 Hz, 1H), 7.99 (d, J =7.6 Hz, 1H), 7.97 (t, J =7.8 Hz, 1H) ,7.62 (d, J = 8.5 Hz, 2H), 6.89 (d, J = 8.6 Hz, 2H), 4.18 (br s, 2H), 3.54(br s, 4H), 2.57 (br s, 2H), 2.50 (m, 4H). 13C NMR (150 MHz, DMSO-d6) δ 163.65, 163.35, 159.51, 134.27, 132.49, 131.69, 131.10, 130.71, 130.60, 128.53, 127.79, 127.50, 122.87, 121.56, 116.43, 111.92, 100.61, 85.15, 66.51, 55.87, 53.73, 37.18. ESI-MS m/z: Calc-d forC26H22N2O4 { [M + H]+ } 427.158 0, found, 427.165 0.2 结果与讨论2.1 化合物A在不同极性溶剂中的光学性能研究笔者首先选取了6种不同大小的极性溶剂(四氢呋喃、二氯乙烷、苯甲腈、正己醇、二甲亚砜、甲醇), 分析A分子在不同溶剂中的光谱数据, 测试浓度均为10 μM ,结果如表1、图2所示.表1 化合物A在不同溶剂中的光谱数据溶剂λabs/nmλem/nmΔλ/nmφτ/ns四氢呋喃399492930.312.02二氯乙烷3994991000.271.71苯甲腈4015101090.211.60正己醇4005161160.161.40二甲亚砜4005291290.090.57甲醇4005471470.060.30注:λabs 为紫外最大吸收波长;λem为荧光最大发射波长;Δλ为斯托克斯位移;φ为荧光量子产率(以硫酸奎宁为参比);τ为荧光寿命.图2 化合物A(10 μM) 在不同溶剂中的紫外吸收光谱(a)及荧光发射光谱(b)由图2(a)可知,化合物A在不同极性溶剂中的紫外吸收峰位置维持在400 nm左右, 基本不变. 图2(b)显示, 在最弱极性溶剂四氢呋喃中, A的最大荧光发射峰在500 nm , 而在溶剂极性最强的甲醇中A的荧光最大发射峰在540 nm , 随着溶剂极性的增大, A相对应的荧光最大发射峰发生红移, 从极性最弱的四氢呋喃到最强的甲醇红移了40 nm . 另外A分子的荧光强度也受到溶剂极性的影响, 在最弱极性溶剂四氢呋喃中荧光强度最强, 而在最强极性溶剂甲醇中荧光强度则最低. 其中A在四氢呋喃中的荧光发射强度是其在甲醇中的7倍, 从而说明了A具有溶致变色效应[16]. 同时在不同溶剂中A的量子产率和荧光寿命均表现出与荧光强度相一致的变化趋势, 其中在四氢呋喃中, A的量子产率为0.31, 荧光寿命为2.02 ns, 而在甲醇中A的量子产率降低到了0.06 , 荧光寿命减小到0.3 ns. 出现以上现象主要是因为A分子中吸电子的酰亚胺基团与供电子的4-羟基苯乙炔共轭连接形成了强的推拉电子结构, 分子在激发态时容易产生分子内电荷转移形成ICT态. 在这种机制下A分子在极性溶剂中的能量会剧烈降低, 导致荧光发射波长向长波方向移动, 产生红移[17], 同时会伴随着荧光量子产率和荧光寿命的降低. 以上结果表明,A分子具有溶致变色效应.2.2 A在四氢呋喃-甲醇混合极性体系中的光学性能研究为了进一步证明A具有溶致变色效应, 笔者选取四氢呋喃和甲醇混合的极性体系, 进一步测定A分子在不同体积百分比的四氢呋喃与甲醇的混合溶剂的紫外吸收光谱和荧光发射光谱,结果如图3所示.图3 化合物A(10 μM) 在甲醇-四氢呋喃混合溶剂中的紫外吸收光谱(a),百分数代表混合溶剂中甲醇的体积含量)和荧光发射光谱(b)图3(a)显示,随着甲醇的含量从10% 逐渐增加到70% , 极性的改变没有对A的紫外吸收光谱造成明显影响, 基本稳定在400 nm 左右. 由图3(b)所示, 随着混合体系中甲醇含量的逐渐增加, 体系的极性逐渐增加, A的荧光最大发射峰从515 nm 到533 nm逐渐红移了18 nm , 并在红移的过程中荧光强度降低了大约3倍, 荧光强度随着极性的增加而逐渐降低. 这些现象均与A在不同溶剂中的行为是一致的. 综上表明,A具有溶致变色效应.此外, 笔者还对比了化合物1和化合物A在四氢呋喃中的紫外-可见吸收光谱和荧光发射光谱. 如图4所示.图4 化合物1和化合物A在四氢呋喃中的紫外-可见吸收光谱和荧光发射光谱图图4显示,化合物1的2个主要紫外吸收峰分别位于338 nm 和354 nm , 化合物A的最大紫外吸收峰位于399 nm, A相对于化合物1的2个紫外吸收峰分别发生了61 nm和45 nm的红移. 同时化合物1在四氢呋喃中的荧光发射强度接近0, 几乎不发射荧光, 而化合物A在四氢呋喃中荧光发射峰的相对强度远大于化合物1. 通过该实验证明,笔者通过结构设计, 增大萘酰亚胺生色团的共轭体系, 构建了一个典型的D-π-A结构的A分子, 赋予了A分子潜在的双光子吸收性能.2.3 化合物A的双光子吸收性能测试为了研究A的双光子吸收性能, 笔者采用参比法[18]对其有效双光子吸收截面进行测定,其中所用标准物质是用pH=11的氢氧化钠的水溶液配制的荧光素, 其不同波长的双光子吸收截面值可查阅相关文献[19].所有测试溶液浓度均为1.0×10-3 mol·L-1. 图5所示为A分子在四氢呋喃中的双光子吸收性能测试结果.嵌入:随着输入功率的增加 ( Iin = 300-800 mW) 与双光子荧光激发强度 (Iout) 的面积相关关系.图5 化合物A在四氢呋喃中的有效双光子吸收截面由图5可以看出,A分子在780 nm到900 nm之间使用飞秒激发器激发都能够发射双光子诱导荧光. 用820 nm飞秒激光为激发光源, 入射能量为0.5 W时, 化合物A出现了最大的有效双光子吸收截面, 达到了90 GM.波长设定为820 nm, 测试四氢呋喃为溶剂的A在不同入射光强度下的双光子荧光光谱,通过进一步对A的双光子吸收性能进行实验验证(图5嵌入图),发现当输入功率从0.3 W逐渐增加到0.8 W时, A的双光子诱导荧光强度(Iout)的面积与输入功率(Iin)之间符合良好的平方关系, 线性斜率为2.01 , 符合双光子吸收性质的规律. 以上实验数据充分说明了A具有良好的双光子吸收性质.2.4 A分子的细胞毒性测试在进行有关生物学应用研究之前有必要进行细胞毒性的测试.采用MTT法[20] 对分子A进行细胞毒性测试, 结果如图6所示.图6 化合物A的细胞毒性测试由图6可以看出,MCF-7细胞在加入10 μM分子A培养24 h之后, 细胞存活率仍然可以达到95%. 因此, 分子A可以在MCF-7细胞中进行生物学方面的应用研究.2.5 分子A的细胞共定位实验为了得到A在溶酶体中的实际定位效果, 首先将其(10 μM)加入MCF-7细胞培养液中进行MCF-7细胞培养约半小时后, 随后向其中加入溶酶体染料Lyso Tracker Red (0.5 μM), 继续培养大约20 min, 经过一系列后续处理后,进行共聚焦荧光成像实验, 结果如图7所示.(a):分子A的荧光发射通道1((520±20) nm), 双光子激发光波长为820 nm;(b): 定位溶酶体的商品化示踪剂Lyso-Tracker Red的荧光发射通道2((600±10) nm), 激发光波长为559 nm;(c): 通道1和通道2的叠加图;(d): 分子A和Lyso-Tracker Red在细胞中荧光强度的散点图.图7 乳腺癌细胞(MCF-7)的共聚焦成像图图7显示,分子A与溶酶体染料Lyso Tracker Red两者在细胞溶酶体中具有大的共定位系数(0.902 6), 证明分子A具有选择性定位于细胞溶酶体的生物应用潜能, 即分子A能够作为一种潜在的双光子的溶酶体示踪剂.3 结束语笔者基于萘酰亚胺为生色团设计合成了一种新型的萘酰亚胺衍生物A, 同时A的结构得到了表征. 另外在结构设计上构建了以萘酰亚胺为生色团的典型的D-π-A结构, 通过引入供电子基团增大分子的共轭体系, 设计出具有双光子吸收性能的分子A. 通过对A分子的光学性质进行测试, 表明其在不同溶剂及混合溶剂体系中均对极性表现出了良好的信号响应, 证明A具有溶致变色效应. 同时通过对A分子在四氢呋喃中双光子吸收截面的计算和进行双光子验证, 充分证明了A分子具有较好的双光子吸收性能, 是一个新型的具有良好双光子吸收性能的荧光材料. 另外, 分子A中的吗啉基团具有亚细胞器定位功能, 通过细胞共定位实验, 证明了其能够定位于细胞溶酶体, 即能够作为一种潜在的双光子的溶酶体示踪剂.参考文献:【相关文献】[1] JIANG W, SUN Y M, WANG X L, et al. Synthesis and photochemical properties ofnovel4-diaryla- mine-1, 8-naphthalimide[J]. Dyes and Pigments, 2008, 77 (1): 125-128. [2] MIAO L F, YAO Y L, YANG F, et al. A TDDFT and PCM-TDDFT studies on absorption spectra of N-substituted 1, 8-naphthalimides dyes[J]. Journal of Molecular Structure: THEOCHEM, 2008, 865 (1/2/3): 79-87.[3] JIN R F, TANG S S. Theoretical investigation into optical and electronic properties of 1, 8-naphthalimide derivatives[J]. Journal of Molecular Modeling, 2013, 19 (4): 1685-1693. [4] WEI S, SUN Y, GUO P, et al. A novel 4- (tetrahydro-2-furanmethoxy)-N-octadecyl-1, 8-naphthalimide based blue emitting probe: solvent effect on the photophysical properties and protein detection[J]. Russian Journal of Bioorganic Chemistry, 2012, 38 (5): 469-478. [5] WANG C C, ZHENG X L, HUANG R, et al. A 4-amino-1, 8-naphthalimide derivative for selective fluorescent detection of palladium (II) ions[J]. Asian Journal of Organic Chemistry, 2012, 1 (3): 259-263.[6] KAI Y M, HU Y H, WANG K, et al. A highly selective colorimetric and ratiometric fluorescent chemodosimeter for detection of fluoride ions based on 1, 8-naphthalimide derivatives[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2014, 118: 239-243.[7] ZHANG J F, LIM C S, BHUNIYA S, et al. A highly selective colorimetric and ratiometric two-photon fluorescent probe for fluoride ion detection[J]. Organic Letters, 2011, 13 (5): 1190-1193.[8] LIU T Y, ZHANG X F, QIAO Q L, et al. A two-photon fluorescent probe for imaging hydrogen sulfide in living cells[J]. Dyes and Pigments, 2013, 99 (3): 537-542.[9] QIAN X H, XIAO Y, XU Y F, et al. “Alive” dyes as fluorescent sensors: fluorophore, mechanism, receptor and images in living cells[J]. Chemical Communications, 2010, 46 (35): 6418-6436.[10] 祝新月, 张海霞. 基于萘酰亚胺骨架的双光子荧光探针构建及应用[J]. 化学传感器, 2016, 36 (4): 1-14.[11] 王启, 蒋伟, 王小亮, 等. 1, 8萘酰亚胺类有机小分子电致发光材料的研究进展[J]. 化工时刊, 2007, 21 (8): 66-70.[12] JIANG J C, TIAN X H, XU C Z, et al. A two-photon fluorescent probe for real-time monitoring of autophagy by ultrasensitive detection of the change in lysosomal polarity[J]. Chemical Communications, 2017, 53 (26): 3645-3648.[13] LOVING G, IMPERIALI B. A versatile amino acid analogue of the solvatochromic fluorophore 4-N, N-dime- thylamino-1, 8-naphthalimide: a powerful tool for the study of dynamic protein interactions[J]. Journal of the American Chemical Society, 2008, 130 (41): 13630-13638.[14] HUANG C S, YIN Q, ZHU W P, et al. Highly selective fluorescent probe for vicinal-dithiol-containing proteins and in situ imaging in living cells[J]. Angewandte Chemie International Edition, 2011, 50 (33): 7551-7556.[15] AMIN F, YUSHCHENKO D A, MONTENEGRO J M, et al. Integration of organic fluorophores in the surface of polymer-coated coll-oidal nanoparticles for sensing the local polarity of the environment[J]. Chemphyschem A European Journal of Chemical Physics & Physical Chemistry, 2012, 13 (4): 1030-1035.[16] 吴世康. 具有荧光发射能力有机化合物的光物理和光化学问题研究[J]. 化学进展, 2005, 17 (1): 15-39.[17] 胡金虎, 沈宏, 田玉鹏, 等. 2-苯硼酸基-4, 6双(4-N, N-二乙基苯乙烯基)嘧啶的合成及光学性质[J]. 安徽大学学报 (自然科学版), 2014, 38 (4): 73-78.[18] AlBOTA M A, XU C, WEBB W W. Two-photon fluorescence excitation cross sections of biomolecular probes from 690 to 960 nm[J]. Applied Optics, 1998, 37 (31): 7352-7356. [19] MAKAROV N S, DROBIZHEV M, REBANE A. Two-photon absorption standards in the 550 - 1 600 nm excitation wavelength range[J]. Optics Express, 2008, 16 (6): 4029-4047.[20] YAO D F, LIN Z, WU J C. Near-infrared fluorogenic probes with polarity-sensitive emission for in vivo imaging of an ovarian cancer biomarker[J]. Acs Applied Materials & Interfaces, 2016, 8 (9): 5847-5856.。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2:待测样品 F:双光子诱导荧光强度 φ:荧光量子效率 c:样品浓度 L:样品通光长度
N:荧光团数密度
10
K:无量纲常数
编辑ppt
双光子诱导荧光法(上转换荧光法)
准确度高,但是必须首先测出样品的荧光量子 效率,准确度很大程度上依赖于所选择标准样 品。
对实验光学装置要求较高。尤其对荧光收集系 统,必须保证两次测量荧光时的荧光收集效率 是相同的。
5
TN
1n1I0L
I0L
TN
1
1 I0L
←均匀光束
TN
1n1I0L
I0L
←高斯光束
h Nc
编辑ppt
非线性透过率法
优点:实验装置简单,测量方便,处理数据容易。
缺点:
(1)待测介质浓度高时,线性吸收会比较大。
(2)入射光强度很高时,其它机制的吸收会对非 线性吸收过程有贡献。
(3)当受激辐射、放大自发辐射、光散射等过程 有重要影响时,δ比实际值偏小;当激发态吸收 等过程有重要影响时,δ比实际值偏大。
12
编辑ppt
双光子瞬态吸收光谱法
根据以下公式可得到待 测样品的双光子吸收截 面:
2
1
AA12 12eexx
1gr 2gr
c1 c2
1:标准样品 2:待测样品 ΔA:双光子激发下瞬态吸收为最 大的波长λmax处的吸收变化值 c:样品浓度 σ: λmax处单光子吸收截面
13
编辑ppt
谢谢大家!
14
由于荧光强度和激发强度之间为平方关系,根 据其偏离程度,可以进一步减小激发光强,以 避免这些效应对测量双光子吸收的影响。
9
编辑ppt
双光子诱导荧光法(上转换荧光法)
比较待测样品和标准样品(具有已知δ)的双光子诱 导荧光,求得待测样品的δ。
1:标准样品
F K NLI2
2
2
1
F2 F1
1 2
c1 c2
编辑ppt
dI 2
dz
式中:
2 3 0c2n2
通常,双光子吸收的强弱用双光子吸收截面δ 来表示:
h Nc
Nc为单位体积的分子数
3
编辑ppt
测量双光子吸收截面的方法
非线性透过率法 Z-扫描方法 双光子诱导荧光法(上转换荧光法) 双光子瞬态吸收光谱法
4
编辑ppt
非线性透过率法
通过改变入射光强的强度, 得到随入射光强变化的非 线性透过率。用公式对实 验中获得的随入射光强变 化的非线性透过率数据进 行拟合,求得非线性介质 的双光子吸收系数β,并可 进一步求得双光子吸收截 面δ。
难以测出非荧光材料的双光子吸收截面。
11
编辑ppt
双光子瞬态吸收光谱法
由激发态泵浦-探测瞬 态吸收光谱法发展而来, 是唯一能精确测出非荧 光材料双光子吸收截面 的方法。
能将直接的双光子吸收 和通过中间实能级实现 的连续分布吸收区分开 来。
和双光子诱导荧光法类 似,该方法也是通过比 较待测样品和已知双光 子吸收截面的标准样品 来求得待测样品的δ。
8
编辑ppt
双光子诱导荧光法(上转换荧光法)
可以有效排除其它非线性效应所产生的影响, 准确地测量介质真实的双光子吸收截面:
入射光强和溶液浓度比非线性透过率法分别低 1和3个数量级,相对于双光子吸收来说,其它 非线性效应的贡献被大大减小。
利用单色仪可以把双光子诱导荧光和其它非线 性产生的效应区分开来。
关于双光子吸收截面的几种测量方法
1
编辑ppt
双光子吸收
当光束通过非线性介质 时,介质同时从光束中 吸收两个光子来激发物 质系统,引起光束的衰 减。
一种三阶非线性效应过 程,可以出现在具有对 称中心的晶体和各项同 性介质中。
2
E2
2
1
E1
编辑ppt
当两束光的频率相同或者只有光强为I的一束 光在介质中传播时,双光子吸收过程的表达 式为:
6
编辑ppt
Z-扫描方法
灵敏度高,单光束测量 缺点与非线性透过率法类似。
7
编辑ppt
双光子诱导荧光法(上转换荧光法)
对于很多有机染料分子,双光子吸收后将伴随着 荧光辐射过程,其荧光发射波长比激发光的波长 短,并且荧光强度与激发光强度之间的依赖关系 为平方关系。通过测量介质的双光子诱导荧光, 也可以得到双光子吸收截面值。
