碳的多样性练习题
高中化学《碳的多样性》同步练习4

煌敦市安放阳光实验学校碳的多样性课时作业一、选择题(包括8小题。
1~6小题只有一个选项符合题意,7~8小题有两个选项符合题意。
)1.下列各变化中,在木炭燃烧时不可能发生的反是()A.2C+O2点燃2COB.C+O2点燃CO2C.CO2+C点燃2COD.CO2=C+O22.(质检)下列有关CO2的中,只能证明CO2的物理性质的是()3.下列说法错误的是()A.铅笔芯的主要原料是石墨,儿童在使用时不会引起中毒B.CO有毒,生有煤炉的居室可放置数盆清水,这样有效地吸收CO,防止煤气中毒C.“汽水”浇灌植物有一的道理,其中CO2的缓释,有利于植物的光用D.所有的碳原子都按一的方式连成一个向空间伸展的络,而C60中每60个碳原子构成一个分子4.(质检)碳是自然界的基本构成元素之一,在自然界中,不停地转化、循环,构成了生机盎然的物质,如图为自然界中碳的循环图。
下列有关分析不合理的是()A.过程①中还可能有另外的含碳物质产生B.碳元素在自然界中的循环主要是通过CO2的生成和消耗来实现的C.加速过程②将有利于社会的可持续发展D.只有使图中所示的各转化的总体保持基本平衡,才能维持大气中CO2的含量相对稳5.(质检)用1 L 10 mol·-1LNaOH溶液吸收08 mol CO2,所得溶液中的CO32-和HCO3-的物质的量浓度之比约是()A.1∶3B.2∶1C.2∶3D.3∶26.(一中质检)将足量CO2通入KOH和Ca(OH)2的混合稀溶液中,生成沉淀的物质的量(n)和通入CO2体积(V)的关系正确的是()7.(质检)旅游洞穴一般是指供游人观览的喀斯特洞穴。
多姿多彩的石钟乳、石笋、石柱、石花碳酸钙沉积体是喀斯特洞穴中的主要景观。
由于游人呼吸有时会使旅游洞穴中二氧化碳浓度大幅度升高,可能造成的后果是()A.抑制碳酸钙沉积体的生长B.促进碳酸钙沉积体的生长C.使游客有憋闷的感觉D.使照明灯下的植物大量死亡8.近期《化志》报道,中国家以二氧化碳为碳源,金属钠为还原剂,在470 ℃、80MPa下合成出石,具有深远意义。
高一化学碳的多样性试题

高一化学碳的多样性试题1.下列气体中,均属于大气污染物的一组是( )A.CO、SO2、NO2B.N2、O2、CO2C.H2、N2、SO2D.CO、CO2、SO2【答案】A【解析】本题属于常识性题目。
常见的大气污染物有硫氧化物、碳氧化物(主要是CO,CO2不是大气污染物)、氮氧化物、碳氢化合物。
【考点】大气污染物的考查点评:对大气污染物的考查体现了化学的实用性。
另外,对于大气污染物还需考虑到这两年新提出的PM2.5(是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物。
)2012年2月,国务院同意发布新修订的《环境空气质量标准》增加了PM2.5监测指标。
2.下列离子方程式正确的是()A.钠与水反应:2Na+2 H2O = 2Na+2OH-+H2↑B.氧化钠与盐酸:O2-+2H+ = H2OC.碳酸氢钠与稀硫酸: CO32-+2H+=H2O+CO2↑D.烧碱溶液与碳酸氢钠溶液:HCO3-+OH-= H2O+CO2↑【答案】A【解析】选项A、正确。
选项B、氧化钠不能拆成离子形式。
正确应为:Na2O+2H+=2Na++H2O。
选项C、碳酸氢根离子不能拆。
HCO3-+H+=H2O+CO2↑选项D、产物错误。
HCO3-+OH-= H2O+ CO32-【考点】离子方程式的书写判断点评:判断离子方程式书写正确与否,主要可以从以下几方面入手:1、以化学反应的客观事实为依据。
如:Cu+2H+=Cu2++H22、以质量守恒定律为依据。
如:Al+3H+=Al3++H23、以离子的电荷守恒为依据。
如:Fe3++Fe=2Fe2+4、以物质的实际状态为依据。
如:BaCO3与稀盐酸的反应:CO32ˉ+2H+=H2O+CO25、以物质的组成为依据。
如:Ba(OH)2与稀硫酸的反应。
Ba2++OH-+H++SO42-=BaSO4+H2O6、以反应条件及物质的状态为依据。
如:CO32ˉ+2H+=H2O+CO23.下列各组离子能在溶液中大量共存的是( )A.HCO3―、Na+、OH―、K+B.CO32―、Ba2+、K+、NO3―C.Ba2+、OH―、Cl―、Na+D.CO32―、Na+、NO3―、H+【答案】C【解析】离子共存的考查,即判断离子相互之间能否发生反应。
碳的多样性 练习

碳的多样性专题训练1.下列叙述正确的是()A.金刚石和石墨是同种物质B.C60和CO2均是碳元素的化合物C.石墨和C60是碳元素的同素异形体 D.O3和C60同素异形体2.下列说法均摘自某些科普杂志,你认为无科学性错误的是()A.铅笔芯的原料是重金属铅,儿童在使用时不可以用嘴吮吸铅笔,以免引起铅中毒B.CO有毒,生有煤炉的居室,可放置数盆清水,这样可有效的吸收CO,防止煤气中毒C.汽水浇灌农田有一定的道理,其中二氧化碳的缓释,有利于作物的光合作用D.用加酶洗衣粉洗涤衣服时,热水比温水好3.下列叙述正确的是()A.碳元素在自然界中主要以单质的形式存在B.蛋白质、淀粉以及天然气的主要成分甲烷等是由碳元素与氢、氧、氮等元素中的一种或几种组成的有机化合物C.大理石的主要成分是碳酸镁D.纯碱是氢氧化钠4.下列关于Na2CO3和NaHCO3的叙述中错误的是()A.等质量的两种盐分别与足量的盐酸反应,在相同情况下,Na2CO3产生的二氧化碳多B.等物质的量的Na2CO3和NaHCO3分别与足量的盐酸反应,在相同情况下产生的二氧化碳体积相等C.等物质的量的Na2CO3和NaHCO3分别与同浓度的盐酸反应,Na2CO3消耗盐酸的体积是NaHCO3消耗盐酸提及的2倍D.将石灰水加入NaHCO3溶液中不产生白色沉淀,而加入Na2CO3溶液中则产生白色沉5.目前,关于二氧化碳是否为大气污染有不同的观点。
认为“二氧化碳不是大气污染物”的理由是()①二氧化碳是重要的化工原料;②二氧化碳是植物光合作用的必需原料;③二氧化碳是无色、无味、无毒的气体;④除二氧化碳外甲烷、一氧化二氮也是温室气体A.①②B.②③C.③④D.①④6.对于IVA族元素,下列叙述中不正确的是()A.SiO2和CO2中,Si和O,C和O之间都是共价键B.C、Si和Ge的最外层电子数都是4,次外层电子数都是8C .CO 2 和 SiO 2 都是酸性氧化物,在一定条件下都能和氧化钙反应D .该族元素的主要化合价式-4和+2 7.下列除去杂质的方法正确的是( )A .除去CO 2中混有的CO :用澄清石灰水洗气B .除去BaCO 3固体中混有的BaSO 4:加过量盐酸后,过滤、洗涤C .除去FeCl 2溶液中混有的FeCl 3:加入过量铁粉,过滤D .除去Cu 粉中混有的CuO :加适量稀硝酸后,过滤、洗涤 8.向下列溶液中通入过量CO 2,最终出现浑浊的是( )A .氢氧化钙饱和溶液B .苯酚钠饱和溶液C .醋酸钠饱和溶液D.氯化钙饱和溶液 9.用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误..的( )10. 某无色混合气体可能含有CO 2、CO 、H 2O (g )、H 2中的一种或几种,依次进行如下连续处理(假定每步处理均反应完全):①通过碱石灰时,气体体积变小;②通过赤热的氧化铜时,固体变为红色;③通过白色硫酸铜粉末时,粉末变为兰色;④通过澄清的石灰水时,溶液变得浑浊。
鲁科版《碳的多样性》同步测试
1.自然界中形成化合物种类最多的元素是
A.O B.N C.C D.H
2.1828年,德国化学家维勒用无机物NH4CNO合成出的有机物是
A.甲烷B.酒精C.醋酸D.尿素
3.在①植物的光合作用②植物的呼吸作用③岩石的风化④海水的吸收⑤工业上制干冰⑥使熟石灰变石灰石等这些过程中,属于自然界消耗CO2的主要过程是A.仅①B.仅①⑥C.①②③D.①③④
4.碳的多样性体现在①碳单质的多样性②含碳化合物的多样性③碳转化的多样性④碳及其化合物应用的多样性等方面。
碳有多种同素异形体,所体现的是上述:A.①B.②C.③D.④
5.大理石可以用作墙面、地面和厨房桌面,其主要成份是碳酸钙。
食醋不慎滴在大理石桌面上,会使其失去光泽,变得粗糙,下列能正确解释此现象的是
A.食醋中的水使碳酸钙溶解B.食醋中的醋酸将碳酸钙氧化
C.食醋中的醋酸将碳酸钙还原D.食醋中的醋酸与碳酸钙发生了复分解反应6.纯净的碳酸氢钙试样在高温下分解,当剩余的固体质量为原试样的质量的一半时,碳酸氢钙的分解率为
A.50%B.75%C.%D.100%
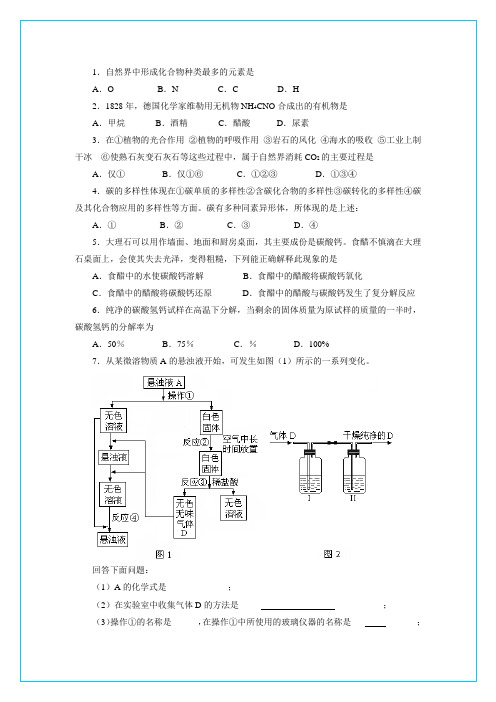
7.从某微溶物质A的悬浊液开始,可发生如图(1)所示的一系列变化。
回答下面问题:
(1)A的化学式是______________;
(2)在实验室中收集气体D的方法是_____ ___________;
(3)操作①的名称是______,在操作①中所使用的玻璃仪器的名称是___ _______;。
高中化学碳的多样性的相关练习和答案

高中化学碳的多样性的相关练习和答案1.(选用) 石灰在工农业生产和建筑业上有着重要用途。
用于生产石灰的主要原料是石灰石(用①表示),在石灰窑中加热焙烧石灰石得到生石灰(用②表示),并放出气体(用③表示)。
生石灰在建筑业上主要用作粘合剂,一般先使它“熟化”变成熟石灰(用④表示),熟石灰与砂子混合成灰泥用于砌筑砖墙。
经过一段时间后灰泥中的熟石灰变成另—固体物质(用⑤表示)。
用下列化学式表示的5种物质都正确的是( )A.①Ca(OH)2,②CaO,③SO3,④CaSO4,⑤CaSO4B.①CaO,②Ca(OH)2,③CO,④CaCO3,⑤CaSiO3C.①CaCO3,②CaO,③CO2,④Ca(OH)2,⑤CaCO3D.①CaCO3,②CaO,③SO2,④CaSiO3,⑤Ca(OH)22.(变式)用石灰水保存鲜蛋是一种化学保鲜方法,对这种保存鲜蛋的方法,有以下解释,其中正确的是( )①石灰具有强碱性,杀菌能力强②Ca(OH)2能与鲜蛋呼出的CO2反应,生成碳酸钙薄膜,起保护作用③石灰水是电解质溶液,能使蛋白质凝聚④石灰水能渗入蛋内中和酸性物质A.①②B.①③C.②③D.③④3.(原创)请据下图回答,经数小时后,U型管A、B两处的液面会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响)( )处上升,B处下降、B两处都下降处下降,B处上升、B两处都不变4.(选用)某无色混合气体可能含有CO2、CO、H2O(气)、H2中的一种或几种,依次进行下列处理(假设每次处理均反应完全):①通过碱石灰,气体体积变小,②通过赤热的氧化铜时,固体全部变为红色,③通过白色硫酸铜粉末时,粉末变为蓝色,④通过澄清石灰水,溶液变浑浊。
由此可以确定混合气体中( )A.一定含有CO2、H2O,可能含有H2、COB.一定含有H2O、CO,可能含有CO2、H2C.一定含有CO、CO2,可能含有H2O、H2D.一定含有CO、H2,可能含有H2O、CO25.(原创) 某固体物质A受热分解,生成B、C、D 三种物质。
碳的多样性练习题

碳的多样性练习题 SANY标准化小组 #QS8QHH-HHGX8Q8-GNHHJ8-HHMHGN#高一化学碳的多样性练习题编写:王海燕 2011-12-11.科学家在不断深入的研究中,发现了一系列新的碳单质,对碳单质的研究已发展成一门独立的科学——碳科学.下列关于碳单质的叙述正确的是( )A.碳的各种单质称之为碳的同素异形体B.碳元素的各种单质结构虽然不同,但性质差别不大C.碳元素的单质性质不同,其用途相同D.碳元素的单质只有金刚石、石墨和C602.将106 g的Na2CO3和84 g NaHCO3先经充分强热后,再分别跟足量的盐酸反应,下列说法错误的是()A.消耗盐酸一样多B.放出CO2的总量一样多C.后者生成的NaCl是前者的一半D.后者消耗盐酸是前者的一半3.实验室用石灰石和盐酸制取CO2时,最佳的除杂试剂和方法是( )A.水、浓H2SO4洗气 B.饱和Na2CO3溶液、浓H2SO4洗气C.饱和NaHCO3溶液、浓H2SO4洗气 D.NaOH溶液、浓H2SO4洗气4.过量的CO通入下列溶液中,最终出现浑浊的是2( )A.氯化钙溶液 B.石灰水 C.饱和碳酸钠溶液 D.氯化钠溶液5.可以用来断定碳酸氢钠粉末中是否混有碳酸钠的实验方法是( )A.加热时有无气体放出B.滴加盐酸时有无气泡放出C.溶于水后,滴加稀的氯化镁溶液有无白色沉淀生成D.溶于水后,滴加澄清石灰水,有无白色沉淀生成的是6.下列叙述可以肯定溶液中大量存在CO2-3( )A.加入AgNO溶液有白色沉淀产生3溶液有白色沉淀产生B.加入Ba(OH)2C.加入MgCl溶液有白色沉淀产生,再加入稀盐酸沉淀溶解,并产生可使澄清石灰水2变浑浊的无色无味气体D.加入稀盐酸有无色无味气体产生,该气体可使澄清的石灰水变浑浊7.为除去括号内的杂质,所选用的试剂或方法不.正确的是( )A.Na2CO3溶液(NaHCO3),选用适量的NaOH溶液B.NaHCO3溶液(Na2CO3),应通入过量的CO2气体C.Na2O2粉末(Na2O),将混合物在氧气中加热D.Na2CO3溶液(Na2SO4),加入适量Ba(OH)2溶液,过滤8.将CO2通入100 mL某浓度的石灰水中,所得沉淀质量与通入CO2体积(标准状况)的关系如图所示,则石灰水浓度为( )A.-1 B.-1 C.-1 D.-1★9.某混合气体中可能有H2、CO、CO2、HCl、NH3及水蒸气中的两种或多种,当混合气体依次通过①适量澄清石灰水(无浑浊现象);②氢氧化钡溶液(有浑浊现象);③浓硫酸(无现象);④灼热的氧化铜(变红);⑤无水硫酸铜(变蓝);则对该混合气体的成分判断正确的是 ( )A.一定没有CO2,肯定有CO和H2B.一定有CO、CO2和水蒸气C.一定有H2、HCl和CO2D.有CO2、NH3和水蒸气10.下列物质既能与HCl 反应又能与NaOH 反应的是 ( )A .Na 2CO 3B .NaOHC .BaCl 2D .NaHCO 311.下列叙述中正确的是 ( )A.向含有CaCO 3沉淀的水中通入CO 2 至沉淀恰好溶解,再向溶液中加入NaHCO 3饱和溶液,又有CaCO 3沉淀生成B.向Na 2CO 3溶液中逐滴加入等物质的量的稀盐酸,生成的CO 2与原Na 2CO 3物质的量之比为1∶2C.等质量的NaHCO 3和Na 2CO 3分别与足量盐酸反应,在同温同压下,生成的CO 2体积相等D.向Na 2CO 3饱和溶液中通入CO 2,有结晶析出12.为了检验某含有NaHCO 3杂质的Na 2CO 3样品的纯度,现将w 1 g 样品加热,其质量变为w 2 g ,则该样品的纯度(质量分数)是 ( )13.向100 mL mol ·L-1的Ca (OH )2溶液中通入CO 2气体,当得到1 g 沉淀时通入CO 2的物质的量是( )A.0.015 mol mol mol mol14.(1)图瓦卢是由多个珊瑚礁形成的岛国.由于大气中CO 2含量的剧增,大量珊瑚礁(主要成分是碳酸钙)被海水侵蚀,其原因是______________________________(化学方程式)(2)温室效应导致海平面上升,引起温室效应的人为原因主要是_____________________(3)为了控制温室效应,各国科学家提出了不少方法和设想.科学家致力于二氧化碳组合转化方面的技术研究,把过多的二氧化碳转化为对人类有益的物质.如将二氧化碳和氢气以1∶4的比例混合,通入反应器,在适当的条件下反应,可获得一种重要的能源.请完成下列化学方程式:CO 2+4H 2===________+2H 2O(4)科学家研究发现,用“汽水”(一种能释放CO 2的弱酸性溶液)浇灌植物能促进植物的生长.原因是它能________________.①加强呼吸作用 ②加强光合作用 ③改良碱性土壤、调节pH ④加强植物蒸腾作用A .①②B .②③C .③④D .②③④(5)快速、有效地减缓大气中CO 2大量增加的生态学措施是________.A .使用天然气等燃料B .控制全球人口增长C .植树造林,保护森林D .立即减少煤和石油的燃烧15.已知NaHCO 33样品a g ,溶于水配成溶液,慢慢滴入 mol/L 稀盐酸并不停地搅拌,反应过程中测得溶液中NaHCO 3的质量与加入盐酸的体积之间的关系如图所示。
3.1《碳的多样性》同步练习(鲁科版必修1)

第三章炭的多样性1、C金刚石、石墨三者互为。
60、的混合物V L缓缓的通入足量的过氧化钠中,气体体积减小了1/5,2、把CO、CO2的体积比为。
则混合物中CO、CO23、某种牙膏中的摩擦剂是碳酸钙,它可以用石灰石来制备,某同学设计了一个制备碳酸钙的方案,其流程图为:石灰石①高温生石灰②加水石灰水③加溶液碳酸钙(1)、请写出上述方案有关的化学方程式:①②③(2)请你仍用石灰石为原料(其他试剂自选),设计了一个制备碳酸钙的方案,其流程图为:石灰石你所设计的方案的优点为:(3)检验牙膏中是否含有碳酸盐的实验方法:4、金刚石、石墨和碳60的性质有所不同,原因是()A、构成原子不同B、各自的原子排列方式不同C、具有不同的几何外形D、硬度不同5、下列物质的化学名称、化学式和俗名一致的是()A、碳酸钙石灰石B、氢氧化钠纯碱C、碳酸钠苏打D、碳酸氢钠苏打6、下列各变化中,在木炭燃烧时不可能发生的反应是()A. B.C. D.7、以下物质的主要成分属于碳酸盐的是()①纯碱②蛋白质③大理石④方解石⑤胡胡萝卜素⑥菱铁矿⑦淀粉A、只有①②④⑥B、只有①②③④⑥⑦C、只有①③④⑤D、只有②③④⑤8、下列反应的离子方程式中正确的是()A、溶液与溶液反应B、溶液与溶液反应C、溶液与盐酸反应D、溶液与溶液反应9、为制备干燥、纯净的,将大理石和盐酸反应生成的气体先后通过由下列物质的两个吸收装置,两个装置中应依次分别盛放()A、水;无水固体B、饱和溶液;浓硫酸C、浓硫酸;饱和溶液D、饱和溶液;稀硫酸10、关于和下列说法中正确的是()A、比易溶于水B、比稳定C、石灰水能和反应,不与反应D、等物质的量的和与足量的盐酸反应,消耗盐酸的物质的量之比为2:111、无色的混合气体可能含有、、水蒸气、中的一种或者几种,依次进行如下连续处理(假定每步处理均反应完全)①通过碱石灰石,气体体积变小②通过赤热的氧化铜时,固体变为红色③通过白色硫酸铜粉末时,粉末变为蓝色④通过澄清石灰水时,溶液变得浑浊,由此可以确定原混合气体中()A、一定含有、,至少含、中的一种B、一定含有、,至少含有、中的一种C、一定含有、,至少含有、中的一种D、一定含有、,至少含有、中的一种12、某二价金属的碳酸盐和碳酸氢盐的混合物跟足量的盐酸反应,消耗的和产生的的物质的量之比为5:4,该混合物中碳酸盐和碳酸氢盐的物质的量之比为()A、1:3B、2:3C、3:4D、4:513、把通入含的石灰水中,充分反应后,下列叙述不正确的是()A、当时,生成沉淀B、当时,生成沉淀C、当时,生成沉淀D、当时,无沉淀生成14、下列应用体现了碳的导电性的有()A、铅笔芯中含有碳B、干电池中用石墨棒作电极C、用墨书写的书画年长日久也不变色D、用碳取暖15、纯净的试样在高温下分解,当剩余固体质量为原试样质量的一半时,的分解率是()A、50%B、75%C、92.7%D、100%16、有10g含有杂质的和足量的盐酸反应,产生了0.1mol,试推断杂质的组成可能是()①和②和③和④和A、①②B、②③C、③④D、①④17、将空气与按体积比5:1混合,跟足量赤热焦炭反应,恢复至原温度,在所得的气体中,一氧化碳体积分数为(假设空气中,其它成分不计)()A、29%B、43%C、50%D、100%18、加热使之分解,并按下图继续变化,最后得到的质量不可能是()A、 B、 C、 D、19、将足量的通入和混合稀溶液中,生成沉淀的物质的量(n)和通入体积(V)的关系正确的是()A B C D20、在一定温度下向足量的饱和溶液中加入1.06g无水,搅拌后静止,最终析出的晶体的质量()A、等于1.06gB、大于1.06g而小于2 .86gC、等于2.86gD、大于2.86g21、(05年全国)已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。
碳的多样性典型_练习题

碳的多样性习题一、选择题1. 下列有关CO2的实验中,只能证明CO2的物理性质的实验是()2.下列说法错误的是()A.铅笔芯的主要原料是石墨,儿童在使用时不会引起中毒B.CO有毒,生有煤炉的居室可放置数盆清水,这样有效地吸收CO,防止煤气中毒C.“汽水”浇灌植物有一定的道理,其中CO2的缓释,有利于植物的光合作用D.金刚石中所有的碳原子都按一定的方式连成一个向空间伸展的网络,而C60中每60个碳原子构成一个分子3. 1828年,德国化学家维勒,将一种无机物直接转变成有机化合物—尿素,由此打破了无机化合物与有机化合物的界限,这种无机化合物是()A. NH4CN OB.(NH4)2CO3 C NH4NO3 D CH3COONH44.判断NaHCO3白色粉末中混有Na2CO3的方法是( )A.加热,观察有无气体放出B.加入盐酸,观察有无气体放出C.加入澄清石灰水中观察有无沉淀D.加入CaCl2溶液观察有无沉淀5 可以用来断定碳酸氢钠粉末中混有碳酸钠的实验方法是()A.加热时有无气体放出C.溶于水后,滴加稀的氯化镁溶液有无白色沉淀生成B.滴加盐酸时有无气泡放出D.溶于水后,滴加澄清石灰水,有无白色沉淀生成6. 将106 g的Na2CO3和84 g NaHCO3都经充分强热,再分别跟足量的盐酸反应。
下列说法错误的是()A.消耗盐酸一样多B.放出CO2的总量一样多C.后者生成的NaCl是前者的一半D.后者消耗盐酸是前者的一半7 .向2.5L0.2mol/L的Na2CO3溶液中徐徐滴加7.5L0.1mol/L稀盐酸溶液,在标准状况下产生二氧化碳的体积是()A.8.4LB.5.6LC.2.8LD.4.2L8. 用1 L 1.0 mol·-1LNaOH溶液吸收0.8 mol CO2,所得溶液中的CO32-和HCO3-的物质的量浓度之比约是()A.1∶3B.2∶1C.2∶3D.3∶29. 某二价金属的碳酸盐和碳酸氢盐的混合物与足量盐酸反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高一化学碳的多样性练习题
编写:王海燕2011-12-1
1.科学家在不断深入的研究中,发现了一系列新的碳单质,对碳单质的研究已发展成
一门独立的科学——碳科学.下列关于碳单质的叙述正确的是( )
A. 碳的各种单质称之为碳的同素异形体
B. 碳元素的各种单质结构虽然不同,但性质差别不大
C. 碳元素的单质性质不同,其用途相同
D. 碳元素的单质只有金刚石、石墨和C o
2.将106 g的NaCO和84 g NaHCQ先经充分强热后,再分别跟足量的盐酸反应,下列
说法错误的是
()
A. 消耗盐酸一样多
B. 放出CQ的总量一样多
C.后者生成的NaCI是前者的一半
D. 后者消耗盐酸是前者的一半
3 . 实验室用石灰石和盐酸制取CO2 时,最佳的除杂试剂和方法是( )
A. 水、浓HSO洗气
B.饱和N Q CO溶液、浓HhSO洗气
C.饱和NaHC酩液、浓HbSO洗气D . NaOH溶液、浓HSO洗气
过量的CO2 通入下列溶液中,最终出现浑浊的是
( )
A. 氯化钙溶液 B .石灰水 C .饱和碳酸钠溶液 D .氯化钠溶液
5.可以用来断定碳酸氢钠粉末中是否混有碳酸钠的实验方法是( )
A. 加热时有无气体放出
B. 滴加盐酸时有无气泡放出
C. 溶于水后,滴加稀的氯化镁溶液有无白色沉淀生成
D. 溶于水后,滴加澄清石灰水,有无白色沉淀生成
6 . 下列叙述可以肯定溶液中大量存在CO 32-的是( )
A. 加入AgNO溶液有白色沉淀产生
B. 加入Ba(OH)2溶液有白色沉淀产生
C. 加入MgC2溶液有白色沉淀产生,再加入稀盐酸沉淀溶解,并产生可使澄清石灰水变浑浊的无色无味气体
D.加入稀盐酸有无色无味气体产生,该气体可使澄清的石灰水变浑浊
7 •为除去括号内的杂质,所选用的试剂或方法不
正确的 是
° 56巩(丫*泌
A. NaCO 溶液(NaHCO ),选用适量的NaOH 容液
B. NaHC (溶液(Na z CO ),应通入过量的CO 气体
C. NaO 2粉末(Na z O ),将混合物在氧气中加热
D. NaCO 溶液(Na z SO ),加入适量Ba (OH )2溶液,过滤 8.将CO 通入100 mL 某浓度的
石灰水中,所得沉淀质量与通入
★ 9.某混合气体中可能有 H 、CO CO 、HCI 、NH 及水蒸气中的两种或多种,当混合气 体依次通过①适量澄清石灰水(无浑浊现象):②氢氧化钡溶液(有浑浊现象):③浓硫酸 (无现象):④灼热的氧化铜(变红);⑤无水硫酸铜(变蓝);则对该混合气体的成分判断 正确的是
( )
A . —定没有CO,肯定有CO 和 H
B . —定有CO CO 和水蒸气
C. 一定有 H 、HCI 和CO
D.有CO 、NH 和水蒸气
10. 下列物质既能与HCI 反应又能与NaOH 反应的是
CO 体积(标准状况)的关
系 如 图 所 示 ( )
石 灰 水 浓 度 为
A . B. C.
-1
D
A . NaCO
B . NaOH
C . BaCb
D . NaHCO
11. 下列叙述中正确的是 ()
A.向含有CaCO 沉淀的水中通入CO 至沉淀恰好溶解,再向溶液中加入NaHC C 饱和溶液, 又有CaCO 沉淀生成
B.
向N&CO 溶液中逐滴加入等物质的量的稀盐酸, 生成的CO 与原NaCO 物质的量之比为
1 : 2
C. 等质量的NaHC C 和NS 2CO 分别与足量盐酸反应,在同温同压下,生成的 CO 体积相等
D. 向N&CO 饱和溶液中通入 CO ,有结晶析出
12. 为了检验某含有NaHCO 杂质的N&CO 样品的纯度,现将 w 1 g 样品加热,其质量变为 w 2 g ,则该样品的纯度(质量分数)是 ( )
A.
13. 向100 mL mol • L-1的Ca (OH 2溶液中通入 CO 气体,当得到1 g 沉淀时通入 CO 3 1 TC'i
ix
115xV2
8Z 1XJC *J
31
的
物
质
A.0.015 mol mol mol mol
14. (1)图瓦卢是由多个珊瑚礁形成的岛国. 由于大气中CO含量的剧增,大量珊瑚礁(主
要成分是碳酸钙) 被海水侵蚀,其原因是___________________________________ (化学方程式)
(2) 温室效应导致海平面上升,引起温室效应的人为原因主要是__________________________
(3) 为了控制温室效应,各国科学家提出了不少方法和设想.科学家致力于二氧化碳组
合转化方面的技术研究,把过多的二氧化碳转化为对人类有益的物质.如将二氧化碳和
氢气以1 :4的比例混合,通入反应器,在适当的条件下反应,可获得一种重要的能源.请
完成下列化学方程式:CO2+4H2=== ______ +2H2O
(4) 科学家研究发现,用“汽水”(一种能释放CO的弱酸性溶液)浇灌植物能促进植物的
生长.原因是它能 __________________ .
①加强呼吸作用②加强光合作用③改良碱性土壤、调节pH ④加强植物蒸腾作
用
A.①② B .②③ C .③④ D .②③④
(5) 快速、有效地减缓大气中CO大量增加的生态学措施是____________ .
A.使用天然气等燃料 B .控制全球人口增长
C.植树造林,保护森林.立即减少煤和石油的燃烧
15. 已知NaHC 3在潮湿的空气中会缓慢分解。
取没有妥善保管已部分变质的
a g ,溶于水配成溶液,慢慢滴入 mol/L 稀盐酸并 不停地搅
拌,反应过程中测得溶液中 NaHC 3的质量 与加入盐酸的
体积之间的关系如图所示。
(1) ________________________________ a g 样品中含NaCO 的质量为 go
(2) ____________________________________ a g 样品未变质前 NaHCO 勺质量为 g
16.
称取一定质量的纯碱,溶于水后与盐酸完全反应放出 CO ,用“增多”或“减少”
填空
(1) 若纯碱中含 NaHCQ
所需盐酸用量 ______________ ,产生的气体 ________________ ;
(2) 若纯碱中含K 2CO
所需盐酸用量 _______________ ,产生的气体 _________________ ;
(3) 若纯碱中含NaCI
所需盐酸用量 _______________ ,产生的气体 _______________ o
NaHg 羊品
0 5
50 K(HCl)(inL)
★ 17.向NaOH容液中通入CO气体制备N&CO,由于通入CO的量难以控制,常混有NaOH 或NaHCQ请利用所学知识设计方案制得纯净的N Q CO溶液:。
