初中化学中考常考化学方程式集锦
初中化学中考常考化学方程式集锦
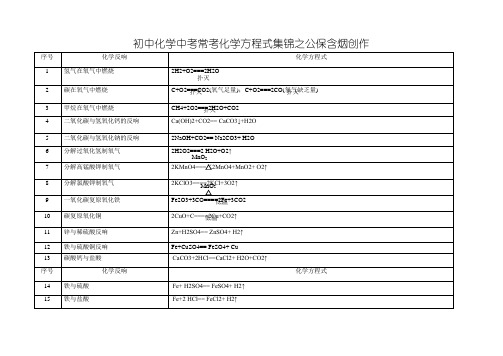
序号
化学反响
14 铁与硫酸
15 铁与盐酸
2KClO3===M=n2OK2Cl+3O2↑ Fe2O3+3CO====低2F温e+3CO2 2CuO+C====低2温Cu+CO2↑ Zn+H2SO4== ZnSO4+ H2↑ Fe+CuSO4== FeSO4+ Cu CaCO3+2HCl==CaCl2+ H2O+CO2↑
Na2CO3+ Ca(OH)2== CaCO3↓+2 NaOH AgNO3+NaCl==AgCl↓+NaNO3 (NH4)2 CO3+BaCl2==BaCO3↓+ 2NH4Cl NaOH+ HCl==NaCl+ H2O 2 NaOH+H2SO4==Na2SO4+2H2O Fe2O3+6HCl===2 FeCl3+3H2O
初中化学中考常考化学方程式集锦之公保含烟创作
序号
化学反响
化学方程式
1 氢气在氧气中燃烧 2 碳在氧气中燃烧
2H2+O2===2H2O 扑灭
C+O2=扑==灭CO2(氧气足量);C+O2===2CO(氧扑气灭缺乏量)
3 甲烷在氧气中燃烧 4 二氧化碳与氢氧化钙的反响
CH4+2O2==扑=2灭H2O+CO2 Ca(OH)2+CO2== CaCO3↓+H2O
CuO+ H2SO4==CuSO4+ H2O 2H2O===通=电2H2↑+ O2↑ CaCO3===低==温CaO+CO2↑ CuSO4+ 2NaOH==Cu(OH)2↓+ Na2SO4
中考最常考的36个化学方程式及相关知识点

中考最常考的36个化学方程式及相关知识点化学方程式和相关知识点是中考化学考试中的重要内容,学好这些知
识点对于取得优异成绩十分关键。
下面将介绍中考最常考的36个化学方
程式及相关知识点。
化学方程式:
1.酸碱中和反应方程式:酸+碱→盐+水。
2.酸与金属的反应方程式:酸+金属→盐+氢气。
3.碳酸盐的热分解反应方程式:碳酸盐→金属氧化物+二氧化碳。
4.金属与盐酸的反应方程式:金属+盐酸→盐+氢气。
5.金属氧化物与酸的反应方程式:金属氧化物+酸→盐+水。
6.金属与酸的氧化还原反应:金属+酸→金属盐+氢气。
7.硫酸和金属氧化物的反应方程式:硫酸+金属氧化物→盐+水。
8.碱金属和水的反应方程式:碱金属+水→碱水+氢气。
9.盐的溶解反应方程式:盐+水→水合物离子+水。
10.燃烧反应方程式:燃料+氧气→二氧化碳+水。
相关知识点:
1.酸碱反应:了解酸和碱的性质,学会判定物质的酸碱性,掌握酸碱
中和反应的方程式。
2.金属与非金属元素的反应:学会判定金属与非金属元素的反应产物,并掌握相应的反应方程式。
3.金属与酸的反应:学会判定金属与酸的反应产物,并掌握相应的反应方程式。
4.碳酸盐的热分解反应:了解碳酸盐的热分解产物,并掌握相关的反应方程式。
5.盐的溶解反应:了解溶解盐的产物,并掌握相关的反应方程式。
6.燃烧反应:了解燃烧的条件和产物,并掌握相关的反应方程式。
上述是中考最常考的36个化学方程式以及相关知识点,希望能对你复习和应对中考化学考试提供帮助。
祝你取得优秀的成绩!。
中考化学方程式大全(必考内容)

中考化学方程式大全(必考内容)一、氧气的性质:1. 镁在空气中燃烧: 2Mg + O点燃 2MgO★2. 铁在氧气中燃烧: 3Fe + 2O2 点燃 Fe3O43. 铜在空气中受热: 2Cu + O2 △ 2CuO4. 铝在空气中燃烧: 4Al + 3O2 点燃 2Al2O3★5. 氢气中空气中燃烧: 2H2 + O2点燃 2H2O★6. 红磷在空气中燃烧(测定空气中氧气含量):4P + 5O点燃 2P2O57. 硫粉在空气中燃烧: S + O点燃 SO28. 碳在氧气中充分燃烧: C + O点燃 CO29. 碳在氧气中不充分燃烧: 2C + O2点燃 2CO10. 一氧化碳在氧气中燃烧: 2CO + O2点燃 2CO211.玻义耳研究空气的成分实验 2HgO △ 2Hg+ O2 ↑★12.加热高锰酸钾: 2KMnO△ K2MnO4 + MnO2 + O2↑★13.氯酸钾和二氧化锰共热制取氧气2KClO3MnO2△2KCl+3O2↑★14.过氧化氢在二氧化锰作催化剂条件下分解反应:2H2O MnO2 2O+ O2 ↑二、自然界中的水:★15.电解水(探究水的组成实验): 2H2O 通电 2H2↑+ O2 ↑16.生石灰溶于水: CaO + H2O = Ca(OH)217.二氧化碳可溶于水: H2O + CO2=H2CO3三、质量守恒定律:18.镁在空气中燃烧: 2Mg + O2 点燃 2MgO★19.铁和硫酸铜溶液反应: Fe + CuSO4 = FeSO4 + Cu★20.氢气还原氧化铜: H2 + CuO △ Cu + H2O四、碳和碳的氧化物:21. 碳在氧气中充分燃烧: C + O点燃 CO2★22.木炭还原氧化铜: C+ 2CuO 高温 2Cu + CO2↑23.焦炭还原氧化铁: 3C+ 2Fe2O3高温 4Fe + 3CO2↑24.煤炉的底层: C + O点燃 CO225.煤炉的中层: CO2 + C 高温 2CO26.煤炉的上部蓝色火焰的产生: 2CO + O2点燃 2CO2★27.大理石与稀盐酸反应: CaCO3 + 2HCl = CaCl2 + H2O + CO2↑28.碳酸不稳定而分解: H2CO3 = H2O + CO2↑29.二氧化碳可溶于水: H2O + CO2=H2CO3★30.高温煅烧石灰石(工业制CO2):CaCO高温 CaO + CO2↑★31.石灰水与二氧化碳反应(检验二氧化碳):Ca(OH)2 + CO2 = CaCO3↓+ H2O ★32.一氧化碳还原氧化铜: CO+ CuO △ Cu + CO2★33.一氧化碳的可燃性: 2CO + O2点燃 2CO2★34.碳酸钠与稀盐酸(灭火器的原理): Na2CO3 + 2HCl =2NaCl +H2O +CO2↑五、燃料及其利用:★35.甲烷在空气中燃烧: CH4 + 2O点燃 CO2 + 2H2O★36.酒精在空气中燃烧: C2H5OH + 3O2点燃 2CO2 + 3H2O★37.氢气中空气中燃烧: 2H2 + O2点燃 2H2O六、金属38.镁在空气中燃烧: 2Mg + O点燃 2MgO39.铁在氧气中燃烧: 3Fe + 2O点燃 Fe3O440. 铜在空气中受热: 2Cu + O2 △ 2CuO41. 铝在空气中形成氧化膜: 4Al + 3O2 = 2Al2O3★42. 锌和稀硫酸(实验室制取氢气) Zn + H2SO4 = ZnSO4 + H2↑★43. 铁和稀硫酸 Fe + H2SO4 = FeSO4 + H2↑44. 镁和稀硫酸 Mg + H2SO4 = MgSO4 + H2↑45. 铝和稀硫酸 2Al +3H2SO4 = Al2(SO4)3 +3H2↑46. 锌和稀盐酸 Zn + 2HCl = ZnCl2 + H2↑47. 铁和稀盐酸 Fe + 2HCl =FeCl2 + H2↑48. 镁和稀盐酸 Mg+ 2HCl = MgCl2 + H2↑49.铝和稀盐酸 2Al + 6HCl =2AlCl3 + 3 H2↑★50. 铁和硫酸铜溶液反应: Fe + CuSO4 = FeSO4 + Cu51. 锌和硫酸铜溶液反应: Zn + CuSO4 =ZnSO4 + Cu52. 铜和硝酸汞溶液反应: Cu + Hg(NO3)2= Cu(NO3)2 + Hg★53.金属铁的治炼原理: 3CO+ 2Fe2O高温 4Fe + 3CO2↑七、酸、碱、盐★54. 氧化铁和稀盐酸反应: Fe2O3 + 6HCl =2FeCl3 + 3H2O★55. 氧化铁和稀硫酸反应: Fe2O3 + 3H2SO4 =Fe2(SO4)3 + 3H2O56. 氧化铜和稀盐酸反应: CuO + 2HCl =CuCl2 + H2O57. 氧化铜和稀硫酸反应: CuO + H2SO4 =CuSO4 + H2O★58.盐酸和烧碱起反应: HCl + NaOH = NaCl +H2O★59. 盐酸和氢氧化钙反应: 2HCl + Ca(OH)2 = CaCl2 + 2H2O60. 氢氧化铝药物治疗胃酸过多: 3HCl + Al(OH)3 = AlCl3 + 3H2O61. 硫酸和烧碱反应: H2SO4 + 2NaOH =Na2SO4 + 2H2O★62.大理石与稀盐酸反(实验室制取CO2 ):CaCO3 +2HCl =CaCl2+H2O+CO2↑★63.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑64.碳酸氢钠与稀盐酸反应: NaHCO3 + HCl= NaCl + H2O + CO2↑★65. 硫酸和氯化钡溶液反应: H2SO4 + BaCl2 == BaSO4 ↓+ 2HCl★66.苛性钠暴露在空气中变质: 2NaOH + CO2 = Na2CO3 + H2O67.苛性钠吸收二氧化硫气体: 2NaOH + SO2 =Na2SO3 + H2O68.苛性钠吸收三氧化硫气体: 2NaOH + SO3 = Na2SO4 + H2O★69.消石灰放在空气中变质: Ca(OH)2 + CO 2 = CaCO 3 ↓+ H 2O70. 消石灰吸收二氧化硫: Ca(OH)2 + SO 2 = CaSO 3 ↓+ H 2O★71. 铁和硫酸铜溶液(波尔多液不能用铁桶装): Fe + CuSO 4 = FeSO 4 + Cu★72.碳 酸钠与稀盐酸(检验NaOH 变质):Na 2CO 3+2HCl=2NaCl+H 2O+CO 2↑★73. 碳酸氢钠与稀盐酸(小苏打治疗胃酸过多)NaHCO 3+HCl=NaCl+H 2O+CO 2↑ ★74. 氢氧化钙与碳酸钠(检验NaOH 变质): Ca(OH)2+Na 2CO 3=CaCO 3↓+ 2NaOH ★75.氯化钠和硝酸银(区别食盐和蒸馏水):NaCl + AgNO 3 =AgCl ↓ + NaNO 3★76.硫酸钠 和氯化钡: Na 2SO 4 + BaCl 2 == BaSO 4↓ + 2NaCl二、中考化学推断题2.A ﹣I 是初中化学所学的物质,其转化关系如图所示.A 、B 、D 、E 、F 是不同类别的物质,C 、G 、H 、I 、F 也是不同类别的物质;A 、B 、C 中含有同种元素,B 是导致“温室效应”的一种气体,D 可用作建筑材料,G 是红色金属单质,E 中含有钠元素,F 有两种元素组成;图中“—”表示两端的物质能发生化学反应,“→”表示物质间存在相应的转化关系(部分反应物、生成物和反应条件未标出).试推断:(1)B 、I 的化学式为:B_____;I_____;物质E 的俗名是_____(写一个)(2)反应D —F 的基本反应类型是_____反应;(3)写出下列反应的化学方程式:①若反应(C →B )为化合反应,则该反应方程式为_____;②反应G →H 方程式为_____;③反应F —I 方程式_____。
中考重要的化学方程式汇总

中考重要的化学方程式汇总化学方程式是描述化学反应的重要工具,它可以简洁地表示反应物与生成物之间的转化关系。
以下是中考重要的化学方程式的汇总,供参考:1.酸碱反应方程式:a)钠氢氧化合物与硫酸反应:2NaOH+H2SO4->Na2SO4+2H2Ob)碳酸氢钠与盐酸反应:NaHCO3+HCl->NaCl+CO2+H2O2.燃烧反应方程式:a)甲烷燃烧:CH4+2O2->CO2+2H2Ob)乙烷燃烧:2C2H6+7O2->4CO2+6H2O3.氧化还原反应方程式:a)锌与盐酸反应:Zn+2HCl->ZnCl2+H2b)铜与硝酸反应:Cu+4HNO3->Cu(NO3)2+2NO2+2H2O4.酯化反应方程式:酒精与柠檬酸酯化:C2H5OH+CH3COOH->C2H5COOC2H5+H2O5.加水反应方程式:a)合成水合铜(II)硫酸物:CuSO4+5H2O->CuSO4·5H2Ob)加水使石膏脱水:CaSO4·2H2O->CaSO4+2H2O6.碳酸酐水解反应方程式:CaCO3+H2O+CO2->Ca(HCO3)27.铵盐分解反应方程式:(NH4)2CO3->2NH3+CO2+H2O8.氢氧化钠与氯化银反应方程式:2NaOH+AgCl->Ag2O+NaCl+H2O9.氨水与盐酸反应方程式:NH3+HCl->NH4Cl10.过氧化氢分解反应方程式:2H2O2->2H2O+O211.铁与硫反应生成硫化亚铁方程式:6Fe+S->Fe2S312.碘化钾与氯化铅反应方程式:2KI+PbCl2->2KCl+PbI2以上是中考重要的化学方程式的汇总,旨在帮助学生对化学反应过程有更深入的理解。
在备考中,要着重记忆和理解这些方程式的含义和应用场景。
同时,也需要练习写出其他类型的化学方程式,以提高解题能力。
中考必考的26个化学方程式

中考必考的26个化学方程式每年的中考都会考及化学方程式知识,而这26个化学方程式是考生必须掌握的重要知识点。
以下就是中考必考的26个化学方程式:1.氧化钠与水反应:NaOH + H2O Na+ + OH- + H22.酸氢钠与水反应:NaHCO3 + H2O Na+ + HCO3- + H23.氧化钾与水反应:KOH + H2O K+ + OH- + H24.氧化钙与水反应:Ca(OH)2 + H2O Ca2+ + 2OH- + H25.水与硝酸反应:NH3 + HNO3 NH4+ + NO3-6.酸钾与水反应:KClO3 + H2O K+ + ClO3- + H27.化钠与水反应:NaCl + H2O Na+ + Cl- + H28.化铵与水反应:NH4Cl + H2O NH4+ + Cl- + H29.化钙与水反应:CaCl2 + H2O Ca2+ + 2Cl- + H210.氧化铵与水反应:NH4OH + H2O NH4+ + OH- + H211.酸钠与水反应:Na2SO4 + H2O 2Na+ + SO42- + H212.氧化钠与碳酸反应:NaOH + CO2 Na+ + HCO3-13.氧化钾与碳酸反应:KOH + CO2 K+ + HCO3-14.氢氧化钠与水反应:NaClO + H2O Na+ + ClO- + H2O15.氢氧化钾与水反应:KClO + H2O K+ + ClO- + H2O16.化锂与水反应:LiCl + H2O Li+ + Cl- + H217.氧化钠与硝酸反应:NaOH + HNO3 Na+ + NO3- + H218.氧化钾与硝酸反应:KOH + HNO3 K+ + NO3- + H219.化锂与硫酸反应:LiCl + H2SO4 Li+ + SO42- + 2HCl20.化铵与硫酸反应:NH4Cl + H2SO4 NH4+ + SO42- + 2HCl21.氢交换反应:Na2SO4 + 2HCl 2NaCl + SO42- + H222.氢交换反应:K2SO4 + 2HCl 2KCl + SO42- + H223.化钠与硝酸反应:NaCl + HNO3 Na+ + NO3- + HCl24.化钾与硝酸反应:KCl + HNO3 K+ + NO3- + HCl25.氧化铝与水反应:Al(OH)3 + H2O Al3+ + 3OH- + H226.氧化镁与水反应:Mg(OH)2 + H2O Mg2+ + 2OH- + H2以上就是中考必考的26个化学方程式,须掌握的知识点。
初三化学所有化学方程式

初三化学所有化学方程式化学方程式是初三化学学习中的重要内容,它是用化学式来表示化学反应的式子。
掌握化学方程式对于理解化学反应的本质、进行化学计算以及解决实际化学问题都具有关键作用。
下面为大家整理了初三化学中常见的化学方程式。
一、氧气的性质1、镁在空气中燃烧:2Mg + O₂点燃 2MgO现象:发出耀眼的白光,生成白色固体。
2、铁在氧气中燃烧:3Fe + 2O₂点燃 Fe₃O₄现象:剧烈燃烧,火星四射,生成黑色固体。
3、铜在空气中受热:2Cu + O₂加热 2CuO现象:红色固体变黑。
4、铝在空气中燃烧:4Al + 3O₂点燃 2Al₂O₃现象:发出耀眼的白光,生成白色固体。
5、氢气在空气中燃烧:2H₂+ O₂点燃 2H₂O现象:产生淡蓝色火焰,放出热量。
6、红磷在空气中燃烧:4P + 5O₂点燃 2P₂O₅现象:产生大量白烟,放出热量。
7、硫粉在空气中燃烧: S + O₂点燃 SO₂现象:在空气中发出淡蓝色火焰,在氧气中发出蓝紫色火焰,生成有刺激性气味的气体。
二、制取氧气的反应1、加热高锰酸钾:2KMnO₄加热 K₂MnO₄+ MnO₂+ O₂↑2、加热氯酸钾和二氧化锰的混合物:2KClO₃加热 2KCl + 3O₂↑3、过氧化氢在二氧化锰作催化剂条件下分解反应:2H₂O₂二氧化锰 2H₂O + O₂↑三、碳和碳的氧化物1、碳在氧气中充分燃烧:C + O₂点燃 CO₂2、碳在氧气中不充分燃烧:2C + O₂点燃 2CO3、一氧化碳在氧气中燃烧:2CO + O₂点燃 2CO₂4、二氧化碳通过灼热的碳层:C + CO₂高温 2CO5、二氧化碳与水反应:CO₂+ H₂O = H₂CO₃6、碳酸不稳定分解:H₂CO₃= H₂O + CO₂↑7、二氧化碳通入澄清石灰水:Ca(OH)₂+ CO₂= CaCO₃↓ +H₂O现象:澄清石灰水变浑浊。
8、高温煅烧石灰石:CaCO₃高温 CaO + CO₂↑四、金属1、锌和稀硫酸反应:Zn + H₂SO₄= ZnSO₄+ H₂↑2、铁和稀硫酸反应:Fe + H₂SO₄= FeSO₄+ H₂↑3、镁和稀硫酸反应:Mg + H₂SO₄= MgSO₄+ H₂↑4、铝和稀硫酸反应:2Al + 3H₂SO₄= Al₂(SO₄)₃+ 3H₂↑5、锌和稀盐酸反应:Zn + 2HCl = ZnCl₂+ H₂↑6、铁和稀盐酸反应:Fe + 2HCl = FeCl₂+ H₂↑7、镁和稀盐酸反应:Mg + 2HCl = MgCl₂+ H₂↑8、铝和稀盐酸反应:2Al + 6HCl = 2AlCl₃+ 3H₂↑9、铁和硫酸铜溶液反应:Fe + CuSO₄= FeSO₄+ Cu现象:铁表面覆盖一层红色物质,溶液由蓝色逐渐变为浅绿色。
九年级常考的15个化学方程式
九年级常考的15个化学方程式以下是九年级常考的一些化学方程式:1. 氧化反应:- 2Mg + O2 →2MgO (镁和氧气生成氧化镁)2. 酸碱中和反应:- HCl + NaOH →NaCl + H2O (盐酸和氢氧化钠生成氯化钠和水)3. 单质与氧气反应:- 2H2 + O2 →2H2O (氢气和氧气生成水)4. 金属与非金属氧化物反应:- 2Al + 3CuO →3Cu + Al2O3 (铝和铜氧化物生成铜和氧化铝)5. 水解反应:- CaCl2 + H2O →Ca(OH)2 + 2HCl (氯化钙和水生成氢氧化钙和盐酸)6. 还原反应:- 2K + 2H2O →2KOH + H2 (钾和水生成氢氧化钾和氢气)7. 燃烧反应:- C3H8 + 5O2 →3CO2 + 4H2O (丙烷和氧气燃烧生成二氧化碳和水)8. 置换反应:- Zn + CuSO4 →ZnSO4 + Cu (锌和硫酸铜置换生成硫酸锌和铜)9. 分解反应:- 2HgO →2Hg + O2 (氧化汞分解成汞和氧气)10. 碱金属与水反应:- 2Na + 2H2O →2NaOH + H2 (钠和水生成氢氧化钠和氢气)11. 碳酸盐分解反应:- CaCO3 →CaO + CO2 (碳酸钙分解成氧化钙和二氧化碳)12. 氢氧化物分解反应:- 2AgOH →Ag2O + H2O (氢氧化银分解成氧化银和水)13. 硫酸盐分解反应:- Na2SO4 →Na2O + SO3 (硫酸钠分解成氧化钠和三氧化硫)14. 过氧化物分解反应:- 2H2O2 →2H2O + O2 (过氧化氢分解成水和氧气)15. 含氧酸盐分解反应:- 2KClO3 →2KCl + 3O2 (高氯酸钾分解成氯化钾和氧气)。
初中化学中考常考化学方程式集锦
5 二氧化碳与氢氧化钠的反应 2NaOH+CO2== Na2CO3+ H2O
6 分解过氧化氢制氧气
2H2O2M=n=O=2 2 H2O+O2↑
7 分解高锰酸钾制氧气 8 分解氯酸钾制氧气 9 一氧化碳还原氧化铁 10 碳还原氧化铜
2KMnO4=== K2MnO4+MnO2+ O2↑ 2KClO3=M=n=O=2 2KCl+3O2↑
初中化学中考常考化学方程式集锦
序号
化学反应
化学方程式
#43;O2点==燃=2H2O C+O2点=燃==CO2(氧气足量);C+O2=点=燃=2CO(氧气不足量) CH4+2O2点==燃=2H2O+CO2
4 二氧化碳与氢氧化钙的反应 Ca(OH)2+CO2== CaCO3↓+H2O
高温
Fe2O3+3CO====2Fe+3CO2
高温
2CuO+C====2Cu+CO2↑
11 锌与稀硫酸反应
Zn+H2SO4== ZnSO4+ H2↑
12 铁与硫酸铜反应
Fe+CuSO4== FeSO4+ Cu
13 碳酸钙与盐酸
序号
化学反应
14 铁与硫酸
15 铁与盐酸
16 碳酸钠与氢氧化钙
17 硝酸银与氯化钠
高温
CaCO3=====CaO+CO2↑ CuSO4+ 2NaOH==Cu(OH)2↓+ Na2SO4
18 碳酸铵氯化钡
19 氢氧化钠与盐酸
20 氢氧化钠与硫酸
21 氧化铁与盐酸
22 氧化铜与硫酸
初三常用化学方程式 100个
初三常用化学方程式1.氢气与氧气发生化合反应:2H2 + O2 → 2H2O2.镁与氧气发生化合反应:2Mg + O2 → 2MgO3.铁与氧气发生化合反应:3Fe + 2O2 → Fe3O44.碳与氧气发生化合反应:C + O2 → CO25.一氧化碳与氧气发生化合反应:2CO + O2 → 2CO26.甲烷在空气中燃烧:CH4 + 2O2 → CO2 + 2H2O7.乙醇在空气中燃烧:C2H5OH + 3O2 → 2CO2 + 3H2O8.氢氧化钠与稀硫酸发生中和反应:NaOH + H2SO4 → Na2SO4 +H2O9.氢氧化钙与稀盐酸发生中和反应:Ca(OH)2 + 2HCl → CaCl2 +2H2O10.二氧化碳与氢氧化钠反应:CO2 + 2NaOH → Na2CO3 + H2O11.氢氧化钠与二氧化碳反应:2NaOH + CO2 → Na2CO3 + H2O12.氢氧化钙与碳酸钠反应:Ca(OH)2 + Na2CO3 → CaCO3↓ +2NaOH13.碳酸钙高温分解:CaCO3 → CaO + CO2↑14.氧化钙与水反应:CaO + H2O → Ca(OH)215.硫酸铜与氢氧化钠反应:CuSO4 + 2NaOH → Cu(OH)2↓ +Na2SO416.氯化铁与氢氧化钠反应:FeCl3 + 3NaOH → Fe(OH)3↓ + 3NaCl17.氯化钡与硫酸钠反应:BaCl2 + Na2SO4 → BaSO4↓ + 2NaCl18.盐酸与硝酸银反应:HCl + AgNO3 → AgCl↓ + HNO319.硫酸与氯化钡反应:H2SO4 + BaCl2 → BaSO4↓ + 2HCl20.硫酸与氢氧化钠反应:H2SO4 + 2NaOH → Na2SO4 + 2H2O21.氧化铁与盐酸反应:Fe2O3 + 6HCl → 2FeCl3 + 3H2O22.氧化铜与硫酸反应:CuO + H2SO4 → CuSO4 + H2O23.氢氧化钠与稀硫酸反应:2NaOH + H2SO4 → Na2SO4 + 2H2O24.氢氧化钙与稀盐酸反应:Ca(OH)2 + 2HCl → CaCl2 + 2H2O25.氢氧化钠与二氧化碳反应:2NaOH + CO2 → Na2CO3 + H2O26.氢氧化钙与碳酸钠反应:Ca(OH)2 + Na2CO3 → CaCO3↓ +2NaOH27.氢氧化钠与氯化铁反应:3NaOH + FeCl3 → Fe(OH)3↓ + 3NaCl28.硫酸与氢氧化铁反应:3H2SO4 + 2Fe(OH)3 → Fe2(SO4)3 + 6H2O29.硝酸银与稀盐酸反应:AgNO3 + HCl → AgCl↓ + HNO330.硝酸银与稀氯化钠反应:AgNO3 + NaCl → AgCl↓ + NaNO331.锌与稀硫酸反应:Zn + H2SO4 → ZnSO4 + H2↑32.镁与稀盐酸反应:Mg + 2HCl → MgCl2 + H2↑33.铝与稀硫酸反应:2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑34.铁与稀盐酸反应:Fe + 2HCl → FeCl2 + H2↑35.铜与硝酸银反应:Cu + 2AgNO3 → Cu(NO3)2 + 2Ag36.铁与硫酸铜反应:Fe + CuSO4 → FeSO4 + Cu37.氧化钙与水反应:CaO + H2O → Ca(OH)238.二氧化碳与氢氧化钠反应:CO2 + 2NaOH → Na2CO3 + H2O39.二氧化碳与氢氧化钙反应:CO2 + Ca(OH)2 → CaCO3↓ + H2O40.二氧化碳与水反应:CO2 + H2O → H2CO341.氢气还原氧化铜:H2 + CuO → Cu + H2O42.碳还原氧化铜:C + 2CuO → 2Cu + CO2↑43.一氧化碳还原氧化铜:CO + CuO → Cu + CO244.碳还原氧化铁:3C + 2Fe2O3 → 4Fe + 3CO2↑45.一氧化碳还原氧化铁:3CO + Fe2O3 → 2Fe + 3CO246.碳酸钙与稀盐酸反应:CaCO3 + 2HCl → CaCl2 + H2O + CO2↑47.碳酸钠与稀盐酸反应:Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑48.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl → NaCl + H2O + CO2↑49.硫酸与碳酸钠反应:H2SO4 + Na2CO3 → Na2SO4 + H2O + CO2↑50.硫酸与碳酸氢钠反应:H2SO4 + NaHCO3 → Na2SO4 + H2O + CO2↑51.氨气与氯化氢反应:NH3 + HCl → NH4Cl52.氢氧化钠与稀硫酸反应:2NaOH + H2SO4 → Na2SO4 + 2H2O53.氢氧化钠与氯化铵反应:NaOH + NH4Cl → NaCl + NH3↑ + H2O54.碳酸氢钠受热分解:2NaHCO3 → Na2CO3 + CO2↑ + H2O55.碳酸氢铵受热分解:NH4HCO3 → NH3↑ + CO2↑ + H2O56.盐酸与硝酸银反应:HCl + AgNO3 → AgCl↓ + HNO357.硫酸与碳酸钠反应:H2SO4 + Na2CO3 → Na2SO4 + CO2↑ + H2O58.硫酸与碳酸氢钠反应:H2SO4 + NaHCO3 → Na2SO4 + CO2↑ +H2O59.硫酸与氢氧化铁反应:3H2SO4 + 2Fe(OH)3 → Fe2(SO4)3 + 6H2O60.硝酸与氢氧化铁反应:3HNO3 + Fe(OH)3 → Fe(NO3)3 + 3H2O61.氧化铁与氢气反应:Fe2O3 + 3H2 → 2Fe + 3H2O62.氧化铁与一氧化碳反应:Fe2O3 + 3CO → 2Fe + 3CO263.氧化铜与氢气反应:CuO + H2 → Cu + H2O64.氧化铜与一氧化碳反应:CuO + CO → Cu + CO265.氧化钙与水反应:CaO + H2O → Ca(OH)266.二氧化碳与氢氧化钙反应:CO2 + Ca(OH)2 → CaCO3↓ + H2O67.二氧化硫与水反应:SO2 + H2O → H2SO368.二氧化硫与氢氧化钠反应:SO2 + 2NaOH → Na2SO3 + H2O69.一氧化碳还原氧化铁:3CO + Fe2O3 → 2Fe + 3CO270.一氧化碳还原四氧化三铁:4CO + Fe3O4 → 3Fe + 4CO271.一氧化碳还原氧化铜:CO + CuO → Cu + CO272.甲烷在空气中燃烧:CH4 + 2O2 → CO2 + 2H2O73.水在直流电的作用下电解:2H2O → 2H2↑ + O2↑74.石灰石与稀盐酸反应:CaCO3 + 2HCl → CaCl2 + H2O + CO2↑75.小苏打受热分解:2NaHCO3 → Na2CO3 + CO2↑ + H2O76.碳酸钠与稀盐酸反应:Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑77.双氧水在二氧化锰催化下分解:H2O2 → H2O + O2↑78.氯酸钾在二氧化锰催化下分解:KClO3 → KCl + O2↑79.硫酸铜与氢氧化钠反应:CuSO4 + 2NaOH → Cu(OH)2↓ +Na2SO480.氯化铁与氢氧化钠反应:FeCl3 + 3NaOH → Fe(OH)3↓ + 3NaCl81.硝酸铵受热分解:NH4NO3 → N2O↑ + 2H2O82.硝酸钾受热分解:KNO3 → KNO2↑ + O2↑83.碳酸氢铵受热分解:NH4HCO3 → NH3↑ + CO2↑ + H2O84.氢氧化钠与稀硫酸反应:NaOH + H2SO4 → Na2SO4 + 2H2O85.硫酸与氢氧化铜反应:H2SO4 + Cu(OH)2 → CuSO4 + 2H2O86.硫酸与氢氧化铁反应:Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 3H2O87.盐酸与硝酸银反应:HCl + AgNO3 → AgCl↓ + HNO388.盐酸与碳酸钠反应:Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑89.氯化钡与稀硫酸反应:BaCl2 + H2SO4 → BaSO4↓ + 2HCl90.硝酸与氢氧化钠反应:HNO3 + NaOH → NaNO3 + H2O91.氯化铵受热分解:NH4Cl → NH3↑ + HCl↑92.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl → NaCl + H2O + CO2↑93.硫酸铜与氢氧化钠反应:CuSO4 + 2NaOH → Cu(OH)2↓ +Na2SO494.硝酸银与氯化钠反应:AgNO3 + NaCl → AgCl↓ + NaNO395.一氧化碳还原氧化亚铁:FeO + CO → Fe + CO296.一氧化碳还原氧化银:Ag2O + CO → 2Ag + CO297.二氧化碳与氢氧化钡反应:CO2 + Ba(OH)2 → BaCO3↓ + H2O98.二氧化硫与氢氧化钾反应:SO2 + 2KOH → K2SO3 + H2O99.一氧化氮与氧气反应:NO + O2 → NO2100.二氧化氮与水反应:NO2 + H2O → HNO3。
中考化学常考化学方程式汇总
中考化学常考化学方程式汇总化学方程式是化学中非常重要的表达方式,能够描述化学反应的反应物、生成物以及反应的化学过程。
在中考化学考试中,常常会涉及到化学方程式的题目,所以熟悉一些常见的化学方程式是非常有必要的。
以下是一些常考的化学方程式汇总,包括了各种常见的化学反应及其方程式。
1.燃烧反应燃烧反应是一种常见的化学反应,包括有机物的燃烧反应和无机物的燃烧反应。
(1)有机物燃烧反应C₇H₁₆(l)+11O₂(g)→7CO₂(g)+8H₂O(g)(石油的主要成分燃烧反应)(2)碳的燃烧反应C(s)+O₂(g)→CO₂(g)2.酸碱反应酸碱反应是指酸和碱在适当条件下相互中和生成盐和水的反应。
(1)直接中和反应HCl(aq) + NaOH(aq) → NaCl(aq) + H₂O(l)(2)非金属氧化物与碱反应CO₂(g) + 2NaOH(aq) → Na₂CO₃(aq) + H₂O(l)(3)金属氧化物与酸反应Fe₂O₃(s) + 6HCl(aq) → 2FeCl₃(aq) + 3H₂O(l)3.酸酐与水的反应酸酐与水的反应是指酸酐溶于水生成酸的反应。
(1)二氧化硫溶于水生成亚硫酸SO₂(g) + H₂O(l) → H₂SO₃(aq)(2)三氧化硫溶于水生成硫酸SO₃(g) + H₂O(l) → H₂SO₄(aq)4.酸与金属的反应酸与金属的反应是指酸与金属反应生成盐和氢气的反应。
(1)直接反应Zn(s) + 2HCl(aq) → ZnCl₂(aq) + H₂(g)(2)间接反应2Al(s) + 3H₂SO₄(aq) → Al₂(SO₄)₃(aq) + 3H₂(g)5.金属氧化物与非金属反应金属氧化物与非金属反应是指金属氧化物与非金属元素反应生成氧化物的反应。
(1)碱金属氧化物与非金属反应2NaOH(aq) + CO₂(g) → Na₂CO₃(aq) + H₂O(l)(2)碱土金属氧化物与非金属反应CaO(s)+CO₂(g)→CaCO₃(s)6.化学焰燃烧化学焰燃烧是指一些金属离子在火焰中激发产生的特殊现象。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
22 氧化铜与硫酸 CuO+ H2SO4==CuSO4+ H2O
通电
23 电解水
2H2O====2H2↑+ O2↑
24 碳酸钙分解
CaCO3===高==温CaO+CO2↑
25 硫 酸 铜 与 氢 氧 CuSO4+ 2NaOH==Cu(OH)2↓+ Na2SO4
化钠
CaCO3+2HCl==CaCl2+ H2O+CO2↑ 化学方程式
号
14 铁与硫酸
Fe+ H2SO4== FeSO4+ H2↑
15 铁与盐酸
Fe+2 HCl== FeCl2+ H2↑
16 碳 酸 钠 与 氢 氧 Na2CO3+ Ca(OH)2== CaCO3↓+2 NaOH 化钙
17 硝 酸 银 与 氯 化 AgNO3+NaCl==AgCl↓+NaNO3 钠
5 二 氧 化 碳 与 氢 2NaOH+CO2== Na2CO3+ H2O
氧化钠的反应
MnO2
6 分 解 过 氧 化 氢 2H2O2===2 H2O+O2↑
制氧气
7 分 解 高 锰 酸 钾 2KMnO4=== K2MnO4+MnO2+ O2↑
制氧气
MnO2
8 分 解 氯 酸 钾 制 2KClO3====2KCl+3O2↑
氧气
高温
9 一 氧 化 碳 还 原 Fe2O3+3CO====2Fe&化铜 2CuO+C====2Cu+CO2↑
11 锌 与 稀 硫 酸 反 Zn+H2SO4== ZnSO4+ H2↑ 应
12 铁 与 硫 酸 铜 反 Fe+CuSO4== FeSO4+ Cu 应
13 碳酸钙与盐酸 序 化学反应
初中化学中考常考化学方程式集锦
序 化学反应
化学方程式
号
点
1 氢 气 在 氧 气 中 2H2+O2=燃==2H2O
燃烧
点燃
点燃
2 碳 在 氧 气 中 燃 C+O2===CO2(氧气足量);C+O2===2CO(氧气不足量)
烧
点
3 甲 烷 在 氧 气 中 CH4+2O燃2===2H2O+CO2 燃烧
4 二 氧 化 碳 与 氢 Ca(OH)2+CO2== CaCO3↓+H2O 氧化钙的反应
18 碳酸铵氯化钡 (NH4)2 CO3+BaCl2==BaCO3↓+ 2NH4Cl
19 氢 氧 化 钠 与 盐 NaOH+ HCl==NaCl+ H2O 酸
20 氢 氧 化 钠 与 硫 2 NaOH+H2SO4==Na2SO4+ 2H2O 酸
21 氧化铁与盐酸 Fe2O3+6HCl===2 FeCl3+3H2O
