高三化学专题复习-无机框图推断题教学案配套课件
合集下载
《无机框图题推断》PPT1 人教课标版

专题复习 无机框图题推断
授课人:高国花 2008.4
高考展望:
无机框图推断是多年来考查元素化合物知识的 热点题型 ,它融元素化合物、基本理论、计算于一 体。侧重考查学生思维的能力和综合应用的能力,具 有很高的区分度和很好的选拔功能,在历年的高考
卷中重现率几乎为100℅。一般氯、硫、氧、氮、 碳、钠、镁、铝、铁等元素单质及化合物之间 的转化关系是这类题的热点。
无机推断题的解题思路:
读懂题意和图意
找突破口或“题眼” 大胆推测 全面分析 验证
正确作答
关键是寻找“题眼”
“题眼”就是抓“特” 字
① ②③④ ⑤ ⑥ 特 特特特 特 特 殊 征殊征 殊 征 颜 反条转 生 数 色 应件化 产 据
1.与碱反应产生气体 (单 1)质 2AA、 llS2i NO aH OH2H 2H2O2NaA2lO 3H2
•
4.娄机为人正直。关心国事。做皇 太子老 师时, 向皇太 子陈说 正直道 理,并 上密奏 章陈述 将帅专权,对军纪的管理松懈,不 对是 非曲直 ,他当 面判断 ,事后 从不再 说;赞 人全面 ,不遗 漏
•
6.多样性意味着差异,我国的民族 多样性 决定了 以民族 为载体 的文化 的多样 性,这 种文化 的多样 性也意 味着各 民族文 化的差 异。
Si2NaOH2ON2aSi3O2H2
(2)铵盐:
N4 H 碱 N3H H 2O
2、与水反应产生气体 (1)单质
2Na 2H2O2NaO H H2 2F22H2O4HF O2
(2)化合物
2MNg3a2NO2232HH22OO34MNgaOOHH 2O22NH3
Al2S3
6H2O2AlOH3
(3)非金属→金属
授课人:高国花 2008.4
高考展望:
无机框图推断是多年来考查元素化合物知识的 热点题型 ,它融元素化合物、基本理论、计算于一 体。侧重考查学生思维的能力和综合应用的能力,具 有很高的区分度和很好的选拔功能,在历年的高考
卷中重现率几乎为100℅。一般氯、硫、氧、氮、 碳、钠、镁、铝、铁等元素单质及化合物之间 的转化关系是这类题的热点。
无机推断题的解题思路:
读懂题意和图意
找突破口或“题眼” 大胆推测 全面分析 验证
正确作答
关键是寻找“题眼”
“题眼”就是抓“特” 字
① ②③④ ⑤ ⑥ 特 特特特 特 特 殊 征殊征 殊 征 颜 反条转 生 数 色 应件化 产 据
1.与碱反应产生气体 (单 1)质 2AA、 llS2i NO aH OH2H 2H2O2NaA2lO 3H2
•
4.娄机为人正直。关心国事。做皇 太子老 师时, 向皇太 子陈说 正直道 理,并 上密奏 章陈述 将帅专权,对军纪的管理松懈,不 对是 非曲直 ,他当 面判断 ,事后 从不再 说;赞 人全面 ,不遗 漏
•
6.多样性意味着差异,我国的民族 多样性 决定了 以民族 为载体 的文化 的多样 性,这 种文化 的多样 性也意 味着各 民族文 化的差 异。
Si2NaOH2ON2aSi3O2H2
(2)铵盐:
N4 H 碱 N3H H 2O
2、与水反应产生气体 (1)单质
2Na 2H2O2NaO H H2 2F22H2O4HF O2
(2)化合物
2MNg3a2NO2232HH22OO34MNgaOOHH 2O22NH3
Al2S3
6H2O2AlOH3
(3)非金属→金属
高三高考化学二轮专题复习无机框图的推断课件

③C+D的化学反应方程式:H__2S__+_2_F_e_C_l_3=__2_F_e_C_l_2+_S__↓_+_2_H。Cl
16
A黑色固体 G溶液
H2S
SO2
C气体 通入足量O2 F
B+G
其中C、F为气体,B、D、E、G (无色)为溶液,D为氯化物,C 通入D中产生浅黄色浑浊,且pH值降低,根据以上事实填空:
①化学式:A__F_e_S____;B__F__e_S_O_4_;C__H__2_S___;G__H_2_S_O__4 ; ②F+E的离子方程式:_2_F_e_3_++__S_O_2_+_2_H__2O__=_2_F_e_2_++__S_O_4;2-+4H+
⑤新制Cu(OH)2与甘油、葡萄糖___绛__蓝__色______。
3. 焰色反应:
Na+(黄色)、K+(紫色)
4.在空气中变为红棕色:
NO
9
三、根据特殊反应推断
【例3】下列关系图中,A是一种正盐,D的分子量比C的分子量大 16,E是酸。
当X无论是强酸还是强碱时都有如下的转化关系:
X
YY
Z
A
B
C
D
无机框图题的推断
1
例1.由单质A和化合物B两种粉末组成的混合物,在一定条件 下可按如图所示关系进行转化:
高温 ①
单质A+ 化合物B
过滤② NaOH溶液
化合物C
盐酸
单质D
NaOH溶液
溶液F
沉淀H
固体
③ 加入D
④ 置于空气中
盐酸
NaOH溶液
溶液G
16
A黑色固体 G溶液
H2S
SO2
C气体 通入足量O2 F
B+G
其中C、F为气体,B、D、E、G (无色)为溶液,D为氯化物,C 通入D中产生浅黄色浑浊,且pH值降低,根据以上事实填空:
①化学式:A__F_e_S____;B__F__e_S_O_4_;C__H__2_S___;G__H_2_S_O__4 ; ②F+E的离子方程式:_2_F_e_3_++__S_O_2_+_2_H__2O__=_2_F_e_2_++__S_O_4;2-+4H+
⑤新制Cu(OH)2与甘油、葡萄糖___绛__蓝__色______。
3. 焰色反应:
Na+(黄色)、K+(紫色)
4.在空气中变为红棕色:
NO
9
三、根据特殊反应推断
【例3】下列关系图中,A是一种正盐,D的分子量比C的分子量大 16,E是酸。
当X无论是强酸还是强碱时都有如下的转化关系:
X
YY
Z
A
B
C
D
无机框图题的推断
1
例1.由单质A和化合物B两种粉末组成的混合物,在一定条件 下可按如图所示关系进行转化:
高温 ①
单质A+ 化合物B
过滤② NaOH溶液
化合物C
盐酸
单质D
NaOH溶液
溶液F
沉淀H
固体
③ 加入D
④ 置于空气中
盐酸
NaOH溶液
溶液G
高考化学二轮专题复习:无机框图题推断(教与学课件)

3. 写出C的溶液中通入过量氯气的离子方程 式______________________________________。
1. 据此推断,写出X、Y、Z名称:X__铁___ Y__溴___Z______。
2. X是最常见的单质,X元素在元素周期表 中位置为_________________。
3. 写出C的溶液中通入过量氯气的离子方程 式______________________________________。
1. 据此推断,写出X、Y、Z名称:X__铁___ Y__溴___Z__氢__气__。
2. X是最常见的单质,X元素在元素周期表 中位置为_________________。
3. 写出C的溶液中通入过量氯气的离子方程 式______________________________________。
点评 此题为无机框图题, 考查学生对常见
单质及化合物的掌握情况, 以及分析、推 理、正逆向思维等能力。
【考点搜索】
【考点搜索】
1. 熟练掌握以Na、Mg、Al、Fe等 金属为代表,以C、Cl、S、N等非金属 为代表的元素及其化合物相互转化的基 础知识。
2、掌握无机框图题推断时常见的突 破口(即“题眼”),如物质的颜色、火焰 的颜色、沉淀颜色的变化、具有唯一性 的特殊现象、特征反应等知识。
2、掌握无机框图题推断时常见的突 破口(即“题眼”),如物质的颜色、火焰 的颜色、沉淀颜色的变化、具有唯一性 的特殊现象、特征反应等知识。
3、掌握限定范围推断和不定范围推 断类型题的解题策略和思路。
2、掌握无机框图题推断时常见的突 破口(即“题眼”),如物质的颜色、火焰 的颜色、沉淀颜色的变化、具有唯一性 的特殊现象、特征反应等知识。
1. 据此推断,写出X、Y、Z名称:X__铁___ Y__溴___Z______。
2. X是最常见的单质,X元素在元素周期表 中位置为_________________。
3. 写出C的溶液中通入过量氯气的离子方程 式______________________________________。
1. 据此推断,写出X、Y、Z名称:X__铁___ Y__溴___Z__氢__气__。
2. X是最常见的单质,X元素在元素周期表 中位置为_________________。
3. 写出C的溶液中通入过量氯气的离子方程 式______________________________________。
点评 此题为无机框图题, 考查学生对常见
单质及化合物的掌握情况, 以及分析、推 理、正逆向思维等能力。
【考点搜索】
【考点搜索】
1. 熟练掌握以Na、Mg、Al、Fe等 金属为代表,以C、Cl、S、N等非金属 为代表的元素及其化合物相互转化的基 础知识。
2、掌握无机框图题推断时常见的突 破口(即“题眼”),如物质的颜色、火焰 的颜色、沉淀颜色的变化、具有唯一性 的特殊现象、特征反应等知识。
2、掌握无机框图题推断时常见的突 破口(即“题眼”),如物质的颜色、火焰 的颜色、沉淀颜色的变化、具有唯一性 的特殊现象、特征反应等知识。
3、掌握限定范围推断和不定范围推 断类型题的解题策略和思路。
2、掌握无机框图题推断时常见的突 破口(即“题眼”),如物质的颜色、火焰 的颜色、沉淀颜色的变化、具有唯一性 的特殊现象、特征反应等知识。
高考化学第一轮复习考点突破:《无机框图题推断》(课件)

(3) 反应①的化学方程式是 _3_F_e_+_4_H_2_O__高=_=_温=__F_e_3O__4_+_4_H_2____,在实验室中 引发反应④的操作是_加__少__量__K__C_l_O_3_,__插__上__镁_ _条__并__将__其__点__燃___
(4) 反应⑥的离子方程式是
________________________________
(3) 反应①的化学方程式是 _3_F_e_+_4_H_2_O__高=_=_温=__F_e_3O__4_+_4_H_2____,在实验室中 引发反应④的操作是_加__少__量__K__C_l_O_3_,__插__上__镁_ _条__并__将__其__点__燃___
(4) 反应⑥的离子方程式是 _2_A__l+_2_O__H__-_+_2_H__2O__=_2_A__lO__2_-_+_3_H__2↑___
(1) 写出B的电子式:
________________________________ (2) 写出生成E的电极反应式:
________________________,反应⑤的现象 是_____________________________________
(3) 反应①的化学方程式是 __________________________,在实验室中 引发反应④的操作是____________________
(3) 反应①的化学方程式是 __________________________,在实验室中 引发反应④的操作是____________________
______________ (4) 反应⑥的离子方程式是
________________________________
(4) 反应⑥的离子方程式是
________________________________
(3) 反应①的化学方程式是 _3_F_e_+_4_H_2_O__高=_=_温=__F_e_3O__4_+_4_H_2____,在实验室中 引发反应④的操作是_加__少__量__K__C_l_O_3_,__插__上__镁_ _条__并__将__其__点__燃___
(4) 反应⑥的离子方程式是 _2_A__l+_2_O__H__-_+_2_H__2O__=_2_A__lO__2_-_+_3_H__2↑___
(1) 写出B的电子式:
________________________________ (2) 写出生成E的电极反应式:
________________________,反应⑤的现象 是_____________________________________
(3) 反应①的化学方程式是 __________________________,在实验室中 引发反应④的操作是____________________
(3) 反应①的化学方程式是 __________________________,在实验室中 引发反应④的操作是____________________
______________ (4) 反应⑥的离子方程式是
________________________________
高中化学复习PPT课件高三《无机物推断》专题复习课堂教学

拓展2:
讨论:N、A、L、J可能是什么物质 拓展3:
讨论:A可能是什么物质
拓展4:
讨论:A、I可能是什么物质 拓展5:
讨论:G、F可能是什么物质
拓展6:
(09四川卷)
已知:A-O分别代表一种物质,以上为它们之间的转 化关系(反应条件略去)。A、B、H分别是由短周期 元素组成的单质。B与冷水缓慢反应,放出氢气。D是 一种离子化合物,其阴阳离子的个数比为2:3,且能 与水反就应得到两种碱。C为淡黄色固体化合物。 问题1:A为: C为: B为: 问题2:写出D与足量的N反应生成E和F的化学方程式:
讨论:解无机推断题在审题、解题等环节应注意哪些 关键细节? 问题:推测NH4ClO加热分解的产物有哪些?
NH4ClO加热分解的产物到底有哪些?有一位同学将其加 热分解产物用如下框图进行描述。
J M +H L J N 学习与生活 一样,只要 你成为有心 人,你将 机 推 断
解 题 思 路
我是一种无机物,我将逐一描述我所具有的性质, 请同学们锁定我的范围,看看哪位同学最先猜出 我是谁?
1、我既能与强酸溶液反应又能与强碱溶液反应 2、我由短周期元素组成,我加热能分解 3、我与氢氧化钠溶液反应生成能使湿润的酚酞试纸 变红的气体 4、我与盐酸反应生成能使品红溶液褪色的气体 5、组成我的各元素的原子个数比为1:4:1:1
A
H I R
T
(白烟)
已知:J为常见的无色无味液体,则R、I、A、H、 L、M分别是什么物质? 问题:A、H、L、M之间存在怎样的特征反应
拓展1: (09年北京理综· 12) A、B、C、D、E、X由短周期元素组成的中学常见 无机物,存在如上图转化关系(部分生成物和反 应条件略去)。
高三化学高考复习《无机框图推断题——框图题的解题思路和技巧》研讨公开课PPT

3、A、B、C是中学化学中常见的单质,常温下甲、乙两种化合物 分别是黑色的固体和无色液体,这些化合物和单质间有如下关系: Fe3O4 。 ①元素A有可变化合价,则单质A是 Fe ,化合物是 ②高温下: ⑴甲+C→A+乙;⑵A+乙→甲+C,欲使反应⑵顺利进 行,应采取的措施是: 升温并及时将H2放出 。 ③甲还能与另一种常见金属在一定温度下反应,并放出大量 的热,其化学 反应方程式为: 8Al+3 Fe3O4 ==== 4Al2O3+9 Fe 。
• 提醒:注意审题---根据要求回答 • 近几年高考中出现很多考生不按要求答题而失分。 如把答案写在密封线内,阅卷时无法看到答案而不给分; 要求写元素名称而错写成元素符号,而要求写元素符号 又答成元素名称或分子式;要求写物质名称而错写成分 子式;要求写结构简式的错写成分子式或名称;要求写 离子方程式而错写成化学方程式;要求画离子结构示意 图而错答为原子结构示意图;把相对原子质量、相对分 子质量、摩尔质量的单位写成“克”;把物质的量、摩 尔浓度、气体体积、质量、溶解度、密度、压强等的单 位漏掉;化学方程式、离子方程式不配平;热化学方程 式不注明物质的状态等。因此答题时必须按题目要求来 回答,避免不必要的失பைடு நூலகம்。
3 、当框图中无明显题眼时,我们也可以从题干 中甚至可以从题肢中寻找新的信息。
解无机框图题的基本思路
原 题 审析
明显条件 抓关键
推断
检验
隐蔽条件 (题眼)
结论
此类题的思维方法:可以是正向思维,即从前向后推导, 也可以是逆向思维,即根据特征先确定后面的物质;还可以从 中间开始向前向后推导,究竟按哪一种思维方式,应根据题干 信息和框图信息找出的突破口的位置确定。
• 提醒:注意审题---根据要求回答 • 近几年高考中出现很多考生不按要求答题而失分。 如把答案写在密封线内,阅卷时无法看到答案而不给分; 要求写元素名称而错写成元素符号,而要求写元素符号 又答成元素名称或分子式;要求写物质名称而错写成分 子式;要求写结构简式的错写成分子式或名称;要求写 离子方程式而错写成化学方程式;要求画离子结构示意 图而错答为原子结构示意图;把相对原子质量、相对分 子质量、摩尔质量的单位写成“克”;把物质的量、摩 尔浓度、气体体积、质量、溶解度、密度、压强等的单 位漏掉;化学方程式、离子方程式不配平;热化学方程 式不注明物质的状态等。因此答题时必须按题目要求来 回答,避免不必要的失பைடு நூலகம்。
3 、当框图中无明显题眼时,我们也可以从题干 中甚至可以从题肢中寻找新的信息。
解无机框图题的基本思路
原 题 审析
明显条件 抓关键
推断
检验
隐蔽条件 (题眼)
结论
此类题的思维方法:可以是正向思维,即从前向后推导, 也可以是逆向思维,即根据特征先确定后面的物质;还可以从 中间开始向前向后推导,究竟按哪一种思维方式,应根据题干 信息和框图信息找出的突破口的位置确定。
高考化学无机推断题的常见题型PPT教学课件
变式训练1 阅读下列信息: Ⅰ.表中①~⑥为部分短周期元素的化合价及相应氢 化物沸点的数据:
元素性质
氢化物的沸 点
(℃) 最高化合价
最低化合价
① -60.7
+6 -2
元素编号 ② ③④ ⑤
-33.4 100 -87.7 19.54
+5
+5
-3 -2 -3 -1
⑥ -84.9
+7 -1
A、B、C均为上表中的元素。 Ⅱ.B与C两元素可形成化合物CB2、CB3,二者均可 用于制备强酸甲。 Ⅲ.A与B两元素可形成化合物AB、AB2,二者均可 用于制备强酸乙。 请回答下列问题: ((12))BA元元素素位气于态周氢期化表物中的第结构二式为周期ⅥA 族。
类型三 利用物质及反应的特殊现象推断的无机推断 【例3】有如图所示的反应(可加热),其中A、B、
C、D为中学化学中常见的单质或化合物,请按 要
求填空。
(1)若A为黑色固态单质,C为无色有刺激性气
味
C+2H2SO4
(的浓气)体,C则O该2↑反+应2S的O化2↑+学2方H程2O式为
。
(2)若A为红色金属单质,该反应在常温下剧烈发生 且产生有色气体,则反应中氧化剂与还原剂的物质的 量之比为 2∶1 。 (3)若A为黑色粉末,C为有色气态单质,则产生 1 mol C时被氧化的B的物质的量为2 mol 。 (4)若A为白色乳状物,且其溶解度随温度的升高而 降低,D可作干燥剂,则该反应在工业上可用于制 备漂白粉(漂粉精) 。
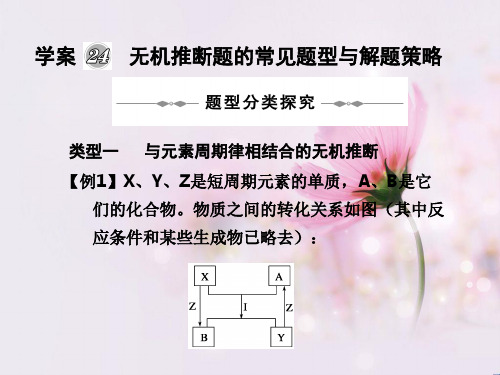
学案 无机推断题的常见题型与解题策略
类型一 与元素周期律相结合的无机推断 【例1】X、Y、Z是短周期元素的单质,A、B是它
们的化合物。物质之间的转化关系如图(其中反 应条件和某些生成物已略去):
高三化学无机框图题归纳总结PPT教学课件

它包含了5种化合物中的所有元素,生成该化合物的化学方程式
是 Ca(OH)2+2CO2===Ca(HCO3)2
。
2+
2-
(3)V的电子式是 Ca C C 。
一、无机框图题的主要特点
1. 低起点,高落点。即叙述简洁,完成起来难度大。 2. 知识覆盖面广。有可能一步推错,整题失分。 3.考题内容多为常见元素及其化合物知识,且常 有气体物质出现。“常见”是指短周期的元素。
2H2↑+O2↑
(2)仅溶质参加反应 :
2HCl 电解 H2↑+Cl2↑ CuCl2 电解 Cu+Cl2↑
(3)溶质、溶剂均参加反应 : 2NaCl+2H2O 电解 Cl2 ↑+H2↑+2NaOH 2CuSO4+2H2O 电解 2Cu+O2↑+2H2SO4
电解
4AgNO3+2H2O 4Ag+O2↑+4HNO3
①NaH+H2O→H2↑ ②Na2O2+H2O→O2↑
①Al2S3+6H2O=2Al(OH)3↓+3H2S↑ ②Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑ ③CaC2+H2O→C2H2↑ ④Al4C3+H2O→CH4↑
·与碱反应产生气体的反应
单
质
Al、Si OH H2 2Al 2NaOH 2H2O
例1.(08全国)V、W、X、Y、Z是由周期表中1~20 号部分元素组成的5种化合物,其中V、W、X、Z均为两 种元素组成,上述5种化合物涉及的所有元素的原子序数 之和等于35。它们之间的反应关系如下图:
(1)5种化合物分别是V CaC2 、W CaO 、X CO2 、
Y Ca(OH)2、Z C2H2 。(填化学式) (2)由上述5种化合物中2种化合物反应可生成一种新化合物,
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
A为AlO2-,D为H+
A为C,D为H2O
A为P,D为Cl2
3、注意几个典型转化关系
例题3:下列关系图中,A是一种正盐,D的分子 式比C的大16,E是酸,当X无论是强酸或强碱 都有如下反应关系: A
X B Y
C Y
D
Z
E
当X是强酸时, A、B、C、D、E均含同一元素; 当X是强碱时, A、B、C、D、E均含另一元素。 回答下列问题(用化学式) (NH4)2S O2 H2O 1、A是______,Y是______ ,Z是______ H2SO4 2、当X是强酸时,E是 ______ 当X是强碱时,E是 ______ HNO3
C A
黑色晶体B H2SO4 OH-
E
O
2
D
OH-
红褐色固体F
FeSO4 A为 Fe B为 Fe3O4 C为___________ Fe(OH)3 D为 Fe2(SO4)3 E为 Fe(OH)2 F为___________
二、根据特征反应现象推断
常见的特征反应现象及对应物质 Na 1.焰色反应显黄色的元素是__,显紫色(透过钴玻璃)的元素是__ K
请回答: (1)写出A、B和C的化学式:A ,B ,C 。 (2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离 子)的离子方程式: , 。 (3)写出将SO2气体通入K溶液中发生反应的离子方程式: (4)写出由F→H的化学方程式: 。 【答案】 (1)NaI; NaClO; AgI (2)2I+ClO+H2O=I2+Cl+OH; I2+5ClO+2OH= 2+5Cl+H2O (3)Fe 3+++2H2O=Fe2+++4H+ (4)Cl2+2NaOH=NaClO+NaCl+H2O
Cu2+ MnO4- 紫色溶液 Fe3+ 棕黄色溶液 血红色溶液 [Fe(SCN)]2+
橙(或黄)色 溶液
Br2(或I2)(水)
蓝色溶液
蓝色晶体
CuSO4· 2O 5H Br2、NO2
BaSO4、BaCO3、 CaCO3、AgCl、 红棕色气体Cu(OH)2 Nhomakorabea黄绿色气体
Cl2
例题1:根据下图所示的关系,确定A、B、C、 D、E、F的化学式,并写有关方程式。
五、根据重要工业生产反应推断
我们学过哪些重要工业生产反应?
1、煅烧石灰石 2、煅烧黄铁矿 3、二氧化硫的催化氧化 4、氨的催化氧化 5、合成氨 6、电解饱和食盐水 7、工业制盐酸 8、高炉炼铁 9、工业制取漂粉精 10、工业制水煤气 11、硅酸盐工业
例题5、根据下列框图关系填空,已知反应 ①、③是工业生产中的重要反应,D、E常温 下为气体、X常温下为无色液体,H与E相对分 子质量之间的关系为:Mr(H) -Mr(E) =34, 又知C焰色反应火焰呈黄色。
无机框图推断题
“无机框图推断题”的命题思想和特点:
“无机框图推断题”作为一种高考的 题型,它有明显的学科特点,不仅考查学 生对元素及其化合物主干知识掌握的情况, 更能考查思维的敏捷性、发散性、严密性 和分析推理综合应用元素化合物知识的能 力。
框图题的“题眼”主要有以下几方面
1、物质的特有颜色 2、特征反应现象 3、特征转化关系 4、特殊反应条件 5、重要工业生产反应 6、特征数据(反应物物质的量比、相对分子 质量、化合物中离子个数比、电子总数、化 合价等)
(1)化合物A中所包含的化学键有: 离子键、非极性键(或共价键) 。 Fe2O3 + 6H+ = 2Fe3+ + 3H2O (2)反应④的离子方程式: 。 Fe 反应⑤的化学方程式: 2(SO4)3 + 6NaOH = 2Fe(OH)3↓+3Na2SO4。 (3)已知每生成16g E,放出106.5kJ热量,则反应①的热化学方程 式为: 。
H 高温 A X
1
高温
4
A I G 的 溶 J 液 K的溶 液
C D E F G的溶液 H
右图装置
2
X
5
X B
3
6
D
【练习】1、 05广东化学22 :钛Ti被称为继铁、 铝之后的第三金属,钛白TiO2是目前最好的白色 颜料。制备TiO2和Ti的原料是钛铁矿,我国的钛铁 矿储量居世界首位。含有Fe2O3的钛铁矿FeTiO3 制取TiO2的流程如下:
Al,NH4HCO3 ,(NH4)2CO3 , NH4HSO3 ,(NH4)2SO3 , (NH4)2S, NH4HS _________________________________________________________
NH3 9.能使湿润的红色石蕊试纸变蓝的气体是_____ Al、Si、铵盐 10.与碱反应产生气体的物质是_________________ H2、NH3 产生气体一般是_________ Na 、F2 、Na2O2 11.与水反应产生气体的物质一般是_________________ 12.既能酸反应,又能与碱反应的物质是 Al 、Al2O3、Al(OH)3、弱酸弱碱盐、弱酸的酸式盐 ___________________________________________________ 13.既产生沉淀又产生气体的物质一般是 CaC2、Al2S3、Mg3N2 与H2O; S2O32-与H+; __________________________________________________ CO32-、HCO3-、 SO32- 、 HSO3-、 S2-、HS- 与Al3+; __________________________________________________ CO32-、HCO3-与Fe3+(双水解) __________________________________________________
H2S 2.有臭鸡蛋气味的气体是 ______
3.在空气中由无色迅速变为红棕色的气体是_________ NO
4.使品红溶液褪色的往往是 SO2 (Cl2使品红溶液褪色后不恢复) __________ I2 5.能使淀粉变蓝的是 __________ 6.与碱溶液反应生成白色沉淀且放置空气中变灰绿色最终变红褐色 Fe2+ 的离子是_________ SCN— Fe3+ 7.滴入_____ 溶液显血红色以及遇苯酚显紫色的离子是 _______ 8.既能跟酸反应又能跟碱反应且生成气体的物质一般是
【答案】 1 4; ⅣB 2 将Fe3+还原为Fe2+; 析出或分离、或得到 FeSO4· 7H2O 3 FeSO4· 7H2O; 石灰或碳酸钙、废碱 4 80 kJ· mol1 ; 防止高温下MgTi与空气中的O2或 CO2、N2作用
【练习】2、05天津26A和B均为钠盐的水溶液,A呈中性,B呈碱 性并具有氧化性。下述为相关实验步骤和实验现象:
1 Ti的原子序数为22,Ti位于元素周期表中第 周期,第 族。 2 步骤①加Fe的目的是 ; 步骤②冷却的目的是 。 3 上述制备TiO2的过程中,可以利用的副产物是 ;考 虑成本和废物综合利用因素,废液中应加入 处理。 4 由金红石TiO2制取单质Ti,涉及到的步骤为:
已知:① Cs+O2g=CO2g; H=3935 kJ· mol1 ② 2COg+O2g=2CO2g; H=566 kJ· mol1 ③ TiO2s+2Cl2g=TiCl4s+O2g; H=+141 kJ· mol1 则TiO2s+2Cl2g+2Cs=TiCl4s+2COg的H= 。 反应TiCl4+2Mg=2MgCl+Ti 在Ar气氛中进行的理由 是 。
例题2:A、B、C、D、四种元素原子核电荷数依次增大 (均小于20),其单质及相应的化合物能发生如下反 应关系: A
E C
B
混合后加水 白色胶状沉淀G NaOH溶液 无色溶液J 臭鸡蛋气味气体H 无色溶液I AgNO3 稀HNO3 焰色反应:紫色
白色沉淀K
F
D
1、写出B、D形成化合物电子式_____________ 2、写出下列有关物质化学式:E ______ J ______ AlCl3 NaAlO2 3、写出C单质与H水溶液反应的离子方程式___________
FeS2 (s) + 11/4 O2 (g) = 1/2 Fe 2 O 3 (s)+ 2SO2 (g) ; △H=-852kJ/mol
A:FeS2 ;
B: Na2O2 ; C:NaOH;
D: O2 ;
E:SO2;
F: Fe2O3 ;
G: SO3 ; H:H2SO4 ; J: 2Fe(OH)3↓ ;
I: Fe2(SO4)3 ;
【练习】3、05MCE126已知A、B、C、D为气体,E、F为固体, G是氯化钙,它们之间的转换关系如下图所示:
(1)D的化学式(分子式)是 ,E的化学式(分子式)是 (2)A和B反应生成C的化学方程式是 。 (3)E和F反应生成D、H和G的化学方程式是 。 答案: (1)NH3; NH4Cl (2)H2+Cl2=2HCl (3)2NH4Cl+Ca(OH)2 ==2NH3↑+2H2O+CaCl2
甲:Na;乙:S;丙: O2 ;A:Na2O; B: Na2O 2;C:SO2; D:SO3;X: Na2S;Y:Na2SO3 ;Z:Na2SO4 ;
解题关键:
小结:
找题眼
特殊颜色
特征反应
特征转化
特殊条件
特征数据
试试看
下图表示各物质之间的转化关系。已知A、D、F、 H均为单质,X常温下为无色液体,B为淡黄色固 体,J溶于酸得到黄色溶液。
Cl2+H2S=S↓+2H++2Cl- 3+ 24、写出E、F反应的离子方程式: Al + S + H2O =
三、根据特征转化关系推断
