【全程复习方略】2013版中考化学 第四单元 第2课时物质的组成与构成课件 新人教版
合集下载
中考化学第一轮复习 第四单元 物质的组成与构成课件 人教新课标

误区.案例剖析
【典例1】下列有关分子、原子和离子的说法正确的是 A.分子是保持物质性质的一种粒子 B.物体有热胀冷缩现象,主要是因为物体中的粒子大小随温 度的改变而改变 C.分子、原子、离子都可以直接构成物质 D.在化学反应中,任何离子都不能再分 【易错角度】A、B、D
【错因分析】
【参考答案】C
【解析】(1)丹桂飘香是因为分子在不断地做无规则运动。 (2)由图示可以看出反应物为甲烷和氧气,反应物中化合物 的化学式为CH4,生成物中水分子与二氧化碳分子个数比为 2∶1。从微观角度可以得出:在化学变化中原子的种类和数 目不变;在化学变化中,分子分裂成原子,原子重新组成新 的分子;在化学变化中分子可以再分,而原子不可再分。 (3)元素符号错误的是硅,第二个字母应小写,改为“Si”; 地壳中含量最多的元素是氧元素,质子数为8,在化学反应 中易得电子。(4)由图示可以看出是NaOH与盐酸的反应, 化学方程式为:NaOH+HCl====NaCl+H2O,当恰好完全 反应时,溶液是氯化钠溶液,其中粒子为:Na+、Cl-、H2O。
策略.专家指导
1.认识物质的微粒性,知道分子、原子、离子等都是构 成物质的基本微粒。能用分子、原子的观点解释某些常见的 变化和现象。
2.知道原子的构成,分子和原子的本质区别和联系,同 种元素的原子和离子之间的相互转化关系。
3.知道元素组成物质,记住且会书写常见元素的名称和 符号;知道元素的简单分类。
【典例1】(2011·滨州中考)下列叙述错误的是( ) A.分子、原子和离子都能直接构成物质 B.原子中原子核与核外电子的电量相等,电性相反,所以整 个原子不显电性 C.决定原子质量大小的主要是质子和电子 D.原子如果得到或失去电子就变成离子
初三化学中考专题复习 物质组成的表示 复习课课件(共33张PPT)

化学式是对物质组成的真实反映,不得随意改动 元素符号右下角的数字!
1、请观察下列试剂瓶的标签,错误的一个是( )
2、已知某元素R只有一种化合价,其氯化物的化学 式为RCl3 ,那么其氧化物的化学式为 R2O3 。
3、 化学用语简洁明了、信息丰富、国际通用。对 下列化学用语解释正确的是( C ) A. Mg+2——镁离子 B.O——氧气 C.2CO2——2个二氧化碳分子 D.2N——2个氮元素
(含苯丙氨酸)、苋菜红
不同元素的原子相互化合时,原子个数比不同。
试一试:请标出下列物质中各元素的化合价:
Cu H2 FeO Fe2O3 NaCl
CaCl2 N2O5 NH3
1、观化察合上述价物的质一中般各元规素律的:化合价,你获取哪些
信1.金息属?与非金属结合时:金属元素显正价, 非金属元素显负价; 2、在化合物中:氢通常显 +1 价,氧显-2价。 3、单质中元素的化合价为零 4、在化合物中,各元素的化合价代数为零
1、现在很多城市已开始使用西气东输工程送来的天 然气,天然气主要成分是CH4,下列四位同学在讨论
化学式CH4的意义,其中错误的是( D )
表示甲烷 这种物质
表示一个 甲烷分子
表示甲烷由碳氢 两种元素组成
表示甲烷由一个 碳原子和四个氢 原子构成
8
2、1985年科学家发现了一种新物质,该物质中有一 种由多个五边形和六边形组成的形似足球的笼状分子, 称为足球烯(如图示)其化学式为化学式为C60, 对该物质的下列说法不正确的是:( B )
B.KC+5lO3
+3 C.HClO2
+5 D. Cl2O5
提示:因为所有物质中都有Cl元素,那先找出各物质中氯元 素的化合价!就有发现。。。
九年级化学上册 第四单元《物质构成的奥秘》物质组成的表示课件

该物质的名称为
+4,
该物质属于
(填二物氧质化类氮别)
氧化物
12/10/2021
第二页,共二十一页。
(3)该物质(wùzhì)的相对分子质量为 46 ,分子中
各原子的个数比为
nN:nO=1:。2
(4)该物质由 2种元素组成,各元素的质量比
为
mN:mO=,7氮:16元素的质量分数为
。
30.4%
12/10/2021
化学式:
(1)金属氧化物 Na2O;
(2)非金属氧化物
CO2 CO H2O H;2O2
(3)酸 H2CO3 CH3COOH ;
(4)碱 NaOH ;
(5)盐
Na2CO3 NaHCO3 ;
(6)非金属单质
(7)金属单质
C Na
O2 H2
。
12/10/2021
第十九页,共二十一页。
10.以下是从元素周期表中截取的三种(sān zhǒnɡ)元素的信息,请 回答下列问题:
中考 导航 (zhōnɡ kǎo)
3、下列(xiàliè)方框中,符合 2H2意义的示意图是( D )
4.研究发现,达菲对甲型HIN1流感病毒有抑制作用,从香
料下八列角(xiàl中iè)对提莽取草的酸莽的草说酸法(不C正7H确6O的5)是是(合成达)菲的C原料之一。
A.它由碳、氢、氧元素组成
B.氢元素质量分数最小 C.莽草酸是氧化物
请回答以下(yǐxià)问题:
( (21))A1中个氮B分元子素中和含氢有元_素__的_质_2个量原比子为。_____。14:3
(3)4种物质中,属于化合物的是_____(A填图D中字母)。
12/10/2021
初中化学_物质的组成PPT课件

1、最灵繁的人也看不见自己的背脊。——非洲 2、最困难的事情就是认识自己。——希腊 3、勇猛、大胆和坚定的决心能够抵得上武器的精良。——达· 芬奇 4、与肝胆人共事,无字句处读书。——周恩来 5、一个人即使已登上顶峰,也仍要自强不息。——罗素· 贝克 6、一切节省,归根到底都归结为时间的节省。——马克思 7、自知之明是最难得的知识。——西班牙 8、勇气通往天堂,怯懦通往地狱。——塞内加 9、有时候读书是一种巧妙地避开思考的方法。——赫尔普斯 10、阅读一切好书如同和过去最杰出的人谈话。——笛卡儿 11、有勇气承担命运这才是英雄好汉。——黑塞 12、只有把抱怨环境的心情,化为上进的力量,才是成功的保证。——罗曼· 罗兰 13、知人者智,自知者明。胜人者有力,自胜者强。——老子 14、意志坚强的人能把世界放在手中像泥块一样任意揉捏。——歌德 15、最具挑战性的挑战莫过于提升自我。——迈克尔· F· 斯特利 16、业余生活要有意义,不要越轨。——华盛顿 17、意志是一个强壮的盲人,倚靠在明眼的跛子肩上。——叔本华 18、最大的挑战和突破在于用人,而用人最大的突破在于信任人。——马云 19、我这个人走得很慢,但是我从不后退。——亚伯拉罕· 林肯 20、要掌握书,莫被书掌握;要为生而读,莫为读而生。——布尔沃 21、要知道对好事的称颂过于夸大,也会招来人们的反感轻蔑和嫉妒。——培根 22、业精于勤,荒于嬉;行成于思,毁于随。——韩愈 23、最大的骄傲于最大的自卑都表示心灵的最软弱无力。——斯宾诺莎 24、知之者不如好之者,好之者不如乐之者。——孔子 25、学习是劳动,是充满思想的劳动。——乌申斯基 26、要使整个人生都过得舒适、愉快,这是不可能的,因为人类必须具备一种能应付逆境的态度。——卢梭 27、越是无能的人,越喜欢挑剔别人的错儿。——爱尔兰 28、意志命运往往背道而驰,决心到最后会全部推倒。——莎士比亚 29、越是没有本领的就越加自命不凡。——邓拓 30、阅读使人充实,会谈使人敏捷,写作使人精确。——培根
初中九年级化学系列复习公开课课件精品PPT第四单元物质构成的奥秘

⑹有的元素有可变化合价
-3 +5
标出NH4NO3中氮元素的化合价 -3
化合价用+n或-m标在元素符号或原子团的 正上方 ,如: NH3 ; 离子所带电荷数用n+或m-标在元素符号或原子团的 右上角,如:CO32-。
有关化学式的计算
类型
举例
计算相对分子质量(符号为Mr) Mr(O2)= Mr[CO (NH2)2]=
结论
元素的性质,特 别是化学性质与 元素原子的最·外层 电子数关系密切
原子与离子的比较
原子
阳离子
阴离子
核电荷数与核外 核电荷数= 电子数的关系 核外电子数
核电荷数 > 核外电子数
核电荷数 < 核外电子数
电性
不显电性
带 正 电荷
带 负 电荷
举例
Na、Cl
Na+
Cl-
Na+
Cl-
Na
结构示意图特点 Cl
化合价规律及其应用
定义 规律 提示
化合价表示原子之间相互化合的数目
⑴化合物中元素正负化合价代数和为 零 。
⑵单质中元+1 价;氧通常显 -2 价。
⑷化合物中,金属元素通常显 正价 ,非金属元素通常显 负价 。
⑸原子团的化合价等于组成元素化合价的 代数和 。
构成的物质 离子化合物(如NaCl、MgCl2等)
原子结构与元素化学性质的关系
元素分类 金属元素 非金属元素
稀有气体元素
最外层电子数 得失电子趋势
一般是是1~3 易失去最外层电子
一般≥4(氢为1) 易得到电子
8(氦为2)
不易 得失 电子 (常称为稳定结构)
化学性质 较易发生 化学反应
不易发生 化学反应
= 核外电子总数 ⑵原子内,质子数与中子数 不一定
物质的组成构成与分类

考考点点六 六元元素素周周期期表表
1.元素周期表合理有序地对所有已知元素进行了排列。表中每一横行表示一个周期, 从左到右元素的核电荷数逐渐变大, 电子层数不变;每一竖列表示一个族,从上到下元素的 电子层数逐渐增多,化学性质相似。
2.原子序数=质子数 (或核电荷数 );周期数= 电子层数。
考点七 物质的分类
【解析】此题考查对原子结构示意图的认识. 圆圈内的数字表示质子数;弧线表示电子 层,弧线上的数字表示该电子层上的电子数;最外层电子数小于 4 时,原子易失去电子形成 带正电荷的阳离子。故 A、B、C 均正确。钠元素为金属元素,故 D 错误。
【答案】 D
某粒子的结构示意图为
A.核内有 14 个质子 C.核外有 3 个电子层
◎知识结构
?? 原子核???质中子子??+不?带电? ? 原子
?+?
?? 核外电子?-?
混合物
?? ??金属 ? ??单质?非金属
? 物质的 ????? ????? ??? 分类
纯净物
?? 稀有气体
化合物
氧化物??? 金非属金氧属化氧物化物
酸、碱、盐 有机物
考考点点二 二原原子子的的构构成成
【解析】此题考查物质的组成。从宏观角度讲,物质是由元素组成的,因此, “低碳生 活”中的“碳”指的是碳元素。
【答案】A
2.(2010·北京)地壳中含量最多的非金属元素是 ( ) A.氧 B.硅 C.铝 D.铁 【解析】 此题考查地壳中的主要元素。地壳中含量较多的四种元素依次是氧、硅、铝、 铁,因此,地壳中含量最多的非金属元素是氧元素。答案为 A。 【答案】 A
【解析】此题考查分子、原子、离子的知识。分子是保持物质化学性质的最小粒子,因 为物质的性质包括化学性质和物理性质,因此不能说分子是保持物质性质的一种粒子,A 错; 物体有热胀冷缩现象,主要是物体中粒子间的间隔随温度变化而变化造成的, 实际上,粒子 大小是不随温度的改变而改变的, B 错;分子、原子、离子都是构成物质的基本粒子, C 正 确;在化学反应中,有些离子是能再分的,如在反应 H2CO3===H2O+CO2↑中, CO23-就分 开了,D 错。
2024年中考化学一轮复习-第2讲 物质的组成与分类(41张PPT)

A. B. C. D.
【解析】氧化物是指由两种元素组成,且其中一种元素是 的化合物。 由一种元素组成,不属于氧化物; 是由 、 两种元素组成的化合物,属于氧化物; 、 均是由三种元素组成的化合物,不属于氧化物。
B
思维点拨 纯净物和混合物的区别是含有一种或不同种物质,单质和化合物都是纯净物。氧化物、酸、碱、盐均为化合物,氧化物的特点是“两种元素、其中含氧”;酸解离后的阳离子全部是 ,碱解离后的阴离子全部是 ;盐由金属离子(或铵根离子)与酸根离子构成。有机化合物与无机化合物以是否含有碳元素区分。
针对训练
1.(2022·广西柳州中考)分类是一种重要的化学观念。下列物质属于单质的是( ) 。
A
A.硫 B.硝酸 C.硫酸铜 D.氢氧化钾
2.(2023·广西桂林二模)下列物质属于有机化合物的是( ) 。
D
A. B. C.C D.
3.(2023·黑龙江绥化中考)“ ”和“ ”分别代表不同元素的原子,下列图像能表示化合物的是( ) 。
②氧化物中一定含氧元素,但含氧元素的化合物不一定是氧化物。例如, 含氧元素,却不属于氧化物。③盐中不一定含有金属离子。例如, 、 等铵盐不含金属离子。
重要考点
2.元素。
定义
具有相同__________(即____________)的一类原子的总称
理解
①一种元素与另一种元素的本质区别在于核内质子数不同。②元素与原子的区别在于:元素是一个宏观概念,用于表示物质的组成,只有种类的含义,而没有数量的含义;原子是一个微观概念,用于表示物质或分子的构成,既有种类的含义,又有数量的含义
一个周期
一个族
(2)规律:同一周期的元素的化学性质不相同,同一纵列的元素的化学性质相似。(3)信息:表中每格包含__________(即质子数、核电荷数、核外电子数)、元素名称、元素符号、______________等信息。
【解析】氧化物是指由两种元素组成,且其中一种元素是 的化合物。 由一种元素组成,不属于氧化物; 是由 、 两种元素组成的化合物,属于氧化物; 、 均是由三种元素组成的化合物,不属于氧化物。
B
思维点拨 纯净物和混合物的区别是含有一种或不同种物质,单质和化合物都是纯净物。氧化物、酸、碱、盐均为化合物,氧化物的特点是“两种元素、其中含氧”;酸解离后的阳离子全部是 ,碱解离后的阴离子全部是 ;盐由金属离子(或铵根离子)与酸根离子构成。有机化合物与无机化合物以是否含有碳元素区分。
针对训练
1.(2022·广西柳州中考)分类是一种重要的化学观念。下列物质属于单质的是( ) 。
A
A.硫 B.硝酸 C.硫酸铜 D.氢氧化钾
2.(2023·广西桂林二模)下列物质属于有机化合物的是( ) 。
D
A. B. C.C D.
3.(2023·黑龙江绥化中考)“ ”和“ ”分别代表不同元素的原子,下列图像能表示化合物的是( ) 。
②氧化物中一定含氧元素,但含氧元素的化合物不一定是氧化物。例如, 含氧元素,却不属于氧化物。③盐中不一定含有金属离子。例如, 、 等铵盐不含金属离子。
重要考点
2.元素。
定义
具有相同__________(即____________)的一类原子的总称
理解
①一种元素与另一种元素的本质区别在于核内质子数不同。②元素与原子的区别在于:元素是一个宏观概念,用于表示物质的组成,只有种类的含义,而没有数量的含义;原子是一个微观概念,用于表示物质或分子的构成,既有种类的含义,又有数量的含义
一个周期
一个族
(2)规律:同一周期的元素的化学性质不相同,同一纵列的元素的化学性质相似。(3)信息:表中每格包含__________(即质子数、核电荷数、核外电子数)、元素名称、元素符号、______________等信息。
【2014年复习参考】2013版中考化学(沪教版)全程复习方略配套课件
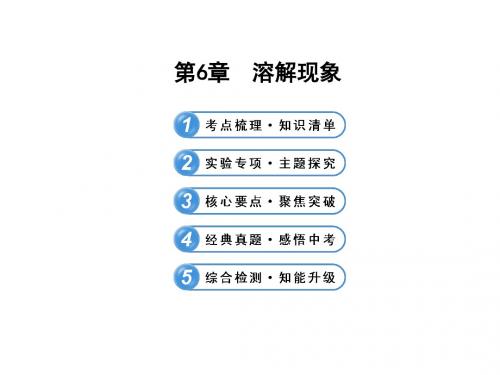
提示:溶质的质量分数是指溶质质量与溶液质量之比,因此,
10%的含义是指每100 g食盐溶液中含有10 g食盐,90 g水。 4.饱和溶液变为不饱和溶液溶质质量分数一定变小。( × )Leabharlann 转移。物质的溶解性 1.概念
一种物质(溶质) 溶解在_________________ 另一种物质(溶剂) 中的_____ 能力 。 _______________
2.影响因素 溶质 和_____ 溶剂 的性质、_____ 温度 。 _____
3.饱和溶液和不饱和溶液 (1)判断依据:
(2)二者转化的条件和方法:
(2)熔点和沸点:少量的固体溶解于水,使稀溶液的凝固温度
降低 ,沸腾温度_____ 升高 。 _____
【思考感悟】1.均一、稳定、无色透明的液体一定是溶液吗?
提示:不一定。均一、稳定的液体可能是纯净物,如水,而溶液
属于混合物;溶液不一定是无色的,如硫酸铜溶液就是蓝色溶液。 2.用汽油清洗衣服上的油污和用洗涤剂清洗油污的原理相同吗? 为什么? 提示:不相同。汽油清洗油污属于溶解现象,洗涤剂清洗油污属
出现较多固体时 ,停止加热,利用_____ 余热 (3)加热到蒸发皿中_______________
将液体蒸干。
坩埚钳 夹持,小心地放在_______ 石棉网 上。 (4)热的蒸发皿应用_______
【思考感悟】通过降低温度的方法可以使任意不饱和溶液转化
为饱和溶液吗? 提示:不是。只有溶解度随温度降低而减小的物质才可以通过 降温的方法将不饱和溶液转化为饱和溶液。
不饱和溶液
增加 溶质、_________ 蒸发溶剂 或_____ 降温 _____
升温 增加 溶剂或_____ _____
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4.常见原子团的化合价 原子团 名称 铵根 NH4+ +1价 氢氧根 硝酸根 硫酸根 碳酸根 磷酸根 OH-1价 NO3-1价 SO42-2价 CO32-2价 PO43-3价
离子 符号 化合价
【思考感悟】 1.元素化合价与离子符号在表示方法上有何不同? 提示:化合价标在元素符号正上方,正负号在前,数值在后, 数值为1时不能省略;离子所带电荷数标在元素符号右上角,
一、化学式与化合价的关系 化学式
确定
书写
化合价
1.已知化学式,标出各元素的化合价
先标出常见元素的化合价;再根据化合物中正负化合价代数和 为零的原则计算某元素的化合价。
2.已知各元素的化合价,写出化学式 (1)确定各元素的位置:一般正价元素符号在前,负价元素符 号在后(NH3、CH4等例外);
(2)根据各元素的化合价确定各元素的原子个数;
②读法
由两种元素组成的化合物,一般读作“某化某”,有时需读出 五氧化二磷 。 四氧化三铁 ,P2O5读作___________ 原子个数,如:Fe3O4读作___________
【思考感悟】1.书写化合物化学式时,正价元素的元素符号一
定在前,负价元素的元素符号一定在后吗? 提示:不一定。书写化合物化学式时,一般正价元素在前,负 价元素在后,但也有例外,如氨气:NH3;甲烷:CH4,两化合物 中都是负价元素在前。
【解析】选B。本题考查考生对化学式含义的理解,解题的关 键是理解宏观组成和微观构成的区别。宏观上:表示一种物质, 表示组成物质的元素种类;微观上:表示由分子构成的物质中 的一个分子,表示构成物质的一个分子中所含各元素的原子数
目。化学式H2O能表示水这种物质,A正确;化学式H2O表示水由
氢元素和氧元素组成,B错误;化学式H2O能表示一个水分子, C正确;化学式H2O能表示一个水分子是由两个氢原子和一个氧 原子构成,D正确。
1
3.一般规律 -2 价。 +1 价,氧元素通常显____ (1)氢元素通常显____
正价 ,非金属元素与氢或金属 (2)金属元素在化合物中通常显_____
负价 ,与氧化合时显_____ 正价 。 元素化合时显_____ (3)一些元素在不同物质中可显不同的化合价。 代数和为零 。 (4)在化合物中各元素正、负化合价的___________ 零。 (5)单质分子中元素的化合价为___
(3)可以利用化学式中某元素质量分数的计算的变形式求相对 分子质量。因某元素质量分数(x%)=[某原子的相对原子质量 (Ar)×原子个数(n)]/相对分子质量×100%,故相对分子质量 =nAr/x%。
【特别提醒】 计算一定质量的某混合物某一元素的质量时可按下式: 混合物中某元素的质量=混合物质量×纯度×该元素的质量分 数,纯度=
【解析】选D。本题考查元素化合价的判断,解答关键是明确
化合物中元素正负化合价的代数和为零,设碘元素的化合价为
x,根据化合物中各元素的正负化合价的代数和为零, +1+x+ (-2)×3=0,x=+5,故选D。
6.(2012·铜仁中考)下列化合物中氮元素化合价为+4价的是 ( )
A.氨(NH3)
C.硝酸钠(NaNO3)
【我的收获】本题主要考查关于物质分类、根据化学式求化合 价。硫代硫酸钠晶体有固定的组成,能用固定的化学式来表示, 因此是纯净物。求硫代硫酸根的化合价时,根据钠元素化合价 为+1价,以及Na2S2O3中各元素正负化合价代数和为3;x=0,x=-2,可以求得硫代硫酸 根的化合价为-2价。
第2课时 化学式与化合价
化学式
1.概念 元素符号 和______ 物质组成 的式子。 数字 的组合表示__________ 用__________
2.表示的意义(以CO2为例)
二氧化碳这种物质
碳、 氧
1个二氧化碳分子 1个碳原子 2个氧原子
【特别提醒】
化学式前面的化学计量数不为1时,只具有微观意义,如2CO2 只表示两个二氧化碳分子。
4.(2012·泰安中考)学习化学知识后,观察物质世界就要从化 学视角看。下列对打火机主要燃料丁烷(C4H10)的看法不正确的
是(
)
A.从组成上看:丁烷由碳、氢两种元素组成 B.从结构上看:1个丁烷分子由4个碳原子、10个氢原子构成 C.从变化上看:丁烷完全燃烧只生成水 D.从性质上看:丁烷具有可燃性
且数值在前,正负号在后,数值为1时省略不写。
2.一种元素在同种化合物中的化合价是否一定相同? 提示:不一定。如硝酸铵(NH4NO3)中,氮元素的化合价分别为 -3价和+5价。
根据化学式的计算 1.求相对分子质量 各原子的相对原子质量 的总和。 相对分子质量=化学式中______________________
是硫代硫酸钠晶体(Na2S2O3·5H2O),该物质属于______(选填 “纯净物”或“混合物”),其中硫代硫酸根的化合价是 _____价。
【易错提醒】
1.纯净物与混合物的本质区别在于纯净物由一种物质组成,具 有固定的组成和性质; 2.根据化合物中各元素正负化合价的代数和为零,计算其中某 元素或原子团的化合价。
【解析】选D。
是钠离子的结构示意图,故A错误;离
子符号的表示方法是在元素符号右上角先写所带电荷数再写正 负号,故B错误;2N表示两个氮原子,两个氮分子应该表示为 2N2,故C错误。
3.(2012·眉山中考)下列对于化学式“H2O”的各种表述不正
确的是(
)
A.表示水这种物质 B.表示水分子由氢元素和氧元素组成 C.表示1个水分子 D.表示1个水分子由2个氢原子和1个氧原子构成
【易错提醒】
该元素的实际质量 ×100%。 混合物质量 2.每天摄入钙元素的质量应为每天摄入的钙片质量×钙片中钙
1.混合物中某元素的质量分数=
元素的质量分数。
【我的收获】本题考查化学式的计算,解题关键是熟悉化学计 算的各种类型。
40 100% 40% 。 100 (2)钙片中钙元素的质量分数为 0.625 g 40% 100% 25% 。 1g (3)每天摄入钙元素的质量为0.625 g×2×40%=0.5 g。
2.求组成物质的各元素的质量比
各原子的相对原子质量 化合物中各元素的质量比=化学式中_____________________
原子个数 之比。 ×_________
3.求物质中某一元素的质量分数 化合物中某元素的质量分数=
化学式中该元素原子相对原子质量 原子个数 100% 化合物的相对分子质量 _______________________________________________ 。
3.周围数字表示的意义
n个原子或n个分子 物质中该元素的化合价为+(或-)y价 该物质的一个分子中含有x个R原子
4.化学式的写法 (1)单质。 一种元素 组成 ①组成特点:只由_________ 元素符号 表示,如氖气___( 稀有气体:用_________ Ne 写化 学式,下同) ②写法 元素符号 表示,如铁___ 金属和固态非金属:用_________ Fe
(3)检查:运用化合价原则检查书写是否正确。 可简单记忆为:正价左、负价右,交叉约简定个数,写右下、
验正误。
【特别提醒】
含有原子团的化合物化学式书写时应注意:当原子团个数不是 1时,先将原子团用括号括起,然后在右下角注明个数,如 Ca(OH)2,当原子团个数是1时,原子团则不能用括号括起。
【典例1】(2012·义乌中考)进行固体熔化实验时常用的药品
【解析】选C。本题考查化学式的意义。由丁烷的化学式可知,
丁烷由碳、氢两种元素组成,1个丁烷分子由4个碳原子、10个
氢原子构成;丁烷完全燃烧生成二氧化碳和水;丁烷用作燃料, 说明具有可燃性。
化合价 【高频考点】据化学式求某元素化合价;正确标注化合价;据 化合价写化学式等 5.(2012·南充中考)我国推广食用的加碘盐是在食盐中加入一 定量的碘酸钾(KIO3)。在碘酸钾中碘元素的化合价为( A.-1 B.-5 C.+1 D.+5 )
3.根据化学式求相对分子质量时,要注意以下几点
(1)“×”和“+”的应用:同种元素的相对原子质量与原子个
数之间用“×”,不同种元素的相对原子质量之间用“+”。 如“H2O”的相对分子质量=1×2+16=18; (2)有括号的计算:当化学式中有括号(即分子中有多个原子团) 时,可以先算出一个原子团的相对质量,再乘以原子团的个数, 如“Ca(OH)2”的相对分子质量=40+(16+1)×2=74;
(1)碳酸钙中钙元素的质量分数为
答案:(1)40%
(2)25%
(3)0.5
化学式及表示的意义
【思考感悟】根据物质名称写化学式;判断化学式的正误;化 学式表示的意义
1.(2012·苏州中考)下列物质名称和对应的化学式都正确的一 组是( A.铝al C.氧化亚铁Fe2O3 ) B.硫酸钠NaSO4 D.氯化铵NH4Cl
(3)求物质中某一元素的质量分数。 在化合物AxBy中,A元素的质量分数 =
A的相对原子质量 x(A的原子个数) 100% A x By的相对分子质量
2.根据化学式计算时的常见错误
(1)元素的质量比与原子个数比混淆,要注意元素的质量比一
定不等于原子个数比; (2)计算分子中原子总数时,常忽略元素符号右下角没有数字 的原子,要注意,当元素符号右下角无数字时,其原子个数为 “1”;同样,计算相对分子质量时,也要注意。
数字 , 非金属气体:在元素符号右下角写_____
O2 如氧气___
(2)化合物。
①写法 右方 ,另一种元素的符号 a.氧化物:一般把氧元素符号写在_____
左方 ,如:CO2、CuO等。 写在_____ b.由金属元素和非金属元素组成的化合物:金属元素符号写在 右方 ,如:ZnS、KCl等。 左方 ,非金属元素符号写在_____ _____
