实验7 二组分固-液相图的绘制
二组分金属固液相图的绘制

专业:材料化学学号:080240008实验人:胡文想同实验人:李会勇实验名称:物化实验气压:101.325Kpa 温度:25℃二组分金属固液相图的绘制实验目的1.掌握热分析法(步冷曲线法)测绘Bi-Sn二组分固-液相图的原理和方法。
2.了解简单二组分固-液相图的特点。
3.掌握KWL-07可控升降温电炉及SWKY-Ⅲ数字控温仪的使用方法。
实验原理热分析法则是观察被研究系统温度变化与相变化的关系,这是绘制金属相图最常用的实验方法。
其原理是将系统加热熔融,然后使其缓慢而均匀地冷却,每隔一定时间记录一次温度,绘制温度与时间关系曲线——步冷曲线。
若系统在均匀冷却过程中无相变化,其温度将随时间均匀下降。
若系统在均匀冷却过程中有相变化,由于体系产生的相变热与自然冷却时体系放出的热量相抵消,步冷曲线就会出现转折或水平线段,转折点所对应的温度,即为该组成体系的相变温度。
二组分系统相图有多种类型,其步冷曲线也各不相同,但对于简单二组分凝聚系统,其步冷曲线有三种类型,见图II-7-1。
图II-7-1 生成简单低共熔混合物的二组分系统图II-7-1A为纯物质的步冷曲线。
冷却过程中无相变发生时,系统温度随时间均匀降低,至b点开始有固体析出,建立单组分两相平衡,f=0,温度不变,步冷曲线出现水平段bc,直至液体全部凝固(c点),温度又继续均匀下降。
水平段所对应的温度为纯凝固点。
图II-7-1B 为二组分混合物的步冷曲线。
冷却过程中无相变发生,系统温度随时间均匀降低,至b点开始有一种固体析出,随着该固体析出,液相组成不断变化,凝固点逐渐降低,到c点,两种固体同时析出,固液相组成不变,系统建立三相平衡,此时f=0,温度不随时间变化,步冷曲线出现水平段cd,当液体全部凝固(d点),温度又继续均匀下降。
水平段cd所对应的温度为二组分的低共熔点温度。
图II-7-1c 为二组分低共熔混合物的步冷曲线。
冷却过程中无相变发生,系统温度随时间均匀降低,至b点,两种固体按液相组成同时析出,系统建立三相平衡,f=0,温度不随时间变化,步冷曲线出现水平段bc,当液体全部凝固(c点),温度又继续均匀降低。
实验七 双液系气液平衡相图的测绘

实验七、双液系气—液平衡相图的测绘专业:11化学姓名:赖煊荣座号:32 同组人:黄音彬时间:2013.12. 3Ⅰ、目的要求1.测定相应组成时的沸点并制作常压下环已烷—无水乙醇双液系的平衡相图。
2.从沸点组成图了解分馏原理。
3.了解沸点的测定技术,掌握两组分液体沸点的测定方法。
4.掌握折光率与组成的关系及阿贝折光仪的使用方法。
Ⅱ、基本原理一、气—液相图两种液态物质混合而成的二组分体系称为双液系。
两个组分若能按任意比例互相溶解,称完全互溶双液系。
液体的沸点是指液体的蒸气压与外压相等时的温度。
在一定的外压下,纯液体的沸点有其确定值。
但双液系的沸点不仅与外压有关,而且还与两种液体的相对含量有关。
根据相律:自由度=组分数-相数+2 。
因此,一个以气—液共存的二组分体系,其自由度为2。
只要任意再确定一个变量,整个体系的存在状态就可以用二维图形来描述。
在T—x相图上,还有温度、液相组成和气相组成三个变量,但只有一个自由度。
一旦设定某个变量,则其它两个变量必有相应的确定值。
二、沸点测定仪沸点仪的构造特点满足:正确测定沸点、便于取样分析、防止过热及避免分馏等。
如图2,是一只带回流冷凝管的长颈圆底烧瓶。
冷凝管底部有一半球形小室,用以收集冷凝下来的气相样品。
溶液中事先加入沸石以减少溶液沸腾时的过热现象及防止暴沸。
三、组成分析本实验选用的环已烷和乙醇,两者折光率相差颇大,而折光率测定又只需少量样品,平衡体系两相组成的获得由事先测得的折光率——组成的工作曲线查得。
折光仪的原理及使用详见参考资料。
Ⅲ、仪器与试剂沸点测定仪一套,普通温度计一支、超级恒温器一套(配接触点温度计、温度计各一支),酒精灯一个、铁架台一附、阿贝折光仪一台、长滴管、烧杯、移液管、擦镜纸等。
环已烷(分析纯)、无水乙醇(分析纯)、丙酮(分析纯)、重蒸馏水等。
Ⅳ、实验步骤1.联接超级恒温器与阿贝折光仪。
调节超级恒温器恒温水浴温度为设定温度25℃,与阿贝折光仪温度一致。
二组分固---液相图的绘制
《物理化学实验》讲义 第三部分 实验 德州学院化学系 王敦青二组分固---液相图的绘制一、实验目的1.学会用热分析法测绘Sn —Bi 二组分金属相图。
2.了解热分析法测量技术。
3.掌握SWKY 数字控温仪和KWL-08可控升降温电炉的基本原理和使用。
二、预习要求了解纯物质的步冷曲线和混合物的步冷曲线的形状有何不同,其相变点的温度应如何确定。
三、实验原理测绘金属相图常用的实验方法是热分析法,其原理是将一种金属或合金熔融后,使之均匀冷却,每隔一定时间记录一次温度,表示温度与时间关系的曲线叫步冷曲线。
当熔融体系在均匀冷却过程中无相变化时,其温度将连续均匀下降得到一光滑的冷却曲线;当体系内发生相变时,则因体系产生之相变热与自然冷却时体系放出的热量相抵偿,冷却曲线就会出现转折或水平线段,转折点所对应的温度,即为该组成合金的相变温度。
利用冷却曲线所得到的一系列组成和所对应的相变温度数据,以横轴表示混合物的组成,纵轴上标出开始出现相变的温度,把这些点连接起来,就可绘出相图。
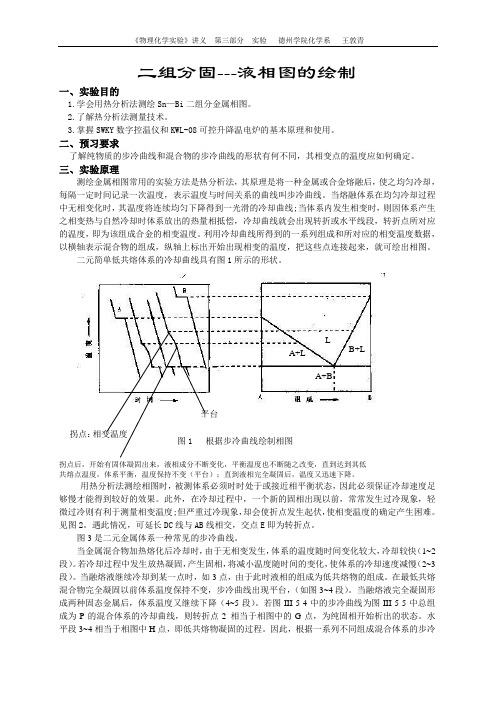
二元简单低共熔体系的冷却曲线具有图1所示的形状。
图1 根据步冷曲线绘制相图 拐点后,开始有固体凝固出来,液相成分不断变化,平衡温度也不断随之改变,直到达到其低共熔点温度,体系平衡,温度保持不变(平台);直到液相完全凝固后,温度又迅速下降。
用热分析法测绘相图时,被测体系必须时时处于或接近相平衡状态,因此必须保证冷却速度足够慢才能得到较好的效果。
此外,在冷却过程中,一个新的固相出现以前,常常发生过冷现象,轻微过冷则有利于测量相变温度;但严重过冷现象,却会使折点发生起伏,使相变温度的确定产生困难。
见图2。
遇此情况,可延长DC 线与AB 线相交,交点E 即为转折点。
图3是二元金属体系一种常见的步冷曲线。
当金属混合物加热熔化后冷却时,由于无相变发生,体系的温度随时间变化较大,冷却较快(1~2段)。
若冷却过程中发生放热凝固,产生固相,将减小温度随时间的变化,使体系的冷却速度减慢(2~3段)。
二组分固液相图

⼆组分固液相图5.4⼆组分系统的固?液平衡5.4.1形成低共熔物的固相不互溶系统当所考虑平衡不涉及⽓相⽽仅涉及固相和液相时,则体系常称为"凝聚相体系" 或"固液体系"0固体和液体的可压缩性甚⼩,⼀般除在⾼压下以外,压⼒对平衡性质的影响可忽略不计,故可将压⼒视为恒量。
由相律:/="= C-^+2-n r=2-d> + 2-l = 3-£Z>因体系最少相数为①=1,故在恒压下⼆组分体系的最多⾃由度数 f * =2,仅需⽤两个独⽴变量就⾜以完整地描述体系的状态。
由于常⽤变量为温度和组成,故在⼆组分固液体系中最常遇到的是T?x (温度?摩尔分数)或T?①(温度?质量分数)图。
⼆组分固?液体系涉及范围相当⼴泛,最常遇到的是合⾦体系、⽔盐体系、双盐体系和双有机物体系等。
在本节中仅考虑液相中可以完全互溶的特殊情况°这类体系在液相中可以互溶,⽽在固相中溶解度可以有差别。
故以其差异分为三类:(1)固相完全不互溶体系;(2)固相部分互溶体系和(3)固相完全互溶体系。
进⼀步分类可归纳如下:F『形成简单低共熔物休系固相完全不互溶体棗形成化合物体系⼻相合熔点化合物怵系不相合熔点化合物俸系EM体疾「没有最1■嚴最⾼熔点型固相完全互熔体茶最瞬点型最⾼熔点型■1固相部分互熔体系,⼀低共熔点型、转熔点型研究固液体系最常⽤实验⽅法为“热分析”法及“溶解度”法。
本节先在“形成低共熔物的固相不互溶体系”中介绍这两种实验⽅法,然后再对各种类型相图作⼀简介。
(⼀)⽔盐体系相图与溶解度法1 ?相图剖析图5-27为根据硫酸铵在不同温度下于⽔中的溶解度实验数据绘制的⽔盐体系相图,这类构成相图的⽅法称为 "溶解度法" 纵坐标为温度t 「C ),横坐标为硫酸铵质量分数(以①表⽰)。
图中FE 线是冰与盐溶液平衡共存的曲线,它表⽰⽔的凝固点随盐的加⼊⽽下降的规律,故⼜称为⽔的凝固点降低曲线。
实验七双液系气液平衡相图的测定

数据处理
1. 将实验中测得的折射率—组成数据列表,并绘制成 工作曲线。
2. 将实验中测得的沸点—折射率数据列表,并从工作 曲线上查得相应的组成,从而获得沸点与组成的关 系。
3. 绘制沸点—组成图,并标明最低恒沸点和组成。 4. 在精确的测定中,还要对温度计的外露水银柱进行
仪器操作
使用方法
3. 调光: 转动镜筒使之垂直,调节反射镜使入射光进入棱镜,
同时调节目镜的焦距,使目镜中十字线清晰明亮。调节消 色散补偿器使目镜中彩色光带消失。再调节读数螺旋,使 明暗的界面恰好同十字线交叉点处重合。这时镜筒的轴与 掠射光线平行。 4. 读数:
从读数望远镜中读出刻度盘上的折射率数值。常用的 阿贝折射仪可读至小数点后的第四位,为了使读数准确, 一般应将试样重复测量三次,每次相差不能超过0.0002, 然后取平均值。
仪器操作
注意事项
1.使用时要注意保护棱镜,清洗时只能用擦镜纸而不能用滤纸 等。加试样时不能将滴管口触及镜面。对于酸碱等腐蚀性液 体不得使用阿贝折射仪。
2.每次测定时,试样不可加得太多,一般只需加2~3滴即可。 3.要注意保持仪器清洁,保护刻度盘。每次实验完毕,要在镜
面上加几滴丙酮,并用擦镜纸擦干。最后用两层擦镜纸夹在 两棱镜镜面之间,以免镜面损坏。 4.读数时,有时在目镜中观察不到清晰的明暗分界线,而是畸 形的,这是由于棱镜间未充满液体;若出现弧形光环,则可 能是由于光线未经过棱镜而直接照射到聚光透镜上。
0.200mL、…、0.900mL的环己烷,再依次移入 0.900mL、0.800mL、…、0.100mL的异丙醇,轻 轻摇动,混合均匀,配成9份已知浓度的溶液(按 纯样品的密度,换算成质量百分浓度)。用阿贝 折射仪测定每份溶液的折射率及纯环己烷和异丙 醇的折射率。以折射率对浓度作图,即可绘制工 作曲线。
物理化学实验报告二组分简单共熔合金相图绘制

一、实验目的1.掌握步冷曲线法测绘二组分金属的固液平衡相图的原理和方法。
2、了解固液平衡相图的特点,进一步学习和巩固相律等有关知识。
二、主要实验器材和药品1、仪器:KWL—II金属相图(步冷曲线)实验装置、微电脑控制器、不锈钢套管、硬质玻璃样品管、托盘天平、坩埚钳2、试剂:纯锡(AR)、纯铋(AR)、石墨粉、液体石蜡三、实验原理压力对凝聚系统影响很小,因此通常讨论其相平衡时不考虑压力的影响,故根据相律,二组分凝聚系统最多有温度和组成两个独立变量,其相图为温度组成图.较为简单的组分金属相图主要有三种:一种是液相完全互溶,凝固后固相也能完全瓦溶成固体混合物的系统最典型的为Cu- Ni系统;另一种是液相完全互溶,而固相完全不互溶的系统,最典型的是Bi— Cd 系统;还有一种是液相完全互溶,而固相是部分互溶的系统,如Pb- Sn或Bi- Sn系统。
研究凝聚系统相平衡,绘制其相图常采用溶解度法和热分析法.溶解度法是指在确定的温度下,直接测定固液两相平衡时溶液的浓度,然后依据测得的温度和溶解度数据绘制成相图。
此法适用于常温F易测定组成的系统,如水盐系统。
热分析法(步冷曲线法)则是观察被研究系统温度变化与相变化的关系,这是绘制金属相图最常用和最基本的实验方法。
它是利用金属及合金在加热和冷却过程中发生相变时,潜热的释出或吸收及热容的突变,来得到金属或合金中相转变温度的方法。
其原理是将系统加热熔融,然后使其缓慢而均匀地冷却,每隔定时间记录一次温度,物系在冷却过程中温度随时间的变化关系曲线称为步冷曲线(又称为冷却曲线)。
根据步冷曲线可以判断体系有无相变的发生。
当体系内没有相变时,步冷曲线是连续变化的;当体系内有相变发生时,步冷曲线上将会出现转折点或水平部分.这是因为相变时的热效应使温度随时间的变化率发生了变化。
因此,由步冷曲线的斜率变化可以确定体系的相变点温度。
测定不同组分的步冷曲线,找出对应的相变温度,即可绘制相图。
物理化学-实验七:二组分固液相图的绘制
实验七 二组分固-液相图的绘制一、实验目的及要求1.掌握用步冷曲线法测绘二组分金属固液平衡相图的原理和方法;2.了解采用热电偶进行测温、控温的原理和装置。
二、实验原理用来表示多相体系的温度、压力与体系中各组分的状态、组成之间关系的平面图形称为相图。
二组分固-液相图是描述体系温度与二组分组成之间关系的图形。
由于固液相变体系属凝聚体系,一般视为不受压力影响,因此在绘制相图时不考虑压力因素。
若二组分体系的两个组分在固相完全不溶,在液相可完全互溶,一般具有简单低共熔点,其相图具有比较简单的形式。
根据相律,对于具有简单低共熔点的二组分体系,其相图可分为三个区域,即液相区、固液共存区和固相区。
绘制相图时,根据不同组成样品的相变温度(即凝固点)绘制出这三个区域的交界线—液相线,即图1(b )中的T 1E 和T 2E ,并找出低共熔点E 所处的温度和液相组成。
步冷曲线法又称热分析法,是绘制相图的基本方法之一。
它是将某种组成的样品加热至全部熔融,再均速冷却,测定冷却过程中样品的温度 – 时间关系,即步冷曲线。
根据步冷曲线上的温度转折点获得该组成的相变点温度。
步冷曲线有三种形式,分别如图1(a )中的a 、b 和c 三条曲线。
a 曲线是纯物质A 的步冷曲线。
在冷却过程中,当体系温度到达A 物质凝固点时,开始析出固体,所释放的熔化热抵消了体系的散热,使步冷曲线上出现一个平台,平台的温度即为A 物质的凝固点。
纯B 步冷曲线e 的形状与此相似。
a b c d e a b c d eA B x B t液相区固液共存区固相区低共熔点T 1T 2TT (a )(b )E图1 步冷曲线b 曲线是由主要为A 物质但含有少量B 物质样品的步冷曲线。
由于含有B 物质,使得凝固点下降,在低于纯A 凝固点的某一温度开始析出固体A ,但由于固体析出后使得B 的浓度升高,凝固点进一步下降,所以曲线产生了一个转折,直到当液态组成为低共熔点组成时,A 、B 共同析出,释放较多熔化热,使得曲线上又出现平台。
二组分固态互溶系统液固平衡相图(共9张PPT)
(1)等边三角形表示法
F=C-P+2=5-P
当Fmin=0 时,Pmax=5,最多可以 有五相共存
当 Pmin=1时, Fmax=4,这四个
变量是T、P和组成x1和x2
★ 等边三角形的三个顶点分别代 表纯组分A、B、C
★ 三条边则代表A-B、B-C、C-A 三个两组分系统
• 11.1 三组分系统相律分析
• 11.2 三组分系统图解表示法 • 11.3 三组分系统一对液体部分互溶的恒温液-液相图
★ 水与醋酸、氯仿与醋酸以任意 比例互溶,水与氯仿部分互溶。 ★ 共轭溶液:氯仿层、水层 ★ d→C过程分析:
连结线---实线、非平行线 会溶点---不是最高点、不止一
个
10 ★
生d→成C化过合程物分的析二:1组-分--凝l 聚系统相2图---α
3---β
2 三组分系统图解表示法
(1)等边三角形表4示-法--α+l 5---β+l 6--- α+β
F=C-P+2=5-P
111三三组组分分系系统统相液律-液分S平析1衡S相2-图-- α+β+l
2 三组分系统图解表示法
F=C-P+2=5-P 11 三组分系统液-液平衡相图 11 三组分系统液-液平衡相图
M g 2 S i(s) 1 1 0 2 C M g 2 S i(l) NaCl2H2O(s) 0 .15 CmNaCl(s)(m1)l
§6.11 三组分系统液-液平衡相图
• 11.1 三组分系统相律分析
§6.9 二组分固态互溶系统液固平衡相图
• 9.1 固态完全互溶系统
• 当Fmin=0 时9,.Pm2ax固=5,态最多部可以分有五互相溶共存系统
固-液二元体系相图二级相变
进一步将N点的原料加温至全部熔
化,冷却过程中首先结晶出来的固
体杂质含量高,最后结晶出来的固
体纯度较高.多次重复此种操作,最
后结晶出来的晶体将极其纯净,从
而得到高纯A.
A
液相
固-液两相平衡
N
P
固相 B→
区域熔炼装置图
加热区域将熔化为液态,当加热 圈向右移动时,左边部分因离开 加热区而冷却凝固.因为杂质B 在固相的浓度比较小,所以凝固 下来的固体端B的浓度较小,原 料的纯度比较高.加热圈从左移 动到右的过程,是将B从作边扫 到右边的过程.
phase diagram of two compounds (1)
• 1区: 单相,熔液,f=2
• 2区: 两相,A2+l,f=1
1
• 3区: 两相,C+l
• 4区: 两相,B+l
F
G
• 5区: 两相,A2+C
• 6区: 两相,A1+C • 7区: 两相,B+C
白硅石A2
2
I E
M
3
D
5
N
鳞石英A1
体系分为两个固相, 其组成分别由E和F 点表示。
此帽形区有一最高会 熔温度。
solid
s1+s2
E
F
P
A
B
固相部分互溶的相图的变化
T
T
liquid
T
liquid
liquid
l+s
l+s
solid
s1
solid
s1+s2
s1+s2
A
s1+s2
A B
A
二组分固-液相图的测绘
T
B
T
B
A
A
ห้องสมุดไป่ตู้
A 0
W(D)/%
步冷曲线与相图
(D)/%
((()(D(
B 100
本实验采用了 JX-3D 型金属相图实验装置,其可以直接测出 Pb-Sn 合金体系的温度~时间步 冷曲线,从该步冷曲线能够之间读出相变点温度,但不需做热电偶工作曲线。 三、仪器试剂 JX-3D 型金属相图实验装置 一套 不锈钢样品管 6支 铅(A.R) 锡(A.R) 铋(A.R) 石墨粉 硅油 四、实验项目 1) 配置样品 按含 Sn 0%,20%, 40%,61.9%,80%,及 100%配好样品(150g) 。为防止样品氧化,样 品表面需覆盖一层石墨粉。每一样品试管内都需另加一小套管,小套管内滴入少量硅油以增 加传热速度。 2) 分别测定上述样品及 3 种纯物质的步冷曲线 打开“JX-3D 型金属相图实验装置”控制箱的仪器电源,将感温探头置于 1#样品的内管 中,同时将“加热炉”的旋钮旋至“1 档” 。按“设置”键,将感温探头调节到比 1#样品的凝 固点高 30℃左右的数值处,读数时间设置为 30 秒,其他各项可用其缺省值。按下“加热”按 钮仪器随之对 1#样品进行加热。当温度达到设定温度后,仪器会自动停止加热。注意观察仪 器上的温度读数。当温度开始下降时,每 30 秒记录一个温度值,直至出现平台后在比此温度 低 20-30℃后停止记录。 同法测定其他样品的步冷曲线。注意:测定几号样品,就将感温探头至于几号样品的内 管中,同时将“加热炉”的旋钮旋至与样品同一号数的档位处。
Pb步冷曲线
350.0 340.0 330.0 320.0 310.0 300.0 290.0 280.0 0 200 400 600 Pb 330.0 310.0 290.0 270.0 250.0 230.0 210.0 190.0 170.0 150.0 0
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验评注与拓展
绘制固液二组分相图的方法通常有溶解度法和热分析法。
溶解度法
指在确定的温度下,直接测定固液两相平衡时溶液的 浓度,然后根据测得的温度和相应的溶解度数据绘制相图, 这种方法使用于常温下易测定组成的体系,如水-盐二组分体 系等。 热分析法 适用于常温下不便直接测定固液平衡时溶液组成的体系(如合 金和有机化合物凝聚体系),通常利用相变时的热效应来测定组 成以确定体系的温度,然后根据选定的一系列不同组成的二组 分体系所测定的温度绘制相图.此种方法简单、易于推广,对 于一些二组分金属体系,若挥发的蒸汽对人体健康有害,则 可采用热分析法的另一种差热分析(DTA)或差示扫描( DSC)法绘制相图。
定压下将体系熔融后,使之从高温逐渐冷却,每隔一定时间记录一次温 度,作温度对时间的变化曲线,即步冷曲线。
当熔融体系在冷却过程中无相变化时,其温度将连续均匀下降并得到一 条光滑的步冷曲线;若冷却过程中体系发生相变,则体系中产生的相变热将与 自然冷却时体系放出的热量相抵偿,步冷曲线会出现转折点,转折点所对应 的温度即为体系发生相变的温度。 测定一系列组成不同样品的步冷曲线,利用步冷曲线所得到的一系列组 成和所对应的相变温度数据,以横轴表示样品的组成,纵轴表示开始出现相 变的温度,把这些点连接起来,可绘制出金属相图。
数据处理
(1)用已知纯Pb、纯Sn的熔点及水 的沸点作横坐标,以各纯物质相变 点的热电势为纵坐标,画出热电偶的 T-E工作曲线. (2)找出各步冷曲线中拐点和平台对 应的热电势. (3)从热电偶的工作曲线上查出各拐 点温度和平台温度,以温度为纵坐 标,以组成为横坐标,绘出Sn—Pb 二元金属相图. (4)从所得相图中求出低共溶点的温度 以及低共溶混合物的组成
提问与思考
(1) 对于不同组成混合物的步冷曲线,其转折点与水平 段有什么不同? (2) 步冷曲线上为什么会出现转折点?纯金属、低共熔 混合物及合金的转折点各有几个?曲线形状有何不同? 为什么? (3)试从实验方法比较测绘气-液相图和固-液相图的 异同点。
参考文献
(1)清华大学化学系物理化学实验编写组编.物理化学实验.北 京:清华大学出版社, 1992 (2)复旦大学等编 庄继华等修订 物理化学实验(第三版).北京 高等教育出版社2005 (3)傅献彩 沈文霞 姚天扬编 .物理化学(第四版).北京:高等教 育出版社,1994 (4) McGRAW HILL, Experiments in physical chemistry, 7thed. 2003
实验评注与拓展
用热分析法测绘相图时,被测体系必须时时处于或接近相平衡状态, 因此必须保证冷却速度足够慢才能得到较好的效果。此外,在冷却过程中, 一个新的固相出现以前,常常发生过冷现象,轻微过冷则有利于测量相变温 度; 但严重过冷现象,却会使折点发生起伏,使相变温度的确定产生困难。 见图。遇此情况,可延长dc线ab线相交,交点e即为转折点。
实验7
二组分固-液相图的绘制
物理化学研究室
何广平
实验目的
(1)学会用热分析法测绘Sn—Pb二组分金属 相图,了解固-液相图的基本特点。 (2) 掌握热电偶测量温度的原理及热电偶的 校正方法。 (3) 了解热分析法测量技术。
什么是相图?
相图是表示多相平衡体系的存在状态与组成、温 度、压力等因素变化的关系图。它包括平衡体系中有 那些相、各相的成分如何,不同相的相对量是多少以 及它们随浓度、温度、压力等变量变化的关系。
问题: (1)请根据相律说说二组分体系中自由度、组分数、独立组 分数、相数之间的关系? (2)二组分体系相图的特点、常用相图形式?
T-X图的绘制方法(热分析法)
• 什么是T-X图? • 以体系中所含物质的组成为自变量、以温度为因变量所得到 的温度-组成图(T-X图)是常见的一种相图。 什么是热分析法?
如何根据步冷曲线绘制相图?
根据步冷曲线绘制相图
仪器与试剂
• 实验仪器 冷却保温炉 1台 台式自动平衡记录仪 1台 调压变压器 (1KVA) 1台 镍铬-镍硅热电偶 1副 电弧焰发生器 硬质玻璃管 8个 • 实验药品 Sn(化学纯); Pb(化学纯) 石墨粉 冰水浴
实验步骤
(1) 热电偶的制备 • 取60cm长的镍铬丝和镍硅丝,将镍铬丝用小绝缘瓷管套好. 在其两端大约5mm处分别与两段各长50cm的镍硅丝紧密地 扭合在一起,,将扭合的部位稍稍加热后立即沾以硼砂粉, 并用小火加热,使硼砂熔化并形成玻璃态,然后放在电弧焰 上小心烧结,直至形成一个光滑的小珠,冷却后将硼砂玻 璃层除去,即为镍铬-镍硅热电偶。 • 也可采用商业镍铬-镍硅热电偶。 • 为绝缘起见,使用时常将热电偶套在较细的硬质玻璃管中 ,管内再注入少量硅油以改善其导电性。 • (2) 热电偶的校正 用纯Pb、纯Sn的熔点及水的沸点对热电偶进行校正, 绘制热电偶工作曲线。
(3) 样品配制 用感量为0.1g的台称分别称取纯Sn、纯Pb各50g,另配制含 锡20%、40%、61.9%、80%的铅锡混合物各50g,分别置于硬质 玻璃管中中,在样品上方各覆盖一层石墨粉。 (4) 绘制步冷曲线 (1) 将热电偶及测量仪器连接好。 (2) 将盛有样品的硬质玻璃管放入加热炉内加热。待样品熔化后 停止加热,用玻璃棒将样品搅拌均匀,并将石墨粉拨至样品表 面,以防止样品氧化。 (3) 将硬质玻璃管移至保温炉中冷却,此时热电偶的尖端应置于 样品中央,以便反映体系的真实温度,同时开启记录仪绘制步 冷曲线。 (4) 用上述方法绘制所有样品的步冷曲线。 (5)用硬质玻璃管装一定量的水,在电炉上加热,将热电偶插入沸 腾的蒸馏水中测定其热电势。测定时热电偶的冷端均为0℃。
