茚三酮显色法测定氨基酸含量
茚三酮 显色剂

茚三酮中文名称:苯并戊三酮,茚三酮英文名称:Ninhydrin分子量:160.13CAS RN:485-47-2熔点:251℃密度: 0.86性状:本试剂近似为白色结晶,或浅黄色结晶粉末,微溶于乙醚及三氯甲烷,100℃以上变为红色。
特性反应:跟酶类或者多肽在加热状况下发生显紫色反应。
作用茚三酮是一个有机化合物,被广泛用于检测氨、一级和二级胺,尤其是氨基酸。
氨基酸与茚三酮水合物在弱酸条件下共加热时,氨基酸被氧化脱氨、脱羧,而茚三酮水合物被还原,其还原物可与氨基酸加热分解产生的氨结合,再与另一分子茚三酮缩合成为蓝紫色化合物,称为罗曼紫(Ruhemann's purple)。
此化合物最大吸收峰在570nm波长处。
由于此吸收峰的大小与氨基酸释放的氨量成正比,因此可作为氨基酸的定量分析方法法医学上这个反应被用于鉴定指纹。
茚三酮反应(Kaiser鉴定)也可用来在固相接肽时检验脱保护基是否已经完成,鉴定和比色法分离氨基酸以及鉴定铵离子(呈紫色)。
茚三酮与氨基酸反应生成蓝紫色化合物,但pro,羟-pro反应时呈黄色。
茚三酮用于脯氨酸含量的测定当用磺基水杨酸提取植物样品时,脯氨酸便游离于磺基水杨酸的溶液中,然后用酸性茚三酮加热处理后,溶液即成红色,再用甲苯处理,则色素全部转移至甲苯中,色素的深浅即表示脯氨酸的含量的高低。
在520nm 的波长下比色,从标准曲线(用脯氨酸标准溶液制得)上查出(或用回归方程计算)脯氨酸的含量。
①茚三酮检出物:氨基酸、胺与氨基糖类。
溶液:本品O.2g溶于乙醇l00ml中。
方法:喷后于110oC加热。
结果:呈红紫色斑点。
茚三酮对一级二级的胺显色肯定没问题的,三级胺有些可以,酰胺应该也没问题的,配制:1.5g 茚三酮 + 100mL of 正丁醇+ 3.0mL 醋酸;显色的时候板子浸湿,用纸擦一下多余液滴,再用电热枪(电吹风太弱了)吹出斑点,显色因为氨基酸的不同而显示不同的紫色黄色等等,你想检测伯胺的话,肯定没有问题的!配制方法:1.5g 茚三酮+ 100mL of 正丁醇+ 3.0mL 醋酸茚三酮不是太好溶解,需要多搅拌才行。
茶叶中游离氨基酸总量的测定实验报告

茶叶中游离氨基酸总量的测定实验报告一、实验目的本实验旨在测定茶叶中游离氨基酸总量,了解茶叶的品质和营养价值,为茶叶的生产、加工和质量控制提供科学依据。
二、实验原理茶叶中的游离氨基酸在一定条件下与茚三酮反应,生成蓝紫色化合物,其颜色的深浅与游离氨基酸的含量成正比。
通过比色法测定反应液在特定波长下的吸光度,与标准曲线对照,即可计算出茶叶中游离氨基酸的总量。
三、实验材料与仪器1、实验材料茶叶样品:选取不同品种、不同产地的茶叶若干。
标准氨基酸溶液:精确配制一定浓度的谷氨酸标准溶液。
茚三酮试剂:称取适量茚三酮,用乙醇溶解并定容。
缓冲溶液:磷酸缓冲液(pH 80)。
2、实验仪器分光光度计分析天平恒温水浴锅容量瓶、移液管、比色皿等玻璃仪器四、实验步骤1、样品处理称取一定量的茶叶样品,用研钵研碎后,置于具塞三角瓶中。
加入适量的沸水,在水浴中浸提一定时间,冷却后过滤,滤液即为待测液。
2、标准曲线的绘制分别吸取不同体积的标准氨基酸溶液于一系列容量瓶中,加入缓冲溶液和茚三酮试剂,定容后摇匀。
将上述溶液置于沸水浴中加热一定时间,取出冷却至室温。
以空白溶液为参比,在分光光度计上于特定波长处测定吸光度。
以氨基酸浓度为横坐标,吸光度为纵坐标,绘制标准曲线。
3、样品测定吸取适量的待测液于容量瓶中,按照绘制标准曲线的步骤加入缓冲溶液和茚三酮试剂,定容、加热、冷却。
测定样品溶液的吸光度,根据标准曲线计算出游离氨基酸的含量。
五、实验结果与分析1、实验数据记录标准曲线测定数据:记录不同浓度标准氨基酸溶液的吸光度值。
样品测定数据:记录样品溶液的吸光度值及对应的计算结果。
2、结果计算根据标准曲线方程,计算样品中游离氨基酸的浓度。
按照样品处理时的稀释倍数,计算茶叶中游离氨基酸的总量。
3、结果分析比较不同茶叶样品中游离氨基酸总量的差异,分析可能的原因,如茶叶品种、生长环境、加工工艺等。
讨论实验过程中可能存在的误差来源,如样品处理的均匀性、反应条件的控制、仪器的精度等,并提出改进措施。
氨基酸显色反应茚三酮反应.ppt

氨基酸显色反应---茚三酮反应
茚三酮ቤተ መጻሕፍቲ ባይዱ应
实验原理
除脯氨酸、羟脯氨酸和茚三酮反应产生黄色物质外,所有α—氨基酸及一切蛋白质 都能和茚三酮反应生成蓝紫色物质。 该反应十分灵敏,1:1 500 000浓度的氨基酸水溶液即能给出反应,是一种常用 的氨基酸定量测定方法。 茚三酮反应分为两步,第一步是氨基酸被氧化形成CO2、NH3和醛,水合茚三酮 被还原成还原型茚三酮;第二步是所形成的还原型茚三酮同另一个水合茚三酮分 于和氨缩合生成有色物质。
实验器材及试剂
器材: 试管、酒精灯、试管夹、试管架 试剂: (1)蛋白质溶液:2%卵清蛋白或新鲜鸡蛋清溶液(蛋清:水=1:9) (2)0.5%甘氨酸溶液 (3)0.1%茚三酮水溶液 (4)0.1%茚三酮—乙醇溶液
实验步骤
(1)取2支试管分别加入蛋白质溶液和甘氨酸溶液1毫升,再各加0.5毫升0.1%茚 三酮水溶液,混匀,在沸水浴中加热1—2分钟,观察颜色由粉色变紫红色再变蓝。 (2)在一小块滤纸上滴一滴0.5%的甘氨酸溶液,风干后,再在原处滴上一滴0.1% 的茚三酮乙醇溶液在微火旁烘干显色,观察紫红色斑点的出现。
茚三酮呈色反应实验报告

竭诚为您提供优质文档/双击可除茚三酮呈色反应实验报告篇一:实验三蛋白质及氨基酸的呈色反应实验三蛋白质及氨基酸的呈色反应一、实验目的1、了解蛋白质和某些氨基酸的特殊颜色反应及其原理2、掌握几种常用鉴定蛋白质和氨基酸的方法二、实验内容对蛋白质及氨基酸的双缩脲反应、茚三酮反应、黄色反应、乙醛酸反应、偶氮反应、醋酸铅反应等颜色及沉淀反应进行定性确定。
三、实验操作(一)双缩脲反应1、实验原理当尿素加热到180℃左右时,两个分子的尿素缩合可放出一个分子氨后形成双缩脲,双缩脲在碱性溶液中与铜离子结合生成复杂的红色配合物,此呈色反应称为双缩脲反应。
由于蛋白质分子中含有多个肽键,其结构与双缩脲相似,故能呈此反应,而形成紫红色或蓝紫色的配合物。
此反应常用作蛋白质的定性或定量的测定。
2、试剂(1)尿素(2)10%naoh溶液(3)1%cuso4溶液(4)蛋白质溶液:将鸡蛋清用蒸馏水稀释10~20倍,3层纱布过滤,滤液冷藏备用。
3、操作(1)取少许结晶尿素放在干燥试管,微火加热,则尿素开始熔化,并形成双缩脲,释放的氨可用湿润的红色石蕊试纸鉴定。
待熔融的尿素开始硬化,试管内有白色固体出现,停止加热,让试管缓慢冷却。
然后加10%naoh溶液1ml和1%cuso42~3滴,混匀后观察颜色的变化。
(2)另取一试管,加蛋白质溶液1ml、10%naoh溶液2ml 及1%cuso42~3滴,振荡后将出现的紫红色与双缩脲反应所产生的颜色相对比。
(二)茚三酮反应1、实验原理除脯氨酸和羟脯氨酸与茚三酮作用生成黄色物质外,所有α-氨基酸与茚三酮发生反应生成紫红色物质,最终形成蓝紫色化合物。
1︰1500000浓度的氨基酸水溶液即能发生反应而显色。
反应的适宜ph为5~7。
此反应目前广泛地应用于氨基酸定量测定。
2、试剂蛋白质溶液(同前);0.5%甘氨酸;0.5%茚三酮水溶液3、操作取2支试管分别加入蛋白质溶液和甘氨酸溶液各1ml,再各加0.5ml0.1%茚三酮水溶液,混匀,在沸水浴加热2~3分钟,观察颜色变化。
游离氨基酸的测定方法

游离氨基酸的测定方法
游离氨基酸咋测定呢?其实有不少方法呢!比如说茚三酮比色法。
先准备好样品,把它处理成合适的状态。
然后加入茚三酮试剂,经过一系列反应后,通过比色来确定游离氨基酸的含量。
这过程中可得小心操作,要是弄错了一步,那结果可就不靠谱啦!那安全性咋样呢?只要按照正确的步骤来,一般没啥大问题。
稳定性嘛,只要试剂没问题,操作规范,结果还是挺稳定的。
这方法能用到好多地方呢!像食品检测领域,你想想,要是不知道食品里的游离氨基酸含量,咋能保证食品的质量和营养呢?优势也不少呢!操作相对简单,成本也不高。
咱举个实际案例哈。
有个食品加工厂,用这个方法检测产品中的游离氨基酸含量,及时调整了生产工艺,提高了产品质量。
这效果多棒啊!
游离氨基酸的测定方法真的超实用,能帮我们了解各种物质中的氨基酸情况,为我们的生活和生产带来很多好处。
咱可得好好利用这些方法,让它们发挥更大的作用。
茚三酮反应

反应原理:参考资料•中文名称:苯硑戊三酮,茚三酮英文名称:NinhydrinNinhydrin (DE)1,2,3-Trioxohydrinden Hydrat (DE)1,2,3-Indantrione1,2,3-Triketohydrindene1H-Indene-1,2,3-trione2,2-Dihydroxy-1H-indene-1,3(2H)-dione分子式:C9H6O4分子量:178.14CAS RN:485-47-2熔点:251℃密度: 0.86特性反应:跟酶类或者多肽在加热状况下发生显紫色反应。
•含量不少于95.0% 净重5g•白色或淡黄色结晶或结晶性粉末•~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~•由于热敏纸(一种对热敏感的纸,如传真纸是其中一种,译者注)在信用卡收据上广泛使用,在热敏纸上显现潜指纹成为警方需解决的突出问题。
众所周知,茚三酮能与指纹汗液中的氨基酸反应,是在多孔表面显现潜指纹的最早方法。
然而,一些热敏纸在使用常规的茚三酮溶液处理时出现对热敏感的正面背景颜色变黑的现象,结果使得收据上的指纹信息受到损毁。
•目前,在热敏纸上显现潜指纹可采用的方法有:1、使用茚三酮衍生物替代茚三酮;2、茚三酮夹心法(用两张含干茚三酮的吸墨纸将热敏纸夹在中间,加压并保持数日);3、二甲氨基苯甲醛烟熏法;4、通过电子探测微量分析仪测绘潜指纹法;5、对新鲜潜指纹使用碘熏法。
•本文介绍的方法是通过降低气压使茚三酮升华,无需溶剂显现热敏纸上的潜指纹。
茚三酮的分子量为178.14,理论上可以从固相直接转化为气相。
已有文献尚没有关于茚三酮的升华和气体分压试验的报道,除了个别文献提及茚三酮在分解时熔点为241℃,有人在常压下曾使用茚三酮烟熏法。
••一、试验设备及方案•整个试验在一个边长为50cm的立体真空箱进行。
真空箱设一个玻璃前门,内部有一个可控温的热源,直径为5cm,位于距真空箱底部上方10cm处。
叶面肥标准—氨基酸含量的测定

1氨基酸含量的测定原理试样用磺基水杨酸沉淀蛋白质后,用EDTA络合金属元素释放氨基酸,各种氨基酸经分离后分别与茚三酮显色,在pH2.2条件下用氨基酸自动分析仪测定各种氨基酸含量,各种氨基酸的总和,即为氨基酸叶面肥料氨基酸的含量。
1.1试剂(1)混合氨基酸标准液(仪器制造公司出售),0.00250mol/L。
(2)乙二胺四乙酸二钠溶液(EDTA)溶液:1%溶液,称1gEDTA溶于100mL 水中。
(3)磺基水杨酸溶液:称取5g磺基水杨酸溶于100mL水中。
(4)盐酸。
(5)盐酸溶液:0.06mol/L。
(6)氢氧化钠溶液:称取50g氢氧化钠溶于100mL水中。
(7)PH2.2的柠檬酸钠缓冲液:称取19.6g柠檬酸钠(Na3C6H5O7·2H2O)和16.5mL盐酸1.1.(4)加水稀释到1000mL,用盐酸和氢氧化钠溶液1.1.(6)调节PH 至2.2。
(8)PH3.3的柠檬酸钠缓冲液:称取19.6g柠檬酸钠和9mL盐酸1.1.(4)加水稀释至1000mL,用盐酸1.1.(4)和氢氧化钠1.1.(6)调节PH至3.3。
(9)PH4.0的柠檬酸钠缓冲液:称取19.6g柠檬酸钠和9mL盐酸1.1.(4)加水稀释至1000mL,用盐酸1.1.(4)和氢氧化钠1.1.(6)调节PH至4.0。
(10)PH6.4的柠檬酸钠缓冲液:称取19.6g柠檬酸钠和46.8g氯化钠(优级纯)加水稀释至1000mL,用盐酸1.1.(4)和氢氧化钠1.1.(6)调节PH至6.4。
(11)茚三酮溶液:a)PH5.2的乙酸锂溶液:称取氢氧化锂(LiO H〃H2O)168g,加入冰乙酸(优级纯)279g,加水稀释到1000mL,用盐酸1.1.(4)和氢氧化钠1.1.(6)调节PH到5.2。
b)茚三酮溶液:称取150mL二甲基亚砜(C2H6OS)和乙酸锂溶液a)50mL 加4g水合茚三酮(C9H4O 3·H2O)和0.12g还原茚三酮(C18H10O 6·2H2O)搅拌至完全溶解。
氨基酸测定方法
4。
1 光度分析法[5] [6]β-氨基丙酸和茚三酮溶液在弱酸的条件下可以生成蓝紫色物质[7],其颜色深浅主要与β-氨基丙酸的浓度有关。
因此可利用此显色反应采用比色法定量测量β—氨基丙酸。
我在实验中发现很多因素如浓度、pH 值、反应温度、以及反应时间等对此显色反应有很大的影响.如忽视这些因素会使实验产生很大的误差.就此显色反应的最佳条件我做了初步的探究.4.1。
1试剂的配制:缓冲液的配制:配制pH= 6。
00的NaAc -HAc 缓冲溶液β—氨基丙酸标准溶液的配制:用电子天平准确称取1。
020 g β-氨基丙酸(生化纯),溶于250ml pH=6.00缓冲溶液中,得到C = 4.080 g/L 标准溶液.茚三酮试剂的配制:称取0.5g 茚三酮溶于100ml 蒸馏水中,得到5g/L 的茚三酮水溶液。
4.1。
2标准曲线的确定分别准确移取0.30ml 、0。
40ml 、0。
50ml 、0.60ml 、0.70ml 、0。
80ml 、0.90ml 、1。
00ml 标准液于8个比色管中,用pH=6.00的缓冲溶液稀释到5.00ml 再加入1ml 茚三酮水溶液充分摇匀,将其放在沸水浴中加热10min 。
冷却到室温,用7230型分光光度计在569nm 下测其吸光度.以吸光度和浓度作一个标准曲线。
4。
1。
3样品的测定稀释待测液于0.24mg/ml-0.73mg/ml,调pH 值到6.00,以相同的反应条件,测其吸光值并与上面的标准曲线对照查出稀释液的浓度,再乘以稀释倍数即为β-氨基丙酸的浓度。
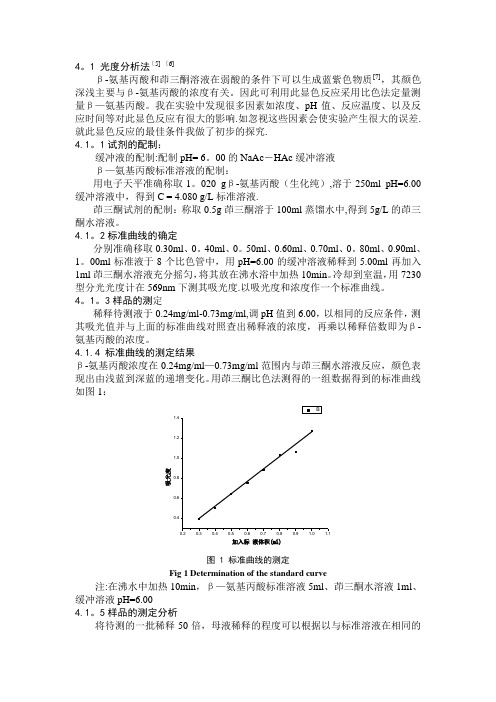
4.1.4 标准曲线的测定结果β-氨基丙酸浓度在0.24mg/ml —0.73mg/ml 范围内与茚三酮水溶液反应,颜色表现出由浅蓝到深蓝的递增变化。
用茚三酮比色法测得的一组数据得到的标准曲线如图1:吸光度加入标液体积(ml)图 1 标准曲线的测定Fig 1 Determination of the standard curve注:在沸水中加热10min ,β—氨基丙酸标准溶液5ml 、茚三酮水溶液1ml 、缓冲溶液pH=6.004.1。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
茚三酮显色法测定氨基酸含量
一、目的
学习茚三酮显色法测定氨基酸含量的方法
二、原理
茚三酮溶液与氨基酸共热,生成氨。氨与茚三酮和还原性茚三酮反应,生成紫色化合物。
该化合物颜色的深浅与氨基酸的含量成正比,可通过测定570nm 处的光密度,测定氨基酸的
含量。
三、 试剂与材料
(1)标准氨基酸溶液:配制成0.3mmol/L 溶液。
(2)pH5.4,2mol/L 醋酸缓冲液:量取86mL 2mol/L 醋酸钠溶液,加入14mL 2mol/L
乙酸混合而成。用pH 检查校正。
(3)茚三酮显色液:称取85mg 茚三酮和15mg 还原茚三酮,用10mL 乙二醇甲醚溶解。
茚三酮若变为微红色,则需按下法重结晶:称取5g 茚三酮溶于15~25mL 热蒸馏水中,加入
0.25g 活性炭,轻轻搅拌。加热30min 后趁热过滤,滤液放入冰箱过夜。次日析出黄白色结
晶,抽滤,用1mL 冷水洗涤结晶,置干燥器干燥后,装入棕色玻璃瓶保存。
还原型茚三酮按下法制备:称取5g 茚三酮,用125mL 沸蒸馏水溶解,得黄色溶液。
将5g 维生素C 用250mL 温蒸馏水溶解,一边搅拌一边将维生素C 溶液滴加到茚三酮溶液
中,不断出现沉淀。滴定后继续搅拌15min,然后在冰箱内冷却到4℃,过滤、沉淀用冷水洗
涤3 次,置五氧化二磷真空干燥器中干燥保存,备用。乙二醇甲醚若放置太久,需用下法除去
过氧化物:在500mL 乙二醇甲醚中加入5g 硫酸亚铁,振荡1~2h,过滤除去硫酸亚铁,再
经蒸馏,收集沸点为121~125℃的馏分,为无色透明的乙二醇甲醚。
(4)60%乙醇。
(5)样品液:每毫升含0.5~50μg 氨基酸。
(6)分光光度计。
(7)水浴锅。
四、操作步骤
1.标准曲线的制作
分别取0.3mmol/L 的标准氨基酸溶液0,0.2,0.4,0.6,0.8,1.0mL 于试管中,用水补
足至1mL。各加入1mL pH5.4,2mol/L 醋酸缓冲液;再加入1mL 茚三酮显色液,充分混
匀后,盖住试管口,在100℃水浴中加热15min,用自来水冷却。放置5min 后,加入3mL60%
乙醇稀释,充分摇匀,用分光光度计测定OD570nm。(脯氨酸和羟脯氨酸与茚三酮反应呈黄色,
应测定OD440nm)。
以OD570nm 为纵坐标,氨基酸含量为横坐标,绘制标准曲线。
2.氨基酸样品的测定
取样品液1mL,加入pH5.4,2mol/L 醋酸缓冲液1mL 和茚三酮显色液1mL,混匀后于100℃
沸水浴中加热15min,自来水冷却。放置5min 后,加3mL 60%乙醇稀释,摇匀后测定
OD570nm(生成的颜色在60min 内稳定)。
将样品测定的OD570nm 与标准曲线对照,可确定样品中氨基酸含量。
