等效平衡规律及练习
等效平衡例题

0
0.5
2g-8m
1.5a (g-3m)a
7
[评注] 比较例2、例3的异同:例2为定T、 V情况下,反应前后气体分子数不变的可 逆反应的等效平衡问题;例3为定T、p情 况下,反应前后气体分子数改变的可逆反 应的等效平衡的问题,解答问题的方法完 全相同。对于例3若N2 、H2 、NH3的加入 量用x、y、z。(mo1)表示,不难导出,达 到等效平衡时,x、y、z应满足的一般条件 是:y=4x,z≥0(当x、y均大于0时,z才能 为0)
8
(3)a、b、c必须满足的一般条件是(请用两个方程式表
示,其中一个只含a和c,另一个只含b和c):
a +c=2
、 b +0.5c=1
。(全国高考题) 3
Ⅱ类:在定T、V情况下, 对于反应前后气体分子数 不变的可逆反应,只要反 应物(或生成物)的物质的 量的比例与原平衡相同, 则二平衡等效。
4
[例2] 在一个固定体积的密闭容器中,保持一定 温度进行以下反应:H2 (g)十 Br2 (g)
平衡状态。
现在该容器中维持温度不变,令a、b、c分别代表初始加
入的SO2 、O2和SO3的物质的量(mo1)。如a、b、c取不同 的数值,它们必须满足一定的相互关系,才能保证达到
平衡时,反应混合物中三种气体的体积分数仍跟上述平
衡时的完全相同。请填写下列空白:
(1)若a=0,b=0,则c= 2 。
(2)若a=0.5,则b= 0.25 和C= 1.5 。
条件下,只改变起始加入情况,只要 通过可逆反应的化学计量数比换算成 平衡式左右两边同一边物质的物质的 量与原平衡相同,则二平衡等效。
2
例1: 在一定温度下,把2molSO2 和1mo1O2通人一个一
高中化学高考总复习《等效平衡》知识讲解及巩固练习题(含答案解析)
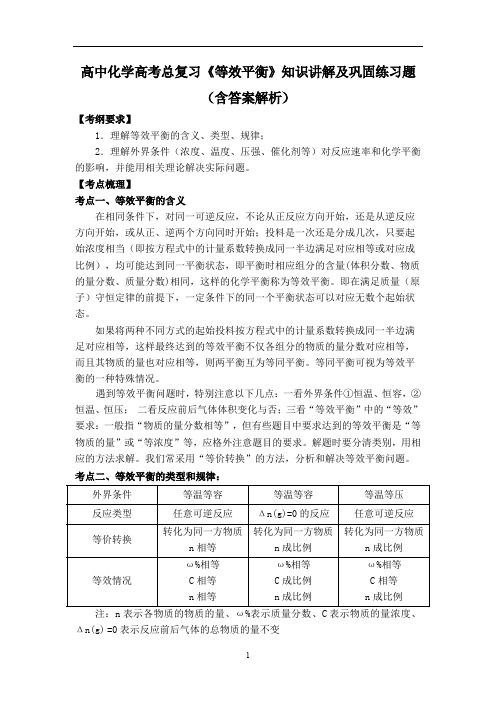
n 相等
n 成比例
n 成比例
ω%相等
ω%相等
ω%相等
等效情况
C 相等
C 成比例
C 相等
n 相等
n 成比例
n 成比例
注:n 表示各物质的物质的量、ω%表示质量分数、C 表示物质的量浓度、
Δn(g) =0 表示反应前后气体的总物质的量不变
1
要点诠释: 等效平衡的解题方法与技巧是:明确等效平衡的种类:一是恒温恒容下的等
【答案】 恒 压 恒
(2)
9
3a
(3)
0.4
1.2
x、y、z 取值必须满足的一般条件:(2 分)y=3x(x≥0);z
≥0
(x、y、z 不同时为
0)
(5)
2
5
(6) 0.75
0.5
容 x、y、z 取值必须满足的一般条件(一个只含 x、z,另一个只
含 y、z):(2 分)2x+z=2;
(2 分)2y+3z
达到平衡前 v(正)>v(逆) D.相同温度下,起始时向容器中充入 2.0molPCl3、2.0molCl2,达到平衡时,PCl3
的转化率小于 80%
【思路点拨】注意容器体积为 2.0L,所给数据为物质的量。
【答案】C
【解析】A.反应在前 50 s 内的平均速率应该是前 50 s 内 PCl3 浓度变化与时间的 比值,而不是 PCl3 物质的量的变化与时间的比值。 B.相同温度下,起始时向容器中充入 1.0molPCl5、0.20molPCl3 和 0.20molCl2 应
=6.
a 与 b 的关系是: a>b
类型二:恒温恒容下,对于反应前后气体体积没有变化的反应来说(即△V=0 的 体系):等价转化后,只要反应物(或生成物)的物质的量的比例与原平衡起 始态相同,两平衡等效。 例 2、在一个固定容积的密闭容器中,保持一定的温度进行以下反应:
等效平衡经典十一题

等效平衡经典十一题一、等效平衡的原理在一定条件(定温、定容或定温、定压)下,只是起始加入情况不同的同一可逆反应达到平衡后,任何相同组分的物质的量分数(或体积分数)均相同,这样的化学平衡互称等效平衡。
二、等效平衡的建立化学平衡状态的建立与条件(如浓度、温度、压强等)有关,而与建立平衡时的途径无关,因而同一可逆反应,从不同的状态开始,只要达到平衡时的条件(浓度、温度、压强等)完全相同,则可形成等效平衡。
如常温常压下,可逆反应:2SO2 + O22 SO3① 2mol 1mol 0② 0 0 2mol③ 1mol 0.5mol 1mol①从正反应开始,②从逆反应开始,③从正、逆反应同时开始,由于①、②、③三种情况如果按方程式的化学计量数比折算成同一方向的反应物,对应各组分的物质的量均相等[如将②、③折算为①],因此三者为等效平衡。
三、等效平衡的规律1、定温、定容条件下的等效平衡Ⅰ类:在定温、定容条件下,对于反应前后气体化学计量数不相等的可逆反应,只改变起始时加入物质的物质的量,若通过可逆反应的化学计量数之比换算成同一边物质的物质的量,所得反应物(或生成物)的物质的量与原起始量对应相同,则两平衡等效。
Ⅱ类:在定温、定容条件下,对于反应前后气体化学计量数相等的可逆反应,只改变起始时加入物质的物质的量,若通过可逆反应的化学计量数之比换算成同一边物质的物质的量,所得反应物(或生成物)的物质的量之比与原起始量之比对应相同,则两平衡等效。
2、定温、定压条件下的等效平衡在定温、定压条件下,对于反应前后气体化学计量数任意型的可逆反应,只改变起始时加入物质的物质的量,若通过可逆反应的化学计量数之比换算成同一边物质的物质的量,所得反应物(或生成物)的物质的量之比与原起始量之比对应相同,则两平衡等效。
四、等效平衡的解题思想——极值法无论平衡从哪个方向建立,在判断时,都可以根据题给条件,把生成物全部推算成反应物或把反应物全部推算成生成物,再与平衡开始时加入的物质的量相比较。
等效平衡原理(精讲+练习)

等效平衡原理一、等效平衡原理在一定条件(定温、定压或定温、定容)下,对于同一可逆应,尽管起始时加入物质的物质的量不同,而达到平衡时,同种物质的百分含量相同,这样的平衡称为等效平衡。
二、等效平衡规律根据反应条件(定温、定压或定温、定容)以及可逆反应的特点(反应前后气体分子数是否相等),可将等效平衡问题分成三类:1、(全等平衡)条件:在恒温、恒容条件下,经等价转换后,与原起始物质的物质的量(或浓度)相等,则两平衡等效。
结果:n、c、%相等例:在一定温度下,把2 mol SO2和1 mol O2通入一个一定容积的密闭容器里,发生如下反应:2SO2+O22SO3当此反应进行到一定程度时,反应混合物就处于化学平衡状态。
现在该容器中,维持温度不变,令a、b、c分别代表初始加入的SO2、O2和SO3的物质的量(mol)。
如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时反应混合物中三种气体的百分含量仍跟上述平衡时的完全相同。
请填空:(1)若a=0,b=0,则c=___________。
(2)若a=0.5,则b=_________,c= _________。
(3)a、b、c取值必须满足的一般条件是(用两个方程式表示,其中一个只含a和c,另一个只含b和c):,。
2、(相似平衡)条件:在恒温、恒容条件下,经等价转换后,对应物质的物质的量之比与原平衡相同,则两平衡等效。
结果:%相等例:在等温、等容条件下,有下列气体反应2A(g)+2B(g)C(g)+3D(g)现分别从两条途径建立平衡:I.A、B的起始浓度均为2mol/L II.C、D的起始浓度分别为2mol/L 和6mol/L,下列叙述正确的是A.I、II两途径最终达到平衡时,体系内混合气体的百分组成相同B.I、II两途径最终达到平衡时,体系内混合气体的百分组成不同C.达到平衡时I途径的v(A)等于II途径的v(A)D.达到平衡后,I途径混合气体密度为II途径混合气体密度的二分之一3、(等同平衡)条件:在恒温、恒压下,经等价转换后,对应物质的物质的量之比与原平衡相同,则与原平衡等效。
化学平衡的移动和等效平衡

化学平衡的移动和等效平衡一.化学平衡的移动1.移动规律:遵循勒夏特列原理。
(1)浓度:增大反应物浓度或减小生成物浓度,平衡向正反应方向移动;减小反应物浓度或增大生成物浓度,平衡向逆反应方向移动。
(2)压强:增大压强,平衡向气体体积减小的方向移动;减小压强,平衡向气体体积增大的方向移动。
(3)温度:升高温度,平衡向吸热反应方向移动;降低温度,平衡向放热反应方向移动。
(4)催化剂:不能使平衡移动,但能减小达到新平衡所需要的时间。
2.例题:(1)反应2A(g)2B(g)+C(g);△H>0,达平衡时,要使v正降低、c(A)增大,应采取的措施是()。
A.加压B.减压C.升温D.降温(2)在容积固定的密闭容器中存在如下反应:A(g) + B(g) 3 C(g);(正反应为放热反应)某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断一定错误的是()。
A、图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高B、图Ⅱ研究的是压强对反应的影响,且甲的压强较高C、图Ⅱ研究的是温度对反应的影响,且甲的温度较高D、图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高[小结] 图像题的解题技巧:①四看:看横纵坐标表示的量,看图像的起点,看图像的转折点,看图像的走势;②联系:将题目的已知条件、图像得出的结论和平衡移动原理联系起来,看是否吻合,即可得出结论。
二.等效平衡规律1.恒温、恒容条件下的体积可变的等效平衡如果按方程式的化学计量关系转化为方程式同一半边的物质,其物质的量与对应组分的起始加入量相同,则建立的化学平衡状态时等效的。
例题:在密闭容器中,加入3molA和1 molB,一定条件下发生反应3A(g)+B(g)2C(g)+D(g),达平衡时,测得C的浓度为w mol/L,若保持容器中压强和温度不变,重新按下列配比作起始物质,达到平衡时,C的浓度仍然为w mol/L的是( )A.6molA+2mol B B 1.5mol A+0.5mol B+1mol C+0.5mol DC. 3mol A+1mol B+2mol C+1mol D D 2mol C+1mol D2.恒温、恒容条件下体积不变的等效平衡如果按方程式的化学计量关系转化为方程式同一半边的物质,其物质的量与对应组分的起始加入量成比例,则建立的化学平衡状态时等效的。
等效平衡专题(较好的资料)
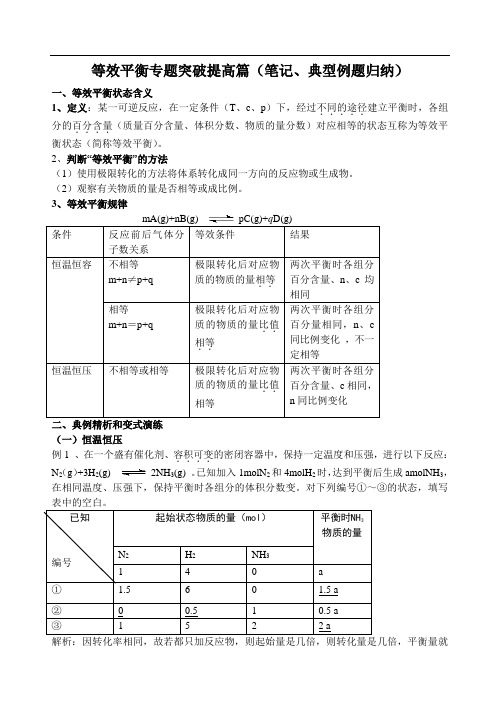
等效平衡专题突破提高篇(笔记、典型例题归纳)一、等效平衡状态含义1、定义:某一可逆反应,在一定条件(T 、c 、p )下,经过不同的途径.....建立平衡时,各组分的百分含量....(质量百分含量、体积分数、物质的量分数)对应相等的状态互称为等效平衡状态(简称等效平衡)。
2、判断“等效平衡”的方法(1)使用极限转化的方法将体系转化成同一方向的反应物或生成物。
(2)观察有关物质的量是否相等或成比例。
3、等效平衡规律二、典例精析和变式演练(一)恒温恒压例1 、在一个盛有催化剂、容积可变....的密闭容器中,保持一定温度和压强,进行以下反应: N 2(g )+3H 2(g) 2NH 3(g) 。
已知加入1molN 2和4molH 2时,达到平衡后生成amolNH 3,在相同温度、压强下,保持平衡时各组分的体积分数变。
对下列编号①~③的状态,填写表中的空白。
解析:因转化率相同,故若都只加反应物,则起始量是几倍,则转化量是几倍,平衡量就是几倍,又因等压条件下物质的量之比等于体积之比,故起始量之比等于平衡量之比。
①和题干量之比是1.5,平衡之比就是1.5。
②的平衡量是题干平衡量的一半,则若没有NH3,只有N2、H2,则其物质的量应分别为0.5和2mol,又因1 mol NH3完全转化生成N20.5 mol,H21.5mol,故原来的N2、H2分别为0 mol 和0.5mol。
③可同理推得。
例2、恒温、恒压..下,在一个可变容积的容器中发生如下发应:A(g)+B(g)C(g)(1)若开始时放入1molA和1molB,到达平衡后,生成a molC,这时A的物质的量为mol。
(2)若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为mol。
(3)若开始时放入x molA,2molB和1molC,到达平衡后,A和C的物质的量分别是ymol 和3a mol,则x=mol,y=mol。
平衡时,B的物质的量(选填一个编号)(甲)大于2 mol (乙)等于2 mol(丙)小于2 mol (丁)可能大于、等于或小于2mol作出此判断的理由是。
化学等效平衡解题规律及练习

化学等效平衡解题规律规律一:在恒温恒容下,对于化学反应前后气体体积发生变化的可逆反应,只改变起始加入物质的物质的量,如果通过可逆反应的化学计量数之比换算成化学方程式的同一边物质的物质的量与原平衡相同,则两平衡等效。
规律二:在恒温恒容下,对于反应前后气体体积不变的可逆反应,只要反应物(或生成物)的物质的量之比与原平衡相同,则两平衡等效。
规律三:恒温恒压下,改变起始时加入物质的物质的量,只要按化学计量数之比换算成化学方程式的同一边物质的物质的量之比与原平衡相同,达到平衡后与原平衡等效。
练习:1、在t℃时,向2L密闭容器中放入1molA和1molB,发生下列反应:A(g)+B(g)C(g)+2D(g),平衡时C的含量为m%,保持其他条件不变,若按下列配比将物质放入容器中达到平衡时,C的含量仍为m%的是()A、2molA和1molBB、2molD和A、B、C各1molC、1molC和2molDD、1molC和1molD2、某温度下,在一容积可变的容器中,反应2A(g) + B(g) 2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、2 mol和4 mol。
保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是()A.均减半B.均加倍C.均增加1 mol D.均减少1 mol3、在一恒温恒容密闭容器中,A、B气体可建立如下平衡:2A(g)+2B(g) C(g)+3D(g)现分别从两条途径建立平衡:Ⅰ. A、B的起始量均为2mol;Ⅱ. C、D的起始量分别为2mol 和6mol。
下列叙述不正确的是:()A、Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成相同B、Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成不同C、达到平衡时,途径Ⅰ的和途径Ⅱ体系内混合气体平均相对分子质量相同D、达到平衡时,途径Ⅰ的气体密度为途径Ⅱ密度的1/24、在恒温、恒压的条件下,向可变容积的密闭容器中充入3LA和2LB,发生如下反应:3A(气)+2B(气)xC(气)+yD(气)达到平衡时,C的体积分数为m%。
高中化学 等效平衡讲义及练习 新人教版选修4

等效平衡讲义及练习一、等效平衡的含义在一定条件下(定温、定容或温定压)下,只是起始加入情况不同的同一可逆反应达到平衡后,任何相同组分的分数(体积、物质的量)均相同这样的化学平衡互称等效平衡。
二、等效平衡的分类1、定温、定容条件下的等效平衡。
①对于一般可逆反应,在定T 、V 条件下改变起始加入情况,只要按可逆反应的化学计量数比换算成平衡式左右两边同一边物质的物质的量比与原平衡相同,则两平衡等效。
②在T 、V 定的情况下,对于反应前后气体分子数不变的可逆反应,只要反应物(或生成物)的物质的量之比与原平衡相同,则两平衡等效。
例1、 在一定温度下,把2molSO 2和1molO 2通入一个一定容积的密闭容器里,发生如下反应:2 SO 2 + O 2 2 SO 3,当此反应进行到一定程度时,反应混合物就处于化学平衡状态。
现在该容器中保持温度不变,令a 、b 、c 分别代表初始加入的SO 2 、O 2和SO 3的物质的量(mol )如a 、b 、c 取不同的数值,他们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中的三种气体的体积分数任跟上述平衡时的完全相同,请填写下列空白: (1) 若a=0、b=0,则c=_________(2) 若a=0.5、则b=_________ c=__________(3) a,b,c 必须满足的一般条件是(请用两个方程式表示其中一个只含a 和b ,另一个只含b 和c )_________________________ ___________________________ 例2、在一个固定体积的密闭容器中,保持一定温度进行以下反应:H 2+Br 2(g)2HBr(g)已加入1molH 2和2molBr 2时,求平衡后生成a molHBr,(见表中“已知”项)在相同条件下,且保持平衡时各组分的体积分数不变,根据下列编号(1)~(3)的状态,填写表中的空白。
催化剂 △2、在定T,P 条件下等效平衡在定T,P 条件下,改变起始加入情况,只要按可逆反应的计量数比换算成平衡式左右两边同一物质的量之比与原平衡相同,达平衡后与原平衡等效。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
等效平衡规律:(1)在恒温、恒容条件下,对于反应前后气体分子数改变的可逆反应,只改变起始时加入物质的物质的量,如果按化学方程式的化学计量关系转化为化学方程式中同一半边的物质,其物质的量与对应组分的起始加入量相同,则建立的化学平衡是等效的恒温、恒容时,I、Ⅱ、Ⅲ这三种情况下达到的平衡完全等效。
IV与I、Ⅱ、Ⅲ不等效。
(2)在恒温、恒容条件下,对于反应前后气体分子数不变的可逆反应,改变起始时加入物质的物质的量,如果按化学方程式的化学计量关系转化为化学方程式同一半边的物质,其物质的量比与对成组分的起始加入量比相同,则建立的化学平衡是等效的。
I、Ⅱ、Ⅲ形成等效平衡,此处等效的含义是各物质的体积分数相同,同时,混合气体的平均摩尔质量也相同,但各物质的浓度、物质的量、混合气体的密度、体系的压强、气体的反应速率等均不相同但成比例。
(3)在恒温、恒压条件下,改变起始时加入物质的物质的量,如果按化学计量数换算成化学方程式同一半边的物质,其物质的量之比与对应组分的起始加入量之比相同,则建立的化学平衡等效。
I、Ⅱ、Ⅲ、Ⅳ形成等效平衡。
说明等效平衡分析方法:“一边倒”——按化学计量关系将生成(反应)物全部转化为反应(生成) 物后再看是否相同或成比例。
随堂练习A组基础巩固型i.恒压下,在-个可变容积的密闭容器中发生如下反应:2NH3(g)+CO2(g)CO(NH2)2(g)+H2O(g)若开始时放入2mol NH3和1mol CO2,达平衡后,生成amol H2 O;若开始时放入xmol NH3、2mol CO2和1mol H2O(g),达平衡后,H2O的物质的量是3a mol,则x为A 1molB 2molC 3molD 4molii.(双选)在密闭容器中,加入3mol A和1mol B,一定条件下发生反应3A(g)+B(g)2C(g)+D(g),达平衡时,测得C的浓度为w mol/L,若保持容器中压强和温度不变,重新按下列配比作起始物质,达到平衡时,C的浓度仍然为w mol/L的是A 6mol A+2molB B 1.5mol A+0.5mol B+1mol C+0.5mol DC 3mol A+1mol B+2mol C+1molD D 2mol C+1mol Diii.一定条件下,向一带活塞的密闭容器中充入2mol SO2和1molO2,发生下列反应:2SO2(g)+O2(g)2SO3(g)达到平衡后改变下述条件,SO3气体平衡浓度不改变的是A 保持温度和容器体积不变,充入1mol SO2(g)B 保持温度和容器内压强不变,充入1mol SO3(g)C 保持温度和容器内压强不变,充入1mol O2(g)D 保持温度和容器内压强不变,充入1mol Ar(g)iv.(双选)在一个固定容积的密闭容器中,加入mmol A、nmol B,发生下列反应:mA(g)+nB(g)pC(g)平衡时C的浓度是wmol/L,若容器体积和温度不变,起始时放入amol A、bmol B、cmol C,若要平衡后C的浓度仍为wmol/L,则a、b、c应满足的关系是A a︰b︰c=m︰n︰pB a︰b=m︰n (ap/m)+c=pC (mc/p)+a=m,(nc/p)+b=nD a=m/3,b=n/3,c=2p/3v.(双选)在VL密闭容器中,通入0.2mol SO2和0.2mol SO3气体,在一定条件下发生反应:2SO2+O22SO3。
平衡时SO3为amol;在相同温度下按下列配比在VL密闭容器中放入起始物质,平衡时有关SO3的正确叙述是A 放入0.2mol SO2、0.1molO2、0.1mol SO3,达到平衡时SO3必小于amolB 放入0.2mol SO2、0.1molO2、0.2mol SO3,达到平衡时SO3必大于amolC 放入0.4mol SO2、0.1molO2,达到平衡时SO3会等于0.4molD 放入0.2mol SO2、0.1molO2,达到平衡时SO3必小于amolvi.(双选)一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g)3C(g),若反应开始时充入2mol A和2mol B,达平衡后A的体积分数为a%。
其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是A 2mol CB 2mol A 1mol B和1mol He(不参加反应)C 1mol B和1mol CD 2mol A 3mol B和3mol Cvii.(双选)一定温度下将amol PCl5充入一密闭容器中达到如下平衡:PCl5(g)PCl3(g)+Cl2(g),此时压强为P1;再向容器中通入amol PCl5,在同温下又达到平衡时的压强为P2,则下列说法中正确的是A 2P1>P2B 2P1=P2C 2P1<P2D P1<P2viii.在恒温时,一固定容积的容器内发生如下反应:2NO2(g)N2O4(g) 达平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数A 不变 B 增大 C 减小 D 无法判断ix.某恒温恒容的容器中,建立如下平衡:2A(g)B(g),在相同条件下,若分别再向容器中通入一定量的A气体或B气体,重新达到平衡后,容器内A的体积分数比原平衡时A 都增大B 部减小C 前者增大后者减小D 前者减小后者增大x.在一定温度下,在一固定容积的密闭容器中存在着如下的平衡:2NO2N2O4现在维持容器温度和容积均不变的情况下,向容器中补充ag NO2,待建立新的平衡时,平衡混和物中NO2的含量比原平衡状态A 增大B 减小C 不变D 以上三种情况都有可能xi.(双选)某密闭容器中放入一定量的NO2,发生反应2NO2N2O4(正反应放热),达平衡后,若分别单独改变下列条件,重新达到平衡后,能使混和气体平均分子量增大的是A 通入N2B 通入NO2C通入N2O4 D 升高温度xii.一定条件下,向一带活塞的密闭容器中充入2mol SO2和1mol O2,发生下列反应:2SO2(g)+O2(g)2SO3(g)达到平衡后改变下述条件,SO3气体平衡浓度不改变的是A 保持温度和容器体积不变,充入1mol SO3(g)B 保持温度和容器内压强不变,充入1mol SO3(g)C 保持温度和容器内压强不变,充入1mol O2(g)D 保持温度和容器内压强不变,充入1mol Ar(g)xiii.把质量相同的N2O4和NO2分别放入体积相同的两个密闭容器a、b中,维持a、b处于相同温度,当达到平衡后,结果是A a中N2O4百分含量比b中的高B a中压强比b中压强小C a中的气体总物质的量比b中少D a、b中各气体的百分含量对应相同xiv.(双选)某温度下,在固定容积的容器中,可逆反应:A(g)+3B(g)2C(g)达到平衡时,测得平衡时的物质的量之比为A︰B︰C=2︰2︰1。
保持温度不变,再以2︰2︰1的体积比充入A、B和C,则A 平衡向正方向移动B 平衡不移动C C的百分含量增大D C的百分含量可能减小xv.两个体积相同的密闭容器A和B,在A中充入SO2和O2各1g。
在B中充入SO2和O2各2g。
加热到相同温度时,有如下反应:2SO2+O22SO3,对此反应下列说法正确的是A A、B两容器中反应速率相等B A、B两容器中SO 2的转化百分率相等C A、B两容器中混合气体达平衡后,各组分的百分含量相等D A、B两容器中混合气体达平衡前后,各自的总质量相等xvi.(双选)在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个带有理想活塞(即无质量、无摩擦力的刚性活塞)的体积可变的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g)A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡。
下列说法中正确的是A 平均反应速度:乙>甲B 平衡时nc(甲)>nc(乙)C 平衡时C的转化率:乙>甲D 平衡时A的物质的量甲>乙xvii.在相间的条件下(T=500K),相同体积的甲、乙网容器,甲容器中充入1g SO2,乙容器中充入2g SO2、2g O2,下列叙述错误的是A 化学反应速度:乙>甲B 平衡后O2的浓度:乙>甲C SO2的转化率:乙>甲D 平衡后SO2的浓度:乙>甲xviii.将1mol SO2和1mol O2通入密闭容器中,在一定条件下反应达到平衡,平衡体系中有SO3 0.3mol,此时若移走0.5mol O2和0.5 mol SO2,则反应达到新平衡时SO3的物质的量为A 0.3mol B 0.15mol C 小于0.15mol D 大于0.15mol,小于0.3mol xix.(双选)定容容器a与定容容器b的体积相同,内皆装入质量相同、按相同物质的量之比混合的SO2和O2,经一定时间在相同温度下达到平衡,下列叙述正确的是A a、b中SO2的转化率相同B b中的反应速度比a中快C b中SO2的转化率比a中高D 若a、b中皆再加入同量氮气,平衡不移动xx.(双选)在恒温、恒容的条件下,有反应2A(g)+2B(g)C(g)+3D(g),现从两条途径分别建立平衡。
途径Ⅰ:A、B的起始浓度均为2mol/L;途径Ⅱ:C、D的起始浓度分别为2 mol/L和6mol/L。
则以下叙述正确的是A 两途径最终达到平衡时,体系内混合气的百分组成相同B 两途径最终达到平衡时,体系内混合气的百分组成不同C 达平衡时,途径Ⅰ的反应速率v(A)等于途径Ⅱ的反应速率v(A)D 达平衡时,途径Ⅰ所得混合气的密度为途径Ⅱ所得混合气密度的1/2xxi.(双选)甲、乙两容器都发生反应2A(g)+B(g)xC(g),两容器温度和初始压强相同。
甲容器中充入2molA和1molB,达平衡后,C在平衡混合气中的体积分数为 、物质的量为n1;乙容器中充入1.4molA、0.7molB和0.6molC,达平衡后C在平衡混合气中的体积分数为 、物质的量为n2。
下列说法中正确的是A 若甲、乙两容器均为恒容容器,则x必等于2B 若甲、乙两容器均为恒压容器,则x必等于3C 若甲为恒压容器、乙为恒容容器,且x≠3,则n1必大于n2D 若甲为恒容容器、乙为恒压容器,且x=3,则n1必大于n2xxii.在恒温时,向某密闭容器中通入2mol X和1mol Y气体,发生如下反应:2X (气)+Y(气)2Z(气),压强一定时,测得在平衡时Z的体积分数为0.4。
(1)与上述平衡保持同温、同压,若向密闭容器中通入4mol X(气)、2mol Y(气),达到平衡,则Z的体积分数为;平衡时,气体的总物质的量是。
(2)若向密闭器中通入X(气)和Y(气)的物质的量分别记为n(X)、n(Y),保持容器容积不变,并满足平衡时Z的体积分数为0.4,则n(X)/n(Y)的取值范围为。
