热学习题课(大学物理)
大学物理第十三章(热力学基础)部分习题及答案

第十三章热力学基础一、简答题:1、什么是准静态过程?答案:一热力学系统开始时处于某一平衡态,经过一系列状态变化后到达另一平衡态,若中间过程进行是无限缓慢的,每一个中间态都可近似看作是平衡态,那么系统的这个状态变化的过程称为准静态过程。
2、什么是可逆过程与不可逆过程答案:可逆过程:在系统状态变化过程中,如果逆过程能重复正过程的每一状态,而且不引起其它变化;不可逆过程:在系统状态变化过程中,如果逆过程能不重复正过程的每一状态,或者重复正过程时必然引起其它变化。
3、一系统能否吸收热量,仅使其内能变化? 一系统能否吸收热量,而不使其内能变化?答:可以吸热仅使其内能变化,只要不对外做功。
比如加热固体,吸收的热量全部转换为内能升高温度;4、简述热力学第二定律的两种表述。
答案:开尔文表述:不可能制成一种循环工作的热机,它只从单一热源吸收热量,并使其全部变为有用功而不引起其他变化。
克劳修斯表述:热量不可能自动地由低温物体传向高温物体而不引起其他变化。
5、什么是熵增加原理?答:一切不可逆绝热过程中的熵总是增加的,可逆绝热过程中的熵是不变的。
把这两种情况合并在一起就得到一个利用熵来判别过程是可逆还是不可逆的判据——熵增加原理。
6、什么是卡诺循环? 简述卡诺定理?答案:卡诺循环有4个准静态过程组成,其中两个是等温线,两个是绝热线。
卡诺提出在稳度为T1的热源和稳度为T2的热源之间工作的机器,遵守两条一下结论:(1)在相同的高温热源和低温热源之间工作的任意工作物质的可逆机,都具有相同的效率。
(2)工作在相同的高温热源和低温热源之间的一切不可逆机的效率都不可能大于可逆机的效率。
7、可逆过程必须同时满足哪些条件?答:系统的状态变化是无限缓慢进行的准静态过程,而且在过程进行中没有能量耗散效应。
二、选择题1、对于理想气体的内能,下列说法中正确的是( B ):( A ) 理想气体的内能可以直接测量的。
(B) 理想气体处于一定的状态,就有一定的内能。
北京化工大学 普通物理学 习题课上(热学).

致冷机的致冷系数定义为:
A Q1 Q2 1 Q2
Q1
Q1
Q1
e Q2 A
Q2 Q1 Q2
七、热力学第二定律的两种表述 不可能从单一热源吸取热量,使它完全变为有用功
而不引起其它变化(即热全部变为功的过程是不可能 的) 热力学第二定律的开尔文表述。
不可能把热量从低温物体自动传到高温物体而不引 起其它变化(即热量不可能自动地从低温物体传向高 温物体) 热力学第二定律的克劳修斯表述。
dQp dT
i2 2
R
迈耶公式:
比热容比:
C p,m CV ,m R
Cp,m i 2
CV ,m
i
CV ,m
1
dE dT
i 2
R
C p,m
i2 2
R,
i
i
2
单原子气体:
CV ,m
3R 2
双原子气体:
CV ,m
5R 2
单原子分子气体: CV ,m 12.47
卡诺循环的效率: T1 T2 1 T2
T1
T1
卡诺致冷机的致冷系数:e Q2 T2
Q1 Q2 T1 T2
七、热力学第二定律
四种热力学过程的主要公式
过程 过程方程 E2 E1
等体 p C
T
M Mm
CV
(T2
T1)
等压 V C
T
M Mm
CV
(T2
T1)
1.25 20.81J 0.028
929J
所以气体在这一过程中所吸收的热量为
(完整版)大学物理热学习题附答案

一、选择题1.一定量的理想气体贮于某一容器中,温度为T ,气体分子的质量为m 。
根据理想气体的分子模型和统计假设,分子速度在x 方向的分量平方的平均值 (A) m kT x 32=v (B) m kT x 3312=v (C) m kT x /32=v (D) m kT x /2=v2.一定量的理想气体贮于某一容器中,温度为T ,气体分子的质量为m 。
根据理想气体分子模型和统计假设,分子速度在x 方向的分量的平均值 (A) m kT π8=x v (B) m kT π831=x v (C) m kT π38=x v (D) =x v 03.温度、压强相同的氦气和氧气,它们分子的平均动能ε和平均平动动能w 有如下关系:(A) ε和w都相等 (B) ε相等,w 不相等 (C) w 相等,ε不相等 (D) ε和w 都不相等4.在标准状态下,若氧气(视为刚性双原子分子的理想气体)和氦气的体积比V 1 / V 2=1 / 2 ,则其内能之比E 1 / E 2为:(A) 3 / 10 (B) 1 / 2 (C) 5 / 6 (D) 5 / 35.水蒸气分解成同温度的氢气和氧气,内能增加了百分之几(不计振动自由度和化学能)?(A) 66.7% (B) 50% (C) 25% (D) 06.两瓶不同种类的理想气体,它们的温度和压强都相同,但体积不同,则单位体积内的气体分子数n ,单位体积内的气体分子的总平动动能(E K /V ),单位体积内的气体质量ρ,分别有如下关系:(A) n 不同,(E K /V )不同,ρ不同 (B) n 不同,(E K /V )不同,ρ相同(C) n 相同,(E K /V )相同,ρ不同 (D) n 相同,(E K /V )相同,ρ相同7.一瓶氦气和一瓶氮气密度相同,分子平均平动动能相同,而且它们都处于平衡状态,则它们(A) 温度相同、压强相同 (B) 温度、压强都不相同(C) 温度相同,但氦气的压强大于氮气的压强(D) 温度相同,但氦气的压强小于氮气的压强8.关于温度的意义,有下列几种说法:(1) 气体的温度是分子平均平动动能的量度;(2) 气体的温度是大量气体分子热运动的集体表现,具有统计意义;(3) 温度的高低反映物质内部分子运动剧烈程度的不同;(4) 从微观上看,气体的温度表示每个气体分子的冷热程度。
《大学物理学》热力学基础练习题
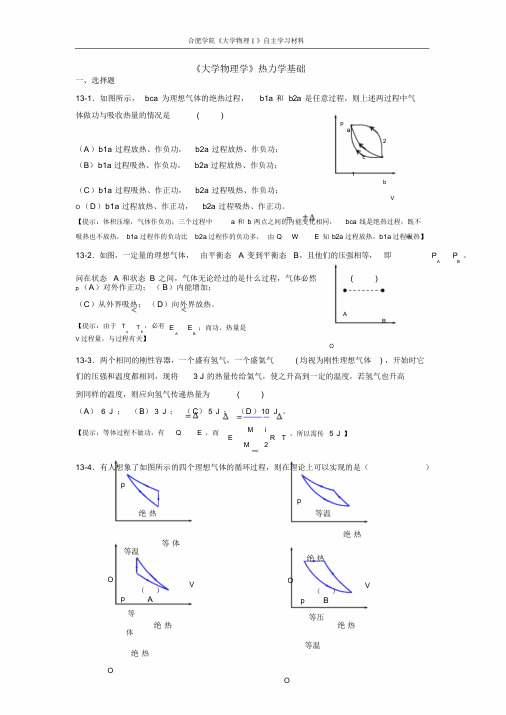
合肥学院《大学物理Ⅰ》自主学习材料《大学物理学》热力学基础一、选择题13-1.如图所示,bca 为理想气体的绝热过程,b1a 和b2a 是任意过程,则上述两过程中气体做功与吸收热量的情况是( )pa2(A)b1a 过程放热、作负功,b2a 过程放热、作负功;c(B)b1a 过程吸热、作负功,b2a 过程放热、作负功;1b(C)b1a 过程吸热、作正功,b2a 过程吸热、作负功;VO (D)b1a 过程放热、作正功,b2a 过程吸热、作正功。
【提示:体积压缩,气体作负功;三个过程中 a 和b 两点之间的内能变化相同,bca 线是绝热过程,既不吸热也不放热,b1a 过程作的负功比b2a 过程作的负功多,由Q W E 知b2a 过程放热,b1a 过程吸热】13-2.如图,一定量的理想气体,由平衡态 A 变到平衡态B,且他们的压强相等,即P P 。
A B问在状态 A 和状态 B 之间,气体无论经过的是什么过程,气体必然( )p (A)对外作正功;(B)内能增加;(C)从外界吸热;(D)向外界放热。
AB【提示:由于T T ,必有A B E E ;而功、热量是A BV 过程量,与过程有关】O13-3.两个相同的刚性容器,一个盛有氢气,一个盛氦气( 均视为刚性理想气体) ,开始时它们的压强和温度都相同,现将 3 J 的热量传给氦气,使之升高到一定的温度,若氢气也升高到同样的温度,则应向氢气传递热量为( )(A) 6 J ;(B)3 J ;(C)5 J ;(D)10 J 。
【提示:等体过程不做功,有Q E ,而M iE R TM 2mol,所以需传 5 J 】13-4.有人想象了如图所示的四个理想气体的循环过程,则在理论上可以实现的是()pp绝热等温绝热等体等温绝热Op 等()AV Op()B等压V 绝热绝热体等温绝热OOVV ()C()D【提示:(A) 绝热线应该比等温线陡,(B)和(C)两条绝热线不能相交】热力学基础-1合肥学院《大学物理Ⅰ》自主学习材料13-5.一台工作于温度分别为327℃和27℃的高温热源与低温热源之间的卡诺热机,每经历一个循环吸热2000J,则对外做功()(A)2000 J ;(B)1000 J ;(C)4000 J ;(D)500 J 。
大学物理热学练习题及答案

大学物理热学练习题及答案第一题:一个物体的质量是1 kg,温度从20°C升高到30°C,如果物体的比热容是4200 J/(kg·°C),求物体吸收的热量。
解答:根据热量公式Q = mcΔθ,其中 Q 表示吸收的热量,m 表示物体的质量,c 表示比热容,Δθ 表示温度变化。
代入数据得:Q = 1 kg × 4200 J/(kg·°C) × (30°C - 20°C)= 1 kg × 4200 J/(kg·°C) × 10°C= 42,000 J所以物体吸收的热量为42,000 J。
第二题:一块金属材料的质量是0.5 kg,它的比热容是400 J/(kg·°C),经过加热后,材料的温度升高了60°C。
求该金属材料所吸收的热量。
解答:根据热量公式Q = mcΔθ,其中 Q 表示吸收的热量,m 表示物体的质量,c 表示比热容,Δθ 表示温度变化。
代入数据得:Q = 0.5 kg × 400 J/(kg·°C) × 60°C= 12,000 J所以金属材料吸收的热量为12,000 J。
第三题:一个热容为300 J/(kg·°C)的物体,吸收了500 J的热量后,温度升高了多少摄氏度?解答:根据热量公式Q = mcΔθ,其中 Q 表示吸收的热量,m 表示物体的质量,c 表示比热容,Δθ 表示温度变化。
将已知数据代入公式:500 J = m × 300 J/(kg·°C) × Δθ解方程得:Δθ = 500 J / (m × 300 J/(kg·°C))= 500 J / (m/(kg·°C)) × (kg·°C/300 J)= (500/300) °C≈ 1.67°C所以温度升高了约1.67°C。
大学物理热力学第一定律习题

热力学第一定律习题讨论★例题1 一些基本过程的Q 、W 、∆U 、∆H 计算过程W Q ∆U ∆H i.g. 自由膨胀0 0 0 0 i.g. 等温可逆 nRTln(V 2/V 1) W 0等压 理想气体可逆 任意物质 p ∆V=Q p -∆U p ∆V=Q p -∆U⎰21T T p dT C ⎰21T T p dT C ⎰21T T V dT CQ p -W⎰21T T p dT C ⎰21T T p dT C 等容 理想气体 可逆 任意物质0 0 ⎰21T T V dT C⎰21T T V dT C⎰21T T V dT C⎰21T T V dT C ⎰21T T p dT C∆U+V ∆pi.g. 绝热可逆 -∆U= γ--11122V p V p0 ⎰21T T V dT C ⎰21T T p dT C i.g. 多方可逆 δ--11122V p V p∆U+W ⎰21T T V dT C⎰21T T p dT C可逆相变 (等温等压) p e ∆V Q p Q p -W Q p 化学反应 (等温等压)p e ∆VQ pQ p -W= nRTH m r ∆-∆Q p =∑Φ∆iim f i H ,ν例题2 气体由温度T 1变至T 2,吸收热量Q ,不做其他功,试分别考虑下列六项热力学关系在甲、乙、丙、丁四种情况下是否成立? (甲) i.g. 等压过程 (乙) i.g. 等容过程 (丙) r.g. 等压过程 (丁) r.g.等容过程∆U=C V ∆T √ √ ⨯ √ ∆H=C p ∆T √ √ √ ⨯ ∆U=Q V ⨯ √ ⨯ √ ∆H=Q P √ ⨯ √ ⨯ ∆U=Q-W √ √ √ √ ∆H=∆(U+pV) √ √ √ √dV V U dT T U dU T V )()(∂∂+∂∂= i.g. T VU)(∂∂=0,dU=C V dTr.g. dV=0, dU=C V dT例题3 1 mol i.g.从0℃分别经等容和等压加热到100℃,两过程的终态是否相同?∆U 、∆H 、W 、Q 是否相等?(目的:说明i.g.的U 和H 仅是温度的函数,Q 和W 与过程有关)解:T 1=0℃, T 2=100℃等容过程1:dV=0W 1=0 Q 1=∆U 1=C V (T 2-T 1)∆H 1=C p (T 2-T 1)等压过程2:dp=0Q 2=∆H 2=C p (T 2-T 1)∆U 2=C V (T 2-T 1)W 2=Q 2-∆U 2= C p (T 2-T 1)- C V (T 2-T 1)=R(T 2-T 1)=p 2V 2-p 1V 1=∆(pV) 因此,两过程的终态不同。
大学物理 热力学第一定律 习题(附答案)

A13 = Q13 = 1.25 × 10 4 ( J)
(5)由(1)有系统终态的体积为
hi
5 R , R = 8.31 J / mol ⋅ K 。 2
na
T V3 = V2 ( 2 ) γ−1 = 40 × 21. 5 = 113 ( l) T1 nRT3 2 × 8.31 × 300 p3 = = ÷ 1.013 × 10 5 = 0.44 ( atm) −3 V3 113 × 10
0 . 44
O
om
p (atm ) 1 2
3
三、计算题: 1.2 mol 初始温度为 27 � C ,初始体积为 20 L 的氦气,先等压过程膨胀到体积加倍, 然 后绝热过程膨胀回到初始温度。 (1)在 p-V 平面上画出过程图。 (2)在这一过程中系统总吸热是多少? (3)系统内能总的改变是多少? (4)氦气对外界做的总功是多少?其中绝热膨胀过程对外界做功是多少? (5)系统终态的体积是多少?
5 = 1 × R × 60 = 1.25 × 10 3 ( J) 2
γ
(B) p 0 γ (D) p 0 / 2
(γ = C
p
/ Cv )
p0
解:绝热自由膨胀过程中 Q = 0,A = 0,由热力学第一定律,有 ∆ E = 0 ,膨胀前后系统
[
]
(A) (B) (C) (D)
这是一个放热降压过程 这是一个吸热升压过程 这是一个吸热降压过程 这是一个绝热降压过程
将状态 a、b 分别与 o 点相连有
om
A
O
V1
V2
V
T B
C
Q
V
等压过程中吸收了相同的热量,则它们对外做功之比为 A 1: A 2 = (各量下角标 1 表示氢气,2 表示氦气)
大学物理热学习题课

dN m 32 4 ( ) e Ndv 2kT
v2
对于刚性分子自由度 单原子 双原子 多原子
i tr
(1)最概然速率
2kT 2 RT RT vp 1.41 m
(2)平均速率
i=t=3 i = t+r = 3+2 = 5 i = t+r = 3+3 =6
6、能均分定理
8kT 8 RT RT v 1.60 m
M V RT ln 2 M mol V1
QA
绝热过程
PV 常量
M E CV T M mol
(2)由两条等温线和两条绝热线 组成的循环叫做 卡诺循环。 •卡诺热机的效率
Q0
Q2 T2 卡诺 1 1 Q1 T1
M P1V1 P2V2 A CV T M mol 1
E 0
•热机效率
A Q1 Q2
M E CV T M mol M Q C P T M mol
A Q1 Q2 Q2 1 Q1 Q1 Q1
A=P(V2-V1) 等温过程
A
E 0
Q1 Q2 •致冷系数 e W Q1 Q2
热机效率总是小于1的, 而致冷系数e可以大于1。
定压摩尔热容
比热容比
CP ( dQ )P dT i2 i
8、平均碰撞次数 平均自由程
z
2d v n
2
CV •对于理想气体:
Cp
v z
1.热力学第一定律
1 2 2d n
二、热 力 学 基 础
Q ( E2 E1 ) A dQ dE dA
准静态过程的情况下
4. 摩尔数相同的两种理想气体 一种是氦气,一种是氢气,都从 相同的初态开始经等压膨胀为原 来体积的2倍,则两种气体( A ) (A) 对外做功相同,吸收的热量 不同. (B) 对外做功不同,吸收的热量 相同. (C) 对外做功和吸收的热量都不 同. (D) 对外做功和吸收的热量都相 同. A=P(V2-V1)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
p
A
B
理学院 孙秋华
D o
C V
热学部分习题课
解:
1 Q2 1 Q DC
Q1
Q AB
1
M M mol
C p ( TC
TD ) 1 TC
TD
1 TC (1 TD TC )
M M mol
C p ( TB
TA
)
TB TA
TB (1 TA TB )
p
p A 1TA pD 1TD pB 1TB pC 1TC
4.掌握内能、功和热量三者的意义。了解做功和传递热量对系统内能的变化 是等效的,但其本质是有区别的。内能是状态的函数。而做功和传递热量则 与过程有关。
5.从普遍的能量转换和守恒定律掌握热力学第一定律及其理想气体各等值过 程中的应用。会计算循环过程的效率。
6.理解热力学第二定律时,掌握热力学第二定律的微观实质。
自由度
3 5 6
一个分子的平 一个分子的平 一个分子的平
均平动动能 均转动动能
均动能
3/2kT
0
3/2kT
3/2kT 2/2kT 5/2kT
3/2kT 3/2kT 6/2kT
3.热力学第一定律: Q (E2 E1 ) A
理想气体无摩擦的平衡过程 M
(E2 E1 ) M mol CV (T2 T1 )
理学院 孙秋华
分布函数
热学部分习题课
f (v) 4 (
m
)
3
/
2
e
m 2kT
v
2
v
2
2kT
三种速率
vp v v2
2kT m
8kT
m
3kT m
2.能量均分定理:在温度为T 的平衡态下,气体分子每个
自由度的平均动能都相等,其大小等于
1 2
kT
。
理学院 孙秋华
热学部分习题课
气体的种类
单原子 双原子 多原子
2.理想气体的压强和温度
理学院 孙秋华
热学部分习题课
压强:所有分子每秒钟施于单位面积器壁的冲量。
p
1 3
nmv 2
2 3
n k
温度:标志物体内分子无规则运动的剧烈程度。
k
3 kT 2
T
2 3
k
k
3.内能:在一个系统内,所有分子的动能和分子间
相互作用势能的总和称为系统的内能。
4.理想气体的内能:所有分子的动能总和。
效率为A和B。试比较A和B的大小。
p
A2
A1
A3
B2
B1
B3
0
V1
V2
V
理学院 孙秋华
热学部分习题课 解: 先计算A1A2A3A1循环过程的效率
Q A1A2 A1 E1
Q A1A2 Q吸
A1A2A3A1过程的方程
p k1V
A1
V2 V1
k1VdV
1 2
k1
V22
V12
E1 CV T2 T1
理学院 孙秋华
热学部分习题课
解:(1) ∵
v0
1
f (v) dv
Kv 3
dv
Kv
4 0
/4
0
0
∴
K
4
/
v
4 0
v0
(2)
v
vf (v) dv
vKv
3
dv
Kv
5 0
/
5
4v 0 / 5
0
0
(3)
∵
1
v1`
v1
f (v) dv Kv 3 dv
16 0
0
K (v1 )4 4 (v1 )4 (v1 )4
PMmol 1.30kg m-3
RT
(3)氧气分子的平均平动动能
k
3 kT 2
6.211021 J
理学院 孙秋华
热学部分习题课
2.已知某粒子系统中粒子的速率分布函数如下所示
Kv 3 f(v)
0
0 v v0 v v0
求:(1) 比例常数K =? (2) 粒子的平均速率? (3) 速率在0~v1之间的粒子占总粒子数的1 / 16时, v1 =? (答案均以v0表示)
热学部分习题课
致冷系数:
Q2 Q2
A Q1 Q2
11. 熵
SB SA
BdQ AT
二、基本定律和定理
1.麦克斯韦速率分布律:在平衡态下,当气体分子间的相
互作用可以忽略时,分子分布在任一速率区间v~v+dv内
的分子数占总分子数的比率为:
dN 4 (
m
)
3
/
2
e
m 2kT
v
2
v
2
dv
N
2kT
理学院 孙秋华
E
M M mol
CV T
热学部分习题课
5.平均碰撞频 率
6.平均自由程:
z 2nd 2v
kT 2d 2 p
7.定容摩尔热容量 8.定压摩尔热容量 9. 摩尔热容比
i
ห้องสมุดไป่ตู้CV
R 2
C P CV R
CP
CV
10.循环过程:
理学院 孙秋华
热机效率: A Q1 Q2
Q1
Q1
(1) 各过程的功,内能增量和传递的热量;
(用T1 和已知常数表示)
(2) 此循环
P
的效率η.
P2
2
理学院 孙秋华
P1 1
V1
V2
3 V3 V
热学部分习题课
解:对双原子分子,
1 2, p V
cv
5 2
R, c p
7 2
R
A12
1 2
( p1
P2 )(V2
V1 )
1 2
( p2V2
p1V1 )
A =Q1+ Q2 =40 J
Q2 = A-Q1 =40-(-100)=140 J
BED过程中系统从外界吸收140焦耳热.
理学院 孙秋华
热学部分习题课
5. 1mol双原子分子理想气体作如图的可逆循环过程, 其中1–2为直线,2–3为绝热线,3–1为等温线. 已知
= 45, T2 =2T1 , V3 = 8V1 试求:
p
A
理学院 孙秋华
B
V1
V2
V
热学部分习题课 解:由摩尔热容的定义:
dQAB C AB dT (CV R)dT CV dT RdT 由热力学第一定律:
dQAB CV dT PdV PdV RdT
再由: PV RT PdV VdP RdT
2PdV VdP 0
积分:
理学院 孙秋华
V2
A pdV
V1
M
V2
Q
M mol
CV (T2
T1 ) pdV
V1
理学院 孙秋华
热学部分习题课
热力学第一定律对理想气体四个过程的应用
过程
E
A
Q
备注
等容 等压 等温 绝热 直线
M M mol
cv T
M M mol
cv T
0
M M mol cv T
0
p(V2 V1 )
M RT ln V2
1 2
R(T2
T1 )
1 2
RT1
M
5
E12 M mol cv (T2 T1 ) 2 RT1
Q12 E12 A12 3RT1
P
2 3绝热过程
Q23 0
P2
2
E23 A23 M
5
P1 1
M mol cv (T3 T2 ) 2 RT1
V1
V2
理学院 孙秋华
3 V3 V
热学部分习题课
p
D
A
E C
B
V
理学院 孙秋华
热学部分习题课 解:正循环EDCE包围的面积为70 J,表示系统对外作正 功70 J;EABE的面积为30 J,因图中表示为逆循环,故 系统对外作负功,所以整个循环过程系统对外作功为:
A=70+(-30)=40 J 设CEA过程中吸热Q1,BED过程中吸热Q2 ,由热一律,
pA pB , pC pD
理学院 孙秋华
A
B
D o
C V
热学部分习题课
TA TD TB TC
1 TC (1 TD TC ) 1 TC 25%
TB (1 TA TB )
TB
p
A
B
理学院 孙秋华
D o
C
V
热学部分习题课
7. 1mol双原子分子理想气体,经如图A B过程。其摩 尔热容为CAB=CV-R.求:该过程的过程方程。
CV R
p2V2 p1V1
CV k1 R
V22
V12
理学院 孙秋华
热学部分习题课
Q1
k1 2R
V22
V12
R 2CV
A净1
1 2
V2
V1
pA2 p A1
k1 2
V2 V1
2
A1A2A3A1循环过程的效率
A
A净 Q1
k1 2R
V22 V12 R 2CV
热学部分习题课
V2
A pdV
V1
a
a2
p
p
V2
V2
A
pdV
V2
a2 dV
a2(
1
1 )
V1
V1 V 2
V1 V2
pV RT p1V1 RT1 利用p a 2
p2V2 RT2
