药物化学作业-喹诺酮类药物的结构修饰
药物化学作业-喹诺酮类药物的结构修饰

喹诺酮类药物的结构修饰及“非经典”生物活性研究摘要:喹诺酮类药物经过近50年的发展,已成为一大类广泛用于临床的广谱、高效、低毒性的抗感染化疗药物。
作为一类全合成药物,喹诺酮类结构中可供修饰的位点较多,其化学性质稳定,易于合成。
结构修饰不仅是寻找抗菌活性更强的新喹诺酮的重要途径,也成为拓展其“非经典”生物活性的有效手段之一。
10余年来,人们有针对性地设计合成了多个系列的喹诺酮类衍生物,评价了它们的“非经典”生物活性,并对其作用机制进行了初步探索,发现了一些苗头化合物。
值得一提的是,喹诺酮类抗肿瘤候选药物SNS-595和HIV-1整合酶抑制剂埃替拉韦(elvitegravir,JTK-303,CS9137)目前均已进入临床试验阶段。
本文系统综述了近年来喹诺酮类的结构修饰及其抗肿瘤、抗病毒、抗缺血活性方面的研究进展。
关键词:哇诺酮类药物,结钩修饰,抗肿瘤,抗病毒,抗缺血1抗肿瘤活性细菌拓扑异构酶Ⅱ是喹诺酮类抗菌药物的主要作用靶点,该酶是细菌DNA复制、转录和修复所必需的酶。
另一方面,哺乳动物拓扑异构酶Ⅱ则是DNA活性抗肿瘤药物的作用靶点之一。
鉴于细菌拓扑异构酶Ⅱ的DNA合成机制与哺乳动物拓扑异构酶Ⅱ具有一定的相似性,故通过结构修饰应该能够筛选出具有潜在抗肿瘤活性的喹诺酮类候选药物【1】。
基于黄酮乙酸(flavoneaceticacid,FAA)对肿瘤具有独特的作用机制,人们设计合成了多个系列2-苯基-4-喹诺酮类化合物,并评价了其抗肿瘤活性。
体外研究结果表明【2】,代表物la和1b对所试验的大多数人体肿瘤细胞系(表皮性脑膜瘤、骨肉瘤、卵巢瘤、黑色素瘤、成神经胶质细胞瘤、肺和乳腺肿瘤)具有很好的活性。
化合物2对Raji细胞中由肿瘤促进剂12-O-十四酰佛波醇-13-乙酸酯(PTA)诱导产生的EB病毒早期抗原(EBV-EA)的抑制率分别为92% ,69%和29 %。
化合物3对RXF-393肾肿瘤及SKMeI-5黑色素瘤细胞系具有明显的细胞毒活性(log GI50< -8.00),对微管蛋白聚合作用的半数抑制浓度(IC50)值为0.46μmol/L。
喹诺酮类抗菌药分类、构效关系.
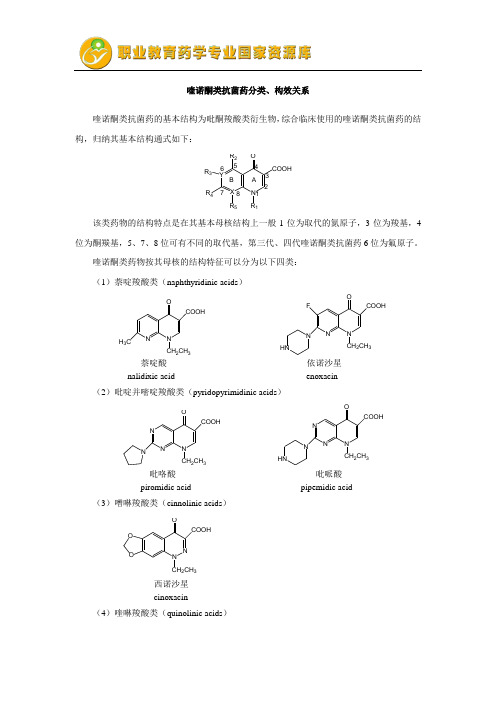
喹诺酮类抗菌药分类、构效关系喹诺酮类抗菌药的基本结构为吡酮羧酸类衍生物,综合临床使用的喹诺酮类抗菌药的结构,归纳其基本结构通式如下:12345678YX N 1COOHR 2R 3R 45O A B该类药物的结构特点是在其基本母核结构上一般1位为取代的氮原子,3位为羧基,4位为酮羰基,5、7、8位可有不同的取代基,第三代、四代喹诺酮类抗菌药6位为氟原子。
喹诺酮类药物按其母核的结构特征可以分为以下四类: (1)萘啶羧酸类(naphthyridinic acids )N N2CH 3H 3CCOOHON N CH 2CH 3NCOOHOFHN萘啶酸 依诺沙星nalidixic acid enoxacin(2)吡啶并嘧啶羧酸类(pyridopyrimidinic acids )N NN 2CH 3COOHONN NN 2CH 3COOHONHN吡咯酸 吡哌酸 piromidic acid pipemidic acid(3)噌啉羧酸类(cinnolinic acids )NN O OCH 2CH 3COOHO西诺沙星 cinoxacin(4)喹啉羧酸类(quinolinic acids )N CH 2CH 3COOHONHNFNOFNHNCOOH诺氟沙星 环丙沙星norfloxacin ciprofloxacinNOCH 3COOHFNN OH 3CNOF COOHOCH 3H NN氧氟沙星 莫西沙星ofloxacin moxifloxacinNOFNHNCOOHF3NH 2H 3CNOFNHNCOOHOCH 33司帕沙星 加替沙星 sparfloxacin gatifloxacin在这四类结构中,喹啉羧酸类药物最多,发展最快。
根据喹诺酮类抗菌药的化学结构和抗菌作用的关系,将该类药物的构效关系总结如下: 1.吡啶酮酸的A 环是抗菌作用的基本药效基团,变化较小,其中3位-COOH 和4位C=O 是抗菌活性必需基团,若被其他取代基取代则活性消失。
大学药物化学考试练习题及答案441

大学药物化学考试练习题及答案41.[单选题]先导化合物是指A)新化合物B)不具有生物活性的化合物C)具有某种生物活性,可作为进行结构修饰或改造的模型,进一步优化得到供临床应用的药物D)理想的临床药物答案:C解析:2.[单选题]a1-受体拮抗剂是( )。
A)盐酸哌唑嗪B)麻黄碱C)去甲肾上腺素D)普萘洛尔答案:A解析:3.[单选题]甾体激素药的基本结构是A)环戊烷并多氢菲B)环己烷并多氢菲C)氢化并四苯D)异喹啉答案:A解析:4.[单选题]较易发生水解反应的药物是A)肾上腺素B)普鲁卡因C)维生素AD)布洛芬答案:B解析:5.[单选题]具有以下结构的化合物,与其药物临床用途相似的是A)顺铂B)青霉素C)氯丙嗪D)地西泮6.[单选题]下列关于氧化还原反应的特点错误的是 ( )A)反应速度较快B)副反应较多C)反应比较复杂D)反应条件对反应速度影响大答案:A解析:7.[单选题]吗啡的3-OH甲基化后得到A)海洛因B)烯丙吗啡C)可待因D)纳洛酮答案:C解析:8.[单选题]解热镇痛药主要用于( )。
A)内脏痉挛绞痛B)创伤性锐痛C)癌症晚期剧痛D)慢性钝痛答案:D解析:9.[单选题]青霉素的结构特点不包括A)含有B-内酰胺环B)结构稳定,不易开环C)含有羧基D)含有酰胺侧链答案:B解析:10.[单选题]利用酸效应系数可选择单独滴定金属离子时的pH值为( )A)最适浓度B)最低pH值C)pH突跃范围D)最高pH值答案:B解析:B)降低C)不变D)与金属离子价态有关答案:B解析:12.[单选题]巴比妥类钠盐水溶液与空气中哪种气体接触发生沉淀A)氧气B)二氧化碳C)氮气D)一氧化碳答案:B解析:13.[单选题]( )间接法配制0.10mol/L HCl溶液时,量取HCl的最合适的量器是A)容量瓶B)量筒C)滴定管D)移液管答案:B解析:14.[单选题]普鲁卡因属于哪种结构类型A)酰胺类B)氨基酮类C)芳酸酯类D)氨基甲酸酯类答案:C解析:15.[单选题]实验操作中,当用0.1mol/L HCl滴定0.1mol/L NaOH时,我们选用的指示剂是( )A)甲基橙B)酚酞C)甲基红D)结晶紫答案:A解析:16.[单选题]精密称取某样品0.5g,其称量范围是( )C)0.450~0.550gD)0.4500~0.5500g答案:D解析:17.[单选题]EDTA水溶液中,溶液酸度越低,EDTA的配位能力( )A)越强B)越弱C)无法确定D)不受影响答案:A解析:18.[单选题]用EDTA滴定Mg2+时,采用铬黑T为指示剂,溶液中少量Fe3+的存在将导致( )A)在化学计量点前指示剂即开始游离出来,使终点提前B)使EDTA与指示剂作用缓慢,终点延长C)终点颜色变化不明显,无法确定终点D)与指示剂形成沉淀,使其失去作用答案:C解析:19.[单选题]下列能与2.4二硝基苯肼反应生成踪的药物是A)硝苯地平B)胺碘酮C)普萘洛尔D)美西律答案:B解析:20.[单选题]关于吲哚美辛描述错误的是A)属于吲哚乙酸类非甾体抗炎药B)酰氨键可水解,(在干燥空气中稳定,水溶液可被强酸,强碱水解,)水解产物不易被氧化成有色物质。
药物化学-喹诺酮类抗菌药

氯喹(先导化合物)
Cl N
O
O
N
O
O OH
O O
O
OH
N
OH O
H3C
N
N CH3
N
N CH3
N
N
CH3
萘啶酸1962
吡咯酸
西诺沙星
第二代 喹诺酮类抗菌药物
吡哌酸,1974年上市,7位引入哌嗪基, 使抗革兰氏阴性菌活性增加;耐药性降低, 对萘啶酸和吡咯酸耐药菌株也有抑制作用, 但随着第三代喹诺酮类抗菌药物的出现, 它目前也已被淘汰
6
5
4 3
7 8
1
2
诺氟沙星是第一个上市的氟喹诺酮类药物,基本 上为喹啉羧酸类,其它氟喹诺酮类主要改造部位在 1位、5位或8位,也可以在7位上进行较小的改变。
第四代喹诺酮类药物
第四代喹诺酮类药物在抗菌活性、药动 学性质及半衰期上有明显提高,增加 对厌氧菌的抗菌活性是第四代的重要 特征。代表药物有莫西沙星、加替沙 星等。
喹诺酮类药物能否影响人体DNA复制?
由于哺乳动物细胞中不含螺旋酶
和拓扑异构酶Ⅳ,而是通过其它途径 进行DNA的复制,故喹诺酮类对细菌
的选择性高,而对人体的不良反应少。
细菌的耐药性
细胞膜对药物的通透性降低 细菌DNA螺旋酶结构改变 细菌产生药泵
喹诺酮类药物分类(根据结构)
萘啶(氮杂萘核)羧酸类
H 3C
Pefloxacin 培氟沙星
NH 2 O F N F CH 3 N COOH
HN
Rufloxacin
氟罗沙星 Fleroxacin
司帕沙星 Sparfloxacin
结构特点
O O
F
OH HN N N
喹诺酮类结构

喹诺酮类结构一、介绍喹诺酮类药物是一种广泛应用于临床的抗菌药物,具有广谱抗菌活性和良好的药代动力学特性。
喹诺酮类结构是一类以喹啉-4-酮环为基础结构的有机分子。
喹诺酮类药物主要通过抑制革兰氏阴性菌的DNA合成酶DNA类II型酶,从而抑制细菌的DNA复制和转录过程,进而导致细菌的生长和繁殖受到干扰。
本文将详细介绍喹诺酮类结构的特征及其与抗菌活性的关系。
二、结构特征2.1 喹啉-4-酮环喹诺酮类药物的基本结构是喹啉-4-酮环,该环具有六个碳原子和一个氧原子。
2.2 扩展环结构喹诺酮类药物还常常在喹啉-4-酮环上引入其他扩展环结构,如环氧、取代基和取代环等。
2.3 戊二酰肼基喹诺酮类药物的另一个重要结构特征是戊二酰肼基,该基团与DNA类II型酶的结合起到了关键作用。
三、喹诺酮类药物的分类3.1 Ⅰ代喹诺酮类药物Ⅰ代喹诺酮类药物包括氧氟沙星、环丙沙星等。
这一代药物的抗菌活性主要针对革兰氏阴性菌。
3.2 Ⅱ代喹诺酮类药物Ⅱ代喹诺酮类药物包括诺氟沙星、左氧氟沙星等。
这一代药物在抗菌活性上相对于Ⅰ代药物有所提高,同时具有更好的药代动力学特性。
3.3 Ⅲ代喹诺酮类药物Ⅲ代喹诺酮类药物包括莫西沙星、加替沙星等。
这一代药物在抗菌活性和耐药性方面都有显著的改进。
四、喹诺酮类药物的抗菌作用机制1.DNA合成酶抑制:喹诺酮类药物与DNA类II型酶结合,使酶的活性受到阻碍,进而抑制细菌的DNA合成。
2.DNA复制的阻断:喹诺酮类药物与DNA双螺旋结构结合,阻止DNA复制过程的进行。
3.转录的抑制:喹诺酮类药物干扰细菌的RNA聚合酶活性,抑制细菌的转录过程。
五、喹诺酮类药物的临床应用5.1 呼吸系统感染喹诺酮类药物对呼吸系统感染的多种病原菌具有良好的抗菌活性,可用于治疗肺炎、支气管炎等疾病。
5.2 泌尿系统感染喹诺酮类药物对泌尿系统感染的致病菌有很好的抗菌效果,可用于治疗尿路感染、前列腺炎等疾病。
5.3 消化系统感染喹诺酮类药物可以有效地治疗胃肠道感染,如伤寒、副伤寒等疾病。
(完整版)药物化学期末试题含答案

药物化学期末试题含答案1.环丙沙星的临床用途是:治疗呼吸道感染.2.环磷酰胺属于氮芥类烷化剂,甲氨蝶呤是叶酸类拮抗剂。
3、当分子结构中引入极性大的羧基、羟基、氨基时,则药物的水溶性增大,脂水分配系数减小.4在磺胺类药物分子中芳伯氨基与磺酰胺基在苯环上必须处于对位,在喹诺酮类药物分子中的6位引入氟原子可大大增加抗菌活性。
6、药物的分配系数P药物对油相及水相相对亲和力的度量7、药物进入体内到产生药效,要经历药剂相、药物动力相、药效相三个重要相。
8、顺铂的化学名全称为顺式二氨基二氯络铂,临床主要用作癌症治疗药.9、药物按作用方式可分为两大类结构非特异性药和结构特异性药。
10、药物和受体的相互作用方式有两种即构象诱导和构象选择。
11、药物在体内的解离度取决于药物的pKa和吸收部位的pH。
12、头孢菌素与青霉素相比特点为过敏反应少、抗菌活性及稳定性高。
13、含氮药物的氧化代谢主要发生在两个部位:一是在和氮原子相连的碳原子上发生N—脱烷基化和脱氮反应,另一是N-氧化反应。
14、药物分子设计大体可分为两个阶段,即先导化合物的产生和先导化合物的优化.15、组胺受体主要有H1受体和H2受体两种亚型,H1受体拮抗剂临床用作抗过敏药,H2受体拮抗剂临床用作抗溃疡药。
16、青蒿素是我国学者子黄花蒿中分离出的具有强效抗疟作用的药物,其分子中的过氧键是必要的药效团.1。
通过I相代谢可使药物分子引入或暴露出(B)A.羟基、卤素、巯基B.巯基、羟基、羧基C.羟基、硝基、氰基D.烃基、氨基、巯基2.具有二氢吡啶衍生物结构的抗心绞痛药是(A)A。
硝苯地平B。
硝酸异山梨酯C。
吉非罗齐D。
利血平3.下列关于青蒿素的叙述错误的一项是(B)A。
体内代谢较快B。
易溶于水C.抗疟活性比蒿甲醚低D。
对脑疟有效4.下列对脂水分配系数的叙述正确的是(C)A。
药物脂水分配系数越大,活性越高B.药物脂水分配系数越小,活性越高C.脂水分配系数在一定范围内,药效最好D。
三种喹诺酮药物结构修饰后体外抗菌活性的变化
测定结果见表3 。
表3样 品含 量 测 定结 果
Ma 0 2 Vo . 0 No 1 y2 1 , 1 , .3 1
只需要在 同一批测定供 试品溶液和对照 品溶 液 中保 持相对的稳定 ( 峰 面积和保 留时间的变化 仅是由于进样量 不准确 、仪器 波动等偶然 因素 引起 的,不包括参 比成分 不稳定等 引起 的变化 )即可 ,而不必要在所 有的样 品中均保持 稳定。经过一定 的试 验设计 ,甚 至还可 以选取 不同 的待测成分 ( 即已知成分 )色谱峰相互作为参 比峰 。
A A C 0M核磁共振 谱仪 ( 国Bue公 司) 、A A A 30 V N E4 0 德 rkr V T R 6 傅立 叶变 换红外光谱仪 ( 美国Nel 公司)、Eqi C i e ot su eL 液相 色谱. r 质
文献标 识码 :B
文章编 号 :1 7- 14 (0 2 3 09 - 2 6 1 89 2 1 )1- 00 0
[】 王静华 , 宏伟 . 定量 气相 色谱 法 测定 吹苯残 渣 中的三 苯含 3 王 叠加
量 [ . 学工 程师 , 9 , 6) 45 . J化 ] 1 7 (0: —5 9 3 5
[ 孙 国 祥, 菊 茹, , . 细 管 电泳 叠加 对 比法 测定 阿 片粉 中 4 】 苗 王宇 等 毛
根 据参 比峰 的选择原则 ,一般可 以在进 样多次后选 取与待测成分
【】 孙 国祥, 6 邓湘昱, 万月生, 毛细管电泳叠加对 比法的误差分析 等.
[ . 药学,04 () 6 -6. J 中南 】 2 0 , 5: 62 8 2 2
色谱峰的保 留时间和峰面积相近且稳定的色谱峰作为参比峰。参比峰
喹诺酮
1 品种及作用喹诺酮类药物化学结构构效关系:1、喹诺酮母核的3位均有羧酸基,6位引入氟原子可增强抗菌作用并对金葡菌有抗菌活性。
2、7位引进哌嗪环可提高对金葡菌及绿脓杆菌的抗菌作用(如诺氟沙星),哌嗪环被甲基哌嗪环取代(如培氟沙星),则脂溶性增加,肠道吸收增强,细胞的穿透性提高,半衰期延长。
3、在8位引进第二个氟原子,可进一步提高肠道吸收,延长半衰期(如洛美沙星等)。
4、N-1修饰以环丙基团(环丙沙星)或噁嗪基团(氧氟沙星)可扩大抗菌谱,增强对衣原体、支原体及分支杆菌(结核杆菌与麻风杆菌等)的抗菌活性,噁嗪环还可提高水溶性,使药物在体内不被代谢,以原形经尿排泄。
分代及特点:第一代 萘啶酸、 吡哌酸对G -杆菌作用强,仅适用于尿路、肠道感染第二代 诺氟沙星、氧氟沙星、环丙沙星对G -菌作用强,体内较稳定,毒性降低,可用于各系统感染第三代 左氧氟沙星 、依诺沙星、氟罗沙星、洛美沙星、司帕沙星、格帕沙星在二代基础上增加了对G +球菌、衣原体、支原体、军团菌和结核杆菌的作用,安全性高,半衰期长第四代 莫西沙星、加替沙星 、克林沙星在三代基础上增加了对抗G +球菌的活性,增加了对厌氧菌的抗菌活性 抗菌作用:1、喹诺酮类药物对肠杆菌科细菌具有强大的抗菌作用,以环丙沙星为最高,左氧氟沙星和氧氟沙星次之;对不动杆菌和铜绿假单胞菌的抗菌作用较肠杆菌科细菌差;流感嗜血杆菌呈高度敏感,奈瑟氏菌属多呈敏感。
X N O OH O F R7R1R2R5R82、喹诺酮类药物对G+球菌亦具有抗菌作用,但其抗菌作用明显较肠杆菌科细菌低,以左氧氟沙星相对最高,环丙沙星和氧氟沙星略低;仅对金黄色葡萄球菌(除甲氧西林耐药外)具抗菌活性。
3、对衣原体、支原体、军团菌和结核分支杆菌及其他分支杆菌具有一定作用。
药动学特性:1、多数品种口服吸收良好,血药浓度相对较高。
2、半衰期较长,多在3-7h。
3、蛋白结合率低,大多为14%-30%。
4、体内分布广泛,组织和体内浓度常高于或等于血药浓度,可达有效治疗水平。
药物化学的构效关系
H N
O O
O O NO2
为活性必需,变 成吡啶环或六氢 吡啶环活性消失
为活性必需,若为乙酰 基或氰基活性降低,若 为硝基则激活钙通道
邻、间位有吸电子基团时活 性较佳,对位取代活性下降
Penicillins青霉素的构效关系
6位侧链是结构修饰 的主要部位,能产 生各式各样的作用
C-7应为L-构型,而酰胺侧链为 b-构型,C-6、C-7的氢为-构 型,绝对构型为6R,7R C-7为同向(Syn-)肟型或较大的取 代基侧链时,对b-内酰胺酶有较 大稳定性,C-7对向构(Anyi-)型时 则不耐酶
四元环与六元环不在同一 平面,在C-6-N-1处折合
R NH
H
S
O NH
O OH
若以氧原子或亚甲基取 代,不降低活性而得到 另一类型b内酰胺抗生素
b受体阻滞剂(普萘洛尔)结构与活性关系
用S,CH2或NCH3取代, 作用降低
可以是苯、萘、杂环、稠环 和脂肪性不饱和杂环等,可 有甲基、氯、甲氧基、硝基 等取代基,2,4-或2,3,6-同 时取代时活性最佳
S构型异构体活性强, R构型异构体活性降低 或消失
O
N H
CH3 CH3
H OH
以叔丁基和异丙基取代活性最高,
维生素A的构效关系
被甲基、氯原子或含氮 杂环取代,活性增强或 OAc 改变体内药代动力学
双键移位则无活性
磺胺类药物的构效关系
其它芳环或引入其它 基团,活性降低或丧失
H2N
OO SNR H
单取代活性增加,杂环取 代更好,双取代活性丧失
以其它基团取代或置换 可保持或丧失活性,氨 基的游离或潜在的游离 状态是活性的关键
药物化学期考简答题
药物化学期考简答题1、烷化剂:在体内能形成缺电⼦活泼中间体或其它具有活泼的亲电性基团的化合物,进⽽与⽣物⼤分⼦中含有丰富电⼦的基团(如氨基、巯基、羟基、羧基、磷酸基等),发⽣共价结合,使其丧失活性或者使DNA分⼦发⽣断裂。
2、前药:如果药物经过化学结构修饰后得到的化合物,在体外没有或很少有活性在⽣物体或⼈体内通过酶的作⽤⼜转化为原来的药物⽽发挥药效时,称原来的药物为母体药物,修饰后得到的化合物为前体药物,简称前药。
3、常见的药物作⽤靶点有哪些?答:酶、受体、离⼦通道、核酸4、代谢拮抗:与⽣物体内基本代谢物的结构有某种程度相似的化合物,使与基本代谢物竞争性或⼲扰基本代谢物的被利⽤,或掺与⽣物⼤分⼦的合成之中形成伪⽣物⼤分⼦,导致致死合成,从⽽影响细胞的⽣长。
5、抗⽣素:是某些细菌、放线菌、真菌等微⽣物的次级代谢产物,或⽤化学⽅法合成的相同结构或结构修饰物,在低浓度下对各种病原性微⽣物或肿瘤细胞有选择性杀灭、抑制作⽤的药物。
6、软药:容易代谢失活的药物,使药物在完成治疗作⽤后,按预先规定的代谢途径和可以控制的速率分解、失活并迅速排出体外7、简述芳基丙酸⾮甾体抗炎药的构效关系。
答:①、含有芳⾹环或芳杂环的平⾯结构及⼀个羧基或相当于羧基的结构;②、羧基与平坦的芳环间隔⼀个碳原⼦,且在此碳原⼦上连有甲基,限制了单键的旋转,使其构象更适合与受体作⽤,活性增强;③、芳环可在对位或间位引⼊芳基、烷基、环⼰基等疏⽔基团,活性增强;④、芳环上有⼀个或多个亲脂性基团,间位-F, -Cl等吸电⼦基也有利于活性提⾼。
⑤、羧基α-位是⼿性碳,S异构体活性好于R构型,但临床使⽤外消旋体。
8、先导化合物的发现途径有哪些?答:主要有四个途径①.从天然资源得到先导化合物②.以现有的药物作为先导化合物:由药物的副作⽤发现先导化合物、通过药物代谢研究得到先导化合物、以现有突破性药物作为先导化合物: “ Me-too”③.⽤活性内源性物质作先导化合物:合理药物设计④.利⽤组合化学和⾼通量筛选得到先导化合物9、简述1,4-⼆氢吡啶钙通道阻滞剂的构效关系。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
喹诺酮类药物的结构修饰及“非经典”生物活性研究摘要:喹诺酮类药物经过近50年的发展,已成为一大类广泛用于临床的广谱、高效、低毒性的抗感染化疗药物。
作为一类全合成药物,喹诺酮类结构中可供修饰的位点较多,其化学性质稳定,易于合成。
结构修饰不仅是寻找抗菌活性更强的新喹诺酮的重要途径,也成为拓展其“非经典”生物活性的有效手段之一。
10余年来,人们有针对性地设计合成了多个系列的喹诺酮类衍生物,评价了它们的“非经典”生物活性,并对其作用机制进行了初步探索,发现了一些苗头化合物。
值得一提的是,喹诺酮类抗肿瘤候选药物SNS-595和HIV-1整合酶抑制剂埃替拉韦(elvitegravir,JTK-303,CS9137)目前均已进入临床试验阶段。
本文系统综述了近年来喹诺酮类的结构修饰及其抗肿瘤、抗病毒、抗缺血活性方面的研究进展。
关键词:哇诺酮类药物,结钩修饰,抗肿瘤,抗病毒,抗缺血1抗肿瘤活性细菌拓扑异构酶Ⅱ是喹诺酮类抗菌药物的主要作用靶点,该酶是细菌DNA复制、转录和修复所必需的酶。
另一方面,哺乳动物拓扑异构酶Ⅱ则是DNA活性抗肿瘤药物的作用靶点之一。
鉴于细菌拓扑异构酶Ⅱ的DNA合成机制与哺乳动物拓扑异构酶Ⅱ具有一定的相似性,故通过结构修饰应该能够筛选出具有潜在抗肿瘤活性的喹诺酮类候选药物【1】。
基于黄酮乙酸(flavoneaceticacid,FAA)对肿瘤具有独特的作用机制,人们设计合成了多个系列2-苯基-4-喹诺酮类化合物,并评价了其抗肿瘤活性。
体外研究结果表明【2】,代表物la和1b对所试验的大多数人体肿瘤细胞系(表皮性脑膜瘤、骨肉瘤、卵巢瘤、黑色素瘤、成神经胶质细胞瘤、肺和乳腺肿瘤)具有很好的活性。
化合物2对Raji细胞中由肿瘤促进剂12-O-十四酰佛波醇-13-乙酸酯(PTA)诱导产生的EB病毒早期抗原(EBV-EA)的抑制率分别为92% ,69%和29 %。
化合物3对RXF-393肾肿瘤及SKMeI-5黑色素瘤细胞系具有明显的细胞毒活性(log GI50< -8.00),对微管蛋白聚合作用的半数抑制浓度(IC50)值为0.46μmol/L。
Clement等【3】研究发现,喹琳并苯并噁嗪类化合物4(A-83669)的原缬氨酸前药(5,A-84441)对小鼠及人体肿瘤的活性与其母体化合物4相当, IC50值分别为0.03~0.49和0.02~0.25mg/L。
进一步研究发现,化合物4中的3-氨基吡咯烷基的立体结构对拓扑异构酶Ⅱ的抑制活性具有一定的影响,如S-异构体的活性优于对应的R-异构体。
Tomita等【4】设计合成了一系列7-取代-1,4-二氢-4-氧代-1-(2-噻唑基)-1,8-萘啶-3-羧酸类化合物,抗肿瘤活性研究结果表明,其中化合物6a~6c(6c为S,S-异构体)的体内外抗肿瘤活性与某些抗癌药物(如依托泊苷和多柔比星)相当,三者对小鼠P388白血病细胞系的IC50值分别为0.021,0.026和0.023mg/L。
Tsuzuki等进一步合成了一系列6-去氟-1,8-萘啶酮类化合物,活性比较结果表明,6-去氟-1,8-萘啶酮类化合物的细胞毒活性是相应的6-氟类似物的2倍,其中代表物SNS-595(S,S-异构体)对人体肿瘤细胞系的细胞毒活性(IC50值为7.5μg/L,是其R,R-异构体的2.8倍,该化合物目前已进人Ⅱ期临床试验阶段。
2抗病毒活性2.1抗单纯疱疹单纯疱疹Ⅰ型病毒(HSV-1)是引起口腔和面部损伤的主要病原体。
随着抗病毒药物的广泛使用,病毒的耐药性逐年增加,如HSV-1(免疫低下患者)可能对临床常用的口服或局部用抗病毒药阿昔洛韦(acyclovir, ACV)产生耐药性,故尽快研发可有效对付耐药病毒的新型抗病毒药物势在必行。
Lucero等【5】基于ACV的结构,向喹诺酮N1-位引人2-羟乙氧甲基,合成了一系列N-(2-羟乙氧甲基)-4(1H)喹诺酮-3-羧酸酯,并评价和比较了其抗HSV-1活性及细胞毒性。
结果表明,这些ACV类似物对HSV-1普遍具有明确的抑制作用和极低的细胞毒性,其中羧酸酸的活性优于相应的羧酸酷。
此外,6-位和(或)7-位取代基对HSV-1抑制活性的贡献似乎大于3-位取代基。
化合物9d和9c对HSV-1的EC50值分别为0.7和0.8μmol/L,而ACV为1.09μmol/L,优于对照药ACV,且均未显示细胞毒性,二者的选择性指数(SI分别为1714和1562)也明显大于ACV(SI为880)。
这类化合物的抗HSV-1作用机制目前正在深人研究中。
2.2抗HIV-1活性早在1996年,Cecchetti等通过对包括氟喹诺酮和非氟喹诺酮类在内的各种喹诺酮类化合物进行随机筛选,发现6-氨基-1-叔丁基-7-[4-(2-吡啶基)-1-哌嗪基]-4-氧代-1,4-二氢-3-喹啉羧酸具有良好的抗HIV-1活性。
为了进一步明确其抗病毒活性的结构特征,人们对该化合物进行了多种结构修饰,设计合成了各种系列的6-氨基喹诺酮衍生物,并对其抗病毒活性进行了初步评价。
微生物学研究结果显示,这类化合物对HIV具有完全不同于已知抗HIV药物的作用机制,其中活性最强的化合物WMS对C8166人体成淋巴细胞中的HIV-1复制具有抑制作用。
构效关系初步研究结果表明,6-氨基喹诺酮抗病毒活性的决定因素包括3-位羧基、6-位连接极性小基团、7-位连接大取代基以及N-连接小取代基。
Cecchetti等[6]以WMS为先导物,进一步合成了6-氨基、6-氢,6-甲氧基、6-羟基和6-三氟甲基等5个系列的1-甲基喹诺酮类衍生物。
体外活性评价结果显示,若干代表物表现出很强的抗HIV-1活性。
其中,6-三氟甲基系列化合物虽抗HIV活性良好,但有明显的细胞毒性而没有研究价值外,其余4个系列中的代表化合物既具有良好的抗HIV活性同时也表现出较低的细胞毒性。
对6-氢系列中的代表物11a(HM12)和11b(HM13)的进一步评价结果显示,二者不但对急、慢性HIV-1感染细胞活性明显,而且对小鼠潜伏期HIV-1感染也表现出良好的体内活性。
3 抗缺血活性在缺氧条件下,缺血性细胞损伤常导致终生残疾甚至死亡,及时服用溶栓药使缺血器官重新恢复血流是目前临床上治疗这类疾病的唯一疗法。
然而,该方案存在种种局限,如限于在缺血发作后3h内实施,且不适于所有患者(因缺血发作时患者可能发生颅内出血症状)。
此外,在再灌注期间,处于氧化应激环境中的细胞常常遭到损害,并导致缺血组织的进一步损害。
因此,寻找具有不同作用模式的新型抗缺血药物就成为近年来该领域研究的热点之一。
环丙沙星具有良好的体内外抗缺血活性。
而其N-环丙基、2-位氢,3-位羧基、4-位羰基、6-位氟和7-位哌嗪基均为环丙沙星具有优秀广谱抗菌(尤其是革兰阴性菌)活性所必需。
基于对环丙沙星抗缺血活性必需结构片段的确证,同时尽可能去除其抗菌活性以改善抗缺血活性的设计理念,Park等【7】对环丙沙星的不同位置取代基进行去除或修饰,设计并合成了一系列环丙沙星类似物。
体外抗缺血活性(SHSYSY细胞系)初步评价结果显示,环丙沙星脱羧物(15,SQ-4002)和6-去氟类似物(16,SQ-4004)组中体外抗菌活性显著降低,大鼠MCAO模型体内抗缺血活性的进一步评价结果表明,缺血前腹膜内给予13(0.01mg/kg),大鼠的脑梗死范围与安慰剂组相比减小32.1%,是相同浓度环丙沙星组的1.7倍。
大鼠心肌梗死(MI)模型心肌保护作用评价结果显示,13(0.01mg/kg)组大鼠的心肌梗死范围减小26.6%。
对MI模型的进一步组织病理学检测结果显示,大鼠心肌组织的细胞凋亡率明显低于安慰剂组。
总之,13具有明确的体内外抗缺血活性,可能在缺血性细胞损伤(包括缺血性脑中风和缺血性心脏病)领域大有作为。
6结语喹诺酮类是目前临床广泛使用的一类广谱、高效、低毒的一线抗感染化疗药物,主要用于治疗由细菌引起的胃肠道、泌尿道和呼吸道等感染。
近年来,人们通过结构修饰除了寻找新的活性更强、不良反应更小的新喹诺酮类抗菌药物外,积极拓展这类化合物“非经典”生物活性的研究,并在抗肿瘤、抗病毒、抗缺血活性等研究领域取得了长足进展,尤其是抗肿瘤候选物SNS-595。
据此,有理由相信,除抗菌作用外,喹诺酮类药物在抗肿瘤、抗病毒等“非经典”领域可能会大有作为,为人类健康做出更大的贡献。
【8】参考文献:【1】冯连顺,刘明亮,郭慧兀细菌拓扑异构酶抑制剂研究进展[J]国外医药——抗生素分册,2009, 30 (1):13-18【2】Xia Y, Y ang ZY, Xia P, et al. Antitumor agents. Part 226: synthesis and cytotoxicity of 2-phenyl-4-quinolone acetic acids and their esters [J] . Bioorg Med Chem Lett, 2003,13 (17):2891-2893【3】Clement JJ, Burres N, Jarvis K, et al. Biological characterization of a novel antitumor quinolone [J] . Cancer Res, 1995,55 (4):830-835【4】Tomita K, Tsuzuki Y,Shibamori K, et al. Synthesis and structure-activity relationships of novel 7-substituted 1,4-dihydro-4-oxo-1-(2-thiazolyl))-1,8-naphthyridine-3-carboxylic acids as antitumor agents. Part 1 [J] . J Med Chem, 2002,45 (25):5564-5575【5】BA Lucero, Claudia Regina B. Gomes. Synthesis and anti-HSV-1 activity of quinolonic acyclovir analogues. Bioorganic & Medicinal Chemistry Letters. V olume 16, Issue 4, 15 February 2006, Pages 1010-1013【6】Violetta Cecchetti, Cristina Parolin, et al. 6-Aminoquinolones as New Potential Anti-HIV agents. J. Med. Chem., 2000, 43 (20), pp 3799–3802【7】TH Park, H Moon, et al. United States Patent Kim et al. US005498615A [ii] Patent Number: [45] Date of Patent: 5,498,615 Mar. 12, 1996【8】冯连顺,刘明亮,哇诺酮类药物的结构修饰及“非经典”生物活性研究进展。
