环己烷的构象.
环己烷的四种典型构象

环己烷的四种典型构象
环己烷是一种环烷烃,分子式为C6H12,由六个碳原子和十二个氢原子组成。
环己烷具有一个六元环的结构,有许多构象。
其中,四种典型的构象为:
1.船形构象:又称弯曲构象,分子呈现出一个V形的结构,两个碳原子之间的距离较近。
船形构象是环己烷的最不稳定的构象,因为分子内部的张力很大。
2.椅形构象:分子呈现出一个六边形的结构,相邻的两个碳原子之间呈现出一个六角星的形状,分子结构较为稳定。
3.锥形构象:分子呈现出一个尖锥形结构,相邻的两个碳原子之间的距离较远。
锥形构象是一种高能量状态的构象,只在极短的时间内存在。
4.扭曲椅形构象:又称为扭曲构象,分子呈现出一个六边形的结构,其中两个对称的碳原子上的氢原子以对称轴为对称对调位置。
这种构象是中等稳定的,可以保持一段时间。
以上四种典型的构象在环己烷分子中不停地交替出现,其中椅形构象是最稳定的构象,可以用来描述环己烷的大部分化学反应。
环已烷及其衍生物的构象
A
4
65
10
3
2
4
8
1B
9 A
10
6
7
5
A环和B环有两个取代基产生一个邻交叉,C1-C9对A环产生二个 1,3-二直立键,C5-C10对B环产生二个1,3-二直立键,其中有两个重 合,所以实际上有三个1,3-二直立键。
反十氢萘: H ≡
H
反式中A、B环都有两个取代基产生一个邻交叉。 顺式比反式能量高11.4KJ/mol。
扭船式构象:所有扭转角都是30°,三个全重叠,三个邻
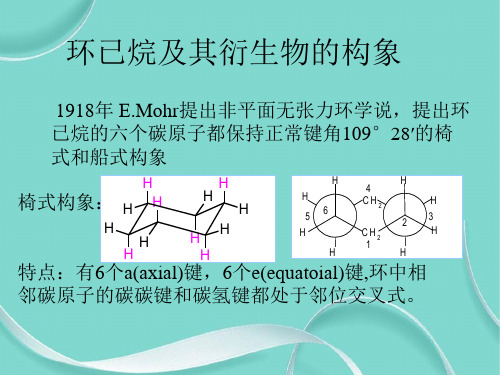
已烷的六个碳原子都保持正常键角109°28′的椅
二个1,3-二直立键
二个1,3-二直立键
邻碳原子的碳碳键和碳氢键都处于邻位交叉式。
顺1,2-二甲基环已烷:
萘
十氢萘
二环[4.
合,所以实际上有三个1,3-二直立键。
Mohr提出非平面无张力环学说,提出环
CH3
H3C
四个1,3-二直立键 二个甲基对位交叉
C H 3 C H 3
两个甲基为邻交叉 二个1,3-二直立键
CH3 CH3
0 一个邻交叉
81
7
9
2
6 5 10 4 3
萘
81
7
9
2
6 5 10 4 3
十氢萘
9 10 1 2 3
8
6
4
75
二环[4.4.0]癸烷(学名)
顺十氢萘:
H
≡
H
1
7
8 9B 3
邻碳原子的碳碳键和碳氢键都处于邻位交叉式。
C2、3、5、6在同一个平面
四个1,3-二直立键
0
在室温下环已烷的一种椅式构象通过σ键旋转迅速转
有机3-环烷烃(2)-(1)_图文

cis-1, 4-二叔丁基环己烷的构象
有较大的1, 3-竖键作用
扭船型构象
多取代环己烷: (1)环己烷多元取代物的最稳定的构象是e-取代最
多的构象; (2)环上有不同取代基是,大的取代基在e-键的构
象最稳定。
课堂练习:
1、画出1,1-二甲基环己烷的椅式构象,指出直立位甲基和平 伏位甲基。
1. 【解析】
椅式构像:① 所有两个相邻的碳原子的碳氢键都处于 交叉式位置;
② 所有环上氢原子间距离都相距较远,无 非键张力。
船式构像:① C2-C3及C5-C6间的碳氢键处于重叠式位 置;
② 船头和船尾上的两个碳氢键向内伸展,相 距较近,比较拥挤,存在非键张力。
环己烷碳架是折叠的
椅式构象
C2, C3, C5, C6 共平面
a, e-
能量相等
e, a-
cis-1, 4-二甲基环己烷
1, 4-cis
a, e-
e, a-
能量相等
trans-1, 4-二甲基环己烷
1, 4-trans
a, a有1. 3-竖键作用
e, e优势构象
不同基团二取代环己烷
1, 2-cis
大基团总是 占据 e键
1, 3-竖键作用较大
优势构象
扭曲式构象
各种环己烷构象的势能图
2. 单取代环己烷的构象分析
甲基环己烷的构象
1,3-竖键作用
CH3与C3为对位交叉 优势构象,室温时占95%
CH3与C3为邻位交叉
取代环己烷的构象1
叔丁基环己烷的构象
优势构象 室温:100%
1. 3-竖键作用非常大
3. 二取代环己烷的构象分析
cis-1, 2-二甲基环己烷
环己烷的四种典型构象

环己烷的四种典型构象
环己烷是一种六元环烷烃,由于其分子中含有六个碳原子,因此存在着多种构象。
在环己烷的分子中,碳原子的空间排列方式不同,导致了不同的构象。
下面将介绍环己烷的四种典型构象。
1. 椅式构象
椅式构象是环己烷最稳定的构象之一。
在椅式构象中,环己烷分子呈现出一个类似于椅子的形状,其中六个碳原子分别位于椅子的底部和顶部。
在椅式构象中,每个碳原子都与两个相邻的碳原子形成了一个平面三角形,这种排列方式使得环己烷分子的键角最大化,从而使得分子更加稳定。
2. 船式构象
船式构象是环己烷的另一种稳定构象。
在船式构象中,环己烷分子呈现出一个类似于船的形状,其中两个碳原子位于船的底部,其余四个碳原子位于船的两侧。
在船式构象中,两个底部的碳原子之间的键角较小,因此这种构象比椅式构象稍微不稳定一些。
3. 扭曲椅式构象
扭曲椅式构象是一种介于椅式构象和船式构象之间的构象。
在扭曲椅式构象中,环己烷分子呈现出一个类似于椅子的形状,但是其中两个相邻的碳原子之间的键角略微扭曲,从而使得分子更加稳定。
4. 锥式构象
锥式构象是环己烷最不稳定的构象之一。
在锥式构象中,环己烷分子呈现出一个类似于锥形的形状,其中一个碳原子位于锥的顶部,其余五个碳原子位于锥的底部。
在锥式构象中,顶部的碳原子与底部的碳原子之间的键角非常小,因此这种构象非常不稳定。
环己烷的四种典型构象分别是椅式构象、船式构象、扭曲椅式构象和锥式构象。
这些构象的不同排列方式导致了环己烷分子的不同稳定性,从而影响了环己烷在化学反应中的表现。
取代环己烷的构象

取代基的电子效应
总结词
详细描述
给电子取代基可以降低环己烷的能垒,使 其更稳定。
给电子取代基如羟基、氨基等具有较高的 电负性,能够诱导环己烷环产生极化,降 低其能垒,使其构象更稳定。
总结词
详细描述
吸电子取代基则会增加环己烷的能垒,使 其不稳定。
吸电子取代基如卤素、硝基等具有较低的 电负性,能够使环己烷环产生去极化,增 加其能垒,使其构象不稳定。
总结词
取代基的电子效应是指取代基的电子性质对环己烷构象的 影响。
详细描述
取代基的电子效应可以通过诱导和共轭两种方式影响环己 烷的构象。诱导效应取决于取代基的电负性,而共轭效应 则与取代基能否与其他不饱和体系形成共轭有关。
总结词
取代基的空间效应是指取代基的空间大小和形状对环己烷 构象的影响。
详细描述
空间效应主要表现在取代基的大小和形状是否与环己烷环 匹配,以及取代基之间的相互位置关系。如果取代基太大 或形状不匹配,可能会引起环己烷构象的变化。
总结词
扭船型构象是一种不稳定的构象,其中取代基难以稳定地占据扭船型位置,导致 分子结构不稳定。
详细描述
在扭船型构象中,环己烷的六个碳原子大致呈扭曲的船的形状排列,其中两个碳 原子位于扭曲船的底部,形成扭船型位置。由于这种构象中取代基难以稳定地占 据扭船型位置,因此扭船型构象是一种不稳定的构象。
02
非极性取代基的位置也会影响其构象稳定性。例如,当非极 性取代基处于直立键位置时,它们与环己烷的碳原子之间的 相互作用更弱,导致更低的构象稳定性。
体积较大的取代基
体积较大的取代基可以与环己烷的碳原子形成更强烈的空间排斥相互作用,这通常会导致较低的构象稳定性。这种相互作用 可以通过计算取代基和环己烷之间的空间排斥力来预测。
环烷烃(环丙烷、环丁烷、环戊烷、环己烷)的构象

环烷烃的构象链状化合物的构象是由基团绕C—Cσ键旋转产生的;而环状化合物的构象至少涉及到两个C—Cσ键和其键角的转动和变化,有时还涉及到键长和键角的变化,比较复杂,常称环的翻转。
一、环丙烷的构象环丙烷是三个碳的环,只能是平面构象,即它的构型。
尽管只有一种构象,但这个环极不稳定,主要因为:1、所有C-H键都是重叠构象,扭转张力大。
2、C原子是不等性杂化或弯曲键,有“角张力”存在。
二、环丁烷的构象环丁烷有两种极限构象:动画演示:平面式构象:象环丙烷一样,不稳定,存在扭转张力和“角张力”。
蝶式构象:能缓解扭转张力和角张力,呈蝶式构象。
通过平面式构象,由一种蝶式翻转成为另一种蝶式构象,处于动态平衡。
蝶式是优势构象。
也有扭转能力和角张力存在。
三、环戊烷的构象环戊烷的构象主要是信封式和半椅式构象。
两者处于平衡。
因为平面构象能量较大,一般认为环戊烷采取这种构象可能性很少。
E相对=19kJ/mol 信封式半椅式四、环己烷的构象环己烷的构象经过近百年的努力才建立起来。
Baeyer 1885年提出张力学说,认为环状化合物是平面构型Sachse 1889年质疑张力学说只适合小环,提出环已烷有船式、椅式两种构象。
Hassel 1930年利用偶极矩测定法和电子衍射法研究环已烷构象,∠CCC=109.5°,气相、液相中环已烷几乎全是椅式构象。
Barton 1950年发展了构象理论,以甾族化合物为对象提出构象分析,把构象分析明确地引入有机化学中。
Hassel 和Barton获1969年Nobel化学奖1、椅式和船式构象环已烷保持碳原子的109.5°键角,提出了椅式和船式构象.1)椅式构象:C1、C2、C4、C5在一个平面上,C6和C3分别在平面的下面和平面的上面,很象椅脚和椅背,故称“椅式”。
2)船式构象:C1、C2、C4、C5在一个平面上,C3和C6在平面上面。
形状象只船,C3和C6相当船头和船尾,故称“船式”。
环烷烃(环丙烷、环丁烷、环戊烷、环己烷)的构象

环烷烃的构象链状化合物的构象是由基团绕C—Cσ键旋转产生的;而环状化合物的构象至少涉及到两个C—Cσ键和其键角的转动和变化,有时还涉及到键长和键角的变化,比较复杂,常称环的翻转。
一、环丙烷的构象环丙烷是三个碳的环,只能是平面构象,即它的构型。
尽管只有一种构象,但这个环极不稳定,主要因为:1、所有C-H键都是重叠构象,扭转张力大。
2、C原子是不等性杂化或弯曲键,有“角张力”存在。
二、环丁烷的构象环丁烷有两种极限构象:动画演示:平面式构象:象环丙烷一样,不稳定,存在扭转张力和“角张力”。
蝶式构象:能缓解扭转张力和角张力,呈蝶式构象。
通过平面式构象,由一种蝶式翻转成为另一种蝶式构象,处于动态平衡。
蝶式是优势构象。
也有扭转能力和角张力存在。
三、环戊烷的构象环戊烷的构象主要是信封式和半椅式构象。
两者处于平衡。
因为平面构象能量较大,一般认为环戊烷采取这种构象可能性很少。
E相对=19kJ/mol 信封式半椅式四、环己烷的构象环己烷的构象经过近百年的努力才建立起来。
Baeyer 1885年提出张力学说,认为环状化合物是平面构型Sachse 1889年质疑张力学说只适合小环,提出环已烷有船式、椅式两种构象。
Hassel 1930年利用偶极矩测定法和电子衍射法研究环已烷构象,∠CCC=109.5°,气相、液相中环已烷几乎全是椅式构象。
Barton 1950年发展了构象理论,以甾族化合物为对象提出构象分析,把构象分析明确地引入有机化学中。
Hassel 和Barton获1969年Nobel化学奖1、椅式和船式构象环已烷保持碳原子的109.5°键角,提出了椅式和船式构象.1)椅式构象:C1、C2、C4、C5在一个平面上,C6和C3分别在平面的下面和平面的上面,很象椅脚和椅背,故称“椅式”。
2)船式构象:C1、C2、C4、C5在一个平面上,C3和C6在平面上面。
形状象只船,C3和C6相当船头和船尾,故称“船式”。
6.2.3 环己烷的构象翻转

H AH BH AH B123456123456234613456半椅式构象中,1,2,3,4四个C 原子在同一个平面上,另两个C 原子(5,6)分别位于该平面的上方和下方。
半椅式构象是用分子力学计算过渡态的几何形象时提出的,是环己烷分子势能最高、最不稳定的构象;与椅式构象之间的势能差约为46kJ/mol 。
2)半椅式构象(Half-chair conformation )H A H B H A H B 123456123563) 扭船式构象(Twist-boat or skew-boat conformation )AB123561245H AH B扭船式构象中,所有的二面角都是30℃,所有的对边都是交叉的。
由椅式构象转变为扭船式构象,需要经历一个半椅式构象。
H H HHH143256123456扭船式构象比椅式构象不稳定,能量差为23.5kJ/mol 。
A H 123456124A B4)船式构象(Boat conformation )1,3,4,6四个C 原子共平面;另两个C 原子(2,5)在这一平面的同一侧;123456123564123456H HHH HH H H H HH H1456321,6和3,4分别为全重叠;1,2、2,3、4,5、5,6分别为邻位交叉。
因此,船式构象不如椅式构象稳定,两者之间的势能差约为29kJ/mol 。
船式构象中,2、5上两个H 原子(称为“旗杆氢”原子)相距较近(183pm ),存在非键空间张力;无键角张力。
1,6和3,4为全重叠式,存在键扭转张力。
H HHH HH HHHH 1234566.2.3 环己烷的构象翻转扭船式构象中,两个“旗杆”H 原子间的距离相对较远,非键空间张力小,因此比船式构象稳定,两者之间的势能差为5.4kJ/mol 。
H H H H HHH1432566.2.3 环己烷的构象翻转H AH BH AB123456123561245A B6312356235641234561245A B63123456AB12356H AH B6.2.3 环己烷的构象翻转船式椅式椅式扭船式半椅式半椅式扭船式势能23.5kJ/mol 46 kJ/mol6.2.3 环己烷的构象翻转6.2.3 环己烷的构象翻转总结:环己烷的椅式构象可以通过C–C键的旋转变成另一个椅式构象,a键和e键随之转换;此过程称为“构象翻转”(Conformational inversion),相应的两个椅式构象互称为“构象转换体”。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
