高中化学必修2 第2节 乙烯学案
乙烯与有机高分子材料(第2课时)课件下学期高一化学人教版(2019)必修第二册

解析 天然橡胶、蛋白质、天然纤维素都属于天然高分子化合物,只有尼龙自然界中不存在,属于合成高分子化合物。
【学业质量评价】
6.人们在日常生活中大量使用各种高分子材料,下列说法中正确的是( )A.天然橡胶易溶于水B.羊毛是合成高分子化合物C.聚乙烯塑料是天然高分子材料D.聚氯乙烯塑料会造成“白色污染”
耳绳
三层无纺布
鼻梁条
环保全塑条(PE)
聚乙烯
聚丙烯
橡胶皮筋
【学习任务三】认识耳绳材料----有机高分子材料“橡胶”
原材料供应种类:1、天然橡胶2、合成橡胶
森林中有一种高大的乔木,叫作“三叶树”。如果用小刀在它的树皮上割开一个小口子,便会有牛奶似的树汁流淌出来。这种树汁,就是今天人们所熟悉的橡胶的最初来源。在印第安人的土语中,“橡胶”就是“树木的眼泪”的意思。
【化学与职业】高分子材料研发人员
化学正在致力使世界变得更加美好!
1、你会看服装标签吗?
2、 从你学校的校服入手,调查衣服的面料与手感、舒适感、透气性的关系
3、 根据所调查的资料和所学知识,你能为不同季节(或用途)的穿衣面料提个建议吗?4、启发?
查阅资料,并参照学案附录“预习资料”,请同学们进行以下调查研究。
【学业质量评价】
D
4. 塑料废弃物的危害有①难以分解,破坏土壤结构,影响植物生长;②污染海洋;③危及海洋生物的生存;④造成海难事件;⑤破坏环境卫生,污染地下水( )A.①②③④⑤ B.①②③④C.②③④ D.①⑤
A
【学业质量评价】
5. 下列物质一定不是天然高分子的是( ) A.橡胶 B.蛋白质 C.尼龙 D.纤维素
目标1:寻找原材料制备聚乙烯
目标2:如何通过乙烯制备聚乙烯?
2020学年新教材高中化学第3章第2节从化石燃料中获取有机化合物第2课时石油裂解与乙烯教案鲁科版必修二

第2课时石油裂解与乙烯[核心素养发展目标] 1.了解石油裂解的基本原理及主要产物,掌握乙烯的主要性质及加成反应的原理,能从多角度动态分析加成反应的本质,培养“变化观念”化学核心素养。
2.了解乙烯的主要用途,能根据乙烯的结构与性质提出有价值的问题,培养“科学探究与创新意识”。
一、石油的裂解1.从石蜡中获取不饱和气态烯烃的实验探究实验操作实验现象酸性KMnO4溶液紫色逐渐褪去溴的四氯化碳溶液逐渐褪色结论:石蜡分解产生了能使酸性KMnO4溶液及溴的四氯化碳褪色的不饱和气态烃。
2.石油的裂解以石油分馏产物为原料,采用比裂化更高的温度,使其中相对分子质量较大的烃分解为乙烯、丙烯等小分子烃的方法。
原料:石油分馏产物(包括石油气)。
目的:获取乙烯、丙烯等小分子不饱和烃。
二、乙烯1.分子结构分子式结构式结构简式球棍模型空间填充模型C2H4CH2==CH22.物理性质颜色气味状态密度水溶性无色稍有气味气体比空气略轻难溶于水3.化学性质 (1)氧化反应①燃烧现象:火焰明亮,伴有黑烟。
化学方程式:C 2H 4+3O 2――→点燃2CO 2+2H 2O ②通入酸性KMnO 4溶液 现象:KMnO 4溶液褪色。
(2)加成反应①有机化合物分子中双键上的碳原子与其他原子(或原子团)直接结合生成新的化合物分子的反应属于加成反应。
②碳碳双键()中的一个键断裂,其他两个原子(或原子团)分别加在双键的两个碳原子上,双键变成单键。
③乙烯的加成反应:有关反应的化学方程式为: a .CH 2==CH 2+H 2――→催化剂△CH 3—CH 3; b .CH 2==CH 2+Br 2―→;c .CH 2==CH 2+H 2O ――→催化剂△CH 3CH 2OH ;d .CH 2==CH 2+HCl ――→催化剂△CH 3CH 2Cl 。
4.用途(1)乙烯是一种重要的有机化工基础原料,用于生产塑料等化工产品。
目前,世界上已将乙烯产量作为衡量一个国家石油化工发展水平的标志。
乙烯的化学性质教案

乙烯的化学性质教案【篇一:高二化学乙烯教案】第一课时教学目标知识技能:初步掌握乙烯分子的组成和结构;学会乙烯的实验室制法和收集方法。
能力培养:培养学生的观察能力、思维能力和实验能力。
科学思想:通过乙醇在不同条件下反应产物不同,即物质所发生的化学反应既决定于物质本身的性质,又决定于反应条件,渗透内因与外因的辩证唯物主义教育。
科学品质:通过乙烯用途的介绍,激发学生的学习兴趣,对学生进行爱国主义教育。
在实验教学过程中,培养学生严谨XX、勇于探索的科学态度。
科学方法:学习用表格的形式对知识进行分类归纳的方法。
重点、难点乙烯的结构和实验室制法;思维能力和实验能力的培养。
教学过程设计教师活动学生活动设计意图【复习提问】我们已经学了烷烃,请大家用系统命名法给下列物质命名:【引入】不饱和烃:分子里碳原子所结合的氢原子数少于饱和链烃里的氢原子数,分子里的这种碳原子还可以结合其他原子或原子团,这类烃叫不饱和烃。
【板书】第四章第四节乙烯【提问】同学们常见塑料,大家想想哪些物品是用塑料制作的?【设问】大家知道我手中这些塑料物品是用什么制造的吗?做命名练习,但对后两个物质感到诧异。
阅读课本第84页,理解概念。
记笔记。
思考并举例。
回答:是乙烯。
温故知新,诱导学生进行对比,从而引出新概念。
培养学生阅读理解能力和自学能力。
激发学生学习兴趣。
续表教师活动学生活动设计意图【讲述】乙烯不仅可以制塑料,还可以制橡胶、纤维等。
国际上评价一个国家的石油工业发展水平的高低就是用乙烯的年产量衡量的。
我国乙烯产量逐年迅猛增长,1997年乙烯产量为359万吨,比1996年增长18%。
【提问】乙烯的用途如此广泛,请大家想想这与乙烯的什么因素有关?【再问】那么乙烯的性质又是由它的什么因素决定的呢?【引入】现在我们就来研究乙烯的结构。
【板书】一、乙烯分子的结构【设问】乙烯分子中的两个碳原子、四个氢原子是怎样结合的呢?【讲述】请大家根据原子趋于达到稳定结构的趋势,试着写出乙烯的分子式、电子式、结构式和结构简式。
高中化学乙烯教案完整版

鲁科版普通高中课程标准教科书化学2(必修)第3章第2节
《乙烯》
乙烯
一、三维目标
1、知识与技能:①掌握乙烯的化学性质
②了解乙烯的分子组成,结构式,物理性质
2、过程与方法:①通过演示实验,培养其理论与实践相结合的哲学
观点。
②通过小组讨论的方法,增加学生们团队协作能力
③通过实验探究,培养学生观察实验能力
3、情感态度与价值观:①培养学生实事求是的科研态度
②形成“结构决定性质”的认知
二、教学重点、难点:
1、重点:掌握乙烯的化学性质
2、难点:简单掌握加成反应和取代反应的差异
三、教学方法
讲授法、问答法、演示法、讨论法等
四、教学用具
多媒体,实验用品,黑板
五、教学过程
二、板书设计
乙烯的结构和性质
1、物理性质
2、分子组成
3、化学性质
(1)氧化反应 ( 可燃烧、能被酸性KMnO4溶液氧化 )
(2)加成反应( 溴水、HCl、H2、H2O等)。
高中化学乙烯性质的教案

高中化学乙烯性质的教案
主题:乙烯的性质
一、教学目标
1. 了解乙烯的结构和命名方法;
2. 掌握乙烯的物理性质和化学性质;
3. 能够根据性质预测乙烯的用途。
二、教学重点
1. 乙烯的结构和命名方法;
2. 乙烯的物理性质和化学性质。
三、教学内容
1. 乙烯的结构和命名方法;
2. 乙烯的物理性质:无色、有特殊气味、易燃、不溶于水;
3. 乙烯的化学性质:与氯气反应生成四氯乙烯、与溴水反应生成1,2-二溴乙烷等。
四、教学过程
1. 导入:引导学生探讨乙烯一词的来源,并询问乙烯的结构和命名方法;
2. 学习乙烯的物理性质和化学性质,并进行实验演示;
3. 深化:让学生通过实验结果总结乙烯的特点,并讨论乙烯的用途;
4. 练习:设计习题,让学生加深对乙烯性质的理解;
5. 总结:总结乙烯的性质和用途,引导学生思考乙烯在生活中的应用。
五、教学资源
1. 实验器材:乙烯气体、氯气、溴水等;
2. 课件、教材和习题。
六、作业布置
1. 自主学习乙烯的性质和用途;
2. 完成相关练习题目。
七、教学反馈
1. 对学生的作业进行批改和评价;
2. 对学生在探究和实验中的表现进行评价。
至此,乙烯性质的教学已圆满结束,希望学生能够掌握乙烯的基本性质,并能够灵活运用在实际生活中。
高中化学乙烯教案doc

高中化学乙烯教案doc教学内容:乙烯一、教学目标:1. 了解乙烯的基本性质和结构;2. 掌握乙烯的物理性质和化学性质;3. 理解乙烯在工业生产和日常生活中的应用。
二、教学重点和难点:1. 乙烯的结构和性质;2. 乙烯的工业生产和应用。
三、教学方法:1. 讲授结合实验;2. 案例分析;3. 课堂讨论。
四、教学内容:1. 乙烯的基本性质和结构:乙烯是一种无色、有毒气体,具有刺激性气味。
它的化学式为C2H4,结构式为CH2=CH2。
乙烯的键长度较短,键能较高,稳定性较弱。
2. 乙烯的物理性质:乙烯是一种无色、有毒气体,易燃。
其密度小于空气,可以溶解在水中。
乙烯具有特殊的刺激性气味。
3. 乙烯的化学性质:乙烯是一种具有不饱和双键的烃类化合物,在化学反应中常表现出特殊的活性。
乙烯可以发生加成反应、氧化反应、卤素加成反应等。
4. 乙烯在工业生产和日常生活中的应用:乙烯是一种重要的工业原料,用于生产乙烯聚合物、合成橡胶、合成衬里等。
此外,乙烯还可用于制备醋酸乙烯酯、氯丙烯等有机化合物。
五、教学过程:1. 讲授乙烯的基本性质和结构;2. 实验演示乙烯的物理性质;3. 分析乙烯的化学性质;4. 讨论乙烯的工业生产和应用;5. 案例分析乙烯在日常生活中的应用。
六、教学总结:通过本节课的学习,学生将了解乙烯的基本性质和结构,掌握乙烯的物理性质和化学性质,理解乙烯在工业生产和日常生活中的应用。
同时,通过案例分析和课堂讨论,提高学生的探究能力和实践能力,培养学生的综合能力和创新思维。
高中化学乙烯说课教案

高中化学乙烯说课教案1. 掌握乙烯的物理性质和化学性质。
2. 了解乙烯的制备方法和应用领域。
3. 能够利用乙烯的化学性质解决实际问题。
二、教学重点与难点:重点:乙烯的物理性质、化学性质及其制备方法。
难点:乙烯与氧化剂的反应机理及其应用。
三、教学过程:1. 激发兴趣,引入话题。
分享一段乙烯在生活中的应用场景,如塑料制品、合成树脂等,引起学生对乙烯的好奇。
2. 学习乙烯的物理性质。
介绍乙烯的物理性质,如密度、熔点、沸点等,让学生了解乙烯的外观和一般性质。
3. 学习乙烯的化学性质。
讲解乙烯与氧化剂的反应、加成反应等化学特性,让学生了解乙烯的化学性质。
4. 学习乙烯的制备方法。
介绍乙烯的制备方法,包括烃分馏、石油裂化等,让学生了解乙烯的生产原理。
5. 讨论乙烯的应用领域。
讲解乙烯在化工、医药、农业等领域的应用,引导学生思考乙烯的广泛用途。
6. 解决实际问题。
通过案例分析乙烯的应用,并让学生利用乙烯的化学性质解决实际问题,培养学生的实践能力。
四、课堂总结:复习乙烯的物理性质、化学性质和制备方法,概括乙烯的应用领域,强调乙烯在生活中的重要性。
五、课后作业:1. 总结乙烯的物理性质、化学性质和制备方法。
2. 结合生活实际,思考乙烯的应用领域及其优缺点。
3. 搜集乙烯相关的新闻报道或材料,并做简要介绍。
六、教学反思:在教学过程中,应注重激发学生的兴趣和培养他们的实践能力,让学生能够将所学知识应用到实际生活中去。
同时,要提高学生的思辨能力,引导他们独立思考和解决问题。
高中化学人教版(2019)必修第二册学案第1课时乙烯
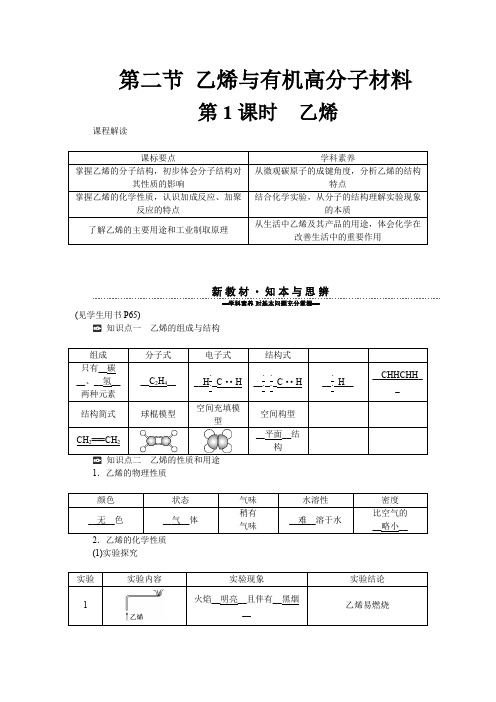
第二节乙烯与有机高分子材料第1课时乙烯课程解读课标要点学科素养掌握乙烯的分子结构,初步体会分子结构对其性质的影响从微观碳原子的成键角度,分析乙烯的结构特点掌握乙烯的化学性质,认识加成反应、加聚反应的特点结合化学实验,从分子的结构理解实验现象的本质了解乙烯的主要用途和工业制取原理从生活中乙烯及其产品的用途,体会化学在改善生活中的重要作用(见学生用书P65)知识点一乙烯的组成与结构组成分子式电子式结构式只有__碳__、__氢__两种元素__C2H4____H··C··H__····C··H__··H____CHHCHH__结构简式球棍模型空间充填模型空间构型CH2===CH2__平面__结构知识点二乙烯的性质和用途1.乙烯的物理性质颜色状态气味水溶性密度__无__色__气__体稍有气味__难__溶于水比空气的__略小__2.乙烯的化学性质(1)实验探究实验实验内容实验现象实验结论1火焰__明亮__且伴有__黑烟__乙烯易燃烧2酸性KMnO 4溶液__褪色__乙烯易被酸性KMnO 4溶液氧化3溴的四氯化碳溶液__褪色__ 乙烯易与溴反应(2)氧化反应(3)加成反应 ①概念:有机物分子中的__不饱和__碳原子与其他__原子或原子团__直接结合生成新的化合物的反应。
②乙烯的加成反应(4)聚合反应①乙烯能发生自身的加成反应生成高分子化合物聚乙烯,反应的化学方程式为__nCH 2===CH 2――→催化剂CH 2—CH 2__。
②聚合反应:由相对分子质量小的__化合物分子__互相结合成相对分子质量大的__聚合物__的反应。
乙烯的聚合反应同时也是加成反应,这样的反应又被称为加成聚合反应,简称__加聚反应__。
③链节、聚合度、单体:聚合反应生成的高分子是由较小的结构单元重复连接而成的。
在聚乙烯分子中“__—CH 2—CH 2—__”称为链节,链节的数目n 称为聚合度。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
§3~2 来自石油和煤的两种基本化工原料
第一课时乙烯
【预习目标】
1、能说出乙烯的来源和用途;
2、能写出乙烯分子的组成和结构;
3、能说出乙烯的物理性质
【预习问题】
一、苯是1825年由英国科学家首先发现的,与乙烯一样是一种重要的 _______,其产品在今天的生活中无处不在,应用广泛。
二、苯
㈠苯的物理性质
1. 色、有特殊气味的有的。
2.比水,溶于水;溶于有机溶剂。
3.沸点是80.1℃(易);
熔点是5.5℃(苯放入冰水混合物中)。
㈡苯分子结构
1.苯的分子式为,结构式
结构简式或
2、分析苯分子的结构特点,推测苯的化学性质有哪些?
㈢苯的化学性质
苯的化学性质与烯烃有很大区别,在一定条件下可发生如下反应:
1.苯的氧化反应:
苯在空气中燃烧:(方程式) _________ 现象:
[思考]你能解释产生这种现象的原因吗?
____________________________________________
2.苯的取代反应
苯在一定条件下,可以与溴发生取代反应
溴苯是色体,密度比水。
[思考]比较烷烃和苯跟卤素单质的取代反应条件有何不同?
3.苯的加成反应
一定条件下可以和氢气、氯气等发生加成反应。
苯在金属镍作催化剂,加热的条件下可以与氢气发生加成反应,生成环己烷,写出此反应的化学方程式。
四、芳香烃
概念:含 的烃,如甲苯(苯的同系物)、二甲苯等。
课内探究学案【学习目标】
知识与技能4、能说出乙烯的来源和用途;
5、能写出乙烯分子的组成和结构;
6、能说出乙烯的物理性质
7、能写出乙烯典型的化学反应方程式,掌握加成反应。
过程与方法从实验现象到乙烯结构的推理,使学生体会科学研究的方法。
情感态度与价值观通过对乙烯分子结构的推理过程,使学生从中体会到严
谨求实的科学态度。
【学习重点&难点】乙烯的化学性质和加成反应的概念。
【学习过程】
一、乙烯的来源和用途
1、来源:从________中获得乙烯,已成为目前工业生产乙烯的主要途径。
2、用途:________________________________
3、价值:________的产量可以用来衡量一个国家的石油化工发展水平。
观察实验现象并记录到下表中:
通入酸性高锰酸钾溶液中
通入溴的四氯化碳溶液中
点燃
(想一想)由实验现象可知,哪些现象证明生成物与烷烃具有相同的性质?哪些现象证明生成物可能具有不同于烷烃的性质?
推测:你认为生成的气体中都是烷烃吗?说明理由______________________________________________________________________________________。
(概念小结) 烯烃:______________________________________________。
二.乙烯的组成和结构
(写一写)分子式:电子式:
结构式:结构简式:
空间构型:
(讨论一下)已知乙烯分子中碳碳双键的键能(615KJ/mol)小于碳碳单键的键能(348KJ/mol)的2倍,同时双键中两个键的键能也不相等。
这说明什么问题呢?
三.乙烯的化学性质
1、氧化反应(1)燃烧:(被____氧化)
化学方程式:______________________________________(2)被_________________氧化,生成__________。
2、加成反应
概念:_________________________________________________
________________________________________________________________。
(练一练)乙烯还能与H2、Cl2、HCl、H2O(H-OH)等发生加成反应,试写出其反应的化学方程式。
3、加聚反应
实践活动乙烯的催熟:
【当堂检测】
1、在1.01×105Pa、150℃条件下,某烃完全燃烧,反应前后压强不发生变化,该烃可能是()
A.CH4
B.C2H6
C.C2H4
D.C2H2
2、除去乙烷中混有的少量乙烯,最好的方法是()
A 将混合气体点燃
B 将混合气体通过溴水
C 将混合气体在催化剂条件下跟氢气反应
D 将混合气体通过酸性KMnO4溶液
3、由乙烯推测丙烯(CH2=CH—CH3)的结构或性质正确的是()
A. 不能使酸性KMnO4溶液退色
B. 能在空气中燃烧
C. 能使溴水退色
D. 与H Cl在一定条件下加成只得到一种产物
4、不可能是乙烯加成产物的是()
A. CH3CH3
B. CH3CHCl2
C. CH3CH2OH
D. CH3CH2Br
【答案】BC、B 、B 、AC
课后练习与提高
1、下列关于乙烯的叙述中,不正确的是()
A.乙烯的化学性质比乙烷活泼
B.乙烯燃烧时火焰明亮,同时冒出黑烟
C.乙烯可作香蕉等果实的催熟剂
D.乙烯双键中的一个键可以断裂,容易发生加成反应和取代反应
2、1mol乙烯与氯气完全加成,再与氯气彻底取代,两个过程共用氯气(
)
A.1mol
B.4mol
C.5mol
D.6mol
3、下列反应中属于加成反应的是()
A.乙烯使酸性高锰酸钾溶液褪色
B.将四氯化碳滴入溴水中,振荡后水层接近无色
C.乙烯使溴水褪色
D.甲烷与氯气混合,黄绿色消失
4、从南方往北方长途运输水果时,常常将浸泡有高锰酸钾溶液的硅藻土放置在盛放水果的容器中,其目的是()
A.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
D.利用高锰酸钾溶液的氧化性,催熟水果
答案:DCCC。
